基于Smart-seq2探究玻璃化冷凍對豬孤雌激活囊胚基因表達的影響


摘 要: 旨在探究玻璃化冷凍對豬孤雌激活(parthenogenetic activation, PA)囊胚基因表達的影響。本研究以豬PA囊胚為研究對象,根據試驗處理分為新鮮組、玻璃化冷凍組Ⅰ和玻璃化冷凍組Ⅱ,隨后從每組挑選3枚形態良好的囊胚,利用Smart-seq2單細胞全長轉錄組測序技術進行轉錄組測序分析。結果顯示,玻璃化冷凍組Ⅰ與新鮮組相比,共鑒定到772個差異表達基因(differential expression genes,DEGs),GO和KEGG富集分析結果顯示,這些DEGs與細胞脂質代謝過程、細胞葡萄糖穩態、MAPK信號通路、PI3K-Akt信號通路等相關;玻璃化冷凍組Ⅱ與新鮮組相比,共鑒定到1 613個DEGs,主要與糖異生、代謝途徑、氨基酸生物合成等相關;玻璃化冷凍組Ⅱ與玻璃化冷凍組Ⅰ相比,鑒定到822個DEGs,主要與丙酮酸代謝過程、N-聚糖生物合成、細胞衰老等相關。綜上,本研究基于Smart-seq2單細胞全長轉錄組測序技術揭示了玻璃化冷凍對豬PA囊胚脂質代謝、能量代謝、MAPK信號通路等相關基因表達的影響。
關鍵詞: Smart-seq2;玻璃化冷凍;豬;孤雌激活;囊胚
中圖分類號: S828.3
文獻標志碼: A 文章編號: 0366-6964(2024)09-3936-11
Exploring the Effect of Vitrification on Gene Expression in Porcine Parthenogenetic
Blastocysts by Smart-seq2
YANG" Baigao" LONG" Xi1, ZHANG" Liang1, XU" Jiehuan3, DAI" Jianjun3, ZHAO" Xueming2, PAN" Hongmei1*
(1.Chongqing Academy of Animal Sciences, Chongqing 402460," China;
2.Institute of
Animal Sciences, Chinese Academy of Agricultural Sciences, Beijing 100193," China;
3.Institute of Animal Science and Veterinary Science, Shanghai Academy of Agricultural Sciences, Shanghai 201106," China)
Abstract:" The aim of this study was to investigate the effect of vitrification on gene expression in porcine parthenogenetic activation (PA) blastocysts. In this study, porcine PA blastocysts were divided into fresh, vitrification group I and vitrification group II according to the experimental treatments, and then 3 well-morphologised blastocysts were selected from each group and analysed by transcriptome sequencing using Smart-seq2 single-cell full-length transcriptome sequencing technology. As a result, compared with the fresh group, a total of 772 differential expression genes (DEGs) were identified in the vitrification group Ⅰ. GO and KEGG enrichment analysis results showed that these DEGs were related to cellular lipid metabolic process, cell glucose homeostasis, MAPK signaling pathway, PI3K-Akt signaling pathway, etc. Compared with the fresh group, a total of 1 613 DEGs were identified in the vitrification group Ⅱ, which mainly related to gluconeogenesis, metabolic pathways, biosynthesis of amino acids, etc. Compared with the vitrification group Ⅰ, 822 DEGs were identified in the vitrification group Ⅱ, which mainly involved in pyruvate metabolic process, N-Glycan biosynthesis, cellular senescence, etc. In summary, this study revealed the effects of vitrification on the expression of genes related to lipid metabolism, energy metabolism, MAPK signalling pathway and other related genes in porcine PA blastocysts based on Smart-seq2 single-cell full-length transcriptome sequencing technology.
Key words: Smart-seq2; vitrification; pig; parthenogenetic activation; blastocyst
*Corresponding author:PAN Hongmei, E-mail:panhm_2118@163.com
玻璃化冷凍技術是利用高濃度保護劑使動物遺傳資源載體在超低溫環境下凝固形成不規則玻璃化樣固體,進而使其可以在超低溫環境下長期保存的冷凍保存方法。目前,玻璃化冷凍技術已成為動物遺傳資源冷凍保存及活體復原的重要技術手段,在牛、馬、羊等家畜動物卵母細胞、精子、胚胎等的保存和傳遞中得到廣泛應用。然而,現有玻璃化冷凍技術在豬胚胎冷凍保存中仍存在不足,如凍后胚胎存活率和孵化率降低[1]。研究顯示,玻璃化冷凍不僅導致豬胚胎線粒體損傷、DNA損傷和細胞骨架機械損傷[2],還引起生長發育、缺氧、線粒體自噬相關基因表達發生改變[3]。因此,亟需加快改善現有豬胚胎玻璃化冷凍體系。
豬孤雌激活(parthenogenetic activation,PA)胚胎來源于單卵母細胞,易于在體外進行大批量生產,是研究豬胚胎玻璃化冷凍體系的理想模型。研究表明,相比于桑葚胚和擴張囊胚,對豬早期囊胚進行玻璃化冷凍可以獲得更高的孵化率,因此,囊胚期是豬胚胎玻璃化冷凍的理想階段[2]。然而,目前有限的研究未能以單囊胚水平解析玻璃化冷凍對豬PA囊胚基因表達的影響[4-5],難以為玻璃化冷凍體系改良提供更為精細的理論基礎。
隨著單細胞全長轉錄組測序技術的進一步發展,Smart-seq2技術以其高精度、高覆蓋率特點,在人[6]、豬[7]、小鼠[8,9]胚胎研究中受到廣泛應用。基于此,本研究利用Smart-seq2單細胞全長轉錄組測序技術對新鮮組、玻璃化冷凍組Ⅰ和玻璃化冷凍組Ⅱ豬PA囊胚進行轉錄組學分析,以期揭示玻璃化冷凍對其轉錄組表達的影響,為豬胚胎玻璃化冷凍技術研究和促進豬種質資源保存進展提供理論依據。
1 材料與方法
1.1 試驗試劑
除特殊說明,所有試劑均購自于美國Sigma公司。
1.2 豬卵母細胞采集和體外成熟
從屠宰場采集豬卵巢,37 ℃生理鹽水(加入青霉素75 μg·mL-1和鏈霉素50 μg·mL-1)清洗3遍,在2 h內運回實驗室。采用10 mL注射器從直徑為2~8 mm的卵泡中抽取卵泡液,采集到的卵泡液靜置15 min后,在體式顯微鏡下挑取含有2~3層卵丘細胞且胞質均勻的豬卵丘-卵母細胞復合物(cumulus-oocyte complexes, COCs)。
COCs在M199中洗滌3次后,每50枚一組移入含500 μL體外成熟(in vitro maturation,IVM)液(M-199含0.1 g·L-1 丙酮酸鈉、0.55 g·L-1 葡萄糖、0.07 g·L-1 半胱氨酸、10 IU·mL-1 FSH、10 IU·mL-1 LH、10 ng·mL-1 EGF和10%豬卵泡液)的培養孔中,隨后在38.5 ℃、5% CO2、飽和濕度條件下培養44 h。
1.3 孤雌激活
使用0.1%透明質酸酶消化去除COCs中的卵丘細胞,在M199中充分洗滌,選擇含第一極體且胞質均勻的卵母細胞用于孤雌激活(parthenogenetic activation, PA)。卵母細胞在電激活液(50 μmol·L-1 CaCl2、0.1 mmol·L-1 MgCl2和0.3 mol·L-1甘露醇)中預清洗30 s,隨后移入電激活池,設置參數為1.2 kV·cm-1、30 μs,脈沖一次。電激活后將卵母細胞移入化學輔激活液(PZM-3+5 μg·mL-1 CB+10 μg·mL-1放線菌酮)中培養4 h,隨后在PZM-3中繼續培養6 d后挑選優質囊胚用于后續試驗。
1.4 玻璃化冷凍和解凍
玻璃化冷凍:囊胚在冷凍液Ⅰ(PZM-3含7.5% EG、7.5% DMSO、20% FBS)中平衡5 min,在冷凍液Ⅱ(PZM-3含0.4 mol·L-1蔗糖、15% EG、15% DMSO、20% FBS)中平衡20 s,隨后移至Cryotop載片,迅速投入液氮。
玻璃化解凍:將含囊胚的Cryotop載片浸入37 ℃預熱解凍液Ⅰ(PZM-3含0.3 mol·L-1蔗糖、20% FBS),輕輕晃動使囊胚滑落,平衡3 min,隨后移入37 ℃解凍液Ⅱ(PZM-3含0.15 mol·L-1蔗糖、20% FBS),平衡3 min后用PZM-3洗滌3次,隨后在PZM-3中培養24 h,挑選形態恢復良好的囊胚用于單細胞轉錄組測序。
玻璃化冷凍組Ⅰ豬PA囊胚按照上述步驟進行冷凍和解凍,玻璃化冷凍組Ⅱ豬PA囊胚采用實驗室改良冷凍液(在冷凍液Ⅰ和冷凍液Ⅱ基礎上添加組分以提高其熱傳遞效率等,申請專利號:202311731656.6)進行,玻璃化冷凍程序不變。
樣本收集:從新鮮組(AA)、玻璃化冷凍組Ⅰ(BB)和玻璃化冷凍組Ⅱ(CC)中各選取3枚形態良好的囊胚,在每管裂解液中放入1枚胚胎,共收集9份測序樣本。
1.5 單細胞全長轉錄組測序文庫構建及上機測序
RNA反轉錄及擴增:在裂解液中加入CA磁珠,充分震蕩后離心5 min,隨后進行反轉錄擴增,取反轉錄產物進行PCR擴增,利用AMPure XP磁珠純化PCR產物,采用Fragment Analyzer 1.0.2.9對擴增產物進行質檢,質檢合格后用于文庫構建。
文庫構建及測序:根據廠商說明,利用KAPA Hyper Prep Kits (KK8504)試劑盒進行文庫構建,對cDNA進行片段化、PCR 富集、AMPure XP 磁珠純化分選片段等步驟后,利用Fragment Analyzer(1.0.2.9)對文庫大小進行質檢,片段主要分布在300~700 bp之間,隨后利用極客基因科技有限公司illlumina Novaseq6000 PE150平臺進行測序。
1.6 生物信息學分析
利用Trimmomatic(v0.39)對原始reads進行過濾,去除adapter序列、低質量的堿基和受污染的序列。隨后使用STAR(v2.7.9a)將過濾后的reads映射到到豬參考基因組Sscrofa11.1上,參數為:-runThreadN 30-alignIntronMax 100000-chimSegmentReadGapMax parameter 3-alignSJstitchMismatchNmax 5-1 5 5。利用featurets(v1.6.5)計算表達量,使用StringTie(v2.1.7)獲得標準化基因水平FPKM值,采用DEseq2計算基因表達差異,以log2(FC)≥1和Plt;0.01為差異顯著。基于Gene Ontology(GO)數據庫和Kyoto Encyclopedia of Genes and Genomes(KEGG)數據庫,利用DAVID(https://david.ncifcrf.gov/)進行基因功能分析。
2 結 果
2.1 轉錄組測序數據
從9個測序樣本中總共獲得34 830萬條讀數,過濾后保留23 226萬條讀數,Q20在98.93%~99.22%之間,Q30在96.61%~97.49%之間,比對到豬參考基因組(Sscrofa11.1)的讀數在80.15%~91.76%之間。本研究中使用的原始數據已上傳到CNSA數據庫,項目號為:CNP0005353。
2.2 新鮮組、玻璃化冷凍組Ⅰ、玻璃化冷凍組Ⅱ豬PA囊胚轉錄組差異分析
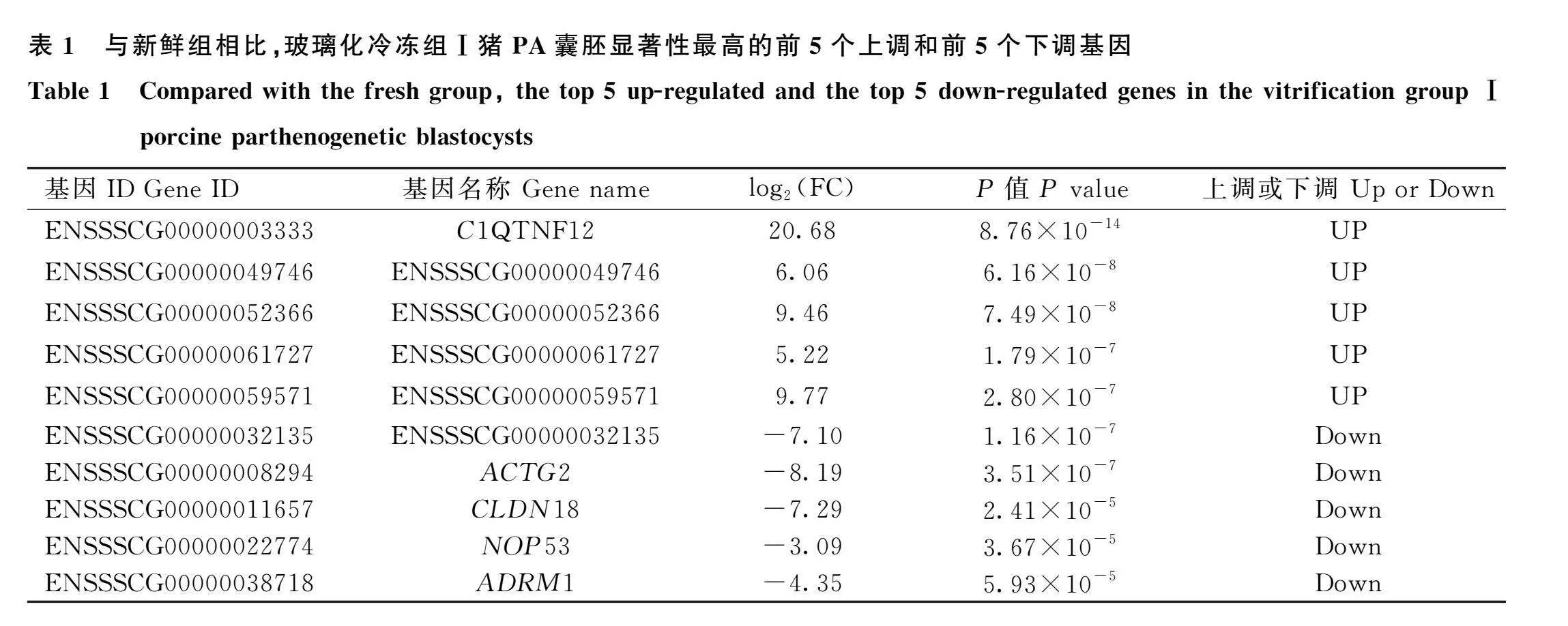
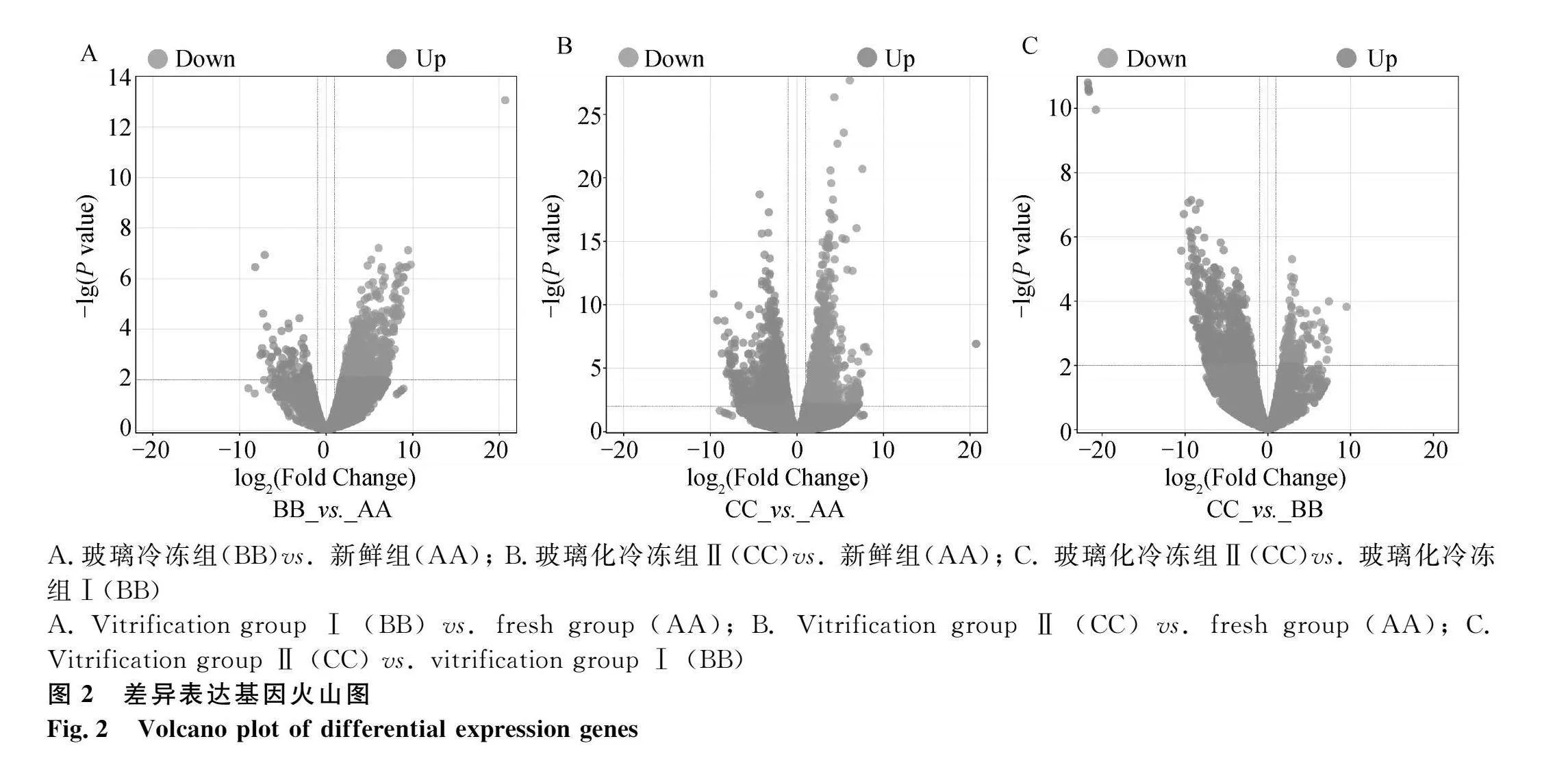
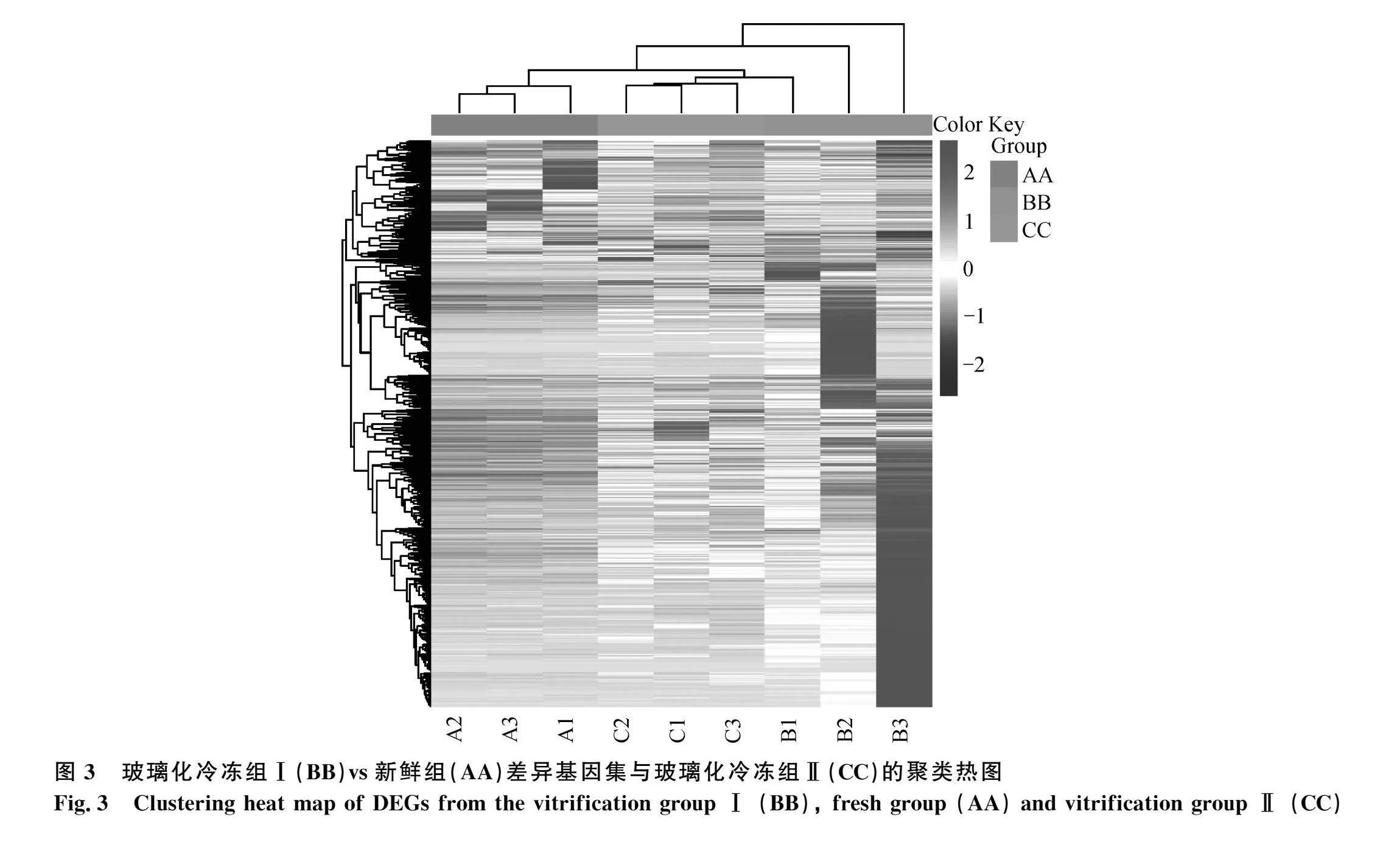
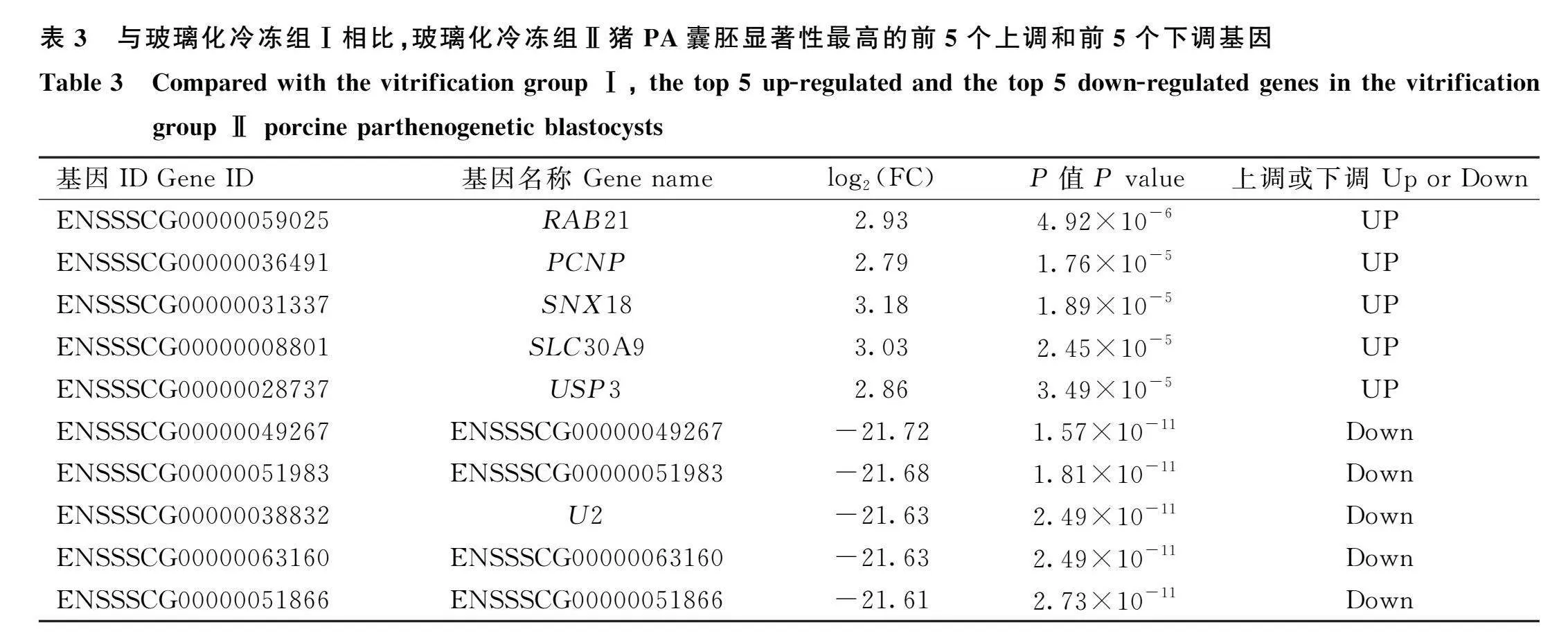
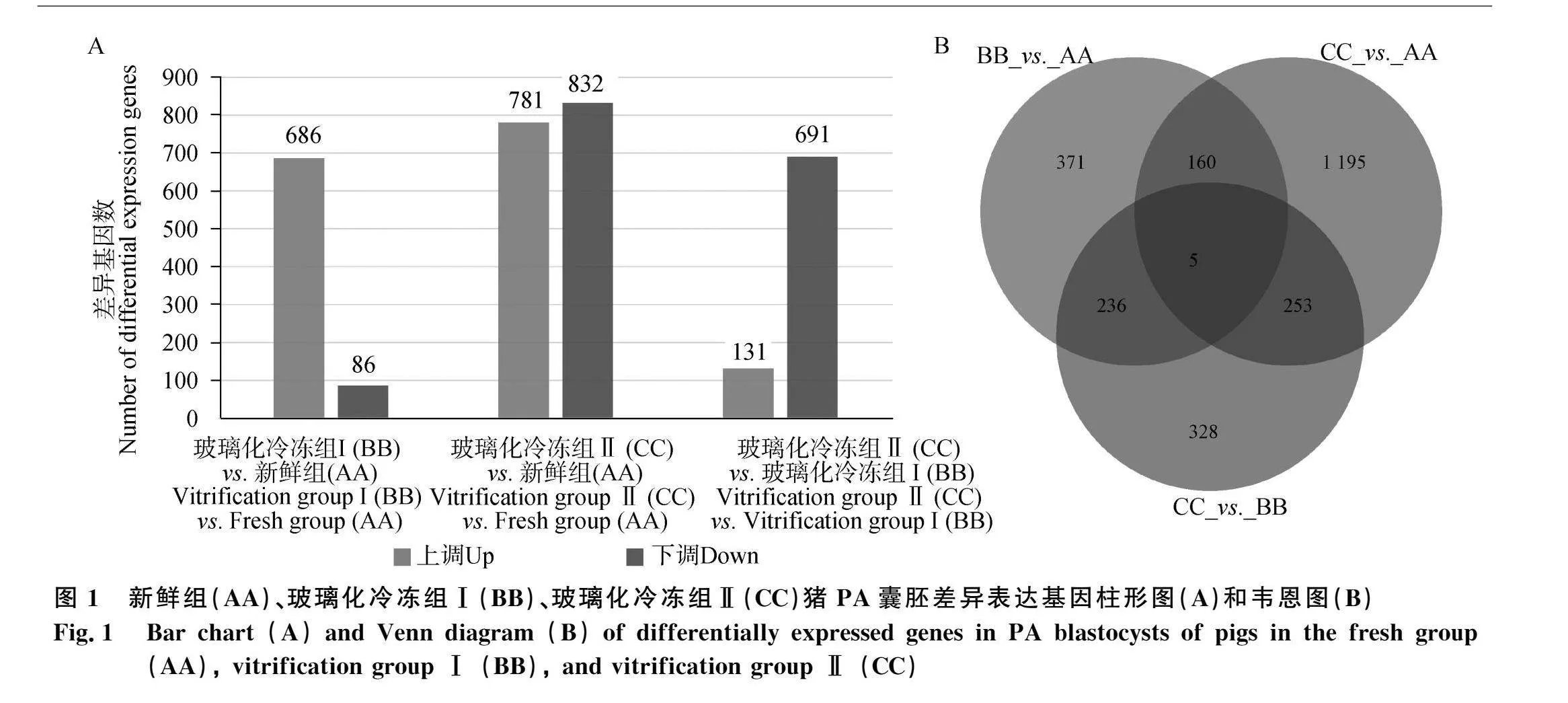
與新鮮組相比,從玻璃化冷凍組Ⅰ豬PA囊胚中鑒定到772個差異表達基因(differential expression genes,DEGs),其中686個上調,86個下調(圖1A,圖2A,表1);與新鮮組相比,從玻璃化冷凍組Ⅱ豬PA囊胚共鑒定到781個上調基因,832個下調基因(圖1A,圖2B,表2);與玻璃化冷凍組Ⅰ相比,從玻璃化冷凍組Ⅱ豬PA囊胚鑒定到131個上調基因,691個下調基因(圖1A,圖2C,表3)。此外,基于玻璃化冷凍組Ⅰ vs._新鮮組差異基因集,在玻璃化冷凍組Ⅱ豬PA囊胚中有607個基因的表達水平與新鮮組相近(圖1B,圖3)。
2.3 基因功能分析
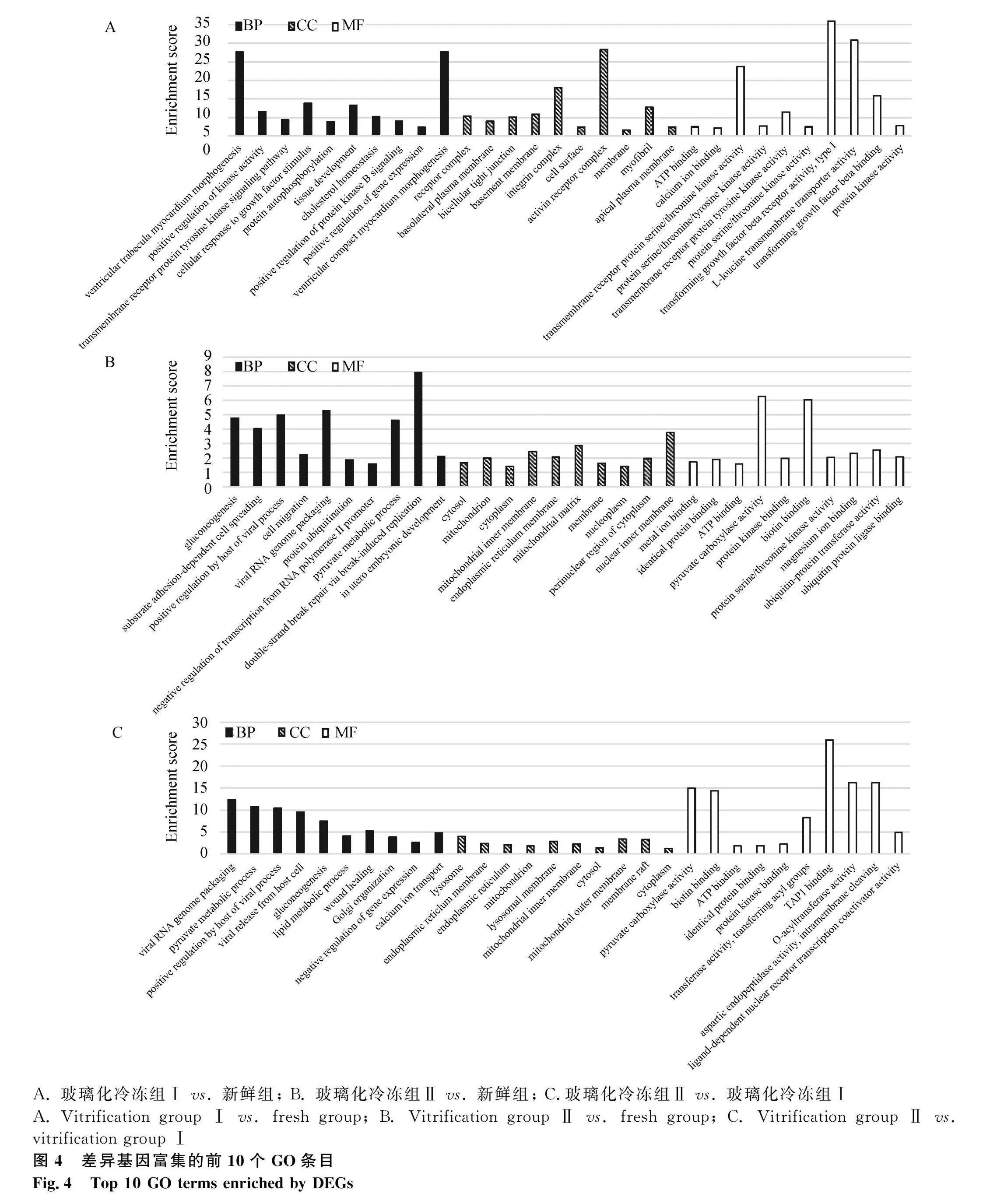
通過GO富集分析,與新鮮組相比,玻璃化冷凍組Ⅰ豬PA囊胚中的差異表達基因被富集到59個生物學過程(biological process, BP)條目,如激酶活性的正向調節、跨膜受體蛋白酪氨酸激酶信號通路、蛋白質自磷酸化等;30個細胞組分(cellular component, CC)條目,如受體復合物、基底外側質膜、雙細胞緊密連接等;47個分子功能(molecular function, MF)條目,如ATP結合、跨膜受體蛋白絲氨酸/蘇氨酸激酶活性、蛋白激酶活性等(圖4A)。
而玻璃化冷凍組Ⅱ與新鮮組相比,差異表達基因被富集到糖異生、細胞遷移、蛋白質泛素化等133個BP條目;細胞質、線粒體、內質網膜等72個CC條目;金屬離子結合、丙酮酸羧化酶活性、蛋白絲氨酸/蘇氨酸激酶活性等77個MF條目(圖4B)。此外,玻璃化冷凍組Ⅱ與玻璃化冷凍組Ⅰ相比,差異表達基因被富集到丙酮酸代謝過程、糖異生、脂質代謝過程等53個BP條目;溶酶體、內質網、線粒體等29個CC條目;丙酮酸羧化酶活性、生物素結合、O-酰基轉移酶活性等26個MF條目(圖4C)。
通過KEGG富集分析,與新鮮組相比,玻璃化冷凍組Ⅰ豬PA囊胚中差異表達基因被富集到35條信號通路,如胞吞作用、MAPK信號通路、PI3K-Akt信號通路等(圖5A)。玻璃化冷凍組Ⅱ與新鮮組相比,差異表達基因被富集到87條信號通路,如代謝途徑、氨基酸的生物合成、碳代謝等(圖5B)。玻璃化冷凍組Ⅱ與玻璃化冷凍組Ⅰ相比,差異表達基因被富集到13條信號通路,如內質網中的蛋白質加工、N-聚糖生物合成、MAPK信號通路等(圖5C)。
3 討 論
3.1 Smart-seq2單細胞全長轉錄組測序技術
相較于常規轉錄組測序技術,單細胞全長轉錄組技術為解析細胞分子機制提供了更精細的視角。Smart-seq2是Picelli等[10]基于Smart-seq改良的單細胞全長轉錄組測序技術,具有高靈敏度、準確性和全長覆蓋率等優點,受到廣泛關注。Li等[11]利用Smart-seq2測序技術揭示了玉米赤霉烯酮對綿羊卵母細胞發育的損傷機制。Yang等[7]通過Smart-seq2測序技術解析了豬對稱及不對稱2細胞期胚胎的轉錄組學差異。Smart-seq2測序技術是研究動物卵母細胞、胚胎分子機制的有力手段。
現有研究表明,玻璃化冷凍導致卵母細胞、胚胎基因表達發生改變。Jia等[12]的研究顯示,玻璃化冷凍引起豬未成熟卵母細胞成熟率降低,其AQP1、MEF2C、MT1A等基因的表達發生改變。Xu等[13]的研究顯示,原核受精卵階段進行玻璃化冷凍會降低其后續發育率以及4細胞和8細胞期胚胎的整體轉錄活性。豬體內胚胎基因表達也會受玻璃化冷凍影響發生變化[3]。易于體外批量生產的豬PA囊胚是加快豬胚胎玻璃化冷凍體系發展的理想研究模型。然而,鮮有報道基于單胚胎轉錄組水平研究玻璃化冷凍對豬PA囊胚基因表達的影響。
本研究采用Smart-seq2測序技術對新鮮組、玻璃化冷凍組Ⅰ、玻璃化冷凍組Ⅱ豬PA囊胚進行轉錄組學分析,以期探究玻璃化冷凍對豬PA囊胚基因表達的影響。
3.2 玻璃化冷凍對豬PA囊胚基因表達的影響
與其他哺乳動物相比,豬胚胎內含有大量以脂滴形式存在的脂質,在胚胎發育過程中發揮重要作用[14-15]。與新鮮組相比,玻璃化冷凍組Ⅰ豬PA囊胚中BBS1、SREBF1、ANGPTL3等23個差異表達基因參與細胞脂質代謝過程、脂質穩態、甘油三脂穩態等生物學過程。BBS1編碼脂質穩態調節相關蛋白,其缺失引起膜相關蛋白的積累[16],以及小鼠體重和脂肪的增加[17]。SREBF1參與脂肪合成,在脂質穩態調節中發揮重要作用,其缺失導致脂肪合成受阻及相關復合物的脂質組成發生變化[16,18]。ANGPTL3編碼分泌蛋白家族成員,在脂質代謝中發揮重要作用,其缺失導致小鼠脂肪酸生成增加[19],ANGPTL3還參與胎兒發育過程[20]。表明玻璃化冷凍可能導致豬PA囊胚的脂質穩態失衡,進而影響其發育能力[21]。
ATP是胚胎發育過程中的重要調節因子,如胚胎細胞增殖、凋亡等[22]。在玻璃化冷凍豬PA囊胚中,C1QTNF12、GCK、NDUFS6等81個差異表達基因參與ATP結合、ATP酶活性、細胞葡萄糖穩態等生物學功能。C1QTNF12參與調節葡萄糖水平,其在豬卵巢顆粒細胞(GC)中表達并通過激活蛋白激酶B(Akt)促進GC增殖和MAPK3/1信號通路促進孕酮、睪酮、雌二醇的分泌[23]。GCK參與糖代謝,GCK調節己糖6-磷酸水平,是胰腺β細胞中的葡萄糖傳感器,其突變可導致葡萄糖糖代謝失調[24]。NDUFS6是線粒體電子傳遞鏈的酶復合物亞基,參與ATP生成,其缺失引起細胞衰老[25]。已有研究表明,玻璃化冷凍導致豬胚胎中ATP水平降低[2,26],這可能與能量代謝相關基因表達的異常有關。
細胞結構是細胞生物學活動的功能基礎,在玻璃化冷凍組Ⅰ豬PA囊胚中,ACTG2、CLDN18、ADRM1等基因的表達下調(表1)。ACTG2編碼的γ肌動蛋白,是細胞骨架的組成部分;CLDN18編碼膜蛋白,主要參與構成緊密鏈接,調節離子轉運和溶質滲透性以及細胞骨架[27],在玻璃化冷凍過程中保護細胞骨架有助于豬胚胎發育[28]。ADRM1編碼粘附調節因子,參與調節細胞粘性[29]。此外,玻璃化冷凍引起豬PA囊胚MAPK信號通路(FGF10、MAPK12、DUSP7等)、PI3K-Akt信號通路(ITGA6、LAMC1、MAGI1等)等重要信號通路相關基因表達水平的改變。MAPK通路活性參與調節胚胎發育,Mo等[30]的研究顯示,利用白血病抑制因子LIF可通過MAPK途徑介導改善牛胚胎體外發育。Wang等[31]的研究顯示,MAPK3參與人胚胎干細胞的維持。PI3K-Akt不僅在卵母細胞成熟過程中發揮重要作用,也參與隨后的胚胎發育,PI3K抑制導致胚胎發育能力降低[32]。因此,由玻璃化冷凍引起的豬PA囊胚細胞結構、MAPK信號通路、PI3K-Akt信號通路相關基因表達水平的變化可能影響其發育能力。
3.3 玻璃化冷凍液成分參與影響豬PA囊胚基因表達
為了探究玻璃化冷凍液成分的變化是否參與影響豬PA囊胚基因表達,本研究在玻璃化冷凍組Ⅰ的冷凍液基礎上調整冷凍液成分,進行玻璃化冷凍組Ⅱ試驗并分析其基因表達水平。
與新鮮組相比,玻璃化冷凍組Ⅱ豬PA囊胚中有1 613個DEGs,差異顯著性最高的上、下調基因中,SLC30A9的表達水平高于新鮮組和玻璃化冷凍組Ⅰ,表明其可能具有更高的鋅離子調節活性[33],研究表明適量補充鋅可促進豬胚胎體外發育[34]。MKNK2編碼蛋白是MAP激酶激活的下游激酶之一,其上調可能促進MAPK通路活性,已經證明其在卵巢癌中促進細胞增殖[35]。ZYX參與調節胚胎發育,其缺失導致胚胎形態缺陷[36],ZYX還通過Akt/mTOR通路調控細胞增殖[37],其下調可能引起胚胎發育障礙。FTL編碼鐵蛋白輕鏈,參與細胞鐵吸收、存儲和釋放,FTL下調可誘導胚胎細胞死亡[38]。MRPL28編碼線粒體核糖體蛋白,參與調節線粒體活性[39];PFKL在糖酵解中催化D-果糖6-磷酸向果糖1-6-二磷酸的轉化,兩者的下調可能引起豬PA囊胚ATP水平下降[40]。此外,其余DEGs參與子宮內胚胎發育(NOTCH2、ACVR1、SMAD4等)、細胞對缺氧的反應(PRKCE、LMNA、PDGFB等)、糖酵解/糖異生信號通路(MINPP1、GPI、PFKL等)等生物學功能。
與玻璃化冷凍組Ⅰ相比,在玻璃化冷凍組Ⅱ豬PA囊胚中有822個DEGs(圖1A),差異顯著性最高的上下調基因中,RAB21編碼蛋白參與調節細胞自噬和能量平衡,其缺失影響葡萄糖攝取和自噬通量增加[41],自噬水平穩態對胚胎發育至關重要[42],而玻璃化冷凍誘導的自噬異常影響胚胎發育[43],SNX18表達水平的改變可能影響胚胎自噬水平[44]。PCNP[45]和USP3[46]參與蛋白質泛素化,PCNP通過與β-catenin結合激活Wnt/β-actin通路,促進卵巢癌細胞的生殖,抑制凋亡[47];USP3參與調節細胞周期[48]。SLC30A9參與子線粒體鋅離子轉運,其缺失引起線粒體鋅離子失衡以及ROS生成增加[49-50]。此外,其余DEGs參與糖異生(PC、SLC25A11)、氧化還原酶活性(POR、HSD17B1、OSGIN1等)、細胞增殖的調節(TFAP2A、LAMA5、TFAP2C等)、細胞凋亡過程(PPP1R15A、BRAT1、EMP2等)、MAPK信號通路(RET、PLA2G4F、MAP3K1)等生物學功能。玻璃化冷凍組Ⅱ與玻璃化冷凍組Ⅰ之間部分基因的表達水平存在差異,基于BB_vs._AA DEGs,在玻璃化冷凍組Ⅱ中有607個基因的表達水平與新鮮組相近(圖1B),表明兩者之間具有不同的基因表達模式,這可能是冷凍液成分變化所致。
綜上所述,玻璃化冷凍引起豬PA囊胚脂質代謝、能量代謝、MAPK信號通路、PI3K-Akt信號通路等相關基因表達水平的改變,可能影響其隨后發育能力。此外,通過比較玻璃化冷凍組Ⅰ和玻璃化冷凍組Ⅱ轉錄組學差異,表明玻璃化冷凍液成分的改變可能參與影響豬PA囊胚基因表達。
4 結 論
本研究利用Smat-seq2單細胞全長轉錄組技術揭示了玻璃化冷凍對豬PA囊胚脂質代謝、能量代謝、MAPK信號通路等相關基因表達的影響,同時發現璃化冷凍液成分的變化參與影響豬PA囊胚的基因表達。本研究為改善豬胚胎玻璃化冷凍技術提供一定理論基礎。
參考文獻(References):
[1] DU X Z,ZHUAN Q R,CHENG K R,et al.Cryopreservation of porcine embryos:recent updates and progress[J].Biopreserv Biobank,2021,19(3):210-218.
[2] XU H X,WANG X G,TAO R X,et al.Optimal stage for cryotop vitrification of porcine embryos[J].Cell Reprogram, 2022,24(3):132-141.
[3] ALMI ANA C,DUBUISSON F,BAUERSACHS S,et al.Unveiling how vitrification affects the porcine blastocyst:clues from a transcriptomic study[J].J Anim Sci Biotechnol,2022,13(1):46.
[4] WIESAK T,GORYSZEWSKA-SZCZUREK E.Effect of vitrification on the expression of genes in porcine blastocysts derived from in vitro matured oocytes[J].Syst Biol Reprod Med,2022,68(4):239-246.
[5] CUELLO C,MARTINEZ C A,CAMBRA J M,et al.Effects of vitrification on the blastocyst gene expression profile in a porcine model[J].Int J Mol Sci,2021,22(3):1222.
[6] SANTORO F,CHIEN K R,SAHARA M.Isolation of human ESC-derived cardiac derivatives and embryonic heart cells for population and single-cell RNA-seq analysis[J].STAR Protoc,2021,2(1):100339.
[7] YANG T,YUAN X,XUE Q S,et al.Comparison of symmetrical and asymmetrical cleavage 2-cell embryos of porcine by Smart-seq2[J].Theriogenology,2023,210:221-226.
[8] FAN X Y,TANG D,LIAO Y H,et al.Single-cell RNA-seq analysis of mouse preimplantation embryos by third-generation sequencing[J].PLoS Biol,2020,18(12):e3001017.
[9] QIAO Y B,REN C,HUANG S S,et al.High-resolution annotation of the mouse preimplantation embryo transcriptome using long-read sequencing[J].Nat Commun,2020,11(1):2653.
[10] PICELLI S,FARIDANI O R,BJ RKLUND K,et al.Full-length RNA-seq from single cells using Smart-seq2[J].Nat Protoc,2014,9(1):171-181.
[11] LI Z S,LIU Y L,MA T,et al.Smart-seq2 technology reveals a novel mechanism that zearalenone inhibits the in vitro maturation of ovine oocytes by influencing TNFAIP6 expression[J].Toxins (Basel),2023,15(10):617.
[12] JIA B Y,XIANG D C,QUAN G B,et al.Transcriptome analysis of porcine immature oocytes and surrounding cumulus cells after vitrification and in vitro maturation[J].Theriogenology,2019,134:90-97.
[13] XU T T,LIU C X,ZHANG M Y,et al.Vitrification of pronuclear zygotes perturbs porcine zygotic genome activation[J].Animals (Basel),2022,12(5):610.
[14] KAJDASZ A,WARZYCH E,DEREBECKA N,et al.Lipid stores and lipid metabolism associated gene expression in porcine and bovine parthenogenetic embryos revealed by fluorescent staining and RNA-seq[J].Int J Mol Sci,2020,21(18):6488.
[15] LIPINSKA P,PAWLAK P,WARZYCH E.Species and embryo genome origin affect lipid droplets in preimplantation embryos[J].Front Cell Dev Biol,2023,11:1187832.
[16] MASEK M,ETARD C,HOFMANN C,et al.Loss of the Bardet-Biedl protein Bbs1 alters photoreceptor outer segment protein and lipid composition[J].Nat Commun,2022,13(1):1282.
[17] ROUABHI M,GUO D F,MORGAN D A,et al.BBSome ablation in SF1 neurons causes obesity without comorbidities[J].Mol Metab,2021,48:101211.
[18] YAN L,RUST B M,PALMER D G.Time-restricted feeding restores metabolic flexibility in adult mice with excess adiposity[J]. Front Nutr,2024,11:1340735.
[19] WANG Y,MCNUTT M C,BANFI S,et al.Hepatic ANGPTL3 regulates adipose tissue energy homeostasis[J].Proc Natl Acad Sci U S A,2015,112(37):11630-11635.
[20] KLID S,MAYM -MASIP E,ALGABA-CHUECA F,et al.The ANGPTL3-4-8 axis in normal gestation and in gestational diabetes,and its potential involvement in fetal growth[J].Int J Mol Sci,2023,24(3):2486.
[21] PAWLAK P,MALYSZKA N,SZCZERBAL I,et al.Fatty acid induced lipolysis influences embryo development,gene expression and lipid droplet Formation in the porcine cumulus cells[J].Biol Reprod,2020,103(1):36-48.
[22] FRAGOULI E,WELLS D.Mitochondrial DNA assessment to determine oocyte and embryo viability[J].Semin Reprod Med,2015,33(6):401-409.
[23] BARBE A,KUROWSKA P,RAME C,et al.Adipolin (C1QTNF12) is a new adipokine in female reproduction:expression and function in porcine granulosa cells[J].Reproduction,2023,167(1):e230272.
[24] OSBAK K K,COLCLOUGH K,SAINT-MARTIN C,et al.Update on mutations in glucokinase (GCK),which cause maturity-onset diabetes of the young,permanent neonatal diabetes,and hyperinsulinemic hypoglycemia[J].Hum Mutat,2009,30(11):1512-1526.
[25] ZHANG Y L,GUO L Y,HAN S,et al.Adult mesenchymal stem cell ageing interplays with depressed mitochondrial Ndufs6[J].Cell Death Dis,2020,11(12):1075.
[26] XIANG D C,JIA B Y,ZHANG B,et al.Astaxanthin supplementation improves the subsequent developmental competence of vitrified porcine zygotes[J].Front Vet Sci,2022,9:871289.
[27] LI G L,FLODBY P,LUO J,et al.Knockout mice reveal key roles for claudin 18 in alveolar barrier properties and fluid homeostasis[J].Am J Respir Cell Mol Biol,2014,51(2):210-222.
[28] SOMFAI T.Vitrification of immature oocytes in pigs[J].Anim Sci J,2024,95(1):e13943.
[29] J RGENSEN J P,LAURIDSEN A M,KRISTENSEN P,et al.Adrm1,a putative cell adhesion regulating protein,is a novel proteasome-associated factor[J].J Mol Biol,2006,360(5):1043-1052.
[30] MO X H,WU G Q,YUAN D S,et al.Leukemia inhibitory factor enhances bovine oocyte maturation and early embryo development[J].Mol Reprod Dev,2014,81(7):608-618.
[31] WANG S H,HAO J,ZHANG C,et al.KLF17 promotes human naive pluripotency through repressing MAPK3 and ZIC2[J].Sci China Life Sci,2022,65(10):1985-1997.
[32] DE SOUZA D K,SALLES L P,CAMARGO R,et al.Effects of PI3K and FSH on steroidogenesis,viability and embryo development of the cumulus-oocyte complex after in vitro culture[J].Zygote,2018,26(1):50-61.
[33] PEREZ Y,SHORER Z,LIANI-LEIBSON K,et al.SLC30A9 mutation affecting intracellular zinc homeostasis causes a novel cerebro-renal syndrome[J].Brain,2017,140(4):928-939.
[34] JEON Y,YOON J D,CAI L,et al.Effect of zinc on in vitro development of porcine embryos[J].Theriogenology,2015, 84(4):531-537.
[35] WANG J,DA C L,SU Y,et al.MKNK2 enhances chemoresistance of ovarian cancer by suppressing autophagy via miR-125b[J].Biochem Biophys Res Commun,2021,556:31-38.
[36] LYNCH A M,ZHU Y Y,LUCAS B G,et al.TES-1/Tes and ZYX-1/Zyxin protect junctional actin networks under tension during epidermal morphogenesis in the C. elegans embryo[J].Curr Biol,2022,32(23):5189-5199.e6.
[37] CAI T Y,BAI J J,TAN P,et al.Zyxin promotes hepatocellular carcinoma progression via the activation of AKT/mTOR signaling pathway[J].Oncol Res,2023,31(5):805-817.
[38] ZHANG N,YU X Q,XIE J X,et al.New insights into the role of ferritin in iron homeostasis and neurodegenerative diseases[J].Mol Neurobiol,2021,58(6):2812-2823.
[39] NING N N,SHANG Z Q,LIU Z P,et al.A novel microtubule inhibitor promotes tumor ferroptosis by attenuating SLC7A11/GPX4 signaling[J].Cell Death Discov,2023,9(1):453.
[40] CHEN S M,WU Y R,GAO Y,et al.Allosterically inhibited PFKL via prostaglandin E2 withholds glucose metabolism and ovarian cancer invasiveness[J].Cell Rep,2023,42(10):113246.
[41] PEI Y F,LV S N,SHI Y,et al.RAB21 controls autophagy and cellular energy homeostasis by regulating retromer-mediated recycling of SLC2A1/GLUT1[J].Autophagy,2023,19(4):1070-1086.
[42] QI J J,ZHANG S X,QU H X,et al.Lysine-specific demethylase 1 (LSD1) participate in porcine early embryonic development by regulating cell autophagy and apoptosis through the mTOR signaling pathway[J].Theriogenology, 2024, 224:119-133.
[43] HARA T,KIN A,AOKI S,et al.Resveratrol enhances the clearance of mitochondrial damage by vitrification and improves the development of vitrified-warmed bovine embryos[J].PLoS One,2018,13(10):e0204571.
[44] ZHEN Y,STENMARK H.Autophagosome biogenesis[J].Cells,2023,12(4):668.
[45] AFZAL A,SARFRAZ M,LI G L,et al.Taking a holistic view of PEST-containing nuclear protein (PCNP) in cancer biology[J].Cancer Med,2019,8(14):6335-6343.
[46] ZHUANG W X,ZHANG L,ZHENG Y,et al.USP3 deubiquitinates and stabilizes the adapter protein ASC to regulate inflammasome activation[J].Cell Mol Immunol,2022,19(10):1141-1152.
[47] DONG P Z,FU H,CHEN L,et al.PCNP promotes ovarian cancer progression by accelerating β-catenin nuclear accumulation and triggering EMT transition[J].J Cell Mol Med,2020,24(14):8221-8235.
[48] LI N,XIONG R,LI G R,et al.PM2.5 contributed to pulmonary epithelial senescence and ferroptosis by regulating USP3-SIRT3-P53 axis[J].Free Radical Biol Med,2023,205:291-304.
[49] KOWALCZYK A,GBADAMOSI O,KOLOR K,et al.Evolutionary rate covariation identifies SLC30A9 (ZnT9) as a mitochondrial zinc transporter[J].Biochem J,2021,478(17):3205-3220.
[50] EN A,TAKANASHI S,OKAZAKI R,et al.A mutation in SLC30A9,a zinc transporter,causes an increased sensitivity to oxidative stress in the nematode Caenorhabditis elegans[J].Biochem Biophys Res Commun,2022,634:175-181.
(編輯 郭云雁)

