信迪利單抗聯合化療治療復發性宮頸癌的臨床療效和安全性研究

【摘要】目的 探討信迪利單抗聯合化療對復發性宮頸癌患者的治療效果及腫瘤標志物、輔助性T淋巴細胞1型/輔助性T淋巴細胞2型(Th1/Th2)細胞因子的影響,并分析其安全性。方法 以隨機數字表法將茂名市人民醫院2021年4月至2023年4月收治的60例復發性宮頸癌患者分兩組,各30例。給予對照組患者常規化療方案治療(紫杉醇+順鉑),3周為1個化療周期;試驗組患者在對照組的基礎上聯合信迪利單抗治療,每3周給藥1次,3周為1個周期,兩組均持續治療2個周期。比較兩組患者治療效果,治療前后腫瘤標志物、Th1/Th2細胞因子水平,以及治療期間不良反應發生情況。結果 試驗組患者疾病控制率高于對照組;與治療前比,治療后兩組患者血清癌胚抗原(CEA)、糖鏈抗原125(CA125)、鱗狀細胞癌相關抗原(SCC-Ag)及血清白細胞介素-10(IL-10)水平均降低,白細胞介素-2(IL-2)、干擾素γ(IFN-γ)水平均升高,試驗組各項指標變化幅度均大于對照組(均P<0.05);兩組不良反應總發生率比較,差異無統計學意義(P>0.05)。結論 在化療的基礎上聯合信迪利單抗治療可明顯提高對復發性宮頸癌的治療效果,并有效下調腫瘤標志物水平,增強機體對腫瘤的免疫應答,且安全性良好。
【關鍵詞】復發性宮頸癌 ; 信迪利單抗 ; 化療 ; 腫瘤標志物 ; 免疫應答
【中圖分類號】R73 【文獻標識碼】A 【文章編號】2096-3718.2024.18.0061.03
DOI:10.3969/j.issn.2096-3718.2024.18.020
人乳頭瘤病毒(HPV)是一種雙鏈DNA病毒,可通過性接觸傳播,其中,高危型HPV,尤其是HPV16和HPV18型,與宮頸癌的發生密切相關。研究發現,遠處轉移和局部復發是宮頸癌治療失敗的主要原因[1]。針對復發性宮頸癌的治療,目前臨床上主要采取化療、放療或手術等單一或聯合治療方法。其中常規化療可通過血液循環發揮全身作用,不僅治療局部病灶,還能影響遠處轉移,對復發性宮頸癌具有較好的治療效果。然而,由于化療藥物的耐藥性和不良反應,使得這些傳統治療方法在療效和安全性上存在一定的局限性。信迪利單抗作為一種新型的免疫檢查點抑制劑,其通過阻斷腫瘤細胞表面的程序性死亡受體1(PD-1)受體與其細胞程序性死亡-配體1(PD-L1)的結合,從而恢復機體對腫瘤細胞的免疫監視和殺傷功能,達到抑制腫瘤生長和擴散的目的[2]。基于此,本研究旨在探討信迪利單抗聯合常規化療對復發性宮頸癌患者的治療效果,現報道如下。
1 資料與方法
1.1 一般資料 以隨機數字表法將茂名市人民醫院2021年4月至2023年4月收治的60例復發性宮頸癌患者分兩組,各30例。對照組患者病理類型[3]:鱗癌12例,腺癌12例,腺鱗癌6例;年齡36~61歲,平均(45.83±6.51)歲。試驗組患者病理類型:鱗癌12例,腺癌10例,腺鱗癌8例;年齡35~60歲,平均(45.64±5.37)歲。兩組一般資料比較,差異無統計學意義(P>0.05),可比。納入標準:⑴符合《宮頸癌診斷與治療指南(第四版)》 [4]中的診斷標準,并經病理學檢查明確診斷為PD-L1陽性復發性宮頸癌;⑵參照實體瘤的療效評價標準(RECIST 1.0)[5]有不少于1個可測量的病灶;⑶美國東部腫瘤協作組體力狀況量表(ECOGPS)[6]評分為0或1分;⑷預計生存期>3個月。排除標準:⑴合并其他惡性腫瘤;⑵重要臟器功能受損;⑶合并精神障礙性疾病。研究已獲得茂名市人民醫院醫學倫理委員會批準,患者及家屬均簽署知情同意書。
1.2 治療方法 給予對照組患者常規化療方案治療:第1天使用紫杉醇注射液(海南全星制藥有限公司,國藥準字H20084033,規格:16.7 mL∶100 mg)260 mg/m2+順鉑氯化鈉注射液(回音必集團江西東亞制藥有限公司,國藥準字H20084385,規格:100 mL∶順鉑0.1 g與氯化鈉0.9 g)70 mg/m2,靜脈滴注,每3周給藥1次,3周為1個化療周期。試驗組患者在對照組的基礎上聯合信迪利單抗注射液[信達生物制藥(蘇州)有限公司,國藥準字S20180016,規格:100 mg(10 mL)/瓶]靜脈輸注治療,劑量為200 mg/次,每3周給藥1次,3周為1個周期,兩組患者均持續治療2個周期。
1.3 觀察指標 ⑴治療效果。參照實體瘤的療效評價標準(RECIST 1.0)[5]對兩組患者治療效果進行評價,分為完全緩解(CR):所有靶病灶消失,且無新病灶出現;部分緩解(PR):靶病灶總直徑相對于基線直徑減少至少30%,無新病灶出現;疾病穩定(SD):靶病灶的總直徑減少不足30%或增加不足20%,且無新病灶出現;疾病進展(PD):靶病灶總直徑相對于最小記錄直徑增加至少20%,或出現新病灶。疾病控制率=[(CR+PR+SD)例數/總例數]×100%。⑵腫瘤標志物水平。于治療前后取患者空腹靜脈血5 mL,離心(3 000 r/min,10 min)取上層血清,采用電化學發光法對血清鱗狀細胞癌相關抗原(SCC-Ag)、癌胚抗原(CEA)、糖鏈抗原125(CA125)水平進行檢測。⑶細胞因子水平。血液采集和血清制備方法同⑵,應用酶聯免疫吸附法檢測血清輔助性T淋巴細胞1型/輔助性T淋巴細胞2型(Th1/Th2)細胞因子水平,包括白細胞介素-2(IL-2)、干擾素γ(IFN-γ)及白細胞介素-10(IL-10)。⑷不良反應。治療期間統計患者腎功能損傷、胃腸道反應、脫發、肝功能損傷、骨髓抑制等的發生情況。不良反應總發生率為各項不良反應發生率之和。
1.4 統計學方法 采用SPSS 26.0統計學軟件分析數據,計數資料以[例(%)]表示,組間比較采用χ2檢驗,等級資料采用秩和檢驗;計量資料經S-W法檢驗證實均符合正態分布,用( x ±s)表示,組間比較采用獨立樣本t檢驗,治療前后比較采用配對t檢驗。P<0.05為差異有統計學意義。
2 結果
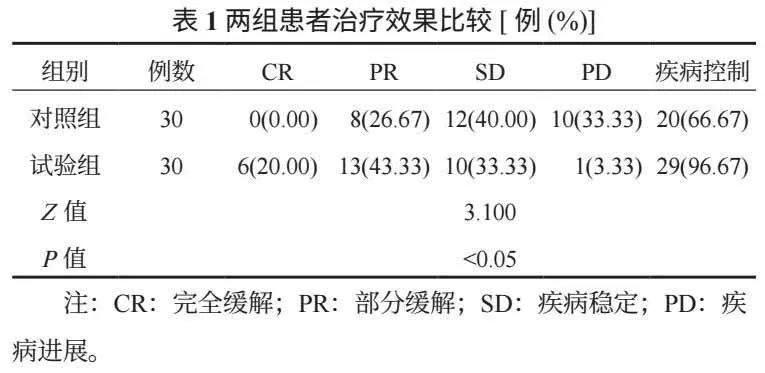
2.1 兩組患者治療效果比較 試驗組患者疾病控制率較對照組更高,差異有統計學意義(P<0.05),見表1。
2.2 兩組患者腫瘤標志物水平比較 與治療前比,治療后兩組腫瘤標志物均降低,試驗組均低于對照組,差異均有統計學意義(均P<0.05),見表2。
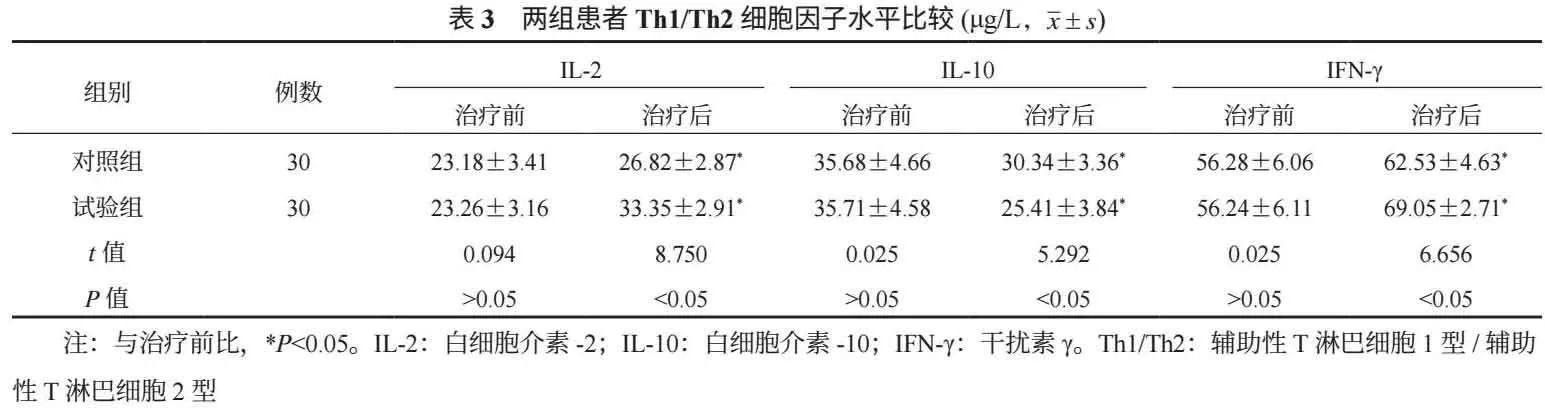
2.3 兩組患者Th1/Th2細胞因子水平比較 與治療前比,治療后兩組血清IL-2、IFN-γ均升高,血清IL-10均降低,試驗組變化幅度均大于對照組,差異均有統計學意義(均P<0.05),見表3。
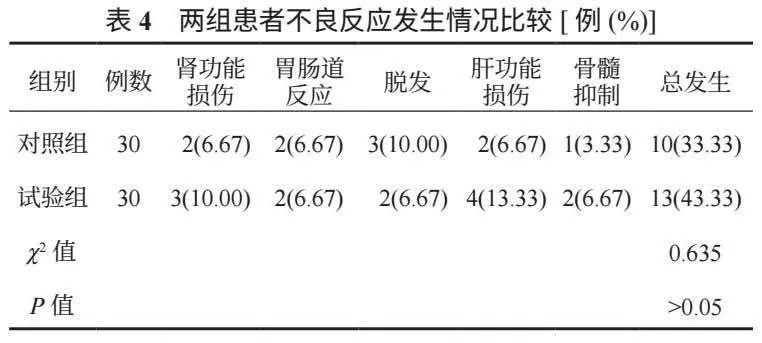
2.4 兩組患者不良反應發生情況比較 兩組不良反應總發生率比較,差異無統計學意義(P>0.05),見表4。
3 討論
紫杉醇聯合順鉑化療對復發性宮頸癌具有顯著療效,能夠縮小腫瘤體積,延長無進展生存期和總體生存期。其中紫杉醇通過干擾癌細胞的微管組裝,順鉑通過與DNA結合阻礙細胞分裂,兩者可發揮協同作用。然而,該化療方案也伴隨一定的不良反應,如骨髓抑制和神經毒性,需根據患者具體情況調整劑量并進行支持治療。
信迪利單抗是一種經過生物工程技術制備的全人源免疫球蛋白G4型(IgG4型)PD-1單克隆抗體,通過阻斷有效PD-1/PD-L1信號通路,解除腫瘤細胞對免疫細胞的抑制作用,使得免疫細胞能夠重新識別并攻擊腫瘤細胞;化療藥物則通過直接殺死腫瘤細胞或干擾腫瘤細胞的生長周期來發揮治療作用;兩者聯用,既能夠增強治療效果,又不增加化療藥物的不良反應[8-9]。本研究中,試驗組患者疾病控制率高于對照組;不良反應總發生率高于對照組,但差異無統計學意義,這提示信迪利單抗聯合化療對復發性宮頸癌患者的治療效果更佳,且安全性良好。
SCC-Ag和CEA在復發性宮頸癌的治療中具有重要作用。SCC-Ag通過輔助診斷、預后評估、治療監測及復發檢測,幫助醫師及時掌握病情變化;CEA雖然主要用于消化道腫瘤,但在復發性宮頸癌中也能輔助診斷、預后評估及監測治療效果。定期檢測這兩種腫瘤標志物的水平及時發現復發,為治療方案的調整提供重要依據。通過對比觀察兩組血清腫瘤標志物的變化情況發現,治療后試驗組腫瘤標志物均低于對照組,這提示在化療的基礎上聯合信迪利單抗治療可明顯降低復發性宮頸癌患者血清腫瘤標志物水平。分析其原因在于,信迪利單抗能夠與腫瘤細胞表面的特定抗原結合,形成抗原 - 抗體復合物,這些復合物可以激活免疫細胞,如自然殺傷細胞(NK)細胞和巨噬細胞,通過釋放細胞毒素和產生細胞因子來直接殺傷腫瘤細胞。此外,信迪利單抗還可以通過抗體依賴性細胞毒性(ADCC)的機制,促使免疫細胞對腫瘤細胞進行殺傷,這種直接的殺傷作用能夠減少腫瘤細胞的數量,從而降低腫瘤標志物水平[9]。
Th1/Th2細胞因子在宮頸癌患者體內存在明顯的失衡。其中,IL-2通過促進Th1細胞的增殖和活化,增強細胞介導的免疫反應,維持Th1/Th2的平衡;而IL-10通過抑制Th1細胞反應和促進Th2細胞反應,可能會導致Th1/Th2失衡。IFN-γ則主要由活化的T淋巴細胞和自然殺傷細胞產生,是一種強有力的免疫調節因子,能夠促進Th1型免疫應答,增強機體對癌細胞的殺傷能力[10]。通過對比觀察兩組Th1/Th2 變化情況發現,試驗組患者血清IL-10低于對照組,血清IL-2、IFN-γ均高于對照組,這提示在化療的基礎上聯合信迪利單抗治療可明顯增強復發性宮頸癌患者機體對腫瘤的免疫應答。這可能是因為,信迪利單抗通過其高度特異性的抗原 - 抗體結合,有效抑制了PD-1與PDL-1的相互作用。這種阻斷不僅解除了PD-1對T細胞活性的抑制,而且促進了T細胞的活化與增殖,活化的T淋巴細胞,特別是CD8+細胞毒性T淋巴細胞,能夠更有效地識別并攻擊腫瘤細胞,從而大大增強了機體對腫瘤的免疫應答[11]。
綜上,在化療的基礎上聯合信迪利單抗治療可明顯提高對復發性宮頸癌的治療效果,并有效下調腫瘤標志物水平,增強機體對腫瘤的免疫應答,且安全性良好。但本研究樣本量較小,且未進行長期隨訪,結論可能存在一定局限性,后期需擴大樣本量,進行遠期觀察深入研究。
參考文獻
李英, 程忠平. 復發性宮頸癌免疫治療的研究進展[J]. 中國婦產科臨床雜志, 2023, 24(1): 108-110.
朱丹, 李月陽, 宋燕青, 等. PD-1抑制劑信迪利單抗的臨床研究進展[J]. 中國醫院藥學雜志, 2020, 40(1): 120-123.
曹姬, 鄭貴星, 馬海丹, 等. 共刺激分子PD-L1、PD-L2和B7-H4在宮頸癌的表達及臨床病理特征分析[J]. 寧夏醫科大學學報, 2014, 36(1): 68-70, 125.
周琦, 吳小華, 繼紅, 等. 宮頸癌診斷與治療指南(第四版)[J]. 中國實用婦科與產科雜志, 2018, 34(6): 613-622.
NISHINO M, JAGANNATHAN J P, RAMAIYA N H, ea al. Revised RECIST guideline version 1.1: What oncologists want to know and what radiologists need to know[J]. AJR Am J Roentgenol, 2010, 195(2): 281-289.
NEEMAN E, GRESHAM G, OVASAPIANS N, et al. Comparing physician and nurse eastern cooperative oncology group performance status (ECOG-PS) ratings as predictors of clinical outcomes in patients with cancer[J]. Oncologist, 2019, 24(12): e1460-e1466.
馮成軍, 張日光, 韋蒙專. 信迪利單抗聯合同步放化療對晚期宮頸癌患者腫瘤標志物及程序性死亡受體-1/程序性死亡配體1的影響[J]. 中華實用診斷與治療雜志, 2022, 36(7): 740-743.
胡柏帆. 信迪利單抗聯合長春瑞濱治療復發轉移性宮頸癌的療效觀察[J]. 西藏醫藥, 2023, 44(2): 91-93.
劉超霞, 冉曉敏, 張克強, 等. 淋巴結轉移的局部晚期宮頸癌行PD-1抑制劑聯合同步放化療的療效及安全性研究[J]. 中國腫瘤臨床, 2023, 50(8): 418-422.
張要盛, 楊秀麗, 任曉. 信迪利單抗聯合卡鉑全身化療用于宮頸癌復發轉移患者的效果[J]. 中國民康醫學, 2023, 35(18): 68-70, 74.
李靜, 孔為民. 晚期復發性宮頸癌靶向治療和免疫治療進展[J]. 中國計劃生育和婦產科, 2021, 13(6): 19-23.
作者簡介:唐雙鳳,大學本科,主治醫師,研究方向:腫瘤科。

