對比培門冬酶與門冬酰胺酶對急性淋巴細胞白血病化療患兒血液指標的影響

【摘要】目的 探討采用培門冬酶與門冬酰胺酶治療急性淋巴細胞白血病對患兒凝血功能及炎癥因子水平的影響,為臨床治療該疾病提供參考依據。方法 回顧性分析北京高博博仁醫院2022年1月至2023年10月收治的急性淋巴細胞白血病患兒131例的臨床資料,按照治療方法不同將其分為兩組,A組[66例,化療聯合門冬酰胺酶治療]和B組(65例,化療聯合培門冬酶治療)。28 d為1個療程,兩組患兒均治療1個療程。比較兩組患兒治療后臨床療效,治療前后凝血功能、炎癥因子水平,以及治療期間不良反應發生情況。結果 與治療前比,治療后兩組患兒凝血酶原時間(PT)、活化部分凝血活酶時間(APTT)水平均延長,且B組均長于A組;纖維蛋白原(FIB)及血清鐵蛋白(SF)、超敏-C反應蛋白(hs-CRP)、白細胞介素-6(IL-6)水平均降低,且B組均低于A組;B組患兒過敏、血糖升高發生率低于A組(均P<0.05);兩組患兒治療后臨床療效、肝損害、胰腺炎、胃腸道反應發生率比較,差異無統計學意義(P>0.05)。結論 與化療聯合門冬酰胺酶的治療方案相比,急性淋巴細胞白血病患兒采用化療聯合培門冬酶治療的臨床療效相當,但其可有效降低血清炎癥因子水平,且安全性良好,但應注意可能導致凝血功能障礙,臨床治療過程中應密切監測患兒凝血功能。
【關鍵詞】急性淋巴細胞白血病 ; 門冬酰胺酶 ; 培門冬酶 ; 凝血功能 ; 炎癥因子
【中圖分類號】R733.71 【文獻標識碼】A 【文章編號】2096-3718.2024.18.0095.03
DOI:10.3969/j.issn.2096-3718.2024.18.031
急性淋巴細胞白血病是一種常見的急性白血病類型,主要特征是骨髓中異常淋巴細胞的大量增殖和正常造血功能的抑制,患兒常表現為貧血、出血、發熱、肝脾及淋巴結腫大、骨關節疼痛和頭痛等,其發病原因與生物因素、物理因素、化學因素、遺傳因素等均有一定關系。門冬酰胺酶是一種提取自歐文菌屬的酶制劑類抗腫瘤藥物,其作為急性淋巴細胞白血病治療領域的主要藥物,通過促進門冬酰胺酶的水解作用,可以使腫瘤細胞蛋白質合成障礙,增殖受到抑制,也可干擾脫氧核苷酸(DNA)和核糖核苷酸(RNA)的合成[1]。然而,在臨床應用中,為確保治療效果的持續性,需要反復且持續地進行注射治療,一旦中斷治療,患兒將面臨較高的疾病復發風險,這在一定程度上限制了該藥物在實際應用中的廣泛性和長期治療效果。培門冬酶是一種新型長效門冬酰胺酶類抗腫瘤藥物,屬于人工合成的酶類,可以選擇性消耗血漿中的門冬酰胺酶,而白血病細胞自身無法合成門冬酰胺,因此,這一過程影響了蛋白質的合成,從而能夠殺滅白血病細胞,最終促使白血病細胞凋亡,以達到治療目的,由于正常細胞能夠合成門冬酰胺酶,因此對正常細胞影響較小[2]。基于此,本研究旨在探究培門冬酶與門冬酰胺酶兩種藥物對急性淋巴細胞白血病患兒的血液指標的影響,現報道如下。
1 資料與方法
1.1 一般資料 回顧性分析北京高博博仁醫院2022年1月至2023年10月收治的急性淋巴細胞白血病患兒131例的臨床資料,按照治療方法不同將其分為兩組,A組(66例)和B組(65例)。A組(66例)中男性患兒38例,女性患兒28例;年齡5~13歲,平均(9.01±0.92)歲;危險度分層[3]:低危26例,中危30例,高危10例。B組(65例)中男性患兒39例,女性患兒26例;年齡4~13歲,平均(8.98±1.01)歲;危險度分層:低危23例,中危34例,高危8例。兩組患兒一般資料比較,差異無統計學意義(P>0.05),組間可比。納入標準:⑴符合《中國慢性淋巴細胞白血病/小淋巴細胞淋巴瘤的診斷與治療指南(2018年版)》 [4]中急性淋巴細胞白血病的診斷標準;⑵首次確診;⑶可耐受化療。排除標準:⑴合并其他嚴重基礎疾病;⑵合并先天性精神疾病;⑶有其他抗腫瘤治療史。本研究經北京高博博仁醫院醫學倫理委員會審核批準。
1.2 治療方法 兩組患兒均進行常規化療治療,:注射用硫酸長春新堿(廣州白云山制藥有限公司,國藥準字H44022399,規格:1 mg/支)于治療開始后第7、14、21、28天(共4次)靜脈滴注,用藥劑量:1.5 mg/(m2·d),最大劑量不得超過2.0 mg/(m2·d);注射用鹽酸柔紅霉素(瀚暉制藥有限公司,國藥準字H33020925,規格:20 mg/支)于治療開始后第8、15天(共2次)靜脈滴注,用藥劑量:25 mg/(m2·d);口服醋酸潑尼松片(天津力生制藥股份有限公司,國藥準字H12020123,規格:5 mg/片)60 mg/(m2·d),連續用藥21 d后減停。A組患兒聯合門冬酰胺酶進行治療,于治療開始后第19~28天采用注射用門冬酰胺酶(廣州白云山制藥有限公司,國藥準字H19993914,規格:10 000 U/支)肌肉注射進行治療,5 000 U/(m2·d)。B組患兒聯合培門冬酶進行治療,于治療開始后第9、23天肌肉注射培門冬酶注射液(江蘇恒瑞醫藥股份有限公司,國藥準字H20090015,規格:5 mL∶3 750 IU),用藥劑量:2 500 IU/(m2·d)。28 d為1個療程,兩組患兒均治療1個療程。
1.3 觀察指標 ⑴臨床療效。于治療后評估兩組患兒臨床療效,治療后貧血、感染、出血等相關臨床癥狀消失,且血紅蛋白恢復至≥90 g/L為完全緩解;治療后貧血、感染、出血等相關臨床癥狀改善明顯,70g/L<血紅蛋白含量<90 g/L為部分緩解;治療后貧血、感染、出血等相關臨床癥狀無改善甚至加重,血紅蛋白含量≤70 g/L為無效[4]。總有效率=完全緩解率+部分緩解率。⑵凝血功能。分別于治療前后采集兩組患兒空腹靜脈血3 mL,抗凝處理后,采用全自動凝血分析儀(希森美康株式會社,型號:CS-5100)檢測凝血酶原時間(PT)、活化部分凝血活酶時間(APTT)、纖維蛋白原(FIB)水平。⑶血清學指標。分別于治療前后采集兩組患兒空腹靜脈血5 mL,離心處理(3 000 r/min,10 min),取上層血清,采用全自動免疫分析儀(美國雅培公司,型號:ARCHITECT i 1 000 sr)檢測鐵蛋白(SF)、超敏-C反應蛋白(hs-CRP)、白細胞介素-6(IL-6)水平。⑷不良反應。觀察統計治療期間兩組患兒過敏、肝損害、胰腺炎、血糖升高、胃腸道反應的發生情況。不良反應總發生率等于各項不良反應發生率之和。
1.4 統計學方法 采用SPSS 22.0統計學軟件分析數據,計數資料以[例(%)]表示,采用χ2檢驗,等級資料采用秩和檢驗;計量資料經S-W法檢驗證實符合正態分布,以( x ±s)表示,組間比較采用獨立樣本t檢驗,治療前后比較采用配對t檢驗。P<0.05為差異有統計學意義。
2 結果
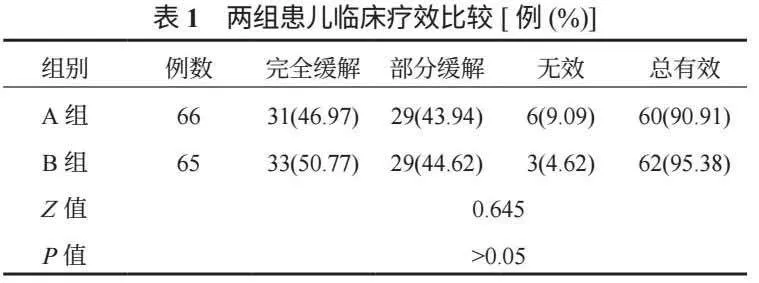
2.1 兩組患兒臨床療效比較 兩組患兒治療后臨床療效比較,差異無統計學意義(P>0.05),見表1。
2.2 兩組患兒凝血功能比較 與治療前比,治療后兩組患兒PT、APPT水平均延長,且B組均長于A組,FIB水平均降低,且B組低于A組,差異均有統計學意義(均P<0.05),見表2。
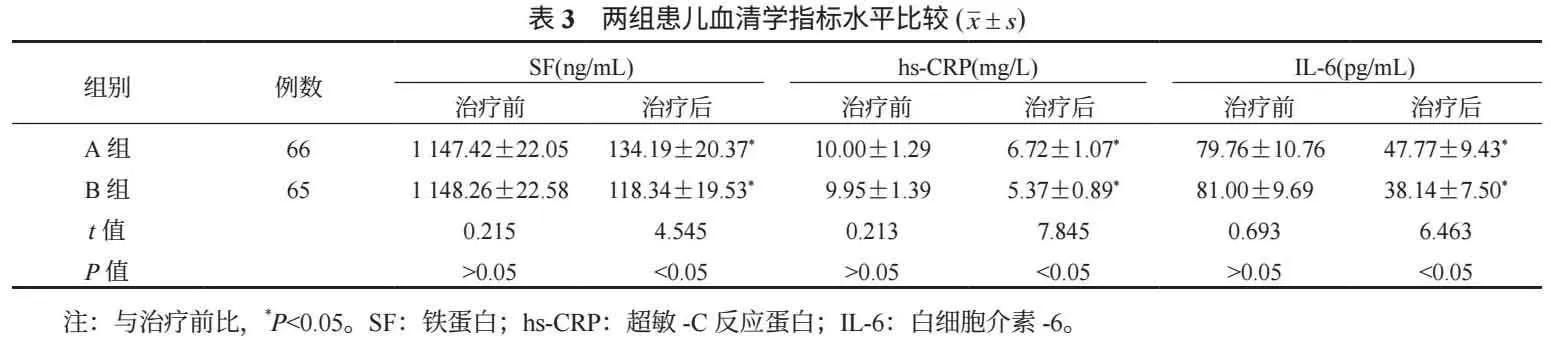
2.3 兩組患兒炎癥因子比較 與治療前比,治療后兩組患兒血清SF、hs-CRP、IL-6水平均降低,且B組均低于A組,差異均有統計學意義(均P<0.05),見表3。
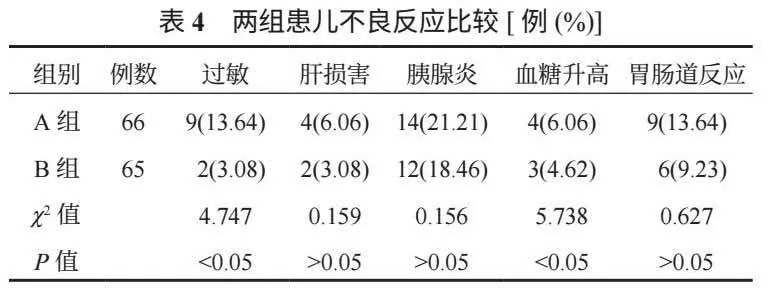
2.4 兩組患兒不良反應比較 B組患兒過敏、血糖升高發生率低于A組,差異均有統計學意義(均P<0.05);兩組患兒肝損害、胰腺炎、胃腸道反應發生率比較,差異均無統計學意義(均P>0.05),見表4。
3 討論
門冬酰胺是蛋白質合成的重要氨基酸之一,人體正常細胞能夠自行合成門冬酰胺,滿足細胞蛋白質合成需要,而腫瘤細胞因缺乏門冬酰胺合成酶,自身并無法合成生長必需的門冬酰胺,主要依賴于宿主供給;門冬酰胺酶為取自歐文菌的酶制劑類抗腫瘤藥物,可抑制腫瘤細胞中蛋白質的合成和增殖,并干擾DNA與RNA的合成,其藥物療效已得到了臨床廣泛認可,但由于其高度的免疫原性,在治療過程中易引發超敏反應,在影響治療效果的同時亦會影響藥物的再次使用[5]。培門冬酶為門冬酰胺酶與聚乙二醇5 000的軛合物,其能夠降解血清中天門冬酰胺,消耗血液中門冬酰胺,使腫瘤細胞缺乏合成蛋白質的必要氨基酸,以阻礙蛋白質合成,抑制腫瘤細胞增殖,而正常組織細胞自身具有合成門冬酰胺能力,并不會受到藥物影響[6]。
本研究結果顯示,治療后B組患兒PT、APPT水平均較A組延長,FIB水平較A組低,兩組患兒臨床療效比較,差異無統計學意義,這表明兩種藥物用于急性淋巴細胞白血病患兒的臨床治療均具有理想療效,但采用化療聯合培門冬酶治療急性淋巴細胞白血病對凝血功能影響較大。分析其原因可能是,培門冬酶可抑制急性白血病患者蛋白質的合成,使腫瘤細胞的增殖受到抑制,且培門冬酶通過消耗機體門冬酰胺,影響了蛋白質的合成,而蛋白質合成異常時,可導致凝血因子和抗凝血因子的合成減少或功能異常,從而影響凝血功能的平衡[7]。在臨床中使用該藥物時,應定期監測患兒凝血功能,及時進行對應的治療。
SF主要存在于骨髓中,在骨髓內前體B或T淋巴細胞克隆增殖中發揮重要作用;急性淋巴細胞白血病作為造血干細胞的惡性克隆性疾病,由于造血干細胞分化受阻、增殖失控、凋亡受阻等機制在骨髓中大量增殖,同時會分泌造血負調控因子,導致白細胞、紅細胞等全血細胞減少,引起炎癥反應[8-9]。本研究結果顯示,治療后B組患兒血清SF、hs-CRP、IL-6水平及過敏、血糖升高發生率均低于A組,這提示急性淋巴細胞白血病患兒以培門冬酶治療能夠有效改善炎癥反應,安全性較高。分析其原因可能是,培門冬酶通過與多聚乙二醇化合物結合,延長了其半衰期,從而使藥物在體內停留時間更長,且可抵抗疾病及化療所引起的炎癥因子,進而減輕炎癥反應;還可使藥物到達腫瘤組織前保持脂質形態,減少了蛋白質酶解及腎臟排泄,使其能夠進一步加強白血病細胞增殖抑制,達到殺滅腫瘤細胞的效果;且因腫瘤細胞對門冬酰胺的依賴性,正常機體內細胞能夠自行合成門冬酰胺,因此對正常機體的影響較小,減少化療藥物對正常細胞損傷,安全性較高[10]。
綜上,與化療聯合門冬酰胺酶的治療方案相比,急性淋巴細胞白血病患兒采用化療聯合門冬酰胺酶治療的臨床療效相當,但其可有效降低血清炎癥因子水平,且安全性良好,但應注意可能導致凝血功能障礙,臨床治療過程中應密切監測患兒凝血功能。
參考文獻
溫大科, 徐旭, 張琳. 左旋門冬酰胺酶、培門冬酶對急性淋巴細胞白血病患兒的治療效果比較[J]. 中國婦幼健康研究, 2024, 35(4): 67-73.
郝杰, 楚小鴿, 李超, 等. 培門冬酶治療成人Ph/BCR-ABL1陰性急性淋巴細胞白血病藥物活性與療效[J]. 內科理論與實踐, 2019, 14(6): 355-360.
侯芳, 李志瑤, 劉瀚翔, 等. 急性淋巴細胞白血病患兒血清PGRN、XCL1與危險度分層和預后的關系[J]. 現代生物醫學進展, 2023(23): 4537-4541.
中華醫學會血液學分會白血病淋巴瘤學組, 中國抗癌協會血液腫瘤專業委員會, 中國慢性淋巴細胞白血病工作組.中國慢性淋巴細胞白血病/小淋巴細胞淋巴瘤的診斷與治療指南(2018年版)[J]. 中華血液學雜志, 2018, 39(5): 353-358.
梁石明, 文飛球. 培門冬酶靜默失活在兒童急性淋巴細胞白血病治療中的新進展[J]. 國際輸血及血液學雜志, 2020, 43(5): 418-422.
趙學勤, 王政委, 莊艷, 等. 左旋門冬酰胺酶及培門冬酶治療小兒急性淋巴細胞白血病的療效及實驗室指標比較[J]. 兒科藥學雜志, 2020, 26(10): 17-20.
李敖龍, 王鐵鋒, 張琪. VDPAP方案對急性淋巴細胞白血病患兒凝血功能及血常規指標的影響[J]. 癌癥進展, 2023, 21(19): 2193-2196, 2200.
侯小瑞, 靳瑞霞, 謝意茹, 等. 培門冬酶對急性淋巴細胞白血病患兒的治療效果及對凝血功能的影響[J]. 癌癥進展, 2020, 18(17): 1813-1816, 1835.
陳娜, 宋春蘭, 景鈺, 等. 兩種門冬酰胺酶治療兒童急性淋巴細胞白血病的近期效果及對患兒血清LDH、SF和ESR的影響[J]. 實用癌癥雜志, 2021, 36(2): 337-340.
王長爽. 培門冬酶與左旋門冬酰胺酶治療兒童急性淋巴細胞白血病的療效及安全性觀察[J]. 中國藥物與臨床, 2021, 21(23): 3871-3873.
作者簡介:呂長俊,大學本科,主管技師,研究方向:血液檢測。

