高錳酸鉀滴定法測定維生素C含量的方法改進



本期點評專家
張永強" 正高級教師,特級教師,湖南省十佳科技教師。科普中國2021年度十大科普人物獎獲得者,全國校園發明創意大賽、湖南省青少年科技創新大賽、湖南省創新編程與智能設計大賽、湖南省科學調查體驗活動評審專家組成員。
一、探究背景
人體所需的維生素C主要來源于水果、蔬菜等食品。測定各類食品中的維生素C含量對食品營養價值的評估具有積極意義。
受實驗條件所限,我采用高錳酸鉀滴定法對食品中的維生素C含量進行測定。用這種方法測定時,高錳酸鉀的反應產物是無色的二價錳離子,此時可以高錳酸鉀原本的顏色作為滴定終點,在觀察到淡紅色出現后停止滴定。
高錳酸鉀是化學實驗中常見的氧化劑,獲取方便,價格低廉。有研究者提出,溶液的適宜酸度應為0.5~0.6 mol/L,若酸度太低,維生素C易氧化分解,且高錳酸鉀的還原產物為褐色的水合二氧化錳沉淀。但酸化需要濃度較高的硫酸,日常難以獲取。如果用市售硫酸標準溶液,酸化50 mL試樣至0.5 mol/L的氫離子濃度至少需要2.5 L硫酸標準溶液,這顯然是不切實際的。
在操作中我發現,如果不用酸化溶液,并不會立即生成棕色的二氧化錳,而是在反應掉一定量的高錳酸鉀后,才可以觀察到棕色的二氧化錳。
所以,我進行了一個補充實驗。向適量高錳酸鉀溶液(0.020 0 mol/L)中滴入數滴維生素C飽和溶液,溶液變為無色,且出現大量褐色絮狀沉淀——溶液酸度過低,導致維生素C與高錳酸鉀反應生成水合二氧化錳沉淀。然后加入過量的維生素C溶液,可觀察到沉淀溶解,溶液變澄清。這說明,水合二氧化錳與維生素C溶液發生了反應。
補充實驗證明,在滴定時,維生素C能提供反應所需的氫離子,這樣就可以在不對溶液進行酸化處理后直接滴定,再計算得到維生素C的值。在實驗過程中,可使用pH計控制溶液的酸度,避免二氧化錳生成。
也就是說,這一方法摒棄了傳統的利用高錳酸鉀自身顏色指示滴定終點的方法。
二、探究過程
(一)實驗準備
高錳酸鉀標準溶液(0.020 0 mol/L)、維生素C溶液(自配)、pH計。試劑均為分析純。
(二)提出假設
通過查找資料了解到,維生素C具有連二烯醇的結構,可定量還原高錳酸鉀,其在水溶液中會電離反應所需的氫離子——這也是不酸化溶液時,維生素C仍能與高錳酸鉀反應的基礎。
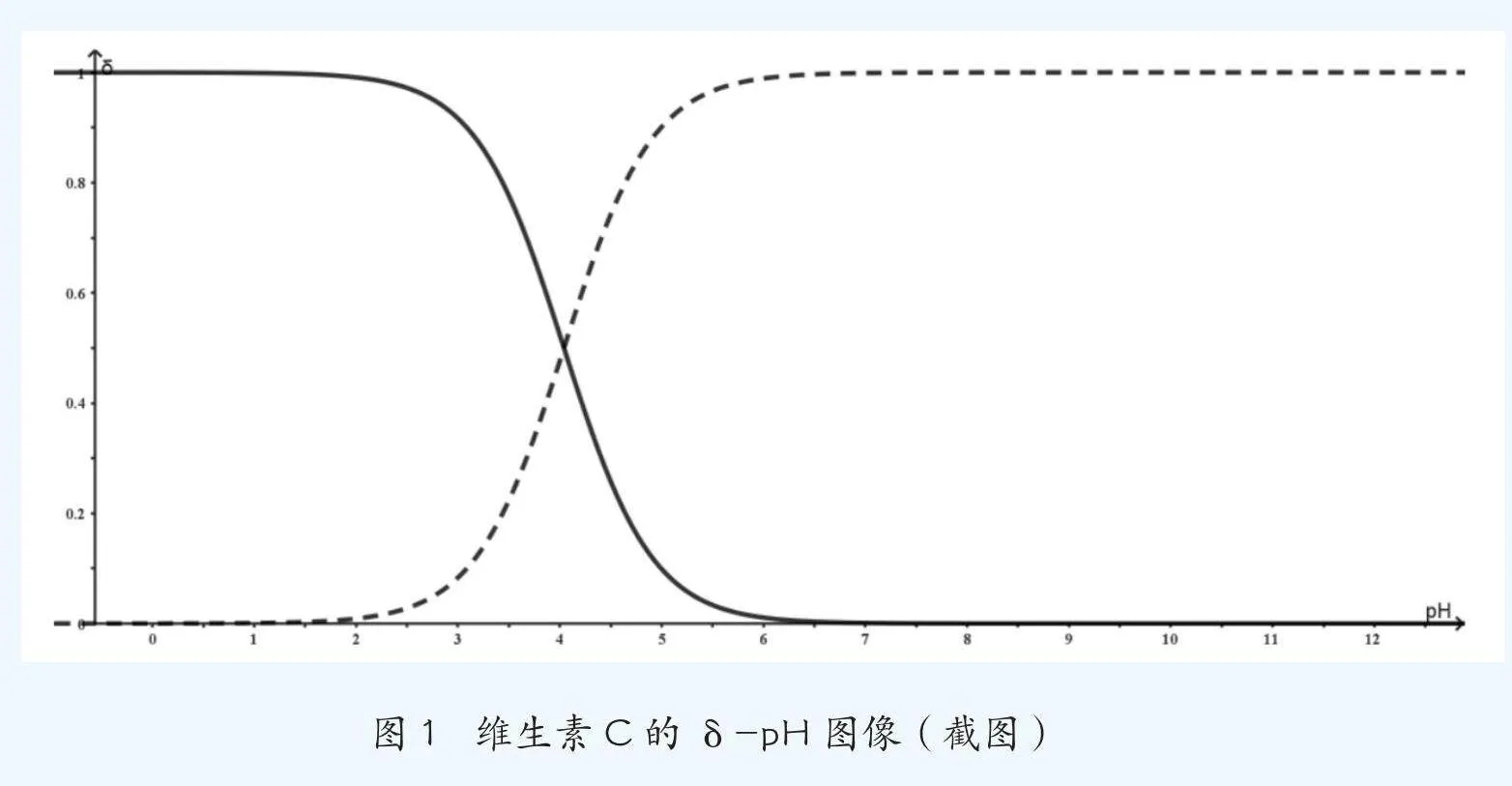
根據維生素C的電離平衡常數Ka,可計算出一定酸度溶液中維生素C的分布系數δ的值,繼而計算出在一定濃度和體積的維生素C溶液中C6H8O6和H+兩種型體的量。根據分布系數計算式計算出維生素C的δ-pH圖像。
從圖像中可以看出,在一般滴定維生素C的方法中,將pH值控制在0.1左右的原因有兩個:一是讓溶液保持酸性,盡可能使高錳酸鉀保持較強的氧化性,避免生成二氧化錳;二是通過控制使C6H8O6型體占比盡可能大,避免在溶液中生成無法進行定量反應分析的C6H6O6。但如果沒有對溶液進行酸化處理,就要考慮以上兩點對溶液的影響,并在計算時引入更多參數來消除這些影響。這會導致計算過程更復雜。
通過推導得出當以一定pH值作為滴定終點時的維生素C含量計算公式,并使用pH計測量溶液滴定結束時的pH值,通過pH值計算溶液中的氫離子濃度。這樣就能在不酸化溶液的情況下,測量滴定結束時溶液的pH值,通過計算得到溶液中維生素C的量。
(三)實驗驗證
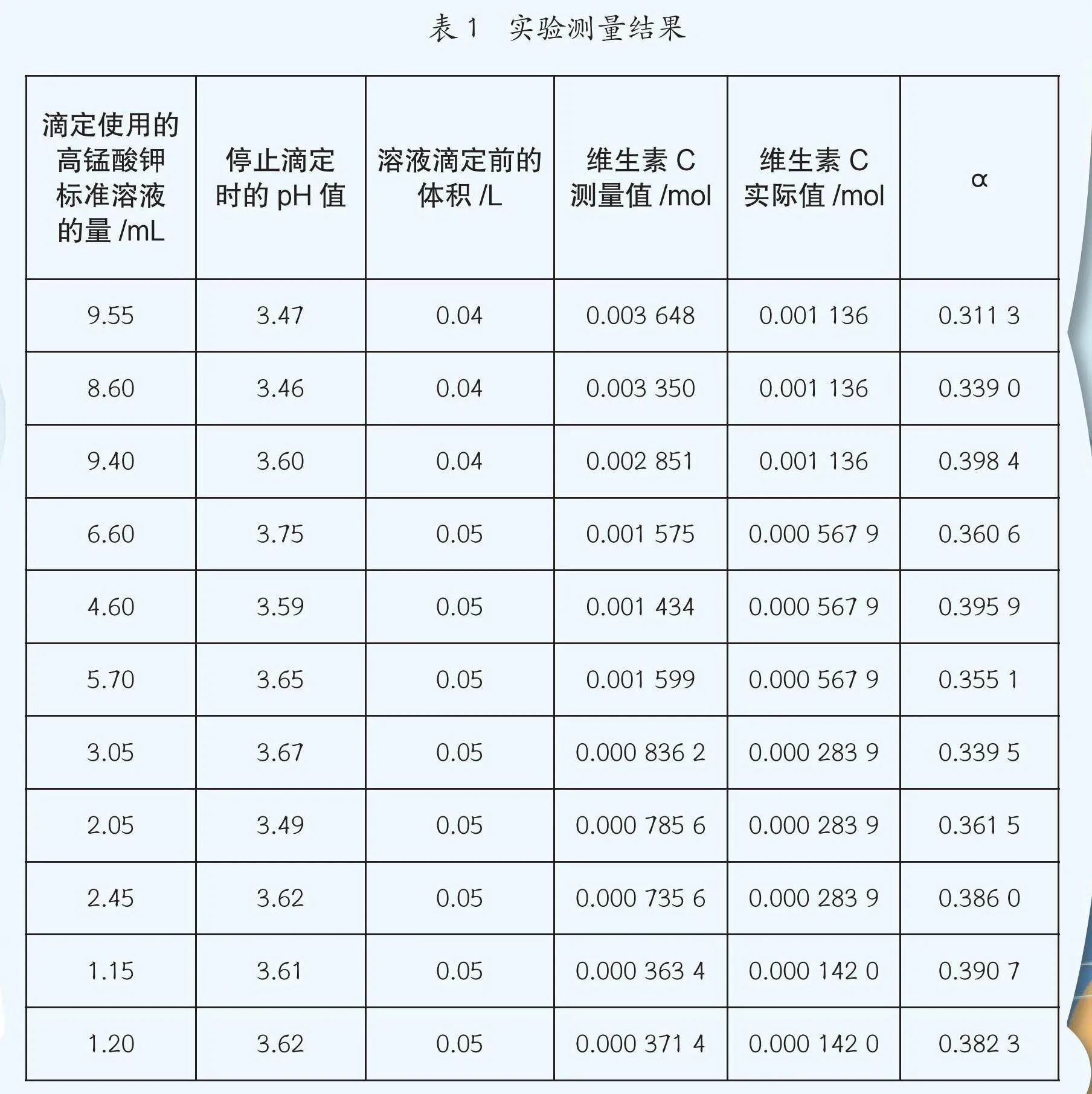
配制濃度為0.05 mol/L的維生素C溶液,準確量取5 mL,加入蒸餾水稀釋至40 mL,待滴定溶液中維生素C的含量為2.25×10-4mol。使用高錳酸鉀標準溶液(0.020 0 mol/L)進行滴定,并測量溶液反應時的pH值。重復3次,滴定結束后,取副反應系數α=1,整理分析數據。實驗結果符合預測——溶液pH值隨高錳酸鉀溶液的增加逐漸增大;當pH值大于7之后開始生成棕色沉淀,且pH值變化出現類似于酸堿中和滴定的pH突躍。這說明,滴定反應消耗了待測物的氫離子,這也間接地證明了我的假設。
改變維生素C溶液濃度,在pH值為3.4至3.7時停止滴定,再進行重復實驗,得到以下數據。
經過大量實驗,得到當pH值為3.4至3.7時,副反應系數α的最佳擬合函數為α=0.253+0.024·ln" " " " " " " " " "。
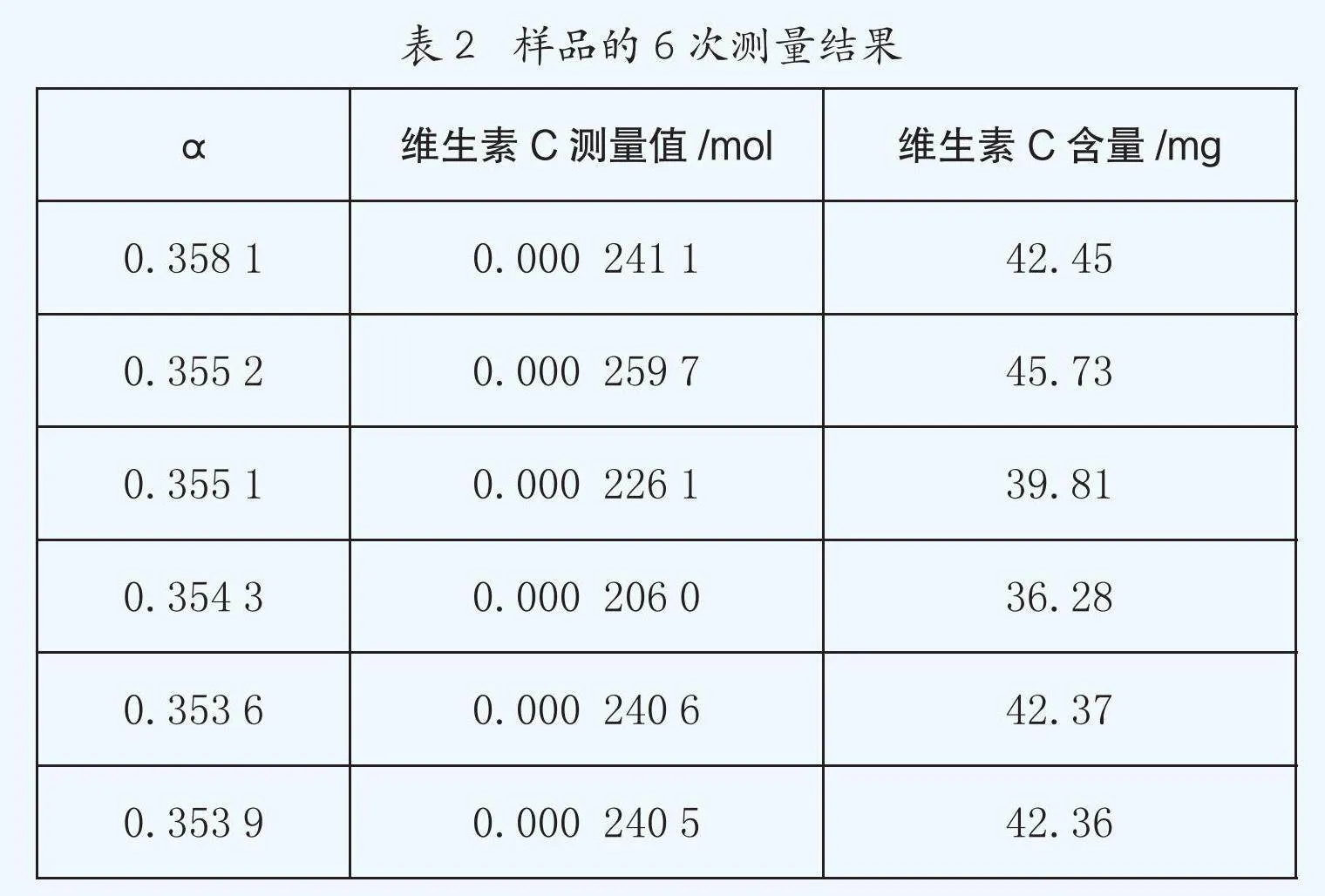
利用統計學方法檢驗改進后的方法。配制標準樣品,準確稱取1.0 g維生素C,溶解于200 mL蒸餾水中,得到濃度為0.028 39 mol/L的維生素C溶液,取8 mL試樣,用蒸餾水稀釋至50 mL,其中的維生素C含量應為2.271×10-4mol,即39.99 mg。依上述方法測量其中的維生素C含量,重復6次,得到以下數據。
根據計算結果,在顯著性水平為99%下,平均值和標準值間無顯著性差異,新方法的相對標準偏差為7.65%,說明其重復性較好,精密度較理想。
有了這個新方法,就可在不酸化溶液的前提下,利用pH計控制滴定時溶液的酸度,得到待測樣品中相對準確的維生素C的含量。除了計算量稍大之外,該方法簡易可行,減少了實驗所需試劑的種類,可作為一種快速測定維生素C含量的方法。
由于條件有限,我只能用維生素C純品配制標準樣品進行實驗,沒有進行實際應用檢驗和比較。在實際應用中,還應考慮金屬離子對維生素C分解的影響等。可采用其他方式對待測試樣進行預處理,對該方法進一步優化。
專家點評
作者提出一種改進的高錳酸鉀滴定法測定維生素C含量的新方法,即在不酸化溶液的條件下,通過控制pH值進行滴定,避免了傳統方法中需要大量酸化劑的不足,降低了實驗成本和復雜度,因而本實驗具有一定的創新性。
作者從化學反應原理出發,詳解二氧化錳與維生素C的反應機制,并通過電化學半電池反應式進行了理論推導,使得新方法有理有據。設計多個實驗驗證新方法的可行性和準確性,證明了新方法在顯著性水平下與標準值無顯著性差異,且方法的重復性和精密度良好。
建議適當增加實驗細節描述如具體操作步驟、溶液配制方法等,以便讀者能更好地復現實驗過程;加強實際應用驗證,驗證新方法在復雜基質中的準確性和適用性;加強拓展,在文末增加對新方法局限性的討論和未來研究方向的展望。
(欄目編輯" 秦銀銀)

