乳腺癌內分泌治療耐藥機制探討
程少萍 韋 偉
北京大學深圳醫院乳腺外科, 廣東 深圳 518036
乳腺癌內分泌治療耐藥機制探討
程少萍 韋 偉
北京大學深圳醫院乳腺外科, 廣東 深圳 518036
乳腺腫瘤;藥物療法;雌激素拮抗劑;芳香酶/拮抗劑和抑制劑;耐藥性
*通訊作者:韋偉
乳腺癌內分泌治療(ednocrine therapy,ET)在臨床面臨的主要問題是原、繼發性耐藥。即使雌激素受體(estrogen recep tor,ER)和孕激素受體(progestogen receptor,PR)均為陽性,也只有70%左右的患者治療有效。即約有30%的受體陽性患者存在內分泌治療原發耐藥,并且幾乎所有初治有效的患者在應用ET藥物一段時間后會出現治療無效,即繼發耐藥。有關ET治療耐藥機制及逆轉的研究已成為臨床亟待解決的主要問題。
根據對ER的依賴性,乳腺癌內分泌耐藥機制分為ER依賴的內分泌耐藥機制及ER非依賴的內分泌耐藥機制,下面將從此兩方面對乳腺癌內分泌治療耐藥機制進行綜述。
1 ER依賴機制
ER與生長因子GF(Growth Factor)通路串話調節機制。
ER通路乳腺癌細胞生長機制為:雌激素通過與ER作用促進乳腺癌細胞生長。ER分為核受體和膜受體兩種,其中核受體是起主要作用的轉錄因子。核受體的經典作用模式為配體E與核受體ER的配體結合區(1igand binding domain,LBD)結合,促使其與另一分子的ER形成二聚體,ER的DNA結合區(DNA binding domain,DBD)與靶基因上的E反應元件(estrogen response element,ERE)結合,啟動轉錄。ER受體特異性的協同活化因子和協同抑制因子傳達一系列的正/負信號調節其轉錄活性。核受體的非經典作用模式為ER與轉錄因子Fos和Jun結合,激活靶基因啟動子區的AP-1(activating protein-I,AP-1)位點,啟動轉錄。ER膜受體還可以與膜表面周圍的多種信號轉導相關的生長因子及激酶相作用,快速誘導細胞內激酶(如p42/44MAPK和3-磷酸肌醇激酶)產生,促進腫瘤生長。
選擇性雌激素受體調節劑(selective estrogen receptor modulators,SERM s)類ET藥物是重要的乳腺癌內分泌治療藥物,其和雌激素競爭性與ER的LBD區結合,形成藥物受體復合物,引起ER構象改變,使DBD區不能暴露,無法與靶基因的ERE結合,抑制腫瘤增殖。代表藥物為他莫昔芬(TAM),這種通過競爭受體達到抗雌激素作用過程中出現耐藥的機制如下:
1.1 ER與表皮生長因子(EGF)及其受體(EGFR)、人表皮生長因子受體2(HER-2)串話調節與內分泌治療耐藥。
表皮生長因子激活的受體酪氨酸激酶傳導通路可以配體非依賴方式直接將雌激素受體第ll8位的Ser殘基激活。將乳腺癌細胞長期置于缺乏雌激素的環境中,雌激素受體表達明顯降低,同時生長因子下游激酶表達活性增強。體外實驗發現,TAM可以刺激HER-2在ER陽性乳腺癌細胞株中的表達上調,認為TAM在阻斷ER通路的同時可以促進HER-2通路的信號傳遞,證實了ER同生長因子信號轉導途徑的交叉作用與內分泌治療耐藥有關[1]。
表皮生長因子受體信號傳導主要通過M APK、AKT通路與ER相互作用,在乳腺癌的抗激素耐藥中起重要作用并致使抗激素治療失敗。
1.2 核受體共調節蛋白因子,包括共激活因子(nuclear receptor coactivators,NCoAs)和共抑制因子(nuclearreceptor corepressors,NCoRs),與內分泌治療耐藥。
ER依據配體本身差異,可與共調節蛋白相互作用,從而使轉錄活性增強(共激活因子)或抑制(共抑制因子)。AIB1(amplified in breast cancer 1)是共激活因子家族成員之一,因在半數以上的乳腺癌患者中過表達而得名。體外研究發現,HER-2陽性TAM 抵抗的乳腺癌細胞系MCF-7富集AIBI等共激活因子復合物到靶基因的啟動子區,而激素敏感的MCF-7細胞富集的是共抑制因子復合物。在TAM 治療敏感后繼發耐藥的乳腺癌患者也觀察到這一現象,A IBI可以大大降低TAM 在HER-2過表達的腫瘤中的拮抗作用。具有相對豐富的共激活因子(如A IB 1)腫瘤,特別是同時具有較強HER-2信號轉導、可以使A IB 1活化的腫瘤,由于提高TAM 結合的ER擬E樣促進轉錄作用,所以TAM治療抵抗[2]。
1.3 配對框2基因產物 PAX 2(the paired box 2 gene product)與內分泌治療耐藥。
英國癌癥研究學會的研究者Antoni Hurtado等[3]報道了 PAX 2(the paired box 2 gene product)為使ErbB2關閉的開關。當ErbB2處于開啟狀態時就產生了(TAM)耐藥性,而TAM通過蛋白PAX2關閉了乳腺癌基因E rb B-2。臨床上觀察到,當PAX 2高表達、Her-2低表達,則預后好。
1.4乳腺癌抗雌激素藥物耐藥性基因1/p130Crk相關底物蛋白(BCAR l/p130Cas )與內分泌治療耐藥
BCAR l/p130Cas 屬于參與很多細胞過程的銜接蛋白中的一個小家族。2000年Brinkman等[4]確定了BCAR l 基因是抗雌激素藥物耐藥細胞表型相關的第一個基因。在最近的研究中,Soni等[5]證實了在TAM耐藥的M CF-7細胞存在乳腺癌抗雌激素耐藥基因(b reast cancer anti-estrogen resistance-1,BCAR-1))產物過表達。Soni等證實阻斷TAM耐藥乳腺癌細胞中BCAR-1的活性,可降低EGFR的水平以及減弱EGFR與ERK/AKT之間的信號傳導,從而抑制癌細胞的增值和促進凋亡,并且可恢復TAM的活性。顯然,在TAM耐藥癌細胞模型中,BCAR-1是調節生長因子信號傳導的重要因子。van derFlier等檢測了937個原發乳腺癌患者提取物中BcARl/pl30cas蛋白的表達水平,比較了該蛋白的表達水平和臨床參數之間的關系,發現BCAR1/p l30Cas蛋白高表達的原發乳腺癌患者疾病復發更迅速,總存活時間更短,且對抗雌激素藥物耐藥的風險更大。
1.5 其他生長因子與內分泌治療耐藥
在乳腺癌細胞中,下面一些生長因子的過表達也是促進TAM治療耐藥的原因。這些生長因子包括PC細胞來源生長因子,也稱顆粒蛋白前體抗原(progranulin);血管內皮生長因子,在體內能促進血管生成,在體外有誘導乳腺癌細胞生長活性;角化細胞生長因子(keratinocyte)[6],在TAM治療敏感的M CF-7細胞中加入角化細胞生長因子能導致耐藥,但是使受體沉默后,TAM治療耐藥獲得逆轉。由此可見,在抗雌激素治療中,可以通過阻斷以上多種生長因子通路途徑實現抑制乳腺癌細胞生長。
芳香化酶抑制劑(aromatase inhibitors,AIs)抑制E合成過程中的關鍵酶芳香化酶,減少E的產生,抑制腫瘤增殖。由于乳腺癌細胞的強大適應性,內分泌治療會引起異常信號通路激活來導致AI或者抗雌激素的耐藥。其中一個重要的猜想是,對雌激素撤退環境的適應與AIs的耐藥有關一耐藥源于腫瘤細胞ER的雌激素超敏感或非依賴性。為了驗證這個假設,不少學者建立了長期雌激素剝奪(1ong-term estrogen deprivation,LTED)乳腺癌細胞并進行研究。這種通過抑制雌激素合成抑制腫瘤細胞增值過程中出現耐藥的機制如下:
1.6 ER超敏與內分泌治療耐藥
Santen等報告中,LTED細胞胰島素樣生長因子受體(IGF-1R)和ER的串話調節誘導快速非經典通路ER信號途徑激活,導致絲裂原活化蛋白激酶(M APK)和磷脂酰肌醇3激酶/蛋白激酶B(PI3K/AKT)活化,最終使乳腺癌在雌激素高敏感的情況下增殖,即LTED細胞的ER水平是野生型的4倍一7倍,且其增殖所需雌激素量僅為野生型MCF一7細胞的的lg4倍[7]。
Brodies[8]的實驗室通過研究LTED乳腺癌細胞發現,其細胞內ER和erbB2含量比野生型高4倍-5倍。Dowsett[9]的實驗室中傳代的LTED細胞,在雌激素缺乏條件下8周傳代后,ER不需雌激素就可發生作用。
而Staka等實驗中不利用LTED細胞,而是在雌激素與生長因子共同缺失的培養基環境中培養一種MCF-7X乳腺癌細胞,對這種細胞研究顯示,(1)跟目前的MCF-7細胞相比,ER的Ser118磷酸化以及雌激素受體轉錄活性沒有明顯的提高,MCF-7X腫瘤細胞ER沒有過表達現象,也沒有對雌激素超敏。(2)在E和生長因子缺失環境中,MCF-7X乳腺癌細胞沒有通過ER與EGFR/HER2或者IGF-IR之間的串話調節通路繼續生長,而是主要通過ER與AKT的串話調節實現腫瘤細胞的繼續增值[10]。
1.7 抗雌激素藥物誘導相關生長因子表達改變引起內分泌治療耐藥
Gee等[11]研究指出在抗雌激素治療的最初階段,抗雌激素藥物就開始誘導相關基因表達以減弱藥物對乳腺癌細胞的生長抑制,最終導致抗雌激素藥物耐藥。這些基因表達產物有:EGFR/HER2,NFkB,Bag1,14-3-3和絡氨酸激酶。另外這些額外表達的基因似乎授予乳腺癌細胞更多惡性潛能,例如表達CD 59的乳腺癌細胞能逃避免疫監視;RhoE、a連環蛋白(a catenin)和 c-Src使乳腺癌細胞更具有侵襲性。這在一定程度上能得出乳腺癌細胞獲得性內分泌治療耐藥原理及內分泌治療耐藥后復發乳腺癌惡性程度更高的原因。
2 ER非依賴性內分泌治療耐藥機制(原發性內分泌治療耐藥機制)
2.1 抗雌激素耐藥基因(BCAR)的表達與內分泌治療耐藥
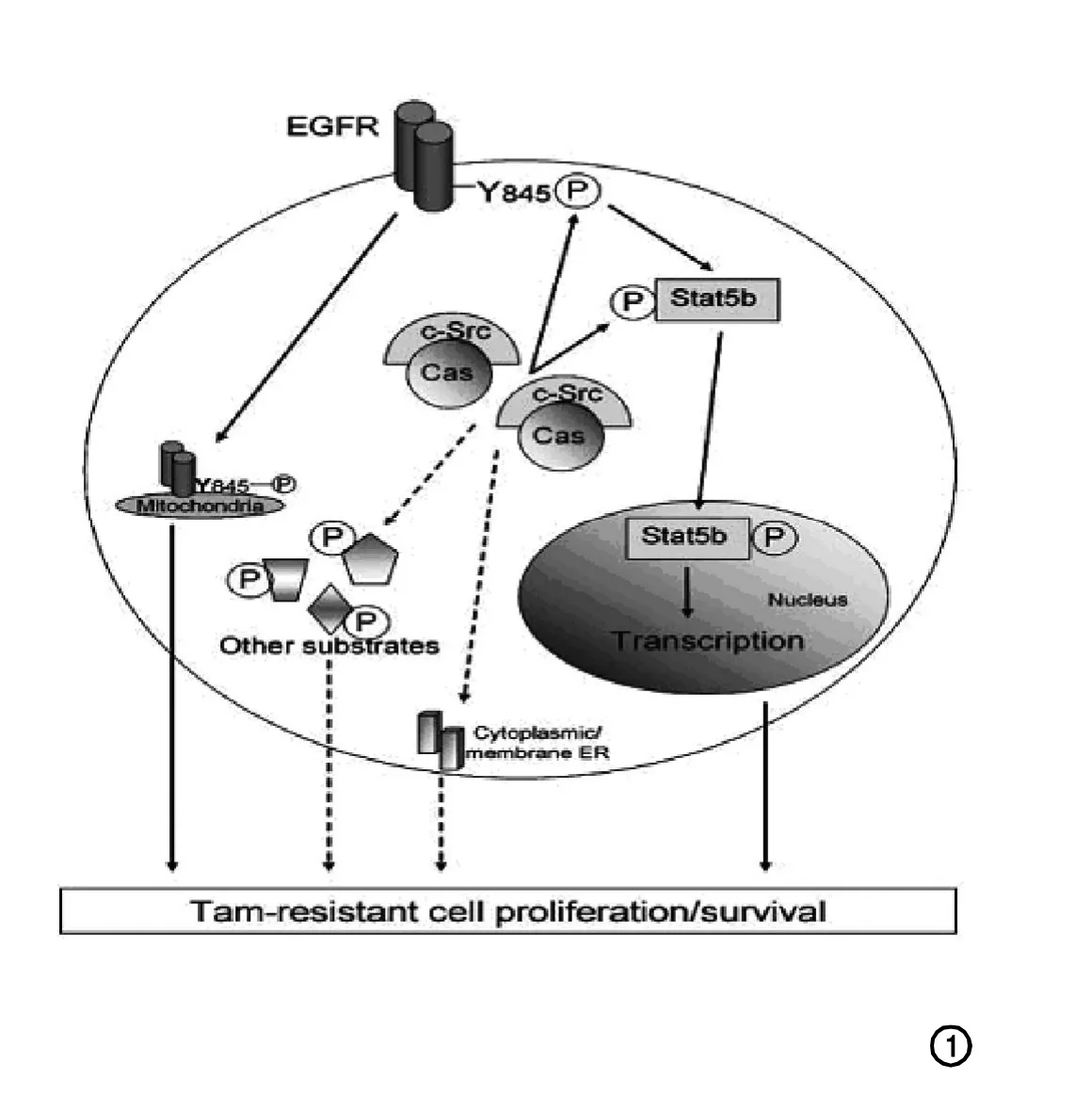
抗雌激素耐藥基因的表達使乳腺癌細胞能通過生長因子通路生長繁殖。Dorssers研究組[12]和van Agthoven研究組[13]分別在1993年和1998年指出乳腺癌抗雌激素藥物耐藥性基因BCAR-1和BCAR-3的表達能使乳腺癌細胞在ER非依賴的環境下生長,大概是通過使生長因子信號通路的效能最大化。2006年Riggins等研究指出BCARl/pl30CAS蛋白在抗雌激素藥物耐藥機制方面起銜接蛋白作用(如圖1)[14]。CAS蛋白通過與c-Src結合,誘導EGFR活化進而導致內分泌治療耐藥細胞生長繁殖。
2.2 其他ER非依賴性內分泌治療耐藥原理
乳腺癌細胞周圍內環境通過旁分泌或內分泌方式釋放大量生長因子,作用于乳腺癌細胞,并且占據了腫瘤細胞生長的主要通路,這跟臨床上觀察到的ER的表達與EGFR/HER-2的表達呈負相關的現象相一致[15]。
3 可能影響乳腺癌細胞生長發育引起內分泌治療耐藥的其它機制
3.1鋅(Zinc)和鋅載體7(Z IP7(HKE 4/SLC 39A 7))與內分泌治療耐藥
Taylor KM等[16]研究表明乳腺癌細胞周圍鋅(Zinc)濃度高和鋅載體7(ZIP7(HKE4/SLC39A7))高表達是導致乳腺癌內分泌治療耐藥的重要機制,通過ZIP7基因沉默或降低Zinc濃度能抑制TAM耐藥的M CF-7的繼續生長。
3.2 DNA甲基化與內分泌治療耐藥
DNA甲基化情況對基因的表達影響深遠,DAN低甲基化可引起DNA表達增加,高甲基化可引起DNA表達沉默。Fan等[17]指出在TAM耐藥MCF-7細胞中,DNA的低甲基化可引起EGFR/HER-2及相關蛋白等的基因激活和表達擴增;而DNA的高甲基化與腫瘤抑制基因和腫瘤凋亡基因的失活有一定的相關性。
4 結 語
綜上所述,乳腺癌內分泌治療耐藥的機制尚未完全闡明,但ER功能相關的分子信號傳導途徑及其輔助因子的相互作用、ER基因的突變及相關基因的多態性等都是導致耐藥發生的重要因素。針對信號傳導途徑關鍵因子的新藥的開發可能成為ET耐藥的乳腺癌患者最有前景的療法。隨著對耐藥的分子機制認識的逐漸深入和藥物基因組學的發展,針對受體后調節及基因改變的靶向和基因治療新藥的將為耐藥腫瘤的治療帶來新的希望。[18]
1.Massarweh S, Schiff R.Unraveling the mechanisms of endocrine resistance in breast cancer: new therapeutic opportunities.Clin Cancer Res.2007 Apr 1;13(7):1950-4.
2.Osborne CK, Bardou V, Hopp TA, Chamness GC, Hilsenbeck SG,Fuqua SA, Wong J, Al lred DC,Clark GM, Schif f R.Role of the estrogen receptor coactivator AIB1 (SRC-3) and HER-2/neu in tamoxifen resistance in breast cancer.J Nat l Cancer Inst.2003 Mar 5;95(5):353-61.
3.Antoni Hurtado, Kelly A.Holmes, Timothy R.Geistlinger,Iain R.Hutcheson, Robert I.Nicholson, Myles Brown, Jie Jiang, Wil liam J.Howat, Simak Ali, Jason S.Carrol l,Regulation of by oestrogen receptor–PAX2 determines response to tamoxifen,Nature 456, 663-666 (12 November 2008) doi:10.1038/nature07483 Letter.
4.Brinkman A,Van der Flier S,Kok EM,et a1.BCAR l,a human homologue of the adapter protein p130Cas,and antiestrogen resistance in breast cancer cel ls [J]. J Nat l Cancer Inst,2000,92 (2 ):112 -120.
5.Soni S, Lin B-T, August A, Nicholson RI, Kirsch KH.Suppression of tamoxi fen resistance by inhibition of p130Cas/BCAR1 signaling.2008;In Press.
6.Chang HL, Sugimoto Y, Liu S, Ye W, Wang LS, Huang YW, Lin YC.Keratinocyte growth factor(KGF) induces tamoxifen(tam) resistance in human breast cancer MCF-7 cel ls.Anticancer Res.2006 May-Jun;26(3A):1773-84.
7.RJ Santen,RX Song,Z Zhang,et a1.Adaptive hypersensitiy to estrogen:mechanisms and clinical relevance to aromatase inhibitor therapy in breast cancer treatment[J].J Steroid Biochem Mol Bi-0l,2oo5,95:155 -165.
8.A Brodie,D Jelovac,G Sabnis,et a1.Model systems :mechanisms involved in the loss of sensitivity to letrosole[J].J Steroid Biochem Mol Biol,2oo5,95:41-48.
9.LAMartin,I Farmer,SR Johnston,eta1.Enhanced estrogen receptor(ER)alpha,ERBB2,and MAPK signal transducfion pathways operate during the adaptation of MCF一7 cel ls to long term estrogen deprivation[J].J Biol Chem,2003,278:30458-30468.
10.Staka CM, Nicholson RI, Gee JM.Acquired resistance to oestrogen deprivation: role for growth factor signal ling kinases/oestrogen receptor cross-talk revealed in newMCF-7× model.Endocr Relat Cancer.2005 Jul;12(Suppl 1):S85-97.
11.Gee JM, Shaw VE, Hiscox SE, McClel land RA, Rushmere NK,Nicholson RI.Deciphering antihormone-induced compensatory mechanisms in breast cancer and their therapeutic implications.Endocr Relat Cancer.2006 Dec;13(Suppl 1):S77-88.
12.Dorssers LC, van Agthoven T, Dekker A, van Agthoven TL,Kok EM.Induction of antiestrogen resistance in human breast cancer cel ls by random insertional mutagenesis using defective retroviruses: identification of bcar-1,a common integration site.Mol Endocrinol.1993 Jul;7(7):870-8.
13.van Agthoven T, van Agthoven TL, Dekker A, van der Spek PJ, Vreede L, Dorssers LC.Identification of BCAR3 by a random search for genes involved in antiestrogen resistance of human breast cancer cel ls.Embo J.1998 May 15;17(10):2799-808.
14.Riggins RB, Thomas KS, Ta HQ,Wen J, Davis RJ, Schuh NR,Donelan SS, Owen KA, Gibson MA,ShupnikMA, Silva CM,Parsons SJ, Clarke R, Bouton AH.Physical and functional interactions between cas and c-src induce tamoxi fen resistance of breast cancer cells through pathways involving epidermal growth factor receptor and signal transducer and activator of transcription 5b.Cancer Res.2006 Jul 15;66(14):7007-15.
15.Hutcheson IR, Knowlden JM, Hiscox SE, Barrow D, Gee JM,Robertson JF, El lis IO, Nicholson RI.Heregulin beta1 drives gefitinib-resistant growth and invasion in tamoxifenresistantMCF-7 breast cancer cel ls.Breast Cancer Res.2007;9(4):R50.
16.Taylor KM, Vichova P, Jordan N, Hiscox S, Hendley R,Nicholson RI.ZIP7-mediated intracel lular zinc transport cont ributes to aber rant growth factor signal ing in antihormone-resistant breast cancer Cel ls.Endocrinology.2008 Oct;149(10):4912-20.Epub 2008 Jun 26.
17.Fan M, Yan PS, Hartman-Frey C, Chen L, Paik H, Oyer SL,Salisbury JD, Cheng AS, Li L, Abbosh PH, Huang TH, Nephew KP.Diverse gene expression and DNA methylation profiles correlate with dif ferential adaptation of breast cancer cel ls to the antiestrogens tamoxifen and fulvestrant.Cancer Res.2006 Dec 15;66(24):11954-66.
18.韋偉 葉靜 劉巧劌等 乳腺正常、癌周和癌組織中ER mRNA表達一致性及其臨床意義的探討 罕少疾病雜志[J]2008 15(6)
R737.9
D
book=46,ebook=57
2009-10-20

