Mfn2基因克隆及pEGFPmfn2真核表達質粒的構建
席少靜,何 軍,滕艷萍,王曉婕,范 倩
(1.寧夏醫科大學,寧夏 銀川750004;2.寧夏醫科大學附屬醫院 心臟中心,寧夏 銀川750004)
線粒體融合蛋白2基因(mitofusin-2,mfn2)是近年來發現的一種新型基因,該基因位于線粒體的外膜,參與線粒體的融合,調節線粒體的新陳代謝和維持線粒體的網狀結構。Mfn2不僅在血管平滑肌細胞(VSMC)中表達,在心、腦 、肺 、腎、肝組織中亦有廣泛分布。陳光慧等[1]發現該基因可以有效地阻遏細胞周期和抑制細胞增殖,是一種新發現的增殖抑制基因。增強型綠色熒光蛋白(EGFP)是綠色熒光蛋白(GFP)的一種突變體,能在異源組織中表達并產生熒光,已作為報告基因廣泛運用于生物醫學研究領域。本文通過大鼠pEGFPmfn2熒光真核表達載體的構建,為下一步轉染VSMC,進一步研究mfn2抑制VSMC的增殖作用奠定實驗基礎。
1 材料與方法
1.1 材料
1.1.1細胞株與質粒 大鼠血管平滑肌細胞株A7r5引自ATCC(CRL-1444);pGEM-T載體購自promega公司,pEGFP-N1載體購自CLONTECH公司。
1.1.2主要試劑 E.Coli DH5α感受態細胞、質粒提取試劑盒購自北京天根生化科技公司,DMEM培養基、胎牛血清、PBS緩沖液、0.25%Trypsin+0.02%EDTA購自美國Hyclone,TRIzol Reagent購自Invitrogen,RT試劑盒、限制性內切酶HindⅢ和 BamHⅠ、T4DNA連接酶、DNA Marker購自美國Fermentas,Hot-StarTaqDNA聚合酶購自TaKaRa,DNA凝膠回收試劑盒購自Axygen,引物合成和測序由上海生工生物工程公司完成。
1.2 方法
1.2.1細胞培養及總RNA的提取 引自ATCC的A7r5,以1∶2接種于新的培養瓶中,放入37℃、5%CO2培養箱中培養,約3-5天傳代一次。取一瓶長至對數生長期的細胞,TRIzol法提取A7r5總RNA,測定總RNA濃度并行1%瓊脂糖凝膠電泳,觀察總RNA的完整性。
1.2.2mfn2基因的擴增和回收 根據GenBank數據庫得到大鼠mfn2基因cDNA序列(收錄號:NM1-30894),通過Primer軟件設計引物,在上下游引物 5′端分別加入限制性內切酶HindⅢ和BamHⅠ酶切位點及保護堿基,用于定向克隆。上游引物5′-AGAAGCTTATGTCCCTGCTCTTTTCTC-3′;下游引物 5′-TAGGATCCCGTCTGCCGGGCTGCAG-3′,擴增 產物 長度為2 274 bp。取A7r5總RNA 3 μ g逆轉錄合成cDNA,取 5 μ l cDNA 行 PCR。擴增條件:95℃5 min、72℃10 min;變性和延伸條件分別為95℃30 s,55℃45 s,72℃1.5 min,5個循環;95℃30 s,64℃45 s,72℃2.5 min,35個循環。1%瓊脂糖凝膠電泳分離特異性產物,按DNA凝膠回收試劑盒說明書回收并測定PCR產物濃度。
1.2.3重組克隆載體的構建 將回收的mfn2cDNA與載體pGEM-T連接成重組克隆載體pGEM-T-mfn2。10 μ l連接體系含純化 PCR 產物 3 μ l,載體 pGEM-T 1 μ l,T4DNA 連接酶1 μ l,10×Buffer 2 μ l,混勻后4℃連接反應過夜。將連接產物10 μ l轉化入 E.coli DH5α感受態細胞并行氨芐青霉素(100 mg/L)篩選,以未轉染菌和轉染載體pGEM-T菌為對照,采用菌落直接PCR、HindⅢ和BamHⅠ雙酶切和序列分析方法,確定目標片段的存在和序列正確性。
1.2.4重組真核表達載體的構建 將轉化重組質粒pGEM-T-mfn2的E.coli DH5α增菌后,提取重組質粒行HindⅢ和BamHⅠ雙酶切。酶切產物在1%瓊脂糖凝膠電泳分離后將目的片段行膠回收并測定濃度,與經相同雙酶切的載體pEGFP-N1連接成重組表達載體pEGFPmfn2。20 μ l連接體系含回收產物 5 μ l,載體pEGFP-N1 1 μ l,T4DNA 連接酶 1 μ l,10 ×Buffer 2 μ l,混勻后4℃連接反應過夜。將20μ l連接產物轉化入E.coli DH5α感受態細胞并行卡那霉素(25 mg/L)篩選,以未轉染菌和轉染載體pEGFP-N1菌為對照,經菌落直接PCR、HindⅢ和BamHⅠ雙酶切途徑確定目標片段的存在。將初步鑒定為陽性克隆菌株送至上海生工生物工程公司進行核苷酸序列測定。
2 結果
2.1 培養的A7r5細胞
倒置顯微鏡下見A7r5細胞呈成纖維細胞樣,貼壁生長(圖1)。
圖1 培養48小時的A7r5細胞
2.2 A7r5總RNA的電泳結果
A7r5總RNA電泳后顯示三個條帶,28 s、18 s、5 s,提示提取的總RNA是完整的(圖2)。
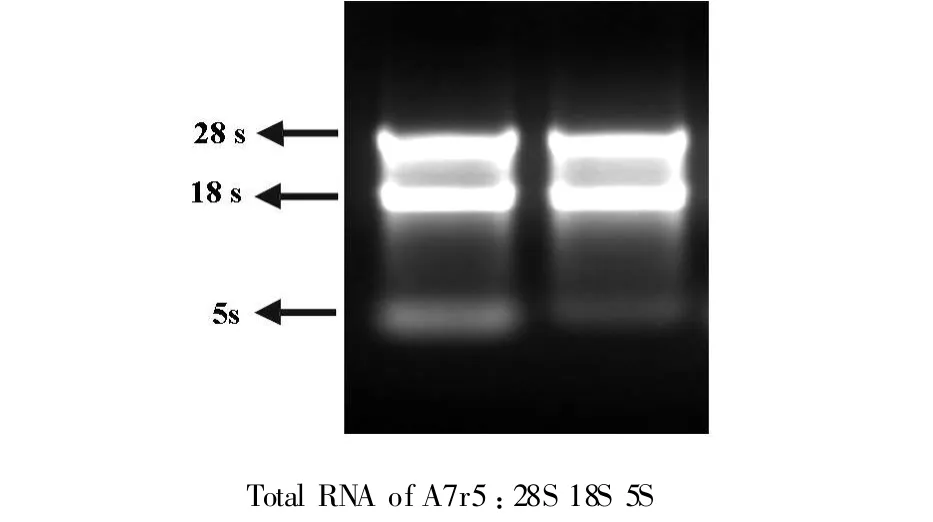
圖2 A7r5總 RNA的電泳結果
2.3 Mfn2基因的克隆與擴增
PCR產物的瓊脂糖凝膠電泳顯示存在約為2.2 kb的特異性條帶,與目的片段(2 274 bp)大小相似,提示Mfn2基因cDNA已獲成功擴增(圖3)。
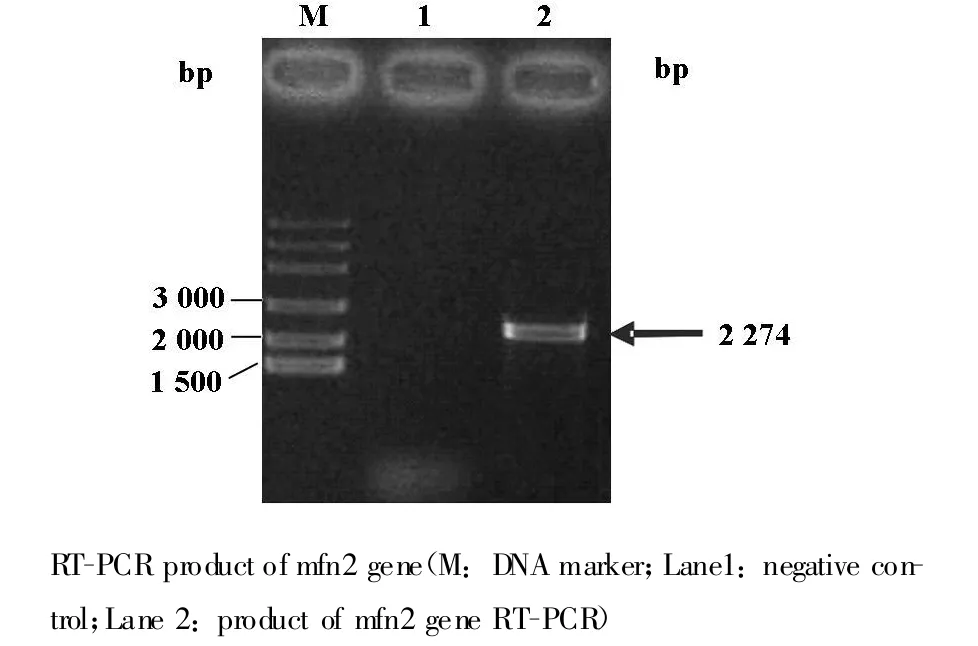
圖3 mfn2目的基因的擴增
2.4 重組質粒pGEM-T-mfn2的構建與鑒定
1為陰性對照,2為重組克隆載體pGEM-T-mfn2陽性菌落直接PCR顯示存在2.2 kb的特異性條帶,3為HindⅢ和BamHⅠ雙酶切得到2.2kb目的條帶和3.0kb的pGEM-T載體,4為HindⅢ單酶切得到的5.2 kb的重組質粒,5為重組質粒未經酶切的電泳圖,提示pGEM-T-mfn2重組質粒獲成功構建(圖4)。
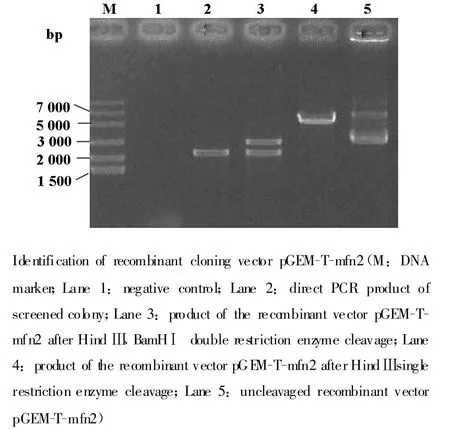
圖4 重組克隆載體pGEM-T-mfn2的鑒定
2.5 重組表達載體pEGFPmfn2的構建與鑒定
1為陰性對照,2為重組表達載體pEGFPmfn2陽性菌落直接PCR顯示存在2.2 kb的特異性條帶,3為HindⅢ和BamHⅠ雙酶切得到2.2kb目的條帶和4.7 kb的pEGFP-N1載體,4為HindⅢ單酶切得到的6.9 kb的重組載體,5為重組質粒未經酶切的電泳圖,提示重組表達載體pEGFPmfn2獲成功構建(圖5)。
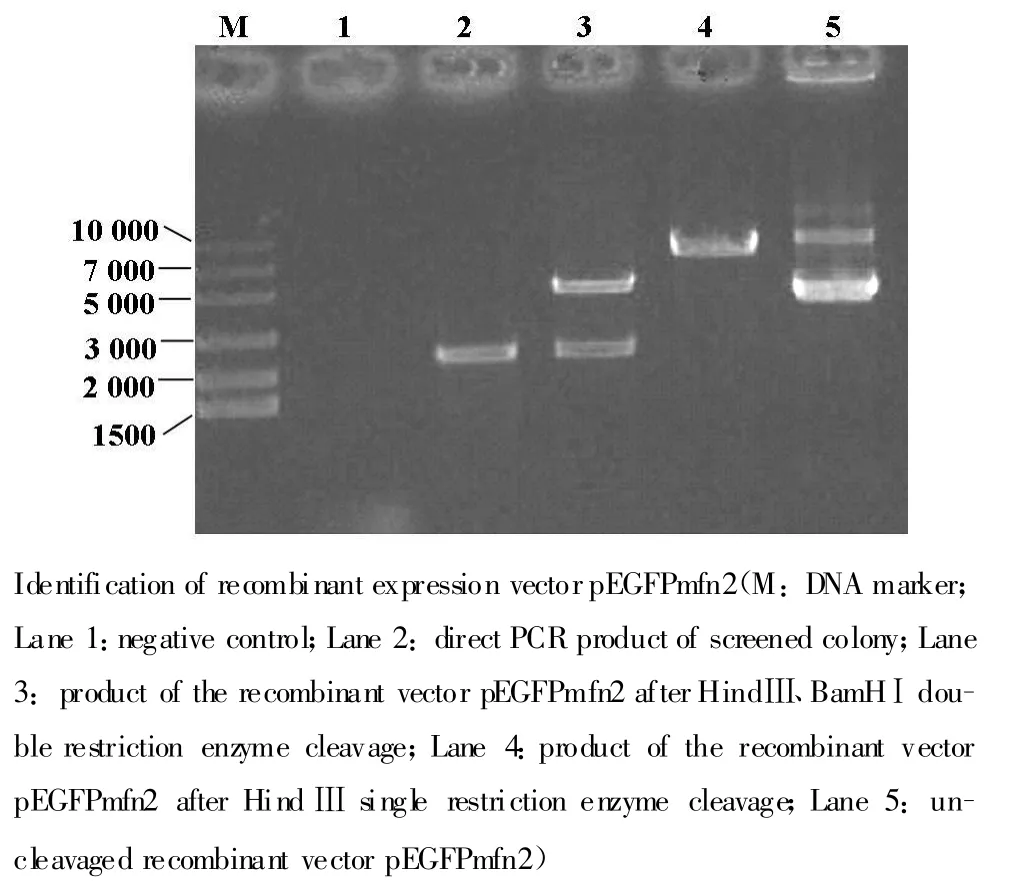
圖5 重組真核表達載體pEGFPmfn2的鑒定
2.6 質粒測序結果
取pEGFPmfn2質粒送上海生工生物工程公司測序,所得結果與genebank報道的4.1 kb大鼠mfn2 mRNA的cDNA序列(NM-130894)的cds(166,2439)區域的序列相同,最終證明mfn2基因已被成功插入pEGFP-N1載體中。
3 討論
Mfn2基因位于大鼠的染色體5q36,其全長cDNA序列為 4 161 bp,收錄至GenBank(編號NM-130894),其開放讀碼框編碼含757個氨基酸的線粒體膜蛋白,參與線粒體的融合,調節和維持線粒體的形態和功能[2]。目前大量研究顯示該基因與多種疾病的發生密切相關[3-6],已有研究顯示Mfn2的表達與VSMC的增殖密切相關,在增殖的VSMC中Mfn2的表達量下降。最新報道mfn2生理學上的重要性提示在線粒體的新陳代謝、凋亡和細胞信號起著重要作用[7],并發現該基因可以經由抑制 Ras-Raf-MEK-MAPK通路,抑制細胞的增殖[8]。
Mfn2基因通過載體導入后表達是目前研究Mfn2抑制細胞增殖作用的主要策略,而轉染導入是最為常用且穩定高效的研究方法。我們設計特異性引物通過RT-PCR克隆了Mfn2基因的編碼序列(2 274 bp),并與載體pGEM-T連接構建了重組克隆載體,完成了Mfn2基因鑒定和大量制備的目的。氨芐青霉素和α-篩選、HindⅢ和BamHⅠ限制性雙酶切和序列分析等方法證實了Mfn2基因的存在和序列正確。載體選擇方面,目前腺病毒在Mfn2基因介導中最為常用,但因轉染腺病毒存在的潛在風險是今后研究,尤其是將來可能的臨床研究所必須正視的。為避免這一問題,我們采用了真核表達載體pEGFPN1,其原因在于其不存在相應風險 ,同時以其為載體構建的重組載體可在E.coli和哺乳動物細胞中穩定高效表達,且可采用卡那霉素進行篩選。這樣,既可利用E.coliDH5α的高效復制特性獲得大量重組載體,也為下一步成功轉染血管平滑肌細胞后的篩選提供技術保障。此外,pEGFP-N1是一種穿梭質粒載體,其5’端連接有增強綠色熒光蛋白(EGFP)基因,外源基因可插入到質粒載體多克隆位點,最終的表達產物為目的基因所表達蛋白與熒光蛋白的融合體。我們將Mfn2基因克隆進多克隆位點,并且與EGFP在同一閱讀框,使其和N端的EGFP融合表達。同時由于EGFP性質穩定,通常不影響目的基因表達產物的生物學活性,因而可以根據EGFP融合蛋白的綠色熒光的分布來分析目的蛋白在細胞中的分布和定位[9]。
VSMC正常位于動脈中層,是動脈硬化斑塊和內膜增生的主要細胞類型。VSMC增殖是高血壓等心血管疾病的一種顯著病理特征。VSMC的增殖和遷移與動脈粥樣硬化、血管成形術后再狹窄、冠狀動脈搭橋術后橋血管閉塞密切相關。而Mfn2基因是新發現的一種增殖抑制基因,因此我們設想通過與載體pEGFP-N1構建真核表達載體,通過轉基因技術研究Mfn2對VSMC的增殖抑制作用。
[1]Chen KH,Guo XM,Ma DL,et al.Dysregulation of HSG triggers vascular proliferative disorders[J].Nature Cell Biol,2004,6:872.
[2]Karbowski M,Lee YJ,Gaume B,et al.Spatial and temporal association of Bax with mitochondrial fission sites,Drp1,and Mfn2 during apoptosis[J].J Cell Biol,2002,159:931.
[3]劉亞萍,溫紹君,劉 雅,等.增殖抑制基因在原發性高血壓患者血管平滑肌細胞增殖中的作用[J].中華心血管病雜志,2007,35(10):914.
[4]Chen CL,Shen T,Chen KH,etal.Inhibition of cardiac hypertrophy by mitofusin2 in neonatal rat cardiomyocytes[J].Beijing Da Xue Xue Bao,2008,40(5):528.
[5]Gastaldi G,Russell A,Golay A,et al.Upregulation of peroxisome proliferator-activated receptor gamma coactivator gene(PGC1A)during weight loss is related to insulin sensitivity but not to energy expenditure[J].Diabetologia,2007,50(11):2348.
[6]Florello A,Vicidoini G,Santini M.Giant solitary fibrous tumors of the pleura:two case reports[J].Thornc Cardiovasc Surg,2007,55(7):458.
[7]Santel A,Frank S,Gaume B,et al.Get the balance right:Mitofusins roles in health and disease[J].Biochim.Biophys Acta,2006,1763:490.
[8]Rojo M,Legros F,Chateau D,et al.Membrane topology and mitochondrial targeting mitofusins,ubiquitous mammalianhomologs of the transmembrane GTPase Fzo[J].J Cell Sci,2002,115(8):1663.
[9]Chen X,Wu R,Feng S,et al.Single cell derived murine embryonic stem cell clones stably express Rex12 specific green fluorescent protein and their differentiation study[J].BiochemBiophys Res Commun,2007,362(2):467.

