從時間生物學角度看肥胖
加勞萊特 等
背景介紹:什么是時間生物學?
從生理角度界定時間的概念是比較困難的,至今也沒有明確的定義。自古以來,人類都是通過鐘表和日歷知道和預知時間。而生物體自身(當然包括人類)也可以衡量時間,其中最受關注的是生物節律(生物體組織的不同層次都會有生物節律),以定期和可預測的方式進行。早在1729年,法國天文學家Jean Jacques d'Ortous De Marian發表了第一篇有關生物節律的詳細研究(含羞草的濾泡運動),結果得出,葉子的張開閉合行為在持續幾天的黑暗條件下依然存在。在20世紀中葉的首批對此領域的研究中,昆蟲生態學家Colin S Pittendrigh進行了一項對果蠅的研究,發現果蠅以環境時間為基本原則活動。這個基本原則就是晝夜節律,并由基因決定。
人類的晝夜節律
雖然有大量與此有關的記錄,包括睡眠和覺醒的時間、攝食和飲水等行為、體溫調節和內分泌、腎和生殖功能等都有晝夜節律。然而,人類的內源性晝夜節律似乎被忽略了,直到1866年William Ogle對人類體溫進行仔細觀察后才提出。正如他自己說的:“早上體溫上升,無論我們是否在睡夢中;晚上體溫下降,無論我們是否清醒。”后來有確鑿的證據證明,人類的體溫節律是內源性的。如今,體溫作為生理變量之一,更廣泛地用于人類時間生物學研究中。
許多激素表達具有晝夜節律。如,皮質醇、生長激素、醛固酮、泌乳素、睪酮、促甲狀腺激素、促黃體激素(LH)和卵泡刺激素。脂肪組織(目前認為它是一個內分泌器官)也具有晝夜節律。從這個意義上說,激素和細胞因子(如,瘦素、降脂素、抵抗素、脂聯素和內脂素),與脂肪組織的晝夜節律密切相關。脂聯素已被提出作為對抗代謝綜合征的 “守護天使”,它的循環水平同樣表現出波動性(慢速釋放)和晝夜變化。對這些物質晝夜節律性的認識,是了解人類生理病理的關鍵要素,特別是肥胖。
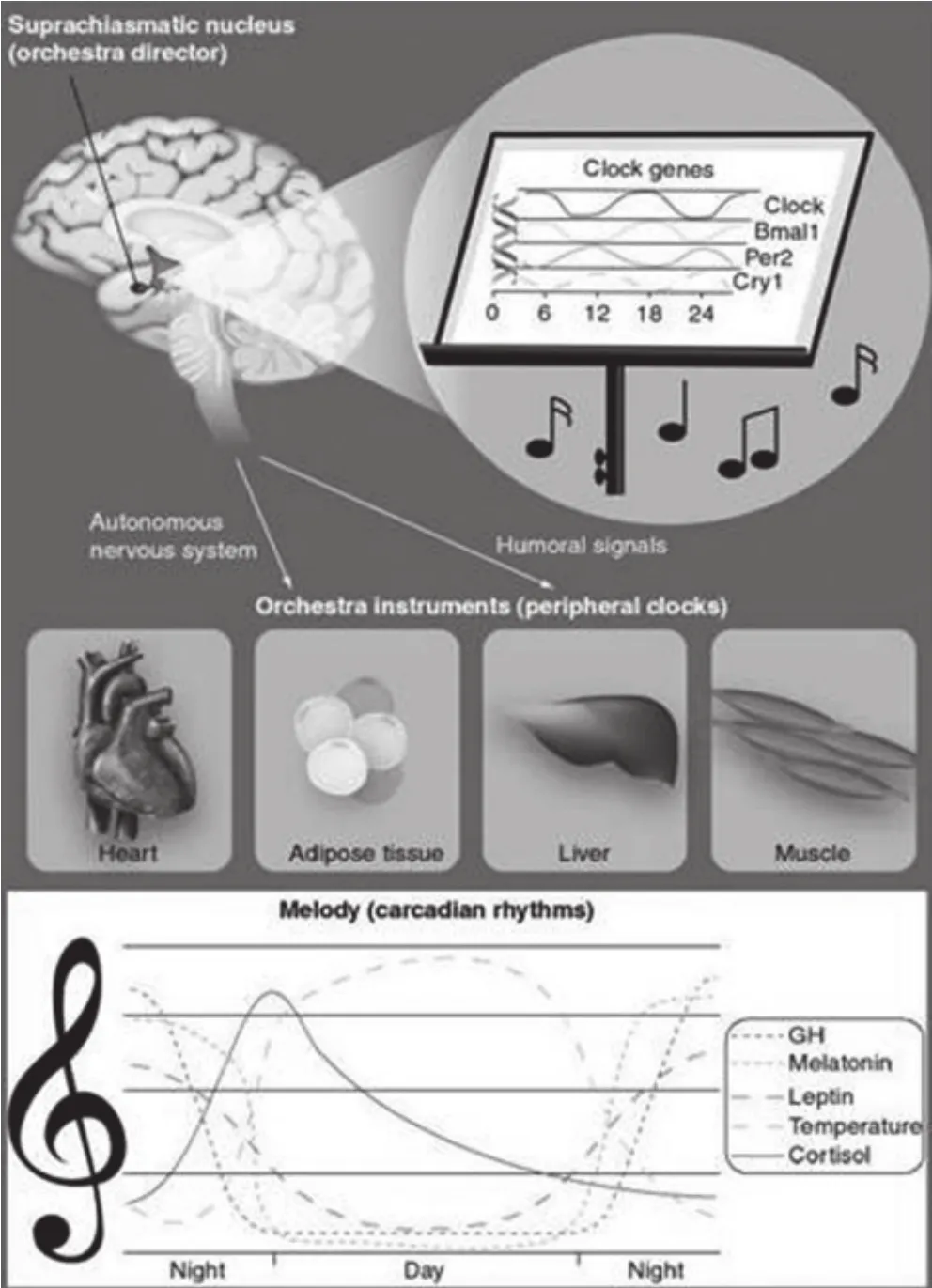
圖1 晝夜節律樂團的組織結構
晝夜節律指揮官——視交叉上核
基于微陣列研究數據,普遍認為每天組織的所有基因表型有10%~25%發生顯著變化。這意味著大多數行為、生理和生化的變量有晝夜節律。因此,在不同變量之間維持一個適當的內部時間秩序對健康至關重要。每一個變量在高峰或低谷時,晝夜節律系統必須精心調校,以保持健康狀態時的節律(圖1)。
晝夜節律樂團的指揮器官是存在于下丘腦上的視交叉上核(SCN)。它是晝夜節律系統的“起搏器(pacemaker)”(也叫生物鐘,激發生物節律并使之穩定維持的內部定時機制),它的每一個神經元有一個反饋環組成的分子齒輪,包括正反饋(Clock 和 Bmal1)和負反饋(Per和Cry)。那么,這個系統是怎么工作的呢?首先,含黑視素的神經節細胞把感受到的光刺激信號直接投射到視交叉上核,使晝夜節律的起搏器與外界環境的光照同步;其次,視交叉上核通過周期性的激素分泌和外周神經系統的活動,使整個晝夜節律樂團的各個不同組織器官節律同步。清楚這一點,我們就不難理解,健康狀態時的晝夜節律和不健康狀態時(節律被擾亂)的區別,僅取決于外周組織器官反饋(波峰)或不反饋(波谷)樂團指揮器官的精確命令。
如前所述,SCN的晝夜節律由基因轉錄—翻譯調節組成的兩個反饋環路形成,包括正反饋和負反饋。正反饋核心元件包括Clock(circadian locomotor output cycles kaput,是細胞內進行生物節律調節的核心調控因子)和BMAL1(brain and muscle ARNT-like-1,是哺乳動物生物鐘轉錄、翻譯反饋環路中的核心成分),兩者表達后相互作用形成異質二聚體,誘導分子齒輪的負反饋成分表達,如Pers(Pers1,2和3)、Crys(Cry1和2)和REV-ERB-α的表達。這些元件形成二聚體(PER-CRY)后經過核移位,對Clock和BMAL1表達形成負反饋抑制。因此,上述這些對SCN的正和負反饋元件的轉錄、翻譯和反饋調控形成了周期振蕩,周期大約接近24小時。
生物鐘(或叫起搏器)的一些元件,如REVERB-α、BMAL1和Clock基因,能誘導額外的基因表達,稱為生物鐘調節基因(CCG,指受生物鐘調節的一類基因),它不直接參與調控生物鐘,但可誘導多種靶基因的表達。
1972年有2個研究團隊都發現了生物鐘結構。每個SCN的神經元可以看作一個小型生物鐘。對這些神經元體外分離,發現它們好幾天都能保持近24 小時的、以一定頻率放電的節律運動。前面提到,SCN的晝夜節律(近24小時)與外環境的光刺激的相位和周期同步。其中,晝夜節律主要同步于白晝—黑夜周期。最近,對血細胞也做了類似的研究,在黑夜給予血細胞強光刺激(已知這個方法能有效調整中樞生物鐘),結果證明血細胞的生物鐘也受外界光線的影響。另外,其他的外部因素(如定期活動、社會接觸)也對生物鐘有同步影響。
生理狀態時,不同的組織器官都有不同的晝夜節律,并受視交叉上核驅動。舉例來說,SCN夜間活化了合成褪黑素的關鍵酶AANAT(arylalkylamine N-acetyltransferase),使褪黑素水平在夜間達到高峰。也有相反的情況,SCN夜間抑制了促腎上腺皮質激素(ACTH)釋放,使皮質醇水平在早晨達到高峰;體溫在白天比夜間略高(下午達到高峰)。成千上萬的生物體內都有這樣的“交響樂團”。
外周組織的晝夜節律各不一樣
心臟、脂肪組織、腎上腺、肺和血管平滑肌都有各自的振蕩器(圖1)。雖然在某些情況下,它們可以獨自振蕩,但通常情況下,從整個樂團節奏一致的潛在需要而言,它們必須保持對指揮器官的“忠誠”。
在我們體內,SCN通過神經、交感神經和副交感神經,選擇性地激活神經遞質(如褪黑素、prokineticine 2,TGF-α和nocturnin),把需要傳達的信息給各個組織臟器。
不難理解,健康狀態時內部的定時機制(正常晝夜節律)和不健康狀態時的節律(晝夜節律被擾亂)是不相同的,造成這種差異的原因在于對指揮器官精準命令的反饋(是否聽從命令),包括積極的(波峰)和消極的(波谷)兩種狀態。
被擾亂的晝夜節律
我們體內的晝夜節律被擾亂的狀態,叫做CD(chronodisruption),這是一個術語,提示晝夜節律不同步時,可能對健康有不良影響。這種擾亂的狀態可能持續幾天、幾個月甚至幾年。有人定義CD為內部的與生理和生化相關行為的定時機制受到干擾。從外界環境看,CD表示內部的晝夜節律和24 小時的外界環境周期的正常相位關系破裂。對此,CD可用節律振幅減少的幅度進行評估,大概有這3種情況,節律全部消失,節律延遲或節律超前,其中當然包括相逆的晝夜節律(如,夜間工作者)。從自身內部環境看,CD表示內部的各個層次的晝夜節律不同步。我們研究現代社會中普遍存在的時差、夜班、夜間光污染、睡眠不足或夜間進食現象,都會引起CD,并與不同疾病的相關因素高度相關,包括肥胖。
與晝夜節律不同步的行為可導致肥胖
夜班
流行病學研究已經表明這一點。另外,一項由Di Milia等作的橫斷面研究(n = 346),旨在調查肥胖與夜班的關系。結果表明,夜班工作者與白班工作者相比,平均BMI顯著增加。另一項重要的橫斷面研究,涉及27,485例工人(來源于the V?sterbotten intervention program),對受試者進行了采血和健康問卷調查,結果顯示,相對于白班工作者,夜班工作者與肥胖、高甘油三酯和低HDL-C的關系更緊密,這提示夜班工作可能和代謝綜合征相關。
夜間進食
有研究結果表示,相對于夜間不進食者,夜間進食者超重或肥胖增加4.4倍。
睡眠不足
臨床研究報告表明,睡眠時間≤5小時的女性相比睡眠時間達到7小時的女性,體重增加大約3.0kg。最近的一項由Van Cauter等人進行的研究,對健康人睡眠時間限制在4小時,連續6夜,結果顯示,這些受試者的糖耐量受損,隨之出現胰島素抵抗。這種后果在兒童中更嚴重,有研究表明,睡眠時間不足是兒童肥胖的一個獨立的危險因素。睡眠不足和肥胖有關,涉及多種因素。一項針對成人的研究結果顯示,睡眠不足和瘦素和/或胃促生長素(ghrelin)的濃度變化相關(這種變化導致增加食欲,攝入更多碳水化合物類零食)。此外,基于增加能量攝入能消除疲勞的慣性理論,不難理解,睡眠不足(疲勞)會導致體重增加和肥胖(通過增加能量攝入)。在兒童,體溫調節的變化也涉及肥胖的形成,隨著年齡的增加,睡眠不足和肥胖的相關性會越來越弱,可能是由于兒童對睡眠的要求比較高。
擾亂晝夜節律的可能因素
被擾亂的晝夜節律是整個樂團在不同層次發生變化的結果。擾亂可以在信息輸入的時候(如光暗周期或進食時間),可以在信息輸出的時候,也可以在中央起搏器(褪黑素和糖皮質激素分泌相關)。
信息輸入時
已證明,光照不足(無論是否由不恰當的時間、次優的頻譜或強度不足所致)可能會導致與CD相關的疾病因素。
進食時間
進食時間也被認為是最重要的外部同步器或授時振蕩器之一。不規律的進食時間有助于CD相關疾病因素的產生。例如,夜間生活方式(醒得晚、不用早餐、晚餐很晚),導致夜間瘦素和褪黑素分泌減少,引發高血糖。因此,夜間生活方式可能是夜間進食綜合征、肥胖和糖尿病的危險因素之一,威脅著現代人的健康。
起搏器
關于起搏器對CD的“貢獻”,最初認為是生物的各個組織器官的晝夜節律不同步,并且是時差和夜班工作引起CD的原因所在。事實上,內部不同步的過渡狀態是SCN和外界環境的振蕩器(光-暗周期)耦合強度不同的結果,或受外界同步器不同的影響(攝食時間或光照)。
被擾亂的晝夜節律也可能是核心生物鐘的分子齒輪(如,分子BMAL1、Per2、Clock)相關的變化,都可影響機體的生理以及晝夜節律。2005年首次證明,生物鐘基因缺陷與肥胖顯著相關。由Turek等人進行的研究發現,Clock基因突變的小鼠,攝食的晝夜節律性大大減弱,表現為貪食、肥胖,并導致了代謝綜合征(高脂血癥、脂肪肝、高血糖及低胰島素血癥)。另一項由Ando等人進行的實驗模型研究發現,肥胖與CD相關。事實上,脂肪組織中的Clock基因和脂肪細胞因子的表達節律性減弱,增加了小鼠的肥胖程度。但是,對于這些問題存在重大爭議。Kennaway的研究結果顯示,擾亂肝臟和骨骼肌的Clock基因表達,沒有引起肥胖;在Clock突變小鼠,血清甘油三酯和游離脂肪酸顯著降低。
信息輸出時
晝夜節律系統信息輸出時被擾亂也會引起CD,主要包括上述提到的褪黑素(其它的如TGF-α和prokineticine2)。眾所周知,褪黑素具有抗氧化抗炎作用,同時也可能是一個合成的調節器(補充褪黑素可調整生物鐘),直接清除自由基。作為保護性激素,它也與肥胖有關(分泌不足會導致肥胖)。事實上,它還能恢復胰島素敏感性,降低血壓和改善血糖。
脂肪組織的晝夜節律
中樞性晝夜節律已被證明與脂肪合成途徑相關。首先,脂肪組織的關鍵代謝酶和脂質代謝相關的轉錄因子相互作用,影響中樞性晝夜節律;其次,中樞性晝夜節律受激素、攝取的營養成分和是否定時用餐的影響。從這個意義上說,晝夜節律系統和肥胖的關系,最重要的問題之一,是要確定,是否脂肪組織延遲了晝夜節律,是否脂肪組織有自己的生物鐘?有研究分析了小鼠的脂肪組織,顯示了強勁的24小時Clock基因的表達。脂肪組織的Clock基因的相對相位與SCN的Clock基因的表達是一致的。此外,微陣列研究表明,高達20%的小鼠或人類的脂肪轉錄是根據晝夜節律表達的。許多不同的研究(無論是實驗模型還是人類血清)已經表明,脂肪組織中的脂肪細胞分泌蛋白具有晝夜節律性。
最近進行了一項對人類白色脂肪組織的Clock基因表達的體外研究,從肥胖者體內取出內臟及皮下脂肪組織,并保存在組織培養液中過夜,然后每6小時操作一次,持續24小時。結果顯示,在脂肪組織中的Clock基因,振蕩準確并獨立于視交叉上核(圖2);其內在的振蕩節律性似乎與其他基因協同,如HPPAR和糖皮質激素相關基因。內臟和皮下的脂肪組織的晝夜節律模式是不同的。
脂肪細胞因子的晝夜節律與肥胖相關。實驗模型已證明,脂聯素、抵抗素、內脂素和瘦素的晝夜節律性由于肥胖會減弱。最近,我們的小組研究的脂聯素mRNA的表達譜及其受體(ADIPOR1和ADIPOR2)清楚地表明,病態肥胖患者的皮下和內臟脂肪組織有24 小時晝夜節律;并且,肥胖與CD相關。對相關基因的晝夜節律和代謝綜合征成分的分析顯示,肥胖(包括腹部肥胖)與脂聯素和脂聯素受體的振幅減少相關。另外,CD和肥胖的相關性可能牽扯到脂蛋白脂酶(LPL)的晝夜節律。這種酶與脂肪酸在脂肪細胞中的積累相關。正常情況下,LPL顯示晝夜節律性,并在用餐時達到最大分泌量,這有利于脂肪在脂肪組織中積累。但是,如果沒有按時進餐,LPL水平會隨之改變(節律被擾亂),游離脂肪酸可能會被儲存在異位組織,產生脂毒性,導致肝臟、肌肉或胰腺合并癥和代謝綜合征。簡而言之,以上的這些數據表明,24小時的晝夜節律對脂肪組織的功能是重要的,脂肪組織的晝夜節律與代謝狀態相關。
營養遺傳學與時間生物學
最新的時間生物學研究涉及到人類的營養遺傳學。基因與環境相互作用的概念得到新的證據支持,主要來自涉及飲食、肥胖和相關危險因素的研究。普遍認為,與脂質代謝、炎癥和肥胖相關的候選基因的變異性,與代謝綜合征經典的和新的生物標志物的血漿水平的改變相關。
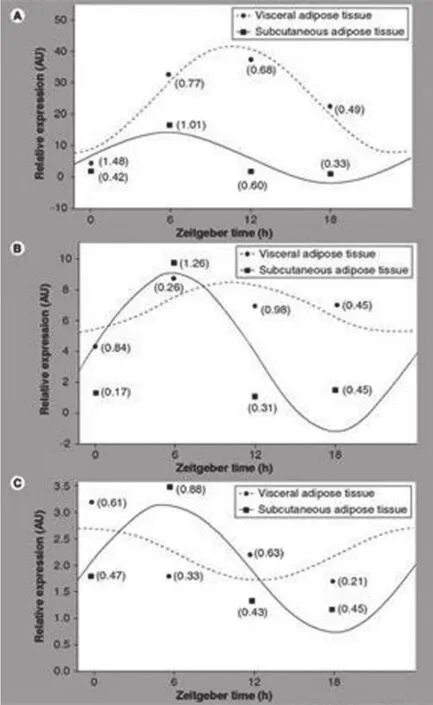
圖2 Clock基因在人體皮下和內臟脂肪組織中的節律性表達(A)hPer2(B) hBmal1和(C)hCry1
2008年,Scott等第一次提出Clock基因變異的多態性與肥胖(特別是腹部肥胖)相關;并認為,Clock基因的遺傳變異性可能在代謝綜合征、2型糖尿病和心血管疾病的發生發展中發揮作用。
我們的團隊在北美群體和來自西班牙東南部的地中海群體,重復了GOLDN(Genetics of Lipid Lowering Drugs and Diet Network)研究。發現這兩個群體的Clock基因具有單核苷酸多態性(SNPs),其中五分之四與肥胖(包括腹部肥胖)和能量攝入增加有關。此外,對于SNP rs4580704位點基因型,少量攜帶者和沒有攜帶者相比,糖尿病風險減少了31%,高血壓風險減少了46%。
地中海群體中,Clock基因rs1801260位點變異與基線水平肥胖相關,并且,此變異基因不利于體重的下降。并且,攜帶該變異基因的等位基因(G)的患者表現出較強的減重抵抗,少量攜帶者和沒有攜帶者相比,失眠(≤6小時/天)的頻率大大提高(59%Vs.41%)。令人感興趣的是Clock基因變異和脂肪酸組成之間的關系。我們可以確定,基因-飲食相互作用,影響Clock基因表達的多態性,并牽扯到代謝綜合征。通過對分單不飽和脂肪酸(MUFAs)攝入,我們發現,rs4580704位點的基因型,對血糖和胰島素抵抗影響不同,并且,僅在大量攝入單不飽和脂肪酸時,次要等位基因對胰島素敏感性才有保護作用。我們還發現,Clock 3111T/C的基因型對飽和脂肪酸的攝入量影響不同,并且,僅在大量攝入飽和脂肪酸時,該基因的變異多態性對腰圍產生有害影響。以上這些結果表明,晝夜節律和代謝綜合征的關系,牽扯到飲食來源和MUFAs攝入量。
結論
人類的晝夜節律系統就像一個生理交響樂團,由指揮器官統領著外周不同的組織,以保證兩者節律能夠同步。健康狀態時的內部節律和不健康狀態時的節律是不相同的,造成這種差異的原因在于外周組織對指揮器官的精準命令的反饋(是否聽從命令),包括積極的(波峰)和消極的(波谷)兩種狀態。肥胖可能是晝夜節律被擾亂的結果。來源于流行病學、生理和遺傳學的許多因素都可能擾亂節律。
未來展望
肥胖和時間生物學相關性的研究才剛剛開始,盡管有些研究人員和醫生對此高度質疑。目前,人們已經普遍接受了分子鐘是代謝異常和肥胖發生中一個有趣而重要的機制,發表的論文數量迅速增加正說明了這一點。
事實上,研究證據與日俱增。從2005年的Clock基因敲除實驗模型研究數據到流行病學證據,以及最近的營養遺傳學研究數據,可以說取得了一個很大的進步。我們的看法是,如果一切都指向同一個方向,時間生物學將不僅能幫助我們深入理解肥胖和代謝綜合征的相關性,更重要的是它可能成為治療肥胖的重要新工具,包括不同的時間生物學問卷、對基因型的分析、以及對各種生理性晝夜節律的測量。那時,我們在考慮肥胖危險因素的同時,還要考慮這些因素產生的時間。

