不同劑量白介素-2在局部進展性腎癌術后免疫治療中的療效評價
王希路 胡海龍 吳長利
腎癌對放療及化療均不敏感,術后用生物免疫制劑治療,以延緩腫瘤的復發及遠處轉移至關重要[1]。中國腎癌內科診療指南2009年修訂版也推薦白介素-2(IL-2)的中、低劑量治療方案可用于我國轉移性腎癌的一線治療(推薦級別B)[2],而目前指南推薦應用的小劑量(18 mIU/m2)治療時仍有大量患者出現不同程度的不良反應而不能夠規律、全程用藥。本文探討用更小劑量IL-2(1、0.5 mIU/m2)治療預防局部侵犯的腎臟透明細胞癌的效果,報告如下。
1 資料與方法
1.1 一般資料 2003年3月—2006年3月我院及天津醫科大學第二醫院收治的行開放或腹腔鏡腎癌根治術后,經病理證實為局部淋巴結轉移或T3期腎癌的患者共38例,男25例,女 13例,年齡 49~72歲,平均(56.6±12.8)歲。16例患者因常規體檢泌尿系彩超發現腎臟占位性病變而就診,22例患者術前出現不同程度的腰部不適癥狀。術前均經超聲、靜脈腎盂造影及CT檢查確診。本組患者中局部淋巴結增大者5例,侵及腎上腺組織者5例,腎靜脈瘤栓者4例,腔靜脈瘤栓者4例,侵及腔靜脈壁者2例。所有患者術后用藥之前均未發現遠處轉移,腫瘤直徑4.8~8.7 cm,平均(6.4±1.3)cm。患者術后病理證實為腎臟透明細胞癌33例,顆粒細胞癌3例,乳頭狀細胞癌2例,均無嚴重的心、腦血管疾病病史,均未出現嚴重術中及術后并發癥。
1.2 方法 患者術后按用藥劑量分為3組,分別予IL-2 18 mIU/m2(A組)、1 mIU/m2(B組)及0.5 mIU/m2(C組)3種劑量進行皮下注射治療,其中A組患者8例,B組患者14例,C組患者16例,各組患者臨床分期情況,見表1。

表1 各組腎癌患者臨床分期情況 (例)
3組患者給藥周期均為隔天用藥,持續8周后間隔4周為1個療程,共4個療程。如患者出現不良反應且不能耐受則退出治療;如出現嚴重骨髓抑制則予粒細胞集落刺激因子治療;如出現發熱可予非甾體類抗感染藥對癥治療。藥物不良反應評估標準依NCI CTC 3.0,其中Ⅰ度不良反應較輕,對患者生活質量無顯著影響,而Ⅱ度以上不良反應通常因影響患者生存質量而需對癥處理[3]。
1.3 統計學分析 采用SPSS 11.5進行統計學處理,組間比較行Fisher確切概率法,以P<0.05為差異有統計學意義。
2 結果
2.1 療效評價 在隨訪期8~30個月,4例患者出現患側腎區的腫瘤局部復發,其中3例患者進行2次手術切除復發腫瘤,病理均證實為腎細胞癌,1例患者未進行外科手術處理。5例患者出現遠處轉移,其中肺轉移3例,肝轉移1例,骨轉移1例。2例肺轉移患者行肺部腫物切除術,1例行放射性粒子植入術,肝轉移患者為肝臟多發轉移,未進行手術處理,1例肺轉移患者帶瘤生存。隨訪期內死亡患者共9例,完全緩緩患者20例,3組患者局部復發、遠處轉移、死亡例數及完全緩解所占比例比較,差異均無統計學意義(P>0.05),見表2。
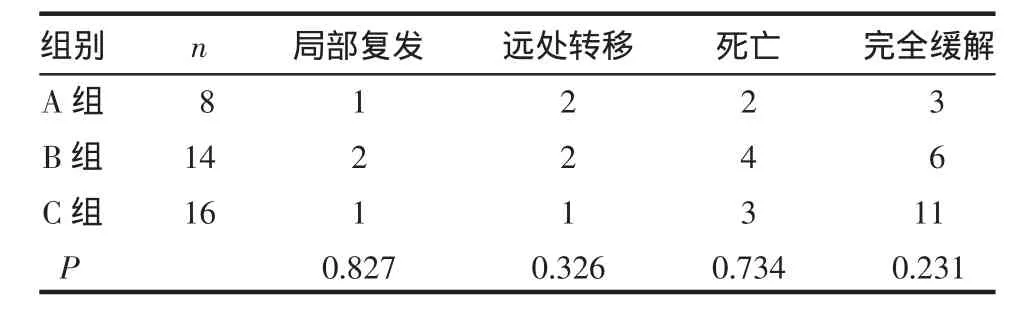
表2 應用不同劑量IL-2進行腎癌術后的治療結果比較 (例)
2.2 不良反應情況比較 在Ⅱ度以上不良反應中,伴發熱患者16例,乏力患者9例,流感樣癥狀患者7例,中性粒細胞減少患者8例。所有患者中,14例出現少見不良反應,包括體質量下降、腹瀉、貧血、皮疹及肝功能異常等。3組Ⅱ度以上不良反應發生比較差異有統計學意義(P=0.044),B組、C組較A組顯著降低,差異有統計學意義(P分別為0.037和0.011),B組、C組間比較差異無統計學意義(P=0.444),見表3。

表3 應用不同劑量IL-2進行腎癌術后不良反應程度情況比較 (例)
3 討論
腎癌對放、化療均不敏感,對多種化療藥物具有抗藥性,主要原因是癌細胞中含多藥耐藥基因,單純化療有效率非常低,目前多采用生物化學治療方案[4]。IL-2在調控T細胞免疫應答中起重要作用,同時在調控自然殺傷(NK)細胞、B細胞、單核巨噬細胞及中性粒細胞活化中也起一定作用[5]。大劑量的IL-2靜脈注射可能會導致1%~4%的患者出現嚴重的多系統不良反應[1]。多項臨床隨機對照試驗證實了小劑量IL-2的應用同樣能夠獲得與大劑量應用相同的總體生存率[6]。
我國腎細胞癌診斷治療指南(2009版)對于局部進展性腎癌,建議首選的治療方法為根治性腎切除術,術后尚無標準的輔助治療方案[7]。由于國人普遍不能耐受大劑量的IL-2靜脈滴注治療,指南(2009版)用于轉移性腎癌的推薦劑量也僅僅為18 mIU/m2。但是在筆者臨床工作中發現,即便是18 mIU/m2仍有較多患者不能耐受并出現較為嚴重的不良反應而停止用藥。
本研究發現,1 mIU/m2組及0.5 mIU/m2組與18 mIU/m2組患者相比,術后局部復發、遠處轉移及病死率差異無統計學意義,但1 mIU/m2組及0.5 mIU/m2組中度以上藥物不良反應的發生率卻比18 mIU/m2組顯著下降。藥物劑量的降低在減少不良反應的同時不可避免會降低治療效果,但本研究的結果卻提示低劑量的IL-2能夠減少不良反應的同時達到理想的治療效果,這可能與應用IL-2引起的組織連鎖性免疫增強效應不能夠僅僅應用藥代動力學進行解釋有關。本研究顯示,1 mIU/m2組及0.5 mIU/m2組間治療效果及不良反應比較差異無統計學意義,且0.5 mIU/m2組5例患者出現了Ⅱ度不良反應,無Ⅲ度不良反應發生。既往研究證實,在晚期轉移性腎癌患者中應用大劑量的IL-2能夠延緩患者的腫瘤進展,但對患者的總體生存率無明顯改善[8]。本項研究入組患者相對較少,并且未按照隨機原則進行患者分組,所得結果尚不完全可靠,而低劑量IL-2在該期腎癌治療中的作用尚待進一步通過大樣本的多中心隨機對照試驗進行評價。
[1]Romo de Vivar Chavez A,de Vera ME,Liang X,et al.The biology of interleukin-2 efficacy in the treatment of patients with renal cell carcinoma[J].Med Oncol,2009,26(Suppl 1):3-12.
[2]郭軍,馬建輝.中國腎細胞癌診治指南內科治療解讀[J].臨床腫瘤學雜志,2008,13(8):748-751.
[3]Trotti A,Colevas AD,Setser A,et al.CTCAE v3.0:development of a comprehensive grading system for the adverse effects of cancer treatment[J].Semin Radiat Oncol,2003,13(3):176-181.
[4]Kapoor AK,Hotte SJ.Current status of cytokine therapy in management of patients with metastatic renal cell carcinoma[J].Can Urol Assoc J,2007,1(2 Suppl):S28-33.
[5]Fehniger TA,Cooper MA,Caligiuri MA.Interleukin-2and interleukin-15:immunotherapy for cancer[J].Cytokine Growth Factor Rev,2002,13(6):169-183.
[6]Malaguarnera M,Ferlito L,Gulizia G,et al.Use of interleukin-2 in advanced renal carcinoma:meta-analysis and review of the literature[J].Eur J Clin Pharmacol,2001,57(4):267-273.
[7]那彥群,孫光.中國泌尿外科疾病診斷治療指南手冊[M].北京:人民衛生出版社,2009:9-22.
[8]Majhail NS,Wood L,Elson P,et al.Adjuvant subcutaneous interleukin-2 in patients with resected renal cell carcinoma:a pilot study[J].Clin Genitourin Cancer,2006,5(1):50-56.

