化療所致惡心嘔吐及其治療藥物的研究進展
施 亮,王 增,樸永鋒,王 磊(浙江省腫瘤醫院藥劑科,杭州市 310022)
化療藥物引起的惡心、嘔吐(Chemotherapy-Induced Nausea and Vomiting,CINV)是化療期間最常見的不良反應之一,發生率為70%~80%。其中10%~44%的CINV患者為預期性惡心、嘔吐[1]。CINV可導致患者體質下降、電解質紊亂、食欲下降[1],嚴重者還會影響癌癥患者的化療進展,從而導致化療失敗。因此,有效地預防和減少CINV的發生具有重要的臨床意義。本文就引起CINV的因素、機制、分類以及相關止吐藥物的進展作如下綜述。
1 CINV的臨床評價
目前臨床對CINV的評價是按照世界衛生組織(WHO)的分級標準進行,將惡心嘔吐分為:0度,無惡心嘔吐;Ⅰ度,惡心,無嘔吐;Ⅱ度,惡心嘔吐每天1~2次,不需治療;Ⅲ度,惡心嘔吐每天3~5次以上,影響進食與正常生活,需治療;Ⅳ度,嚴重惡心嘔吐每天5次以上,需臥床、輸液治療。止吐療效評價:以無惡心嘔吐,或輕度惡心,嘔吐每天1~2次為有效。
2 CINV的易感因素及致吐藥物的分類
研究發現,女性患者,年齡小于50歲,有飲酒史和化療史的患者在化療期間往往比較容易發生CINV,少數患暈動癥或懷孕的患者也會發生CINV[2]。
根據化療藥物的致吐作用程度,分最強的致吐藥物、中高度致吐藥物、中度致吐藥物、低致吐藥物。抗腫瘤藥物致吐情況見表1。

表1 抗腫瘤藥物致吐情況[3]
3 CINV的機制
CINV的機制非常復雜,到目前為止尚無定論。多數學者認為CINV主要通過3個途徑引發[3]:(1)化療藥物損傷消化道黏膜,導致腸嗜鉻細胞釋放5-羥色胺(5-Hydroxytryptamine Agonists,5-HT)等物質,刺激腸壁傳入迷走神經上的5-HT3受體,興奮延髓的嘔吐中樞而導致嘔吐。(2)化療藥物可作用于大腦第四腦室的催吐化學感受區(Chemoreceptor trigger zone,CTZ)而引起嘔吐。(3)感覺、精神因素直接刺激大腦皮質通路導致嘔吐。
4 CINV的分類
CINV可分為急性、遲發性、預期性、突發性、難治性5種類型。急性嘔吐是指化療后24 h內出現的嘔吐;遲發性嘔吐發生于給藥24 h后,多在24~72 h出現,也可晚至化療后4~5 d才出現的嘔吐;預期性嘔吐是指既往化療時有過嘔吐的患者,在受到與化療相關事物的刺激時產生的條件反射性嘔吐,發生于化療前或化療中;突發性嘔吐是指在使用止吐劑的5 d內突然發生的嘔吐;難治性嘔吐是指在前期化療中使用止吐劑治療失敗,并在后期化療中發生的嘔吐。
5 CINV的治療指南
由2008年版美國國家綜合癌癥網絡(NCCN)治療指南可見:中、高度嘔吐采用5-HT3受體拮抗藥、地塞米松和阿瑞吡坦的三聯用藥方案;對于低發或者極低發嘔吐通常是在化療前給予地塞米松;對于預期性、突發性嘔吐應當加強患者的心理治療,使患者建立信心去接受化療,有必要時可根據患者實際情況給于抗焦慮藥治療;對于難治性嘔吐目前治療的手段不多,主要則是應用大麻素類、加巴噴丁[4],具體見表2。

表2 NCCN治療指南表
6 止吐藥物
目前臨床應用的止吐藥物有多巴胺受體拮抗藥、皮質類固醇類、5-HT受體拮抗藥、神經激肽(NK)1受體拮抗藥、多靶點的止吐藥物奧氮平及大麻素等其它類和中藥。
6.1 多巴胺受體拮抗藥
多巴胺D2受體拮抗藥的代表藥物為甲氧氯普胺,對遲發性嘔吐有一定療效,可能與其鎮靜和中樞效應有關。本品作用于延髓催吐化學感應區(CTZ)中的多巴胺受體,提高CTZ的感受閾值而發揮中樞性止吐作用;此外本品可提高胃腸道括約肌的張力,加強胃和食管蠕動,促進胃排空,從而減少膽汁和胃泌素分泌,起到協同止吐的作用[5]。另外,本品對5-HT3受體亦有輕度抑制作用,與糖皮質激素聯用,可增加療效并減輕不良反應。但長期反復或大劑量使用,因阻斷多巴胺受體,膽堿能受體相對亢進而發生神經中樞抑制或錐體外系反應,表現為肌震顫、發音困難、共濟失調等。因此,多巴胺受體拮抗藥的臨床應用受到限制。
6.2 皮質激素
皮質激素的主要代表藥物是地塞米松,能有效地預防CINV,常常作為預防惡心嘔吐的首選藥物。作用機制目前尚未明確,有研究者認為可能是通過抗炎及抗毒素的作用,減輕外周神經的損害,保持正常的胃腸動力,從而減輕遲發性嘔吐[6];另有學者認為地塞米松通過外周和中樞2種途徑抑制5-HT產生和釋放而起到止吐作用;也可能是地塞米松改善血腦屏障對血清蛋白的通透性,降低血液中5-HT濃度,減輕腦組織水腫而起到止吐作用。
值得注意的是地塞米松在治療輕、中度致吐性化療導致的嘔吐中會引起重度失眠、腹脹、消化不良、精神亢奮、食欲增加等不良反應,需要引起臨床重視。
6.3 5-HT受體拮抗藥
5-HT受體拮抗藥選擇性強,已逐漸發展成為治療CINV的主流藥物。該類藥物通過作用于延髓第四腦室兩側閂上方的最后區、孤束核的迷走神經傳入纖維末梢和胃腸道的嗜鉻細胞,阻斷5-HT與5-HT3受體結合,阻止信號傳入嘔吐中樞和CTZ從而起到止吐作用。因此,5-HT3受體拮抗藥對胃腸嗜鉻細胞釋放5-HT所致的急性嘔吐具有強有效的止吐作用。但對遲發性嘔吐,由于存在其他機制,止吐效果不如急性嘔吐。5-HT受體拮抗藥的藥理作用強弱主要與受體親合力有關,作用持續時間則與CYP450代謝酶系和其自身的半衰期有關。由表3可知,多拉司瓊與5-HT受體結合的親合力最弱,帕洛諾司瓊最強,其它5-HT受體拮抗藥基本相似。在作用時間方面,帕洛諾司瓊最長,其它5-HT受體拮抗藥基本相似。
5-HT受體拮抗藥對心臟的不良反應應引起臨床關注,有心臟并發癥的患者使用時應慎重,或者首選格拉司瓊。恩丹司瓊有明顯的中樞神經系統(Central nervous system,CNS)不良反應,肝功能不全的患者對恩丹司瓊的代謝會受影響,使用時應調整劑量,做到劑量個體化[7]。
目前唯一的一個第2代5-HT受體拮抗藥帕洛諾司瓊已獲批用于預防中、高度致吐藥物引起的急性CINV,以及有中度致吐作用藥物引起的遲發性CINV。與第1代相比,其與受體親合力(pKi)更高,半衰期更長(見表3),有研究報道,高度的CINV患者在接受順鉑(60 mg·m-2)化療前預防性給予帕洛諾司瓊聯合地塞米松或昂丹司瓊聯合地塞米松,結果發現在治療遲發性嘔吐和整個化療周期,帕洛諾司瓊聯合地塞米松組明顯優于昂丹司瓊聯合地塞米松組[8]。此外臨床研究表明,單獨使用帕洛諾司瓊治療中度的急性或遲發性CINV比昂丹司瓊和多拉司瓊更有效[9,10]。然而,有資料表明,低血鉀或低血鎂患者、先天性QT綜合征患者、服用抗心律失常藥物或可能導致QT延長藥物的患者,及接受過高劑量蒽環類化療的患者應慎用此藥[11]。
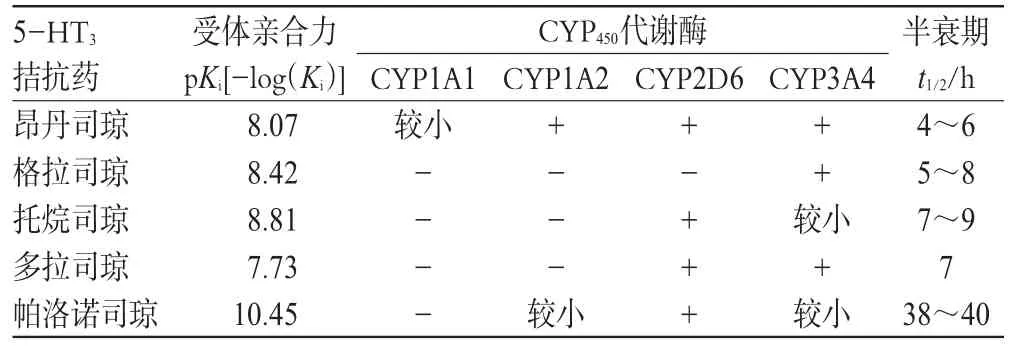
表3 5-HT受體拮抗藥藥理作用和代謝情況表
6.4 NK1受體拮抗藥
P物質是一種速激肽,存在于胃腸嗜鉻細胞、腹部迷走神經、腦干孤束核和最后區等化療嘔吐產生的關鍵部位[12],通過與NK1受體結合產生嘔吐。NK1受體拮抗藥通過與P物質競爭NK1受體而起到止吐作用。不過,NK1受體拮抗藥需進入CNS才能發揮作用,具體的作用位點尚未明確,可能的區域為孤束核、嘔吐中樞和迷走神經背側運動核[3],主要代表藥物有阿瑞吡坦(Aprepitant)、福沙吡坦(Fosaprepitant)、Casopitant。
6.4.1 阿瑞吡坦。阿瑞吡坦是第1個獲準應用于臨床的NK1受體拮抗藥。獲批適應證為與其它致吐藥物聯用以預防順鉑及/或表柔比星(HEC)等所致的急性或遲發性CINV。本品的平均絕對生物利用度為60%~65%,達峰時間約為4 h,正常進食不影響生物利用度。
單用阿瑞吡坦治療急性嘔吐效果與昂丹司瓊相當,特別是對于順鉑方案所導致的遲發性嘔吐更為有效[13]。多項研究表明,阿瑞吡坦聯合5-HT3受體拮抗藥和地塞米松使急性嘔吐控制率增加20%,遲發性嘔吐控制率增加30%~40%,這種改善能維持多個化療周期[14~16]。同時在治療中度致吐化療方案的研究中發現,在化療后的24 h內阿瑞吡坦、昂丹司瓊、地塞米松聯合方案明顯優于昂丹司瓊和地塞米松方案,但對惡心沒有改善[17]。
阿瑞吡坦耐受性良好,未見嚴重不良反應報道,但是疲勞、虛弱、呃逆的發生率更高。值得注意的是本品為中等程度的CYP3A4代謝酶抑制劑,因此在與其它主要經CYP3A4途徑代謝的藥物(匹莫齊特、特非那定、阿司咪唑和西沙必利等)合用時,應該格外慎重。此外,長期使用本品,藥物的相互作用譜可能會發生改變,因而不推薦長期持續使用。
6.4.2 福沙吡坦。福沙吡坦是阿瑞吡坦的前體藥物,為阿瑞吡坦磷酸化的注射劑型,注射該藥30 min后可在體內轉化為具有活性的阿瑞吡坦,從而發揮藥效。福沙吡坦用于不能口服的、吞咽困難的或消化功能低下的患者。其生物等效性和AUC均與阿瑞吡坦相似[13],在治療順鉑引起的嘔吐方面,福沙吡坦比昂丹司瓊更有效[14]。有研究表示,福沙吡坦的耐受劑量為150 mg。
6.4.3 Casopitant。Casopitant(GW679769)是一種哌嗪類衍化物,在速激肽、P物質和其它神經激肽介導的嘔吐方面有治療潛力。該藥能競爭性地和NK1受體結合,從而抑制P物質和NK1受體結合,通過拮抗NK1受體的活性起到止吐作用[18]。Casopitant及其去鐵胺鹽正被發展用于CINV及術后惡心、嘔吐、焦慮。Casopitant可顯著提高患者對地塞米松和昂丹司瓊的敏感性,合用后能有效提高地塞米松和昂丹司瓊對于化療引起的中、高度嘔吐反應的治療效果[19,20]。此外,目前的Ⅱ、Ⅲ期臨床研究尚未觀察到Casopitant相關的嚴重不良反應[18]。
6.5 多靶點的止吐藥物及其它止吐藥物
6.5.1 奧氮平。奧氮平是美國食品藥物管理局(FDA)批準的抗精神藥,能阻斷多巴胺神經遞質D1、D2、D3受體及5-HT神經遞質 5-HT2a、5-HT2c、5-HT3、5-HT6受體[21,22]、兒茶酚胺類神經遞質、α1-腎上腺素受體、毒蕈堿的乙酰膽堿受體和H1組胺受體等多種神經遞質,對多巴胺神經遞質和5-HT神經遞質的作用特別強,對控制急性和遲發性中、高度CINV也安全有效[23]。Ⅱ期實驗表明,奧氮平聯合地塞米松和帕洛諾司瓊在控制急性和遲發性中、高度CINV也具有一定的療效,是一種高效的止吐藥[24]。
6.5.2 大麻素類。CINV相關的大麻素類藥物主要是屈大麻酚和大麻隆,用于治療突發性和難治性的CINV,療效優于丙氯拉嗪、甲氧氯普胺、氯丙嗪、氟哌啶醇、多潘立酮、阿立必利等[25]。然而對于大麻素治療CINV的機制尚不清楚,最近有資料表明,大麻素可以通過干預腦干的大麻受體1(CB1)受體神經元可以間接影響嘔吐[26]。
6.5.3 中藥。中醫從扶正、健脾、解毒、降逆多方面著手治療化療致吐,作用日益顯著。王德山等采用止嘔合劑與昂丹司瓊對照組止吐效果比較,無顯著差異;但中藥不良反應卻遠遠小于昂丹司瓊對照組。試驗表明,中藥在防治化療致吐中具有一定的優勢。李云華等經臨床觀察證實,肺癌患者在化療時,采用昂丹司瓊、胃復安和潔白膠囊聯合應用,可以明顯降低化療引起的惡心、嘔吐癥狀。
7 總結
經過30多年的臨床實踐,約有70%的CINV已被有效地控制,特別是NK1受體拮抗藥在臨床的應用使得急性CINV的控制率提高了20%,遲發性CINV的控制率提高了30%。盡管如此,在治療CINV的過程中仍存在一些問題,主要有3方面:(1)在CINV的機制研究方面:預期性、難治性CINV的機制缺乏深入研究,使得預期性、難治性CINV目前尚未得到有效控制,這將是下一步需解決的難題。(2)在止吐藥物研究方面:傳統止吐藥物不良反應較多,已限制了其應用。5-HT3受體拮抗藥和NK1受體拮抗藥雖然療效突出,但也存在著價格昂貴、遠期不良反應尚不清楚等問題。此外目前應用于臨床的止吐藥物雖然品種較多,但高效、多靶點的止吐藥物只有奧氮平一種。(3)在治療CINV的研究方面:目前的研究主要集中在治療CINV止吐藥物的開發上,對于如通過改良化療藥物劑型,或者制成潛藥、靶向制劑從根源上降低CINV的發生的研究卻鮮有報道。總之,CINV的發生原因和機制復雜多變,只針對一兩個作用靶點很難達到治愈目的。我們只有在源頭上解決問題,比如減少化療藥物本身的不良反應從而降低CINV的發生,同步開發低毒、有效、經濟、多靶點止吐藥物,擴大CINV的治療手段才能從根本上控制各種化療所致惡心、嘔吐反應。
[1] Effective interventions for CINV:NCCNAntiemesis Clinical Practice Guidelines in Oncology[J].ONS News,2004,19(9 Suppl):17.
[2] Schwartzberg L.Chemotherapy-induced nausea and vomiting:state of the art in 2006[J].J Support Oncol,2006,4(2 Suppl 1):3.
[3] 王梅子,許建衡.化療止吐藥物的研究進展[J].汕頭大學醫學院學報,2008,21(2):123.
[4] Lohr L.Chemotherapy-induced nausea and vomiting[J].Cancer J,2008,14(2):85.
[5] 金有豫.藥理學[M].第5版.北京:人民衛生出版社,2001:263.
[6] 張開芳.格拉司瓊聯合地塞米松預防含順鉑方案化療所致惡心嘔吐的療效觀察[J].中國臨床醫學,2004,11(2):180.
[7] Longfield V.Compatibility and stability of 5-HT3receptor antagonists:a pharmacology review[J].Oncol Nurs Forum,2002,29(10):1 469.
[8] Aapro MS,Grunberg SM,Manikhas GM,et al.A phaseⅢ,double-blind,randomized trial of palonosetron compared with ondansetron in preventing chemotherapy-induced nausea and vomiting following highly emetogenic chemotherapy[J].Ann Oncol,2006,17(9):1 441.
[9] Gralla R,Lichinitser M,Van Der Vegt S,et al.Palonosetron improves prevention of chemotherapy-induced nausea and vomiting following moderately emetogenic chemotherapy:results of a double-blind randomized phaseⅢtrial comparing single doses of palonosetron with ondansetron[J].Ann Oncol,2003,14(10):1 570.
[10] Eisenberg P,Figueroa-Vadillo J,Zamora R,et al.Improved prevention of moderately emetogenic chemotherapyinduced nausea and vomiting with palonosetron,a pharmacologically novel 5-HT3 receptor antagonist:results of a phaseⅢ,single-dose trial versus dolasetron[J].Cancer,2003,98(11):2 473.
[11] 黃海輝,王東林,梁后杰.等.國產鹽酸托烷司瓊治療順鉑化療所致惡心、嘔吐的療效與安全性評價[J].中國藥房,2005,16(17):1 318.
[12] 張曉靜,張 頻.腫瘤化療所致惡心嘔吐的發生機制和藥物治療的研究進展[J].癌癥進展,2006,4(4):348.
[13] Cocquyt V,Van Belle S,Reinhardt RR,et al.Comparison of L-758 298,a prodrug for the selective neurokinin-1 antagonist L-754 030,with ondansetron for the prevention of cisplatin-induced emesis[J].Eur J Cancer,2001,37(7):835.
[14] Van Belle S,Lichinitser MR,Navari RM,et al.Prevention of cisplatin-induced acute and delayed emesis by the selective neurokinin-1 antagonists, L-758,298 and MK-869[J].Cancer,2002,94(11):3 032.
[15] Chawla SP,Grunberg SM,Gralla RJ,et al.Establishing the dose of the oral NK-1 antagonist Aprepitant forchemotherapy-induced nausea and vomiting[J].Cancer,2003,97(9):2 290.
[16] De Wit R,Herrstedt J,Rapoport B,et al.The oral NK-1 antagonist,aprepitant,given with standard antiemetics provides protection against nausea and vomiting over multiple cycles of cisplatin-based chemotherapy:a combined analysis of two randomized,placebo-controlled phase Ⅲ clinical trials[J].Eur J Cancer,2004,40(3):403.
[17] Warr DG,Hesketh PJ,Gralla RJ,et al.Efficacy and tolerability of aprepitant for the prevention of chemotherapyinduced nausea and vomiting in patients with breast cancer after moderately emetogenic chemotherapy[J].J Clin Oncol,2005,23(12):2 822.
[18] Navari RM.Casopitant,a neurokinin-1 receptor antagonist with anti-emetic and antinausea activities[J].Curr Opin Investig Drugs,2008,9(7):774.
[19] Grunberg SM,Aziz Z,Shaharyar A,et al.PhaseⅢ results of a novel oral neurokinin-1(NK-1)receptor antagonist,casopitant:single oral and 3-day oral dosing regimens for chemotherapy-induced nausea and vomiting(CINV)in patients(pts)receiving moderately emetogen-ic chemotherapy(MEC)[J].J Clin Oncol,2008,26(20 Suppl):9 540.
[20] Strausz J,Rolski J,Aziz Z,et al.PhaseⅢ results for the novel neurokinin-1(NK-1)receptor antagonist,casopitant:3-DayⅣ/oral dosing regimen for chemotherapy-induced nausea and vomiting(CINV)in patients(Pts)receiving highly emetogenic chemotherapy(HEC)[J].J Clin Oncol,2000,26(Suppl):20 585.
[21] Bymaster FP,Calligaro D,Falcone J,et al.Radioreceptor binding profile of the atypical antipsychotic olanzapine[J].Neuropsychopharmacology,1996,14(2):87.
[22] Bymaster FP,Falcone JF,Bauzon D,et al.Potent antagonism of 5-HT3and 5-HT6receptors by olanzapine[J].Eur J Pharmacol,2001,430(2~3):341.
[23] Navari RM,Einhorn LH,Loehrer PJ,et al.A phaseⅡtrial of olanzapine for the prevention of chemotherapyinduced nausea and vomiting[J].Support Care Cancer,2005,13(7):529.
[24] Navari RM,Einhorn LH,Loehrer PJ,et al.A phaseⅡtrial of olanzapine,dexamethasone,and palonosetron for the prevention of chemotherapy-induced nausea and vomiting[J].Support Care Cancer,2007,15(11):1 285.
[25] Tramer MR,Carroll D,Campbell FA,et al.Cannabinoids for control of chemotherapy-induced nausea and vomiting:quantitative systematic review[J].BMJ,2001,323(7 303):16.
[26] Martin BR,Wiley JL.Mechanism of action of cannabinoids:how it may lead to treatment of cachexia,emesis,and pain[J].J Support Oncol,2004,2(4):305.

