牛血清白蛋白對魯米諾電化學發光的增敏作用
萬明怡,周夢云,龍玉梅,嚴吉林,屠一鋒
(蘇州大學 材料與化學化工學部,江蘇 蘇州 215123)
電化學發光(ECL)分析是基于電化學反應引發的化學發光而建立起來的一種分析方法[1-3],常用的發光試劑有魯米諾、聯吡啶釕等,電化學氧化可使這些發光試劑氧化激發而發光,也可以通過氧化其它物質再與發光試劑發生化學氧化反應而發光,因此電化學發光可以有不同的發光歷程,形成多種方式的分析機理.相對于較為經典的化學發光分析法,電化學發光分析有較為顯著的優勢,化學發光分析通過試劑混合發生化學反應產生發光,因而發光過程可控性較差,一般主要通過對反應試劑流路的控制來實現對發光信號的可重復的測量,但這種流路控制技術需要有較高的自動化程度和精度,需要較為復雜和較高成本的儀器設備,而電化學發光分析由于是以電化學氧化作為發光的能量源,因此發光過程可控性好,通過施加電壓的方式來調節發光過程,可以實現在時間和空間上對發光過程的控制,測量易于實施,使用普通形式的電化學池即可實現分析目的,其靈敏度、重現性和穩定性等性能都十分優越,目前研究工作比較豐富,也已經有一定范圍的應用,作為一種高靈敏的分析檢測技術也越來越多地應用于生物體系.由于以魯米諾為發光試劑的發光體系在中性介質中的ECL較弱,因此尋找更多可靠而實用的增敏劑很有研究意義.已有文獻報道增敏劑如溶解氧[4]、H2O2[5]、氨基酸[6]及I-[7]等能增強其發光,并應用于一些生物活性分子的檢測[8].本文將報道牛血清白蛋白(BSA)對魯米諾ECL的增敏作用,實驗發現,在pH8.0的緩沖溶液中,牛血清白蛋白對魯米諾的電化學發光有較明顯的增敏作用,本研究為探索一種新方法用于測定蛋白質提供了可能,也將擴大電化學發光分析的研究和應用范圍.
1 實驗部分
1.1 實驗試劑及儀器
魯米諾購自Fluka,牛血清白蛋白(BSA)購自Sigma.實驗用水均為二次亞沸水,其它試劑均為分析純.
儀器裝置見參考文獻[9],以數字脈沖發生器為信號源,經恒電位儀施加于三電極系統,以Pt電極為工作電極,Ag/AgCl為參比電極,Pt絲為對電極.微弱光測量儀采用光電倍增管測量電化學發光信號,負高壓為800V,光電流經放大轉換后由數字化接口傳入計算機進行記錄.
電極預處理:Pt電極經拋光劑拋光、亞沸水清洗即可.
1.2 實驗條件及方法
脈沖幅值1.15V,上限電位0.85V,下限電位-0.3V;脈沖周期2s.
在電化學發光池中加入1mL待測溶液,用微量進樣器注入20μL 10-4mol/L魯米諾溶液,將電極系統置入其中并施加電壓,用微弱光測量儀檢測光強.
1.3 研究內容
1.3.1 pH值及牛血清白蛋白濃度對魯米諾電化學發光強度的影響
文獻表明蛋白質在pH=7.4左右時活性最大,pH過大或過小都容易使蛋白質失活.而魯米諾的電化學發光以在較強的堿性溶液中發光強度較大,因此測定牛血清白蛋白需要選擇一個合適的化學環境,既要使蛋白質保持活性,又要使魯米諾有足夠的發光強度,在pH6.0-10.0的緩沖溶液中測試相同濃度BSA的增敏效益,選取最佳條件.在所選定的最佳pH條件下,測定加入不同濃度BSA時魯米諾ECL強度與BSA濃度之間的關系,考察BSA對魯米諾ECL的增敏性能.
1.3.2 循環伏安法研究BSA對魯米諾氧化還原的影響
在電化學池中加入1mL含魯米諾的磷酸緩沖溶液,用微量注射器加入BSA,將電極置入其中并施加電壓,掃描循環伏安曲線,并討論兩者之間的相互作用.
2 結果與討論
2.1 BSA測定條件的選擇
由于溶液酸堿度一方面影響魯米諾的ECL強度,同時又影響BSA的活性,因此是本研究中最主要考察的影響因素.較高的pH值條件下魯米諾具有較強的ECL,產生很大的測量背景,同時也可能造成BSA的變性而失去其原有的功能;過低的pH值條件下,魯米諾所產生的ECL信號很弱,同樣對測定不利.研究中在pH6.0-10.0范圍內,檢測不同pH緩沖溶液中BSA對魯米諾電化學發光的增敏作用,結果表明在pH=8.0時BSA對魯米諾電化學發光信號增敏效果最佳,如圖1所示.因此將此pH值的磷酸鹽緩沖溶液作為研究中使用的支持電解質溶液.
2.2 BSA濃度與發光強度的關系
在pH=8.0的磷酸鹽緩沖溶液中,不同濃度BSA對魯米諾電化學發光的影響見圖2.隨著BSA濃度的增加,ECL信號增強,在BSA濃度達到1.2×10-8g/mL時,ECL達到信號最強.隨后濃度增加信號減弱,這可能是由于BSA為生物大分子,濃度過高時可能會發生散射,導致ECL強度降低.
2.3 BSA對魯米諾氧化還原行為的影響
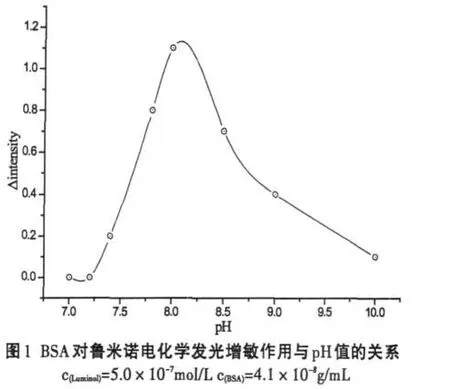
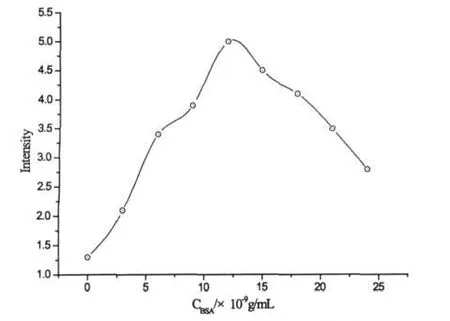
圖2 不同濃度BSA對魯米諾電化學發光的影響c(Luminol)=2.0×10-6mol/L
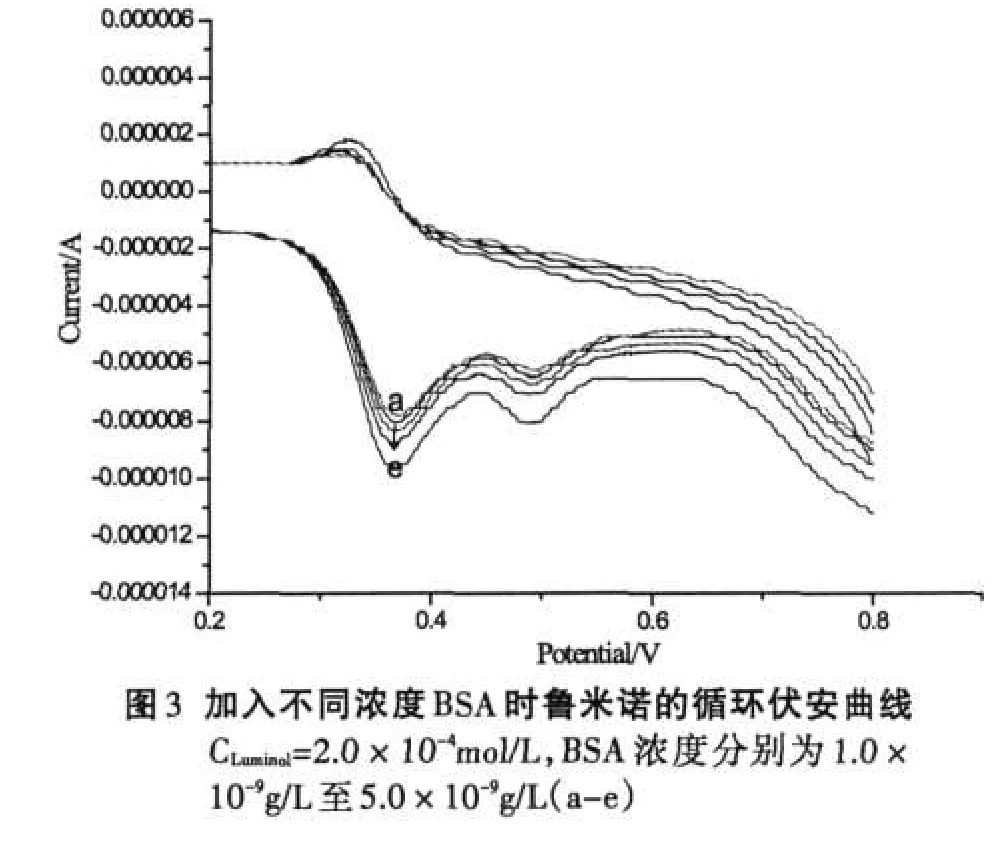
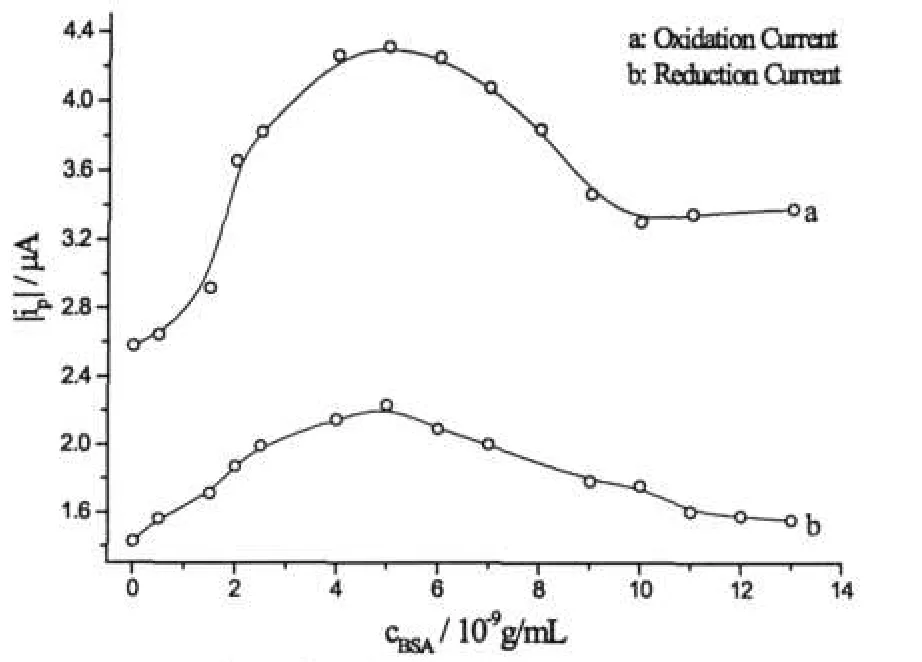
圖4 BSA濃度對魯米諾氧化還原峰電流的影響c(Luminol)=2×10-4mol/L
采用循環伏安法研究BSA存在時魯米諾的氧化還原行為有助于理解BSA增敏魯米諾ECL的原因,當在魯米諾溶液中加入較低濃度BSA時,可以明顯觀察到魯米諾的氧化還原電流增大,其循環伏安曲線見圖3,但峰電位及形狀未發生變化,表明其電化學行為未發生任何變化,只是氧化還原反應發生的程度有所提高.但隨著BSA濃度的增加,魯米諾的氧化還原峰電流又趨于減小,圖4所示為魯米諾氧化還原峰電流隨BSA濃度的變化.
由圖3、4可以看出,魯米諾的氧化還原峰電流隨著BSA濃度的增加而增加,但當加入BSA的濃度過大時,氧化還原峰電流又會逐漸減小.上述實驗盡管在測定中由于靈敏度等因素而選擇使用不同的魯米諾濃度,因此BSA對魯米諾的ECL或CV行為產生影響的濃度上略有差異,但表現出的規律是一致的,即低濃度BSA的加入無論對魯米諾的電化學氧化還原還是電化學發光都具有明顯的促進作用,而當BSA濃度較大時,這種促進作用逐步減弱.
在上述條件下,在BSA濃度為1.00×10-9~1.20×10-8g/mL的范圍內,魯米諾的電化學發光強度和BSA的濃度成線性關系,線性方程為I=0.87+0.37CBSA,r=0.9941,這為利用魯米諾的ECL測定蛋白質提供了一種靈敏的新方法.
3 機理討論及結論
由上述實驗結果可知,在pH8.0的磷酸緩沖溶液中,BSA對魯米諾的電化學氧化還原過程表現出了一定程度的促進作用,但這種促進作用并不改變魯米諾的氧化還原機理,因此可以推測為當在魯米諾溶液中加入一定濃度BSA時,魯米諾分子被吸附于BSA表面,同時由于BSA在電極上有一定的吸附性,從而使電極表面對魯米諾發生一定程度的富集,使魯米諾的電化學氧化還原得以增強,同時,由于魯米諾的ECL過程是基于魯米諾的氧化激發,因此電極表面有更多魯米諾發生氧化時,其激發態的數量也相應增加,從而導致ECL強度的增強.而當BSA濃度進一步增加時,BSA分子間可能發生聚合,則上述由于吸附引起的對魯米諾的氧化還原的促進作用減弱,同時由于BSA聚合體體積增大、數量增加,溶液的散射程度也會增加,導致所檢測到的ECL強度逐步減小.該研究為測定蛋白質提供了一個新方法,同時也擴大了電化學發光分析的應用范圍.
[1]尹學博,楊秀榮,汪爾康.毛細管電泳-電化學/電化學發光及其微芯片技術[J].化學進展,2005,17(2):181-185.
[2]張成孝,漆紅蘭.電化學發光分析研究進展[J].世界科技研究與發展,2004,26(4):7-13.
[3]混旭,章竹君.納米粒子修飾電極電化學發光傳感器的研究進展[J].陜西師范大學學報,2009,37(5):56-66.
[4]黃炳強,郭文英,徐揚,等.溶解氧對魯米諾電化學發光的增強效應研究[J].光譜學與光譜分析,2003,23(5):849-851.
[5]Sakura S.Electrochemiluminescence of hydrogen peroxide-luminol at a carbon electrode[J].Anal Chim Acta,1992,262:49-57.
[6]儲海虹,郭文英,狄俊偉,等.半胱氨酸對魯米諾電化學發光的增敏作用[J].分析科學學報,2005,21(6):676-678.
[7]Seitz W R,Hercules D M.Quantitative study of chemiluminescence from the iodine-luminol reaction[J].J Am Chem Soc,1974,26:4094-4098.
[8]Tu Y F,Qi Y Y,Wu Y,et al.Quenching electrochemiluminescential analysis of pico-molar level glutathione[J].Chem J Internet,2003,5(12):97.
[9]屠一鋒,郭文英,黃炳強,等.影響魯米諾體系電致化學發光因素的研究[J].光譜實驗室,2001,18(2):185-188.

