鼻咽癌調(diào)強(qiáng)放療劑量驗證的探討
陳開強(qiáng),柏朋剛,張秀春,李奇欣
(福建省腫瘤醫(yī)院 放療科,福建 福州 350014)
0 前言
隨著計算機(jī)技術(shù)的飛速發(fā)展和直線加速器等醫(yī)療設(shè)備的不斷改進(jìn),IMRT(調(diào)強(qiáng)適形放療)這一技術(shù)日趨完善成熟,但它是目前一項較復(fù)雜的放療技術(shù),有關(guān)它的質(zhì)量保證和質(zhì)量控制是一個急需解決和必須重視的問題,其中劑量學(xué)驗證是極其重要的一方面。調(diào)強(qiáng)放療的劑量學(xué)驗證方法很多,主要有膠片法、MAPCHECK法、MATRIXX法等[1-4]。本文使用MAPCHECK進(jìn)行調(diào)強(qiáng)驗證,它是一種二維半導(dǎo)體探測器陣列,常用于驗證調(diào)強(qiáng)放療計劃二維面劑量分布。
1 資料與方法
1.1 一般資料
30例鼻咽癌患者行CT定位掃描。
1.2 儀器設(shè)備
定位CT掃描采用ASTCION-VF系列全身螺旋CT機(jī)(日本TOSHIBA公司),配置CT SIM激光系統(tǒng)(美國Gammex RIM公司),并采用PRECISE帶有40對多葉光柵(MLC)的直線加速器(瑞典ELEKTA公司),同時使用PLATO三維治療計劃系統(tǒng)(荷蘭核通公司),MAPCHECK驗證系統(tǒng)(美國SUN NUCLEAR公司),固體水模(SOLID WATER),WELLHOFER DOSE1劑量儀,0.6cm3指型電離室。
1.3 方法
1.3.1 固體水模體CT模擬定位
模體為30cm×30cm×30cm的固體水模板,驗證模體進(jìn)行CT掃描時,在其中央插杠處置入一根0.6 cm3FARMER型電離室,距離表面深度為5cm,該電離室每年送國家劑量院校正一次。按照測量位置擺放,在模體上貼上三個標(biāo)記點,對準(zhǔn)激光,CT掃描層厚為3mm。將模體CT斷層影像傳輸至PLATO計劃系統(tǒng),
1.3.2 QA計劃生成
模體CT圖象傳入治療計劃系統(tǒng)后,將臨床醫(yī)生確認(rèn)的30例鼻咽癌患者治療計劃(患者同樣需要CT模擬定位)移植到模體,計劃采取均分布野(7野)。機(jī)架角全部改為0,計算后將驗證計劃傳至加速器,并分別計算出每個調(diào)強(qiáng)射野在模體中的劑量分布,選擇模體中感興趣的面劑量分布,從計劃系統(tǒng)中傳至MAPCHECK驗證軟件系統(tǒng)。
1.3.3 驗證方法
將MAPCHECK(多序列平面劑量儀)面板放在加速器床上,中心十字線與加速器光野十字線對齊,為了保證探頭處的等校深度為5cm,必須在MAPCHECK面板上放置一塊3cm的固體水模板,調(diào)用模體驗證計劃數(shù)據(jù)進(jìn)行模擬照射,每野執(zhí)行一次,分別測量出實際的感興趣的面劑量分布,與計劃系統(tǒng)計算結(jié)果想比較,驗證相對劑量和絕對劑量。驗證絕對劑量時,必須進(jìn)行加速器劑量標(biāo)定,用DOSE1劑量儀和0.6 cm3電離室對10cm×10cm照射野、源皮距100cm、加速器預(yù)設(shè)100MU對加速器進(jìn)行劑量輸出校準(zhǔn),以消除加速器自身劑量輸出波動造成的影響。
2 結(jié)果
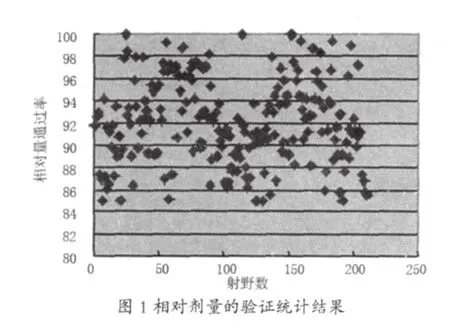
采用DTA(distance-to-agreement,距離符合度)分析方法,AAPM 53#報告建議劑量位置誤差限定為3%/3mm或3%/4mm[5]。我院采取3%/3mm標(biāo)準(zhǔn),圖1、圖2給出了調(diào)強(qiáng)計劃的所有射野在模體中的相對劑量和絕對劑量的驗證統(tǒng)計結(jié)果,在相對劑量方面,通過率在85%~100%之間;絕對劑量方面,通過率在80.7%~100%。
3 討論
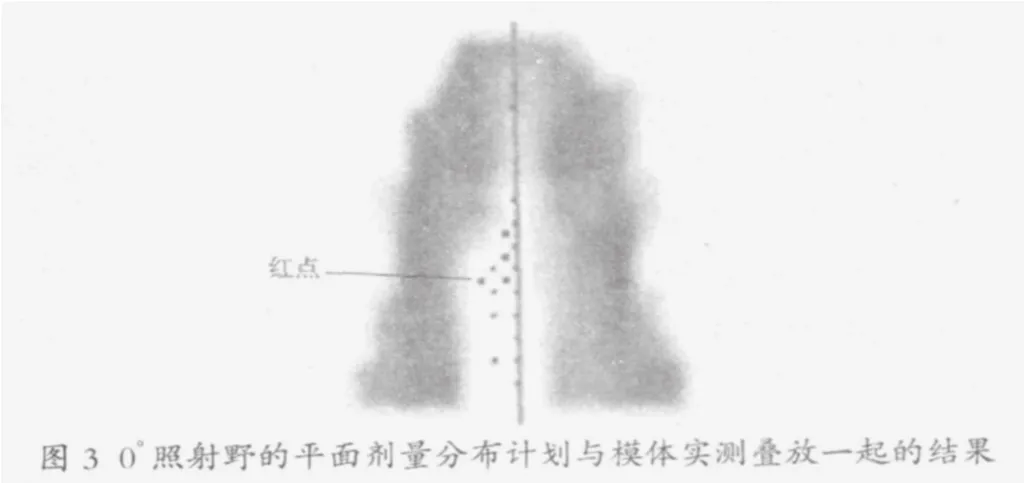
絕對劑量和相對劑量驗證是實施IMRT治療過程中的可靠保證,是目前國內(nèi)外調(diào)強(qiáng)放療劑量驗證普遍采用的基本劑量驗證方法。2005年以來,我院鼻咽癌患者主要在PLATO治療計劃系統(tǒng)上進(jìn)行計劃設(shè)計,此系統(tǒng)不能直接限制總子野數(shù)、最小子野MU、最小子野面積等計劃參數(shù),而這些參數(shù)在加速器下輸出的穩(wěn)定性將直接影響劑量的準(zhǔn)確性。Sharpe等[6]報道當(dāng)子野為1cm×1cm時,如果MLC葉片位置誤差為2mm,吸收劑量就會相差16%,為1mm時相差8%。限于篇幅,圖3給出一例患者0°照射野的平面劑量分布計劃與模體實測疊放一起的結(jié)果,圓點為實測誤差點,其中紅色圓點代表實測值高于TPS計算的點,從圖3中可看出,高劑量區(qū)(即腫瘤靶區(qū))TPS(腫瘤治療計劃系統(tǒng))計算值與實測值相當(dāng)接近,低劑量區(qū)(腫瘤靶區(qū)邊緣或以外)則有一定偏差,考慮為MLC葉片間的漏射或小子野及小跳數(shù)野的輸出誤差。我們認(rèn)為這就是我院驗證結(jié)果中某些點的劑量通過率在90%以下的原因。
對于絕對劑量通過率的結(jié)果分析,我們認(rèn)為作為平面測量劑量儀,MAPCHECK在IMRT絕對劑量測量方面,不如單個電離室有優(yōu)勢,因此在絕對劑量測量中,為了提高測量的準(zhǔn)確性,使用單個電離室在模體中模擬測量方法。我院柏朋剛等[7、8]利用0.6 cm3指型電離室實際測量模體中感興趣點與TPS點的劑量比較,得出絕對誤差在0.06%~3.38%,平均誤差在1.72%,這符合臨床上最大誤差控制在5%的要求。國內(nèi)外眾多文獻(xiàn)報道[9]使用0.15 cm3電離室驗證更加精確。
MAPCHECK是一種快速的劑量測量系統(tǒng),可以在短時間內(nèi)獲得大量照射野劑量方面的信息,能較好地驗證TPS與實際測量的準(zhǔn)確性,并且簡單易行,極大地簡化了驗證工作量,國內(nèi)外已逐漸取代電離室加膠片的組合驗證方法。因此MAPCHECK在IMRT質(zhì)量控制和質(zhì)量保證中可以作為一種常規(guī)的測量工具進(jìn)行使用。
[1]張曉軍,王建華,涂或.二維電離室矩陣在調(diào)強(qiáng)適形放療劑量學(xué)驗證中的應(yīng)用[J].國際放射醫(yī)學(xué)核醫(yī)學(xué)雜志,2007,31(5):318-320.
[2]鄒華偉,賈明軒,吳榮,等.調(diào)強(qiáng)適形放射治療計劃劑量學(xué)的驗證[J].中華放射與防護(hù)雜志,2004,24(3):256-258.
[3]Daniel Letourneau,Misbah Gulam,Di Yan,et al.Evaluation of a 2D diode array for IMRT quality assurance[J].RADIOTHERAPY &ONCOLOGY,2004,70:199-206.
[4]賈明軒,紀(jì)天龍,張梁.Seven29TM二維電離室矩陣劑量學(xué)的評價[J].中華放射腫瘤學(xué)雜志,2009,18(1):65-68.
[5]Fraas b,Doppke k,Hunt m,et al.American Association of Physicsts in Medicine Radiation Therapy Committee Task Group 53:quality assurance for clinical radiotherapy treatment planning[J].Med Phys,1998,25:1773-1829.
[6]Sharpe MB,Miller BM,Yan d,et al.Monitor unit settings for intensity modulated beams delivered using a step-and-shoot approach[J].Med Phys,2000,27:2719-2725.
[7]柏朋剛,張秀春,潘建基,等.靜態(tài)調(diào)強(qiáng)適形放射治療設(shè)計及劑量驗證分析[J].福建醫(yī)科大學(xué)報,2006,40(3):248-250.
[8]周一兵.整體擋鉛適形治療方法及劑量驗證[J].中國醫(yī)療設(shè)備,2008(6):17-18.
[9]謝耩,王運(yùn)來,馬林,等.電離室靈敏體積對調(diào)強(qiáng)放射治療劑量學(xué)驗證準(zhǔn)確性的影響[J].中華放射醫(yī)學(xué)與防護(hù)雜志,2007,27(6):582-584.

