高溫熔鹽的熱物性測試及熱穩定性分析*
胡寶華,丁 靜,魏小蘭,彭 強,廖 敏
(1.中山大學工學院,廣東廣州 510006;2.華南理工大學化學與化工學院)
高溫熔鹽的熱物性測試及熱穩定性分析*
胡寶華1,丁 靜1,魏小蘭2,彭 強1,廖 敏2
(1.中山大學工學院,廣東廣州 510006;2.華南理工大學化學與化工學院)
為滿足太陽能高溫傳熱、蓄熱的要求,以價格便宜的氯化物為原料,通過靜態熔融的方法配制出新型混合熔鹽,并采用熱重差熱聯用熱分析儀及其他實驗手段對熔鹽的熔點、相變潛熱及熱穩定性進行了表征。實驗結果表明:氯化物的混合熔鹽具有較低的熔點,合適的潛熱值及高溫下良好的熱穩定性的特點。氯化物熔鹽的適宜使用溫度在 550~800℃。該實驗研究為氯化物熔鹽在太陽能高溫利用中的使用提供了寶貴數據。
熔鹽;太陽能;氯化物
無機物熔融鹽 (簡稱為熔鹽)具備使用溫度范圍廣、導熱系數大、黏度低及與金屬材料有良好相容性的特點,是一種理想的高溫傳熱蓄熱介質。國外對混合熔融硝酸鹽進行了深入研究,證明兩種混合硝酸鹽 Solar Salt與 Hitec非常適合聚光太陽能高溫熱發電的使用[1-4]。目前使用的高溫熔鹽的溫度上限為 600℃,一旦溫度超過使用上限,則熔鹽開始變得不穩定[5],會發生緩慢的反應,并放出氣體,使混合物的熔點升高甚至導致熔鹽的變質。因此,隨著工業中加熱需求溫度的不斷升高,對于塔式太陽能熱發電和聚光太陽能熱化學利用如熱解制氫等需要更高溫 (600~800℃)的情況下,混合硝酸鹽就不能滿足要求,必須尋求一種使用溫度更高、穩定性能更好的高溫熱載體。筆者參照相圖數據,以價格便宜、高溫下性質穩定的氯化物為原料,通過靜態熔融的方法制備出一種新型混合熔鹽,然后通過熱重差熱聯用分析儀及其他實驗手段對混合熔鹽的熔點、潛熱及熱穩定性進行表征,以尋求氯化物混合熔鹽的最適宜使用溫度。
1 實驗部分
1.1 實驗原料及儀器
氯化鈉、無水氯化鈣,均為分析純。
混合熔鹽的熔點、相變潛熱和比熱在 SDT Q600熱重差熱聯用熱分析儀 (美國 TA公司)上測定。熔鹽持續高溫和循環熱穩定性在程序控溫的 SX-4-10型箱式電阻爐 (天津市泰斯特儀器有限公司)中進行,相應的溫度數據用安裝在 PC機上的昆侖工控軟件 (MCGS)采集。熔鹽質量用 TB-114型電子天平 (美國丹佛儀器有限公司,精度為 0.1 mg)稱量。熱分析、持續高溫和熱循環實驗所用容器為氧化鋁坩堝。熔鹽持續高溫和熱循環前后的化學穩定性用 D/Max-II IA型粉末 X射線衍射儀 (日本理學電機,功率為 3 kW;測角范圍為 1~120°;靈敏度為3%~5%;測角精度為 ±0.002°)確定。
1.2 混合熔鹽的制備
按照比例稱量經過干燥處理后的各種組分鹽,研磨并充分混合。混合鹽放在馬弗爐中加熱(700℃)至熔化狀態并保持 3 h,使之形成均一液體。最后熔鹽自然冷卻到室溫,粉碎后得到熔鹽樣品,干燥密封保存。
1.3 熔點、相變潛熱等熱物性測定
混合熔鹽的熔點、相變潛熱及高溫穩定性用熱重 -差熱 (TG-DSC)聯用分析儀測定。測定用熔鹽約 10 mg,在氮氣中進行,氮氣流量為100 mL/min,溫度范圍為 30~900℃,升溫速度為20 ℃/min。
1.4 熱穩定性分析
熔鹽的熱穩定性可以從 5個方面進行評價:1)微量熔鹽的熱重分析。10 mg熔鹽的熱重曲線開始下降處的溫度,就是熔鹽的最高使用溫度。2)多量熔鹽的質量損失率曲線分析。把盛有 30 g熔鹽的氧化鋁坩堝放入馬弗爐內,恒溫加熱一段時間后取出冷卻稱量,用質量損失對時間作圖即得到該溫度下熔鹽的質量損失率。改變恒溫溫度,重復實驗,可得到不同溫度下的質量損失率曲線。根據質量損失率曲線下降情況可判斷多量樣品的最高使用溫度。該溫度一般比微量分析得到的溫度高。3)熱循環儲放熱分析。把 30 g熔鹽放在馬弗爐內從 400℃程序升溫 120 min到 650℃,再經 120 min降到400℃,多次重復循環。利用工控軟件 (MCGS)每5 s在線采集坩堝內熔鹽的一個溫度數據。10個周期后,以溫度對熔鹽循環時間作圖,得到熔鹽的冷熱循環曲線。穩定的熔鹽在多次升降溫的過程中應該保持熔化溫度和凝固溫度基本不變。4)持續高溫和熱循環前后的組成變化。測定熔鹽在持續高溫和熱循環前后的 XRD圖,比較它們的變化。穩定的熔鹽在持續高溫和熱循環前后的 XRD圖基本不變,不會出現表征新物質的衍射峰。
2 結果與討論
2.1 熔鹽的熱物性
圖 1為混合熔鹽的 TG-DSC曲線。從圖 1可知,在 100℃之前出現混合熔鹽物理吸附水的脫水峰,大約 100~200℃是熔鹽化學吸附水的脫水峰,說明熔鹽容易吸收空氣中的水。在后續的質量損失研究中 TG曲線在 150℃之后轉入平穩狀態直到800℃,說明熔鹽沒有質量損失。但 DSC曲線在200~497.67℃持續下降,說明固體熔鹽的比熱可能隨溫度升高而下降,直到 497.67℃時曲線出現明顯的吸熱,說明熔鹽在該溫度下熔化,即熔鹽的熔點為 497.67℃,該數據比文獻值 500℃[6]略小。混合熔鹽在熔化的相變過程中吸收一定熱量,計算可得相變潛熱為 86.85 J/g。繼續升溫,熔鹽的 DSC曲線隨溫度升高而升高,說明液體熔鹽的比熱隨溫度升高而增大,該現象對液體熔鹽用作傳熱介質十分有利。從 TG曲線可知,熔鹽在大約 800℃開始出現質量減少,說明混合熔融鹽在 498~800℃十分穩定,可以用作傳熱介質。考慮到熔鹽的使用溫度應該比熔點高 50℃,由此可見熔鹽的最佳使用溫度為550~800℃。
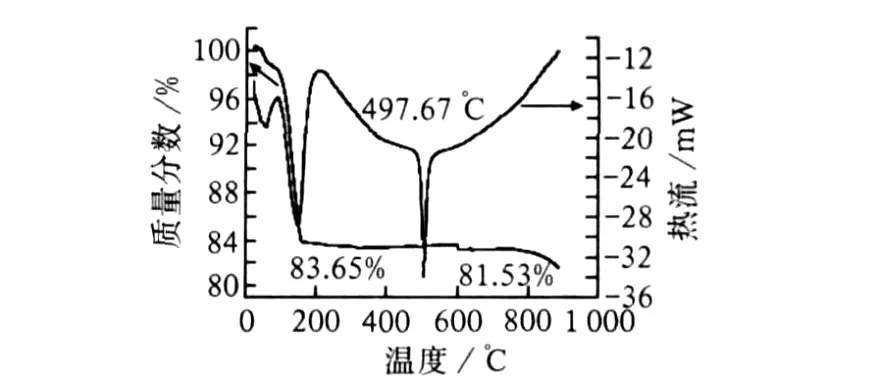
圖 1 混合熔鹽的 TG-DSC曲線
2.2 熱穩定分析
氯化物熔鹽雖然不像硝酸鹽和碳酸鹽熔鹽那樣在高溫下存在熱分解反應,但是文獻 [7]顯示熔融態的氯化物在高溫下體現出較高的蒸汽壓,因此有必要對氯化物熔鹽的高溫熱穩定性進行研究。
2.2.1 熔鹽在高溫下的質量損失
TG測試過程中熔鹽的質量在 3~10 mg,并且有 N2作為載氣流過,造成熔鹽損失偏大;而恒溫質量損失實驗的熔鹽在 30 g左右,處于靜態空氣馬弗爐環境中,和熔鹽作為傳熱蓄熱工質的環境類似,因此質量損失數據比較可靠。圖 2為熔鹽恒溫質量損失曲線。圖 2結果表明:熔鹽在 800℃下比較穩定,850℃以上出現明顯的質量損失,說明熔鹽開始變得不穩定。這一結論與 TG-DSC測定的結果一致。
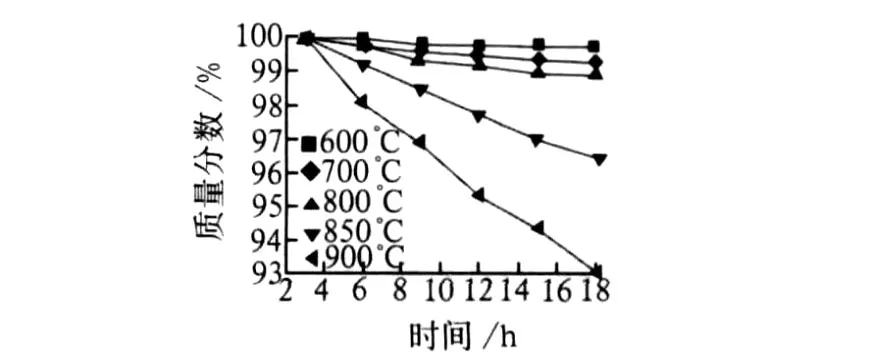
圖 2 熔鹽恒溫質量損失曲線
2.2.2 熔鹽蓄放熱性能實驗
熔鹽作為一種高溫傳熱蓄熱介質,在應用過程中也必須考慮材料抵抗溫度變化的能力,氯化物熔鹽在溫度緩慢變化下的蓄放熱性能實驗能夠很好地反應這種能力。
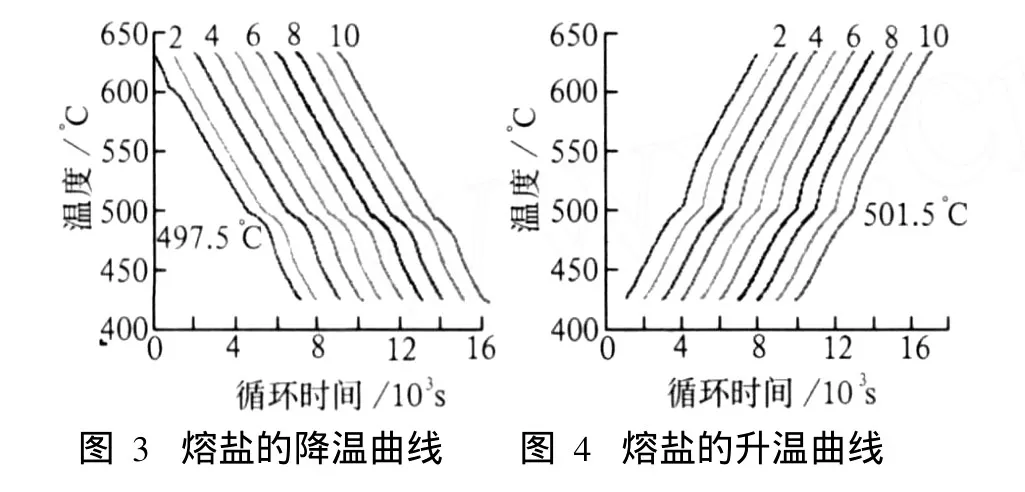
圖 3和圖 4分別為熔鹽的降溫和升溫曲線。由圖 3和圖 4可知,熔鹽在循環 10個周期之后,凝固和熔化溫度基本保持不變。凝固溫度為 497.5℃,與DSC測試熔點 497.67℃比較接近。熔化溫度為501.5℃,熔鹽熔化和凝固溫差為 4℃,過冷現象不明顯,熔鹽在用作傳熱介質時需要注意保溫,以防熔鹽在管道中凝結堵塞管道造成事故。
2.2.3 熔鹽在高溫下的化學穩定性
圖 5為熱循環 10次及高溫 50 h后熔鹽的 XRD曲線對比。由圖 5知,熱循環 10次后熔鹽材料的XRD譜圖與原始熔鹽圖形類似,沒有出現表征新物質產生的衍射峰,說明材料在熱循環中熔鹽組成基本沒有變化。熔鹽持續高溫 (800℃)50 h后,在XRD圖箭頭所指的位置出現新峰,查圖譜,與 AlCl3的峰值較接近,說明熔鹽與氧化鋁坩堝發生了反應。
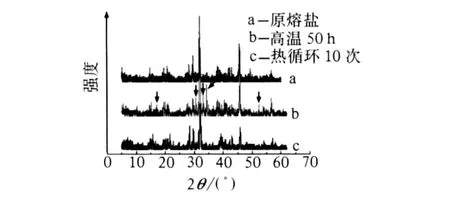
圖 5 熱循環 10次及高溫 50 h后熔鹽的 XRD曲線對比
3 結論
1)通過靜態熔融法制備了混合熔鹽,混合熔鹽的熔點比純鹽的更低。2)混合熔鹽的熔點為497.67℃,相變潛熱為 86.85 J/g,最高操作溫度為800℃。3)所制混合熔鹽具有持續高溫和高低溫熱循環穩定性。4)混合熔鹽作為高溫傳熱蓄熱介質的使用溫度范圍是 550~800℃,滿足太陽能超臨界發電和規模化制氫的溫度要求。
[1] Kearney D,Herrmann U,Nava P,et al.Assess ment of a molten heat transfer fluid in a parabolic trough solar field[J].Journal of Solar Energy Engineering,2003,125(2):170-176.
[2] Herrmann U,Kelly B,Price H.Two-tank molten salt storage for parabolic trough solar power plants[J].Energy,2004,29(5/6):883-893.
[3] Kearney D,Kelly B,Herr mann U,et al.Engineering aspects of a molten salt heat transfer fluid in a trough solar field[J].Energy,2004,29(5/6):861-870.
[4] Brosseau D,Kelton J W,Ray D,et al.Testing of thermocline filler materials and molten-salt heat transfer fluids for thermal energy storage systems in parabolic trough power plants[J].Journal of Solar Energy Engineering,2005,127(1):109-116.
[5] Bradshaw RW,MeekerD E.High-temperature stabilityof ternary nitrate molten salts for solar thermal energy systems[J].Solar EnergyMaterials,1990,21(1):51-60.
[6] Janz G J,Allen C B,Bansal N P,et al.Physical properties data compilations relevant to energy storage.Molten salts:data on single and multi-component salt systems-Ⅱ(18181)[M].New York:Molten Salts Data Center,Cogs well Laboratory,Rensselaer Polytechnic Insititute,1976:285.
[7] LideD R.Handbook of chemistry and physics[M].84th ed.America:CRC PressLLC,2004.
Test of thermal physics and analysis on thermal stability of high temperature molten salt
Hu Baohua1,Ding Jing1,Wei Xiaolan2,PengQiang2,Liao Min2
(1.School of Engineering,Sun Yat-sen University,Guangzhou510006,China;
2.School of Chem istry and Chem ical Engineering,South China University of Technology)
To meet the requirement of high temperature solar heat transfer and ther mal storage,a new kind of molten saltwith cheap chloride as raw materialwas prepared by a statically molten method.Its melting point,latent heat of phase change,and ther mal stabilitywere characterized by TG-DSC and other experimentalmethods.Results showed that the chloride-molten saltmixture has low melting point,proper latent heat value,and preferable ther mal stability at high temperature.The optimum using temperature of chloridemolten saltwas between 550℃and 800℃.This experimental research provided valueable data,which were useful to the application of chloride molten salt in high temperature solar energy utilization.
molten salt;solar;chloride
TQ124.42
A
1006-4990(2010)01-0022-03
國家高技術研究發展計劃項目 (國家“863”項目)(2006AA050103-2);廣州市科技計劃項目 (2008Z1-D571)。
2009-07-10
胡寶華 (1984— ),男,在讀碩士,主要從事太陽能高溫熔鹽材料的研究。
聯系方式:hubaohua@mail2.sysu.edu.cn

