利莫那班對局灶性腦缺血/再灌注損傷大鼠的保護作用
樂樂樂 董 志
(重慶醫科大學藥學院藥理教研室 重慶市生物化學與分子藥理學重點實驗室,重慶 400016)
利莫那班對局灶性腦缺血/再灌注損傷大鼠的保護作用
樂樂樂 董 志
(重慶醫科大學藥學院藥理教研室 重慶市生物化學與分子藥理學重點實驗室,重慶 400016)
目的 探討大麻素1(CB1)受體拮抗劑利莫那班對大鼠局灶性腦缺血/再灌注損傷的保護作用。方法 線栓法制備大鼠局灶性腦缺血/再灌注模型。36只雄性大鼠隨機分為假手術組、手術組、尼莫地平對照組、利莫那班低劑量組、中劑量組和高劑量組。再灌注24 h后進行神經功能評分(NFS),TTC染色測定梗死面積,HE染色檢測腦組織病理變化,免疫組化染色觀察P-erk1/2和caspase-3免疫陽性表達,并檢測大鼠腦組織勻漿中超氧化物歧化酶(SOD)和丙二醛(MDA)變化。結果 利莫那班能明顯改善大鼠的神經行為,縮小梗死面積,并使腦組織病理改變減輕,SOD活性明顯升高,MDA含量明顯降低,下調caspase-3的表達,上調P-erk1/2的表達。結論 利莫那班對局灶性腦缺血/再灌注大鼠有明顯的保護作用,其機制可能與拮抗大麻素受體、抑制細胞凋亡有關。
利莫那班;局灶性腦缺血/再灌注超氧化物歧化酶;丙二醛;半胱氨酸酶-3
缺血性腦血管疾病是嚴重的神經疾病,常見于中年以上的人群,嚴重者可發生意識障礙和肢體障礙。尋找有效的治療藥物,促進中樞神經系統功能恢復,一直是相關學科研究的重點。選擇性大麻素1(CB1)受體拮抗劑利莫那班直接作用于中樞神經系統,臨床上用于改善超重或肥胖者心血管病代謝危險因素〔1〕。但是對于利莫那班其他可能潛在的療效,國內外的文獻報道不多,其機制的研究更少。本實驗通過模擬局灶性腦缺血再灌注損傷模型,研究利莫那班對腦缺血損傷的保護作用并初步探討其作用機制。
1 材料與方法
1.1 材料
1.1.1 動物 清潔級Sprague-Dawley雄性大鼠,體重200~240 g,鼠齡3~4個月,由重慶醫科大學實驗動物中心提供,動物合格證號:SCXK(渝)2009-0001。
1.1.2 藥品與試劑盒 利莫那班,鄭州荔諸生物科技有限公司;紅四氮唑(TTC),中國醫藥上海化學試劑總廠;超氧化物歧化酶(SOD)試劑盒、丙二醛(MDA)試劑盒,南京建成試劑公司;半胱氨酸酶-3(caspase-3)、P-erk多克隆抗體,Bioworld Technoiogy;其余試劑均為國產分析純。
1.2 方法
1.2.1 分組與給藥 成年健康雄性SD大鼠36只,隨機分為6組(n=6),飼養于實驗室內,自由進食及飲水,讓其適應環境3 d。手術前1 d禁食禁水。①假手術組:分離頸總動脈(CCA)、頸內動脈(ICA)和頸外動脈(ECA),線栓插入約10 mm;②局灶性腦缺血/再灌注組:線栓法制備;③藥物組:局灶性腦缺血/再灌注 +利莫那班(5、10、20 mg/kg)組;④對照組:局灶性腦缺血/再灌注+尼莫地平(1 mg/kg)。藥物利莫那班用二甲基亞砜配置,于手術前30 min腹腔注射,假手術組及手術組于手術前30 min腹腔注射二甲基亞砜。
1.2.2 腦缺血/再灌注模型的制備 采用Longa等〔2〕的方法制備局灶性腦缺血/再灌注模型。給藥30 min后,腹腔注射3.5%水合氯醛(0.1 ml/kg)麻醉。仰臥位固定在手術板上,頸正中切口,鈍性分離皮下組織和肌肉,暴露左側的血管和神經,分離出CCA、ICA和ECA。結扎CCA的近心端和ECA,用動脈夾夾閉ICA,并在CCA上剪開一小口,插入線栓,松開夾住ICA的動脈夾,將線栓緩緩向顱內推進,約18 mm處感覺到輕微阻力即可。將線栓和ICA結扎固定,逐層縫合肌肉和皮膚。2 h后拔出線栓造成血流再灌注模型。假手術組分離CCA、ICA和ECA,線栓插入約10 mm,其余同上。
1.2.3 神經功能缺損評分 大鼠缺血/再灌注24 h后,按照Zea-longa系統進行神經功能缺損評分。標準如下:0分,無神經功能缺損癥狀;1分,不能完全伸展左側前爪,輕度神經功能損傷;2分,向左側轉圈,中度局灶性神經功能缺損;3分,行走時向左側傾倒,重度局灶性神經功能缺損;4分,不能自發行走,意識昏迷。
1.2.4 腦梗死容積百分比 神經功能缺損評分后,立即將大鼠斷頭取腦,取出小腦、嗅球。于-20℃冰箱中速凍20 min,冠狀切面,第一刀在腦前極與視交叉連線中點處;第二刀在視交叉部位;第三刀在漏斗柄部位;第四刀在漏斗柄與后葉尾極之間。將五片切片置于2%TTC溶液中,用錫箔紙蓋住避光,放入37℃溫箱15~30 min,不時翻動腦片,均勻接觸到染色液。取出觀察并拍照,采用圖像處理軟件(ADOBEPHOTOSHOP 7.0)計算梗死面積(粉紅色區為正常腦組織,白色區為梗死區)。腦梗死容積百分比=梗死面積之和×2/正常大腦半球容積。
1.2.5 SOD活性和MDA含量變化 神經功能損傷評分后,斷頭取腦,切取左側大腦,稱重,用0.9%生理鹽水制成1%的腦組織勻漿液,離心3 500 r/min×15min,取上清液,-20℃保存。根據試劑盒說明書測定SOD活性及MDA含量。
1.2.6 蘇木素-伊紅(HE)染色 神經功能損傷評分后,經左心室緩慢注入生理鹽水100 m l,血液和灌注液從右心耳流出,再緩慢注入4 g/L多聚甲醛的磷酸鹽緩沖液200 ml進行固定。斷頭取腦,冠狀位切取前囟及其后約4 mm處的腦組織放于4%多聚甲醛溶液中固定過夜,石蠟包埋,切片,染色,觀察基底節和海馬神經元形態變化。
1.2.7 免疫組織化學染色 神經功能損傷評分后,載體灌流,斷頭取腦,冠狀位切取前囟及其后約4 mm處的腦組織放于4%多聚甲醛溶液中固定過夜,石蠟包埋,切片,按試劑盒說明書采用SABC法進行免疫組化染色。
1.3 統計學分析 應用SPSS11.5統計軟件進行分析,數據以±s表示,組間比較采用T檢驗。
2 結果
2.1 神經功能缺損評分 經利莫那班處理的大鼠神經行為學明顯改善,且呈劑量依賴性。與假手術組比較,手術組大鼠神經功能評分(3.68±0.17)明顯升高(P<0.001),說明大鼠出現腦損傷,模型建立成功;與手術組比較,利莫那班高劑量組神經功能評分(2.45±0.10)明顯降低(P<0.05),而利莫那班中、低劑量組大鼠神經功能評分與手術組比較無顯著差異(P>0.05),分別為(3.57±0.08,3.65±0.11);與尼莫地平對照組(2.38±0.09)相比,利莫那班高劑量組無顯著差異(P>0.05)。
2.2 腦梗死容積百分比 大鼠腦缺血/再灌注24 h后均出現不同程度的缺血梗死。腦梗死容積百分比利莫那班高劑量組為34.76%,明顯小于中劑量組(41.85%)和低劑量組(57.96%)(P<0.05),大于對照組(32.37%)(P<0.05)。給藥組的腦梗死面積百分比均顯著小于手術組(70.45%)(均P<0.05)。
2.3 腦組織SOD活性及MDA含量 手術組與假手術組相比,腦組織中SOD活性降低,MDA含量增加(P<0.01)。與手術組相比,利莫那班處理組升高了局灶性腦缺血/再灌注腦組織SOD活性(P<0.05),降低MDA含量(P<0.01)。見表1。
表1 利莫那班對腦缺血/再灌注大鼠腦組織勻漿中SOD活性及MDA含量的影響(±s,n=6)
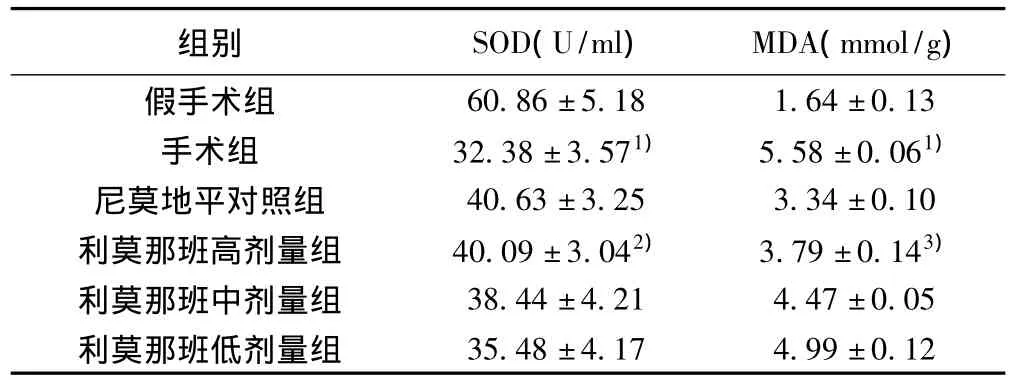
表1 利莫那班對腦缺血/再灌注大鼠腦組織勻漿中SOD活性及MDA含量的影響(±s,n=6)
與假手術組比較:1)P<0.01;與手術組比較:2)P<0.05,3)P<0.01
組別 SOD(U/ml) MDA(mmol/g)60.86±5.18 1.64±0.13手術組 32.38±3.571) 5.58±0.061)尼莫地平對照組 40.63±3.25 3.34±0.10利莫那班高劑量組 40.09±3.042) 3.79±0.143)利莫那班中劑量組 38.44±4.21 4.47±0.05利莫那班低劑量組假手術組35.48±4.17 4.99±0.12
2.4 病理學改變 假手術組大鼠缺血側腦組織神經元胞體密度大,呈圓形,胞核規整,染色質分布均勻,胞膜完整。手術組腦組織神經元胞體水腫、疏松,可見大量神經元胞體為三角形,梗死灶周圍出現部分細胞核固縮,核溶解,核仁模糊或消失,水腫空泡形成,神經元間隙擴大;利莫那班高劑量組可見少量神經元胞體呈三角形;利莫那班中、低劑量組較多神經元胞體呈三角形。見圖1。

圖1 利莫那班對腦組織病變的影響(×400)
2.5 缺血區caspase-3、P-erk的表達 見圖2、圖3。假手術組大鼠腦組織caspase-3呈弱性表達。手術組大鼠皮層和海馬caspase-3主要在胞核表達,部分細胞也可見胞質表達。給藥后,利莫那班能下調caspase-3的表達。假手術組有極少數的P-erk陽性細胞。手術組皮層和海馬可見較多陽性細胞,主要在胞質表達。給藥后,利莫那班能上調P-erk的表達。

圖2 capase-3在大腦皮層的表達(×400)

圖3 P-erk在大腦皮層的表達(×400)
3 討論
實驗結果顯示,利莫那班能明顯改善腦缺血/再灌注大鼠的神經功能損傷,明顯減小左側大腦的梗死面積,明顯減輕腦缺血/再灌注大鼠皮層區域神經元的核固縮和細胞數目的減少,結果證實利莫那班對腦缺血/再灌注大鼠腦損傷有保護作用。有研究表明,腦缺血/再灌注損傷與細胞凋亡有密切關系〔2,3〕。本文結果提示,在缺血區域凋亡細胞數目明顯增加,凋亡在腦缺血損傷中具有重要的作用。因此,減少細胞凋亡,阻斷細胞凋亡通路是改善腦組織缺血的一個重要的治療方向。
神經元凋亡與缺血周邊組織復雜的信號轉導通路激活有密切關系,其中起重要作用的是絲裂原活化蛋白激酶(MAPK)家族中的細胞外調節激酶通路。缺血后活化的細胞外信號調節激酶(ERK)1/2通路可調控某些凋亡因子,如caspase-3,從而調控細胞凋亡。caspases依賴的凋亡途徑是細胞程序性死亡的一種重要方式,caspase-3是caspase級聯瀑布下游最關鍵的凋亡蛋白酶,抑制DNA修復并啟動DNA降解。caspase-3可以被多種因素活化,大鼠腦缺血/再灌注損傷后,Fas與配體結合而活化,其中caspase-8是這一凋亡過程中首先被活化的白細胞介素轉化酶(ICE)家族蛋白酶,caspase-8活化后引起caspase-3和caspase-7活化,這兩種酶都可以剪切多聚ADP核糖聚合酶(PARP),引起DNA的降解。另外,caspase-3還可以活化caspase-6,后者可以降解層蛋白 B〔4,5〕。經利莫那班處理過的大鼠基底節和海馬caspase-3的表達明顯減少,從而推測利莫那班通過對caspase-3的抑制作用,保護腦缺血引起的細胞損傷。
MAPK信號傳遞途徑是大麻素1受體(CB1R)介導的經典信號通路之一。胞外信號調節激酶(extracellular signal-regulated kinase,ERK)是MAPK家族的一員,它的信號傳遞途徑是涉及調節細胞生長、發育及分裂的信號網絡的核心〔6,7〕。利莫那班治療組P-erk的表達水平明顯高于手術組,提示利莫那班通過調節P-erk的活化水平而調控凋亡的進程。利莫那班拮抗CB1R,刺激erk磷酸化,調節凋亡因子,同時激活轉錄因子刺激片段基因產生抗凋亡的作用〔8〕。但是有研究發現,激活CB1R同樣也可以對腦缺血的大鼠產生保護作用〔9〕。造成這些實驗結果不一致的原因可能是多方面的,也許與實驗條件、病變程度和給藥時間有關,或者只有在早期當腦損傷程度較輕的時候給予大麻素才有保護作用,而在進展期給予則無效〔10〕。
1 Pertwee RG.Pharmacology of cannabinoid receptor ligands〔J〕.Curr Med Chem,1999;6(8):635-64.
2 Wakade C,Khan MM,De Sevilla LM,et al.Tamoxifen neuroprotection in cerebral ischemia involves attenuation of kinase activation and superoxide production and potentiation ofmitochondrial superoxide dismutase〔J〕.Endocrinology,2008;149(1):367-79.
3 Cho BB,Toledo-Pereyra LH.Caspase-independent programmed cell death following ischemic stroke〔J〕.J Invest Surg,2008;21(3):141-7.
4 Barone FC,Irving EA,Ray AM,et al.SB 239063,a second-generation p38 mitogen-activated protein kinase inhibitor,reduces brain injury and neurological deficits in cerebral focal ischemia〔J〕.J Pharmacol Exp Ther,2001;296(2):312-21.
5 朱 麗,董 志,張國棟,等.大麻素對腦出血大鼠皮層內PKAC-β、c-fos及BDNF表達量的影響〔J〕.中國藥理學通報,2010;26(4):535-8.
6 Kim R,EmiM,Tanabe K,etal.Regulation and interplay of apoptotic and non-apoptotic cell death〔J〕.JPathol,2006;208(3):319-26.
7 Gong N,Li G,Xiao J,et al.Impact of MAPK cascade pathway and P53 pathway upon liver transplant〔J〕.JHuazhong Univ Sci Technolog Med Sci,2005;25(5):555-7.
8 Hill M,Wernig A,Goldspink G.Muscle satellite(stem)cell activation during local tissue injury and repair〔J〕.JAnat,2003;203(1):89-99.
9 Demuth DG,Molleman A.Cannabinoid signaling〔J〕.Life Sci,2006;78(6):549-63.
10 Ryberg E,Vu HK,Larsson N,etal.Identification and characterisation of a novel splice variantof the human CB1 receptor〔J〕.FEBSLett,2005;579(1):259-64.
Protective effect of rimonabant on cerebral ischem ia reperfusion in jury in rats
YUE Le-Le,DONG Zhi.
Department of Pharmacology,Key Laboratory of Biochem istry and Molecular Pharmacology,Chongqing M edical University,Chongqing 400016,China
Objective To investigate the protective effects of rimonabant on cerebral ischemia reperfusion(CIR)injury in rats.M ethods The CIR model was built through thread block.36 male rats were random ly divided into sham operation,operation,nimodipine,low,middle and high dose rimonabant groups.24 h later,the neurologic deficit score and infarction area weremeasured.Then pathological change in injury brain tissue was detected by HE stain.The caspase-3 and P-erk protein expressions were detected by immunohistochemistry.At the same time,the levels of superoxide dismutase(SOD)and malondialdehyde(MDA)in brain tissue were observed.Results Rimonabant reduced cerebral infarction area,and relieved the injury of brain tissue.It increased the activity of SOD and decreased the contents of MDA.It also reduced the expression of caspase-3,and increased the expression of P-erk.Conclusions Rimonabant has an obviously neuroprotective effecton ischemic cellular injury by antagonising CB1.The Neuronal apoptosismay be involved in the protectivemechanism.
Rimonabant;Cerebral ischemia reperfusion;SOD;MDA;Caspase-3
R-33
A
1005-9202(2011)12-2226-03
重慶市自然科學基金資助(CSTC2009BA5086)
董 志(1960-),男,博士,教授,博士生導師,主要從事神經藥理學研究。
樂樂樂(1986-),女,在讀碩士,主要從事神經藥理學研究。
〔2010-10-12收稿 2010-12-12修回〕
(編輯 袁左鳴/徐 杰)

