肝癌特異性啟動(dòng)子調(diào)控的雙靶位慢病毒載體的構(gòu)建、鑒定及其在肝癌基因治療中的應(yīng)用*
徐震 牛堅(jiān) 劉斌
(1.徐州醫(yī)學(xué)院研究生院,江蘇徐州221002;2.徐州醫(yī)學(xué)院附屬醫(yī)院普外科,江蘇徐州221006)
基因治療是一種新的治療腫瘤的方法,其難點(diǎn)是效益基因在腫瘤細(xì)胞中的靶向性及其高效表達(dá)。而survivin基因在成人正常細(xì)胞中不表達(dá),在肝癌細(xì)胞中表達(dá)其啟動(dòng)子具有良好的靶向性。胰島素樣生長(zhǎng)因子1類(lèi)受體表達(dá)與腫瘤發(fā)生關(guān)系密切。
本實(shí)驗(yàn)通過(guò)構(gòu)建AFP-PRIME-miR30-shRNA-IGF1R慢病毒,探討其對(duì)肝癌細(xì)胞生物學(xué)行為影響,為肝癌基因治療拓展新的思路。
1 資料與方法
1.1 主要試劑
兔抗人 IGF1R多克隆抗體:Sant Cruze公司;Lipofectamin2000:Invitrogen公司;限制性內(nèi)切酶ScaI、ClaⅠ、SpeI、PmeI、XhoⅠ、EcoRⅠ、ApaI和 NheI,T4 DNA連接酶,購(gòu)于大連寶生物公司;CCK-8試劑盒:DOJINDO公司;質(zhì)粒提取試劑盒、回收試劑盒購(gòu)于上海生物工程有限公司;PCR引物和其他試劑購(gòu)于博亞公司。
1.2 主要材料
1.3 包膜質(zhì)粒pMD2G-anti-AFP-scFv質(zhì)粒的構(gòu)建
以表達(dá)anti-AFP-scFv的質(zhì)粒pMON-scFv為模板,設(shè)計(jì)兩端含SacⅠ和ClaⅠ的酶切位點(diǎn)的引物。

將anti-AFP-scFv基因片段插入包膜質(zhì)粒pMD2G的SacⅠ和ClaⅠ位點(diǎn),構(gòu)建pMD2G-anti-AFP-scFv質(zhì)粒。
1.4 穿梭質(zhì)粒pPRIME-miR30-shRNA-IGF1R的構(gòu)建
從NCBI里找到人IGF1R基因的cDNA序列全長(zhǎng),genbank號(hào)為NM_00875。利用網(wǎng)上的設(shè)計(jì)工具(genesil等)進(jìn)行siRNA片段的篩選,將選出合適的目標(biāo)序列進(jìn)行合成,并引入XhoⅠ、EcoRⅠ酶切位點(diǎn)。

形成穿梭質(zhì)粒pPRIME-miR30-shRNA-IGF1R。酶切電泳鑒定及測(cè)序鑒定。
1.5 survivin-CMV肝癌特異性啟動(dòng)子的克隆
以含survivin-CMV肝癌特異性啟動(dòng)子的pBluescriptII-survivin-CMV為模板,設(shè)計(jì)上游含apaI和下游含NheI的酶切位點(diǎn)的引物。

1.6 穿梭質(zhì)粒survivin-CMV-pPRIME-miR30-shRNA-IGF1R的構(gòu)建
survivin-CMV啟動(dòng)子PCR擴(kuò)增產(chǎn)物以ApaI和 NheI雙酶切,連接至同樣雙酶切的pPRIME-miR30-shRNA-IGF1R,替換穿梭質(zhì)粒pPRIME中的CMV啟動(dòng)子,轉(zhuǎn)化大腸桿菌DH5α,擴(kuò)增,提取質(zhì)粒,用ApaI和NheI雙酶切鑒定,測(cè)序,提取質(zhì)粒名為sur-CMV-pPRIME-miR30-shRNA-IGF1R。
1.7 病毒的包裝、鑒定和擴(kuò)增純化
1.7.1 病毒的包裝、鑒定 將質(zhì)粒(pPRIME、pMD2G、psPAX2)、(sur-CMV-pPRIME-miR30-shRNA-IGF1R、pMD2G-anti-AFP-scFv、psPAX2)分別通過(guò)Lipofectamin2000共轉(zhuǎn)染293T細(xì)胞,經(jīng)過(guò)病毒空斑純化,包裝成完整病毒顆粒。提取重組病毒DNA,PCR分析、測(cè)序鑒定正確者,即為目的病毒PRIME、AFP-PRIME-miR30-shRNA-IGF1R。
1.7.2 病毒的擴(kuò)增及滴度測(cè)定 取96孔板,每孔加293T細(xì)胞1×104個(gè),加液量200μL,孵箱培養(yǎng)24h后更換無(wú)血清培養(yǎng)液;待測(cè)病毒用DMEM完全培養(yǎng)液稀釋10-1、10-2、10-3、10-4、10-5、10-6等稀釋度。每一濃度設(shè)3復(fù)孔,每孔每一濃度取病毒溶液200μL,同時(shí)設(shè)培養(yǎng)液對(duì)照;在37℃、5%CO2孵箱中繼續(xù)培養(yǎng)36~48h。鏡檢觀察CEP現(xiàn)象,按公式計(jì)算出病毒滴度:病毒滴度(pfu/mL)=每孔細(xì)胞數(shù)×病毒稀釋倍數(shù)×10/加入的病毒溶液量(mL)。
煤成說(shuō)學(xué)代表者有郭則華(1981年)、陳安定等(2004年)認(rèn)為:瀝青煤是石油烴類(lèi)的衍生礦物,石油的演化是形成瀝青煤的主要機(jī)理。這種瀝青煤實(shí)際上就是碳瀝青。其成因?yàn)楣庞筒卦馐芷茐亩纬桑从蜌馍⑹н^(guò)程中,在油氣逸散通道中,由于重質(zhì)成分不斷殘存、充填,最終完全堵塞了裂縫和孔洞而形成的。
1.8 RT-PCR檢測(cè)IGF1R在mRNA水平的變化
將L-02、SMMC7721細(xì)胞低密度鋪于6孔板,一天后用MOI=10的PRIME、AFP-PRIME-miR30-shRNA-IGF1R感染細(xì)胞,未處理的細(xì)胞作為對(duì)照組。48h后Trizol法提取各組細(xì)胞的總RNA,逆轉(zhuǎn)錄反應(yīng)使用隨機(jī)引物OligdTs合成第一鏈(嚴(yán)格按照廠家說(shuō)明書(shū)進(jìn)行),在20μL反應(yīng)體系中加入2μg總cDNA。IGF1RmRNA檢測(cè)引物序列為:上游:5'-GGAGGCTGAATACCGCAAAGTC-3',下游:5'-AAAGACGAAGTTGGAGGCGCT-3',擴(kuò)增產(chǎn)物為 398bp;內(nèi)參照 β-actin,上游:5'-GTGAAGGTGACAGCAGTCGGTT-3',下游:5'-CAGTGTACAGGTAAGCCCTG-3'。退火溫度均為55℃。在同一條件下,每次PCR以β-actin為內(nèi)參照,PCR產(chǎn)物經(jīng)2%瓊脂糖凝膠電泳,凝膠成像儀掃描成像,表達(dá)豐度以特異基因條帶亮度與內(nèi)參照的比值表示。
1.9 Western-blot鑒定IGF1R的表達(dá)
將L-02、SMMC7721細(xì)胞鋪于6孔板,一天后用MOI=10.0的PRIME、AFP-PRIME-miR30-shRNA-IGF1R感染細(xì)胞,未處理的細(xì)胞作為對(duì)照組。48h后提取核蛋白,取40μg細(xì)胞裂解液與上樣緩沖液混合,煮沸10min后上樣,進(jìn)行SDS-聚丙烯酰胺凝膠電泳。電泳條件:60伏,30min;160伏,1.5h。電泳結(jié)束后,電轉(zhuǎn)移法將蛋白從凝膠中轉(zhuǎn)移到PVDF膜上,甲醇固定PVDF膜后,用含5%脫脂奶粉的封閉液40℃孵育過(guò)夜。一抗10mL(1∶1000稀釋?zhuān)┦覝胤跤?h,二抗10mL(1∶5000稀釋?zhuān)┦覝胤跤?h后,PVDF膜用ECL化學(xué)發(fā)光試劑盒處理并在暗室顯影。
1.10 競(jìng)爭(zhēng)性抑制試驗(yàn)
選擇AFP陽(yáng)性率的SMMC7721細(xì)胞株為觀察對(duì)象,在細(xì)胞感染慢病毒前6h事先加入抗AFP單抗,然后加入慢病毒共同培養(yǎng)48h,觀察綠色熒光細(xì)胞數(shù)量的變化。
1.11 CCK-8法檢測(cè)細(xì)胞生長(zhǎng)
參照DOJINDO的Cell Count Kit-8,具體操作如下,分別取對(duì)數(shù)生長(zhǎng)期的各組細(xì)胞,以每孔4×104~5×104個(gè)細(xì)胞接種于96孔板中,每孔體積為200μL;24h后換不含胎牛血清的DMEM培養(yǎng)液,繼續(xù)培養(yǎng)24h使細(xì)胞靜止;將MOI=10的 PRIME、 AFP-PRIME-miR30-shRNA-IGF1R感染SMMC7721細(xì)胞,感染48h后,吸盡待測(cè)孔內(nèi)培養(yǎng)上清液;在酶聯(lián)免疫分析儀上測(cè)定各孔光吸收值(OD)繪制生長(zhǎng)曲線,觀察各組細(xì)胞連續(xù)7d的細(xì)胞的增殖情況。每孔設(shè)3個(gè)復(fù)孔。
1.12 統(tǒng)計(jì)學(xué)處理
數(shù)據(jù)以均數(shù)±標(biāo)準(zhǔn)差表示,經(jīng)SAS6.12統(tǒng)計(jì)軟件進(jìn)行t檢驗(yàn)分析,P<0.05為差異有顯著意義。
2 結(jié)果
2.1 anti-AFP-scFv基因片段PCR及電泳結(jié)果
以表達(dá)anti-AFP-scFv的質(zhì)粒pMON-scFv為模板,設(shè)計(jì)兩端含SacⅠ和ClaⅠ的酶切位點(diǎn)的引物。ScFv基因由696bp構(gòu)成,包含312bp中的VL和339bp的VH和兩者之間有45bp的連接序列,擴(kuò)增片段696bp(圖1)。與預(yù)期結(jié)果吻合,測(cè)序正確。

圖1 VH、VL和ScFv基因PCR擴(kuò)增產(chǎn)物凝膠電泳
2.2 穿梭質(zhì)粒pPRIME-miR30-shRNA-IGF1R的鑒定
將pPRIME-miR30-shRNA-IGF1R行XhoⅠ、EcoRⅠ酶切鑒定(圖2),鑒定結(jié)果與預(yù)期相符。片段大小為96bp左右,但因?yàn)槠翁〔灰子^察到,電泳結(jié)果示:pPRIME-miR30-shRNA-IGF1R與對(duì)照組pPRIME酶切相比,未見(jiàn)1100bp左右的帶型,且后面的帶位于同一條線上,結(jié)果與預(yù)期相符。此時(shí)命名慢病毒重組載體為pPRIME-miR30-shRNA-IGF1R。

圖2 pPRIME-m iR30-shRNA-IGF1R的雙酶切鑒定
2.3 survivin-CMV嵌合啟動(dòng)子的鑒定
以含survivin-CMV肝癌特異性啟動(dòng)子的pBluescriptII-sur vivin-CMV為模板,PCR擴(kuò)增產(chǎn)物經(jīng)ApaI和NheI、雙酶切,連接至同樣雙酶切的pPRIME-miR30-shRNA-IGF1R,轉(zhuǎn)化大腸桿菌DH5α,挑取重組陽(yáng)性克隆,經(jīng)ApaI和NheI雙酶切鑒定(圖3),片段大小為860bp左右,結(jié)果與預(yù)期相符。測(cè)序測(cè)序結(jié)果表明合成的surn-CMV嵌合啟動(dòng)子插入正確,此時(shí)命名慢病毒重組載體為sur-CMV-pPRIME-miR30-shRNA-IGF1R。

圖3 survivin-CMV嵌合啟動(dòng)子的雙酶切鑒定
2.4 轉(zhuǎn)染293T細(xì)胞的效應(yīng)
表達(dá)質(zhì)粒共轉(zhuǎn)染293T細(xì)胞,細(xì)胞部分融合,多核復(fù)合體出現(xiàn),隨著病毒增殖,細(xì)胞內(nèi)可見(jiàn)多量病毒顆粒,并逐漸從壁上脫落,出現(xiàn)細(xì)胞病理效應(yīng)。病毒滴度測(cè)定結(jié)果顯示重組慢病毒表達(dá)克隆的滴度為4.58×l09pfu/L。
2.5 RT-PCR結(jié)果
RT-PCR產(chǎn)物經(jīng)2%瓊脂糖凝膠電泳,398bp可見(jiàn)特異性IGF1R目標(biāo)條帶(圖4),AFP-PRIME-miR30-shRNA-IGF1R中IGF1R的表達(dá)較對(duì)照組明顯減低,經(jīng)灰度掃描及與內(nèi)參照比較分析,干擾組IGF1RmRNA的表達(dá)量?jī)H為對(duì)照組的4%(P<0.05),而轉(zhuǎn)染正常胎肝細(xì)胞L-02后IGF1R的表達(dá)與對(duì)照組比較無(wú)明顯變化。

圖4 RT-PCR檢測(cè)感染慢病毒AFP-sur-CMV-PRIME-miR30-shRNA-IGF1R后IGFIRmRNA的表達(dá)
2.6 Western blot檢測(cè)結(jié)果
實(shí)驗(yàn)發(fā)現(xiàn)慢病毒AFP-sur-CMV-PRIME-miR30-shRNA-IGF1R轉(zhuǎn)染SMMC7721細(xì)胞,48h后細(xì)胞內(nèi)的IGF1R的表達(dá)與對(duì)照組比較明顯下降,約為對(duì)照組的9%(P<0.05),而轉(zhuǎn)染正常胎肝細(xì)胞L-02后,IGF1R蛋白的表達(dá)與對(duì)照組比較無(wú)明顯變化。見(jiàn)圖5。
2.7 競(jìng)爭(zhēng)性抑制試驗(yàn)
選擇AFP陽(yáng)性率的SMMC7721細(xì)胞株為觀察對(duì)象,在細(xì)胞感染慢病毒前6h事先加入抗AFP單抗,然后加入慢病毒共同培養(yǎng)48h,加單抗為(7.5±0.4)%,未加單抗為(76±1.2)%(P<0.05),見(jiàn)圖6。
2.8 AFP-PRIME-miR30-shRNA-IGF1R對(duì)SMMC7721細(xì)胞增殖的影響
從實(shí)驗(yàn)組和對(duì)照組的細(xì)胞生長(zhǎng)曲線(圖7)可以看出,實(shí)驗(yàn)組細(xì)胞的生長(zhǎng)明顯慢于對(duì)照組(P<0.05)。

圖5 Western-blot檢測(cè)感染AFP-sur-CMV-PRIME-m iR30-shRNA-IGF1R后IGFIR蛋白的表達(dá)
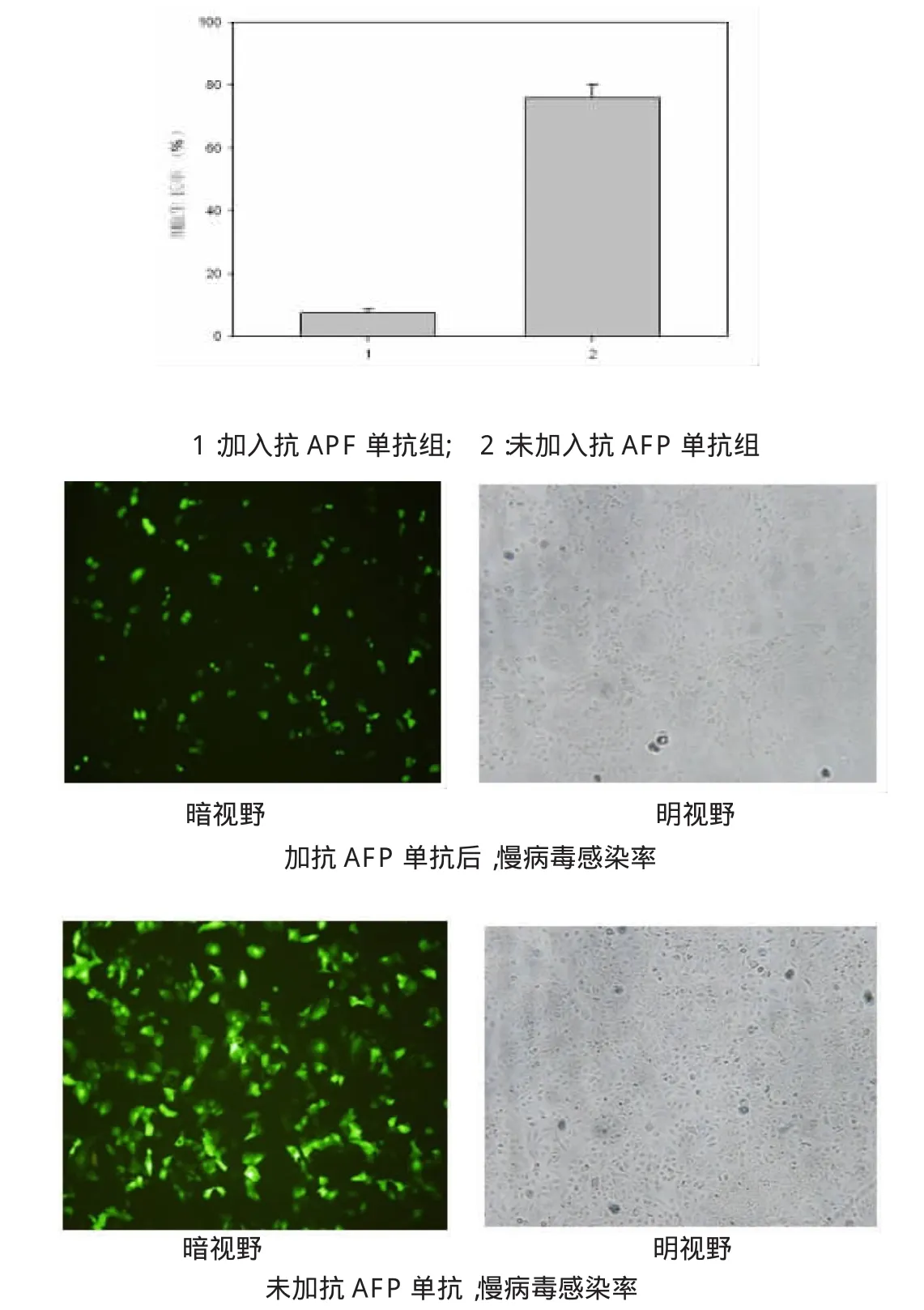
圖6 競(jìng)爭(zhēng)性抑制試驗(yàn)結(jié)果
3 討論
腫瘤的基因治療中,表達(dá)基因的靶向性和高效表達(dá)是關(guān)鍵。survivin的組織分布特征具有明顯的細(xì)胞選擇性[1],在終末分化的成人組織中不表達(dá)(除胸腺、生殖腺外),而在絕大多數(shù)腫瘤組織,包括淋巴瘤、肝癌、結(jié)腸癌、胃癌等呈高表達(dá)[2]。研究表明,survivin啟動(dòng)子較CMV啟動(dòng)子,可以在腫瘤細(xì)胞中特異性表達(dá),具有良好的靶向性,在腫瘤的基因治療中具有良好的前景[3]。Van Houdt等[4]克隆了survivin基因起始密碼子上游第-230~+30位和第-1430~+30位兩個(gè)survivin啟動(dòng)子基因片段,證實(shí)兩者在轉(zhuǎn)錄活性、殺滅腫瘤細(xì)胞效果、體內(nèi)抑瘤效果等方面沒(méi)有顯著差異。在實(shí)驗(yàn)構(gòu)建的載體中,重組入的片段過(guò)長(zhǎng)會(huì)使載體的結(jié)構(gòu)發(fā)生變化,可能影響預(yù)期功能的完成。而survivin全長(zhǎng)的啟動(dòng)子已達(dá)1.5kb左右,若要完成預(yù)期作用則啟動(dòng)子后面的功能基因片段長(zhǎng)度則可能受到限制,有時(shí)無(wú)法滿足實(shí)驗(yàn)的需要。Li等[5]報(bào)道survivin基因起始密碼子上游第-268~+1位片段已具備啟動(dòng)子功能。本實(shí)驗(yàn)構(gòu)利用高活性的巨細(xì)胞病毒早期基因增強(qiáng)子(CMVE)[6]增強(qiáng)啟動(dòng)子的活性,構(gòu)成了860bp左右的sur vivin-CMV特異性啟動(dòng)子,提高survivin啟動(dòng)子的活性,并成功表達(dá)。

圖7 細(xì)胞生長(zhǎng)曲線
慢病毒載體具有可以長(zhǎng)時(shí)間表達(dá)外源基因,容量大,感染細(xì)胞種類(lèi)多而且高效,可以感染體內(nèi)、體外分裂細(xì)胞與非分裂細(xì)胞,滴度高,低免疫原性,安全性高[7,8]等優(yōu)點(diǎn),成為肝癌基因治療的理想載體。
AFP是目前肝癌生物治療和診斷中用得較多的靶抗原,抗AFP的ScFv在原發(fā)性肝癌的生物治療和診斷中都具有重要的作用[9]。
IGF1R是一種跨膜酪氨酸蛋白激酶,在多種腫瘤細(xì)胞中有高水平表達(dá)[10-12]。但在正常肝組織表達(dá)量極少,表皮生長(zhǎng)因子(EGF)受體對(duì)細(xì)胞的有絲分裂作用及轉(zhuǎn)化潛能必須通過(guò)IGF1R才能發(fā)揮,而過(guò)表達(dá)的IGF1R則不需要EGF受體即可引起細(xì)胞轉(zhuǎn)化。研究還表明IGF1R的數(shù)量水平在細(xì)胞生存中起著決定性作用,只有達(dá)到某一水平,才能將細(xì)胞由不進(jìn)行有絲分裂的模式轉(zhuǎn)化為有絲分裂模式[13]。RNA干擾技術(shù)是重要的生物學(xué)研究工具,在基因治療中具有良好的前景[14]。針對(duì)IGF1R基因的RNA干擾片段裝入特定質(zhì)粒中,再轉(zhuǎn)染入人肝癌細(xì)胞株,雖然作用時(shí)間有所延長(zhǎng),但維持沉默效應(yīng)的時(shí)間有限[15],因此本實(shí)驗(yàn)在載體選擇和實(shí)驗(yàn)方法上有新的嘗試,是一種有意義的探索。
本實(shí)驗(yàn)經(jīng)PCR、測(cè)序鑒定證實(shí)survivin-CMV肝癌特異性啟動(dòng)子啟動(dòng)的AFP-survivin-CMV-PRIME-miR30-shRNA-IGF1R慢病毒載體構(gòu)建成功,對(duì)肝癌SMMC7721細(xì)胞和胎肝L-02細(xì)胞進(jìn)行體外研究表明,AFP-sur-CMV-PRIME-miR30-shRNA-IGF1R能夠抑制肝癌SMMC7721細(xì)胞的生長(zhǎng),并具有特異性。為腫瘤基因治療提供了理論依據(jù)和新的思路。
[1]Marusawa H,Matsuzawa S,Welsh K,et al.HBXIP functions as a co-fac-tor of survivin in apoptosis suppression[J].EMBO J,2003,22(11):2729-2740.
[2]Ouban A,Muraca P,YeatmanT,et al.Expression and distribution of in-sulin-like growth factor-1 receptor in human carcinomas[J].Hum Pathol,2003,34(8):803-808.
[3] Konopka K,Spain C,Yen A,et al.Correlation between the levels of survivin and survivin promoter-driven gene expression in cancer and non-cancer cells[J].Cell Mol Biol Lett,2009,14(1):70-89.
[4]Van Houdt WJ,Haviv YS,Lu B,et al.The human survivin promoter:a novel transcriptional targeting strategy for treatment of glioma[J].J Neurosurg,2006,104(4):583-592.
[5]Li F,Altieri DC.Transcriptional analysis of human survivin gene expression[J].Biochem J,1999,344(Pt 2):305-311.
[6]Richards CA,Austin EA,HuberB E.Transcriptional regulatory sequences of carcinoembryonic antigen:identification and use with cytosine deaminase for tumor specific gene therapy[J].Hum Gene Ther,1995,6(7):881-893.
[7]Bauer G,Dao MA,Case SS,et al.In vivobiosafety model to assess the risk of adverse events from retroviral and lentiviral vectors[J].Mol Ther,2008,16(7):1308-1315.
[8]Haynes JR,Dokken L,Wiley JA,et al.Influenzapseudotyped Gag virus-like particle vaccines provide broad protection against highly pathogenic avian influenza challenge[J].Vaccine,2009,27(4):530-541.
[9] 黃建生,郭秋明.基因工程抗體[M].廣州:華南理工大學(xué)出版社,1997:56-70.
[10]Okada E,Murai Y,Matsui K,et al.Survivin expression in tumor cell nuclei is predictive of a favorable prognosis in gastric cancer patients[J].Cancer Lett,2001,163(1):109-116.
[11]Wang YH,Wang ZX,Qiu Y,et al.Lentivirus-mediated RNAi knockdown of insulin-like growth factor-1 receptor inhibits growth,reduces invasion,and enhances radiosensitivity in human osteosarcoma cells[J].Mol Cell Biochem,2009,327(1-2):257-266.
[12]Ma Z,Dong A,Kong M,et al.Silencing of the type 1 insulin-like growth factor receptor increases the sensitivity to apoptosis and inhibits invasion in human lung adenocarcinoma A549 cells[J].Cell Mol Biol Lett,2007,12(4):556-572.
[13]Bauer G,Dao MA,Case SS,et al.In vivobiosafety model to assess the risk of adverse events from retroviral and lentiviral vectors[J]. Mol Ther,2008,16(7):1308-1315.
[14]Ren K,Jin H,Bian C,et al.MR-1 modulates proliferation and migration of human hepatoma HepG2 cells through MLC2/FAK/Akt signaling pathway[J].J Biol Chem,2008,283(51):35598-35605.
[15]牛堅(jiān),錢(qián)海鑫,黃健,等.RNA干涉胰島素樣生長(zhǎng)因子1類(lèi)受體的研究[J].中華實(shí)驗(yàn)外科雜志,2006,23(7):872-873.

