硫化鐵熱電池初始峰壓產生機理研究
劉 杰,安建民,郭永全,趙晉峰, 鄧士梅
(1.空軍駐京津地區軍代表室,天津 300308;2.中國電子科技集團公司第十八研究所,天津 300381)
熱電池是用電池本身的加熱系統把不導電的固體狀態鹽類電解質加熱熔融成離子導體而進入工作狀態的一種熱激活貯備電池(GJB2279)。目前,最常見的熱電池為硫化物/鋰合金體系熱電池,其中硫化物正極材料常用的有FeS2和CoS2,其放電容量較大,適用于體積大、放電時間長、容量大等熱電池的制備。但由于硫化物/鋰合金體系熱電池在電池放電初期有電壓尖峰現象[1-2],這給電池的設計帶來了困難,特別是隨著熱電池電壓精度要求的提高,控制初始峰壓,尤其顯得重要。對于初始峰壓產生機理,近些年文獻也有報道。通常認為,Li(M)/FeS2體系熱電池在放電初期電壓尖峰的產生有以下幾種因素:(1)電堆激活時,電堆溫度高,特別是局部過熱,導致FeS2分解,產生單質硫,鋰合金/硫的電勢比鋰合金/二硫化鐵的電勢高[3];(2)電池激活時,電堆溫度很高,導致熱電池的電動勢隨溫度的升高而增加[3];(3)陰極材料FeS2不純,存在少量雜質,如單質S[3]或氧化物[4];(4)正極材料中含氧量的高低與瞬變峰值的產生,有著密切關系[3-4];(5)此外,脈沖峰的產生及大小還與電解質熔化導致鋰離子活度變化或二硫化鐵的粒度大小有關[3,5]。在我們的實際工作中發現,在電池調試過程中,保持其他條件不變,不同批次的正極材料制備的熱電池,初始峰壓差異較大,顯示正極材料對峰壓有較大影響,但何種雜質導致峰壓及雜質的標定方法有待研究。
本文工作不涉及電池熱設計及其他方面研究,僅從陰極材料入手,考察雜質存在對電池初始峰壓的影響,以期對初始電壓峰的產生機理有一定的認識。
1 實驗
1.1 酸溶鐵的測定
取稀鹽酸(體積比:1∶1)100 mL,加入FeS2樣品 5 g,水浴煮沸溶解1 h;雙層中速濾紙過濾,取濾液,以原子發射光譜法測定其中鐵含量。
1.2 熱電池制備
正極:FeS2正極,FeS2正極 +M(不同的雜質);負極:LiSi合金;電解質:三元全鋰電解質;加熱藥:活性Fe粉+KClO4。
電池尺寸:Φ45 mm×50 mm;單體:Φ32 mm;單體數:10片。
1.3 放電條件
4 A恒流放電。
2 實驗結果與討論
2.1 雜質分析
熱電池用陰極材料FeS2來源于天然產出的黃鐵礦,礦石經粉碎、過篩、提純、洗滌、干燥等工序成為熱電池可用的二硫化鐵材料。對純二硫化鐵材料用原子發射光譜法進行雜質檢驗,表1為測定結果。
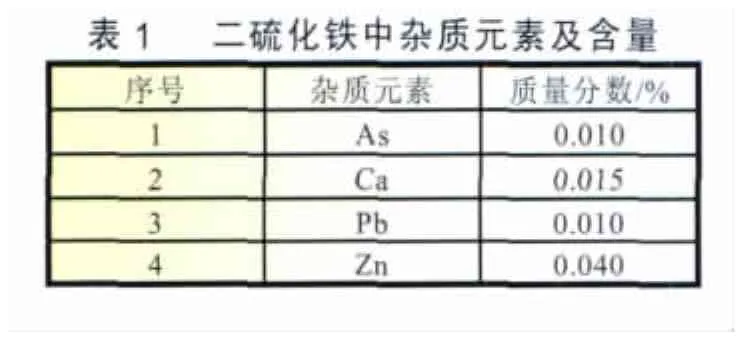
文獻[6-7]對一般黃鐵礦的雜質元素含量也有報道,較多的元素為:As、Zn、Ni、Co、Pb、Sb 等,一般含量都在千分之一以下;我們認為,這種含量級別的雜質不會對初始電壓峰產生影響,構成初始峰的主要因素應該是Fe化合物雜質及S雜質。
2.2 正極攙雜對初始峰壓的影響
以正常正極材料和分別添加了不同比例添加劑的十二種實驗正極材料按1.2的實驗條件制備電池,恒流放電,初始電壓峰值數據見表2,其中正常正極材料(無添加劑)制備電池初始電壓峰值為18.62 V。
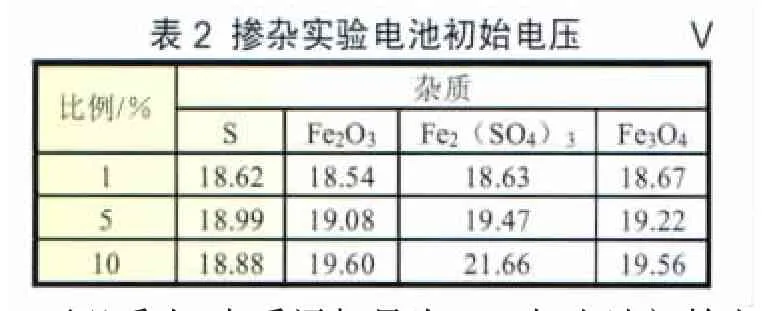
從表2可以看出,雜質添加量為1%時,電池初始電壓峰無變化,但隨著添加量的提高,添加了 Fe2O3、Fe2(SO4)3或Fe3O4的電池初始電壓有明顯的提高,而添加了單質S的電池僅提高少許。
有研究認為,FeS2分解產生FeS與硫蒸汽,鋰合金/硫的電勢比鋰合金/二硫化鐵的電勢高,故這也是產生熱電池電壓初始峰的一個因素。我們認為,硫蒸汽作為氣體,囿于界面反應的困難,很難在電池中作為活性物質形成電壓回路,不應該是產生熱電池電壓初始峰的緣故。在我們的材料實驗中,保持其他條件不變,不同批次的FeS2正極材料制備的熱電池,峰壓差異較大;我們認為該結果不能歸因于電堆激活時,電堆溫度高,導致FeS2分解,產生單質硫蒸汽;因為,同型號電池中,各批次正極材料的熱分解差異不會很大;這也進一步證明了硫蒸汽不是產生熱電池初始峰壓的主要原因。
除上述的摻雜實驗外,我們同時制備了一只實驗電池,電池去除了正極層,但在鐵粉加熱藥外側刮制了一薄層硫磺粉,目的在于使電池激活時產生硫蒸汽;放電結果,激活早期,單體電壓在1.0~1.1 V之間,這應該是由鐵粉加熱藥與負極產生的電勢差;實驗中未見硫蒸汽對初始峰壓產生影響。
二硫化鐵中存在雜質硫;由表2可見,電池的峰壓隨著單質S含量增大到一定程度,確有變化,但差異較小。由于全鋰電解質共熔點為432℃,接近硫的沸點444℃,所以,電池激活時,雜質硫同樣存在變成氣相的可能性,這也會影響到硫初始峰壓的建立。因此我們認為,硫可能是產生峰壓的一個原因,但不會是主要原因。
隨著添加量的提高,添加了 Fe2O3、Fe2(SO4)3或 Fe3O4的電池初始電壓提高明顯,說明黃鐵礦中若含有這些高價鐵化合物雜質,確實能產生初始電壓峰;文獻[5]也認為,FeS2受潮氧化,生成FeSO4·H2O。而實際上,FeSO4·H2O在空氣中很不穩定,極易被空氣氧化生成Fe2O3或Fe3O4。
在對陰極材料進行X射線衍射分析中,也發現其中有少量的Fe3O4雜質存在。
由于這些鐵化合物溶于酸,而FeS2僅微溶于酸,所以將這些雜質以稀鹽酸(體積比:1∶1)水浴煮沸溶解下來,以原子發射光譜法測定溶解的鐵量,名為酸溶鐵。
在酸溶鐵中,二價鐵的電位(Fe2++2e-→Fe)同樣高于FeS2電位;為檢驗二價鐵對脈沖峰的影響,在正極材料中加入5%的活性鐵粉,制成電池,放電實驗,結果如表3。
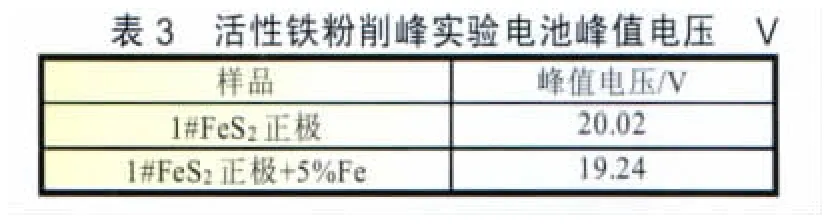
由表3數據看出,活性鐵粉的加入,消除了正極粉的高初始電壓峰,而活性鐵不能還原Fe2+;說明脈沖峰的產生主要是由于正極材料中有三價鐵雜質的存在。
2.3 酸溶鐵的來源
黃鐵礦中一般含有少量赤鐵礦和磁鐵礦雜質,國內黃鐵礦中氧含量會高達4%~7%[4];此外,礦物在粉碎、浮選等處理過程中,硫化物在潮濕氣氛并有氧氣存在下會被氧化成硫酸鹽,反應式如下[8]:
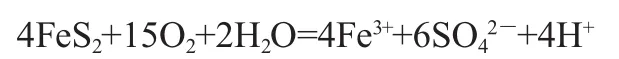
所以,用于熱電池正極的FeS2材料中,不可避免的存在Fe2O3、Fe3O4及 Fe2(SO4)3等雜質成分。文獻[9]對黃鐵礦的氧化也有詳細的論述,最終產物也是上述三種化合物。
在以FeS2為原材料的熱電池正極材料制備過程中,酸溶鐵含量會有較大幅度的提高。我們分別對純的FeS2和以其為原材料制備的1#FeS2正極材料(有較強的初始電壓峰)進行了酸溶鐵測定,結果列于表4。

由表4數據可以看出,純FeS2在制備正極材料過程中產生了大量的酸溶鐵成分;這是由于在正極材料制備過程中,鋰化劑的加入將FeS2還原為FeS,而FeS溶于酸,使酸溶鐵含量上升;而在此過程中,鋰化劑將三價鐵還原到二價或零價,達到消除初始電壓峰的目的。
從上述分析可得出結論,酸溶鐵的來源為原料固有和正極材料制備過程產生兩種。
熱電池用陰極材料FeS2來源于天然產出的黃鐵礦,本身就含有一定量的氧化物雜質;在正極材料制備工藝過程中,有鋰化削峰和恒溫恒濕除鋰步驟;在鋰化削峰步驟,鋰化劑加入,與高價鐵雜質反應,生成二價或0價鐵,此過程沒有減少材料中酸溶鐵含量,但削減了材料初始脈沖峰壓;在恒溫恒濕除鋰步驟中,水的存在導致FeS2被氧化,氧化產物含有高價鐵雜質,這些新生雜質也可能與鋰化劑反應,高價鐵被還原,此過程使材料中酸溶鐵含量上升;但材料中總的三價鐵含量降低,最終達到削峰目的。
3 結論
①一般黃鐵礦的雜質元素含量較低,除硫、鐵外的雜質元素化合物不會對初始電壓峰產生影響,構成初始峰的主要因素應該是Fe化合物雜質及S雜質。
②正極中雜質硫可能是產生峰壓的一個原因,但不會是主要原因。正極熱分解產生的硫蒸汽對電池初始峰壓無影響。
③正極酸溶鐵雜質中三價鐵化合物是熱電池產生峰壓的主要原因,高價鐵雜質來源為原料固有和正極材料制備過程產生兩種。
④在正極材料制備過程的鋰化削峰步驟,鋰化劑加入,與高價鐵雜質反應,生成二價或0價鐵,材料中總的三價鐵含量降低,最終達到削峰目的。
[1]孫淑洋,劉延東,曹軍記,等.二硫化鈷作高功率熱電池正極材料的研究[J].電源技術,2003,1:28-30.
[2]劉延東,褚德威.LiSi-CoS2體系熱電池的電化學特性[J].電源技術,2004,11:693-696.
[3]陸瑞生,劉效疆.熱電池[M].北京:國防工業出版社,2005:223.
[4]蘇祖祺,黃英俊.熱電池用高純二硫化鐵質量要求[J].江蘇冶金,1999,4:6-7.
[5]劉志堅,段偉,李志友,等.正極材料狀態對Li-B/FeS2熱電池放電特性的影響[J].粉末冶金材料科學與工程,1999,1:49-54.
[6]陳壽根.黃鐵礦和磁黃鐵礦物的微量光譜分析法研究[J].分析化學,1987,15(11):1016-1018.
[7]吳景缽,陳燕敏,王宗花.黃鐵礦中微量元素的光譜測定[J].巖石礦物及測試,2011,2:175-177.
[8]PATRA P,NATARAJAN K A.Microbially-induced flocculation and flotation for pyrite separation from oxide gangue minerals[J].Minerals Engineering,2003,16:965-973.
[9]HU G L,DAM-JOHANSEN K,WEDEL S,etc.Decomposition and oxidation of pyrite[J].Progress in Energy and Combustion Science,2006,32:295-314.

