慢性阻塞性肺疾病穩定期血清肺表面活性蛋白D和C-反應蛋白與各因素之間的關系探討
周忠海,雷 霆,顏春松
慢性阻塞性肺疾病 (COPD)是呼吸系統的常見病和多發病,我國40歲以上人群的 COPD患病率達8.2%[1]。目前COPD居全球死亡原因第四位,到2020年COPD死亡率將上升至第三位。COPD被認為是一種炎癥疾病,以進行性氣流受限和肺實質破壞為特征。該炎癥過程不僅僅局限于肺部,還存在持續的低水平全身炎癥反應[2]。C-反應蛋白 (CRP)被認為是一種非特異性系統炎癥標志物,血清濃度與COPD患者的住院率和死亡率密切相關,但CRP主要產生于肺外器官,受多種因素影響,缺乏肺組織特異性。然而,肺表面活性蛋白D(SP-D)主要由肺部的Ⅱ型肺泡上皮及Clara細胞分泌,在肺損傷時血清SP-D顯著升高[3]。本研究通過檢測COPD穩定期CRP與SP-D濃度,探討其濃度變化與其他因素的關系。
1 對象與方法
1.1 研究對象 2009年1月—2010年3月在我院門診隨訪COPD患者35例 (COPD組)和門診健康體檢者13例 (對照組)。納入標準:患者符合《COPD診治指南 (2007年修訂版)》中的診斷標準,急性加重緩解后超過2個月;排除標準:支氣管擴張、結核、糖尿病、心力衰竭、心肌梗死、全身其他部位急性和慢性炎癥性疾病、腫瘤性疾病、間質性肺疾病、風濕性疾病以及其他可能致血清CRP和SP-D濃度發生變化的疾病。
1.2 資料收集方法 在研究對象門診隨訪及體檢時,收集年齡、性別、吸煙量、是否戒煙,測量身高、體質量等臨床信息,并測定肺功能 (通氣功能+舒張試驗)。
1.3 血標本收集和處理 抽取晨起空腹靜脈血,CRP、中性粒細胞比例、白細胞數由本院檢驗科檢測;5 ml不抗凝,靜置1~2 h,待上層血清析出,立即以1 000 g轉速離心10 min,將血清與血細胞迅速分離,取上層血清1 ml,裝入編號EP管中,放入-70℃冰箱中凍存,待標本收集完全后,采用人SP-D定量ELISA試劑盒 (上海西唐生物有限公司)測定。
1.4 統計學方法 采用SPSS 13.0軟件進行統計學分析,計量資料以 (±s)表示,采用方差分析,對各因素采用Pearson相關分析,以P<0.05為差異有統計學意義。
2 結果
2.1 COPD組與對照組臨床狀況比較 年齡、吸煙量、性別構成、白細胞數、中性粒細胞比例間差異無統計學意義 (P>0.05),而COPD組血清CRP與SP-D顯著高于對照組,COPD組1 s用力呼氣量占預計值百分數 (FEV1%預計值)、1 s用力呼氣量占用力肺活量百分數 (FEV1/FVC)、體質指數顯著低于對照組,差異有統計學意義 (P<0.05),具體見表1。
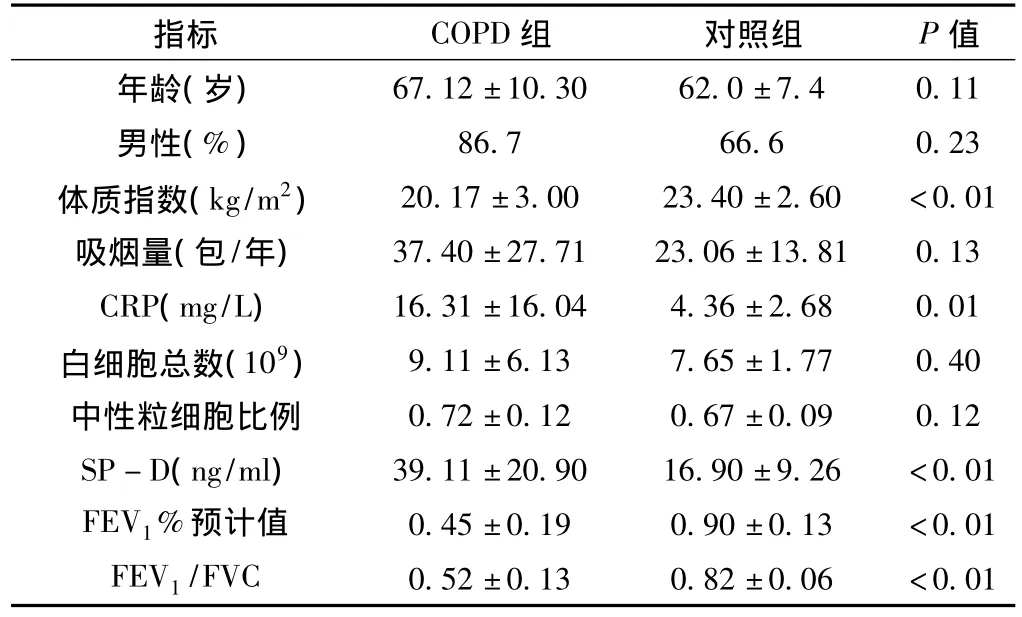
表1 COPD組與對照組的臨床狀況比較Table 1 Comparisons of clinical data between the COPD group and the control group
2.2 CRP及SP-D與其他指標的關系 COPD患者的體質指數與CRP之間具有顯著正相關,Pearson相關系數為0.21;COPD患者血清SP-D與FEV1%預計值具有顯著負向相關,Pearson相關系數為-0.48;CRP與SP-D無顯著相關性,具體見表2。
3 討論
COPD被認為是一種具有氣流受限特征的可以預防和治療的疾病,氣流受限不完全可逆、呈進行性發展,與肺部對香煙煙霧等有害氣體或有害顆粒異常炎癥反應有關[1]。本臨床研究的主要目的是為探索COPD穩定期血清CRP、SP-D的變化及與其他因素的相關性,本研究發現CRP和SP-D顯著高于健康對照組,CRP與體質指數顯著正相關,SP-D與FEV1%預計值顯著負相關,二者與中性粒細胞比例、白細胞數、吸煙量及FEV1/FVC無顯著相關性。
心血管危險因素、癌癥以及可致急慢性炎癥的疾病均可使CRP升高[4],運用RT-PCR和免疫組織化學技術,發現SPD廣泛存在于全身多處黏膜表面,表達SP-D的器官還包括:氣管、大腦、唾液腺、心臟、前列腺、腎臟和胰腺,表達SP-D的細胞還包括:肺泡巨噬細胞、皮膚、食道、小腸、泌尿道的上皮細胞等[5],上述部位的急慢性炎癥病變均有可能使SP-D升高,本研究在制定納入和排除標準時考慮到上述因素對SP-D的影響。CRP于炎癥發生后6~8 h開始升高[6],Koutsokera等[7]研究顯示,Anthonisen I型COPD急性加重患者經治療后可在3 d顯著降低,提示CRP隨著炎癥變化較快;另有研究顯示,急性肺損傷小鼠血清SP-D受損后第5天開始顯著升高,21 d時仍高于基礎水平,1個月后與基礎SP-D無顯著差異[8],提示SP-D恢復正常需要1個月左右,故本研究選擇COPD急性加重緩解超過2個月作為入選標準,以避免急性加重對二者濃度影響。
有證據顯示,COPD存在“肺外或系統炎癥”,并可通過系統炎癥標志物升高的水平確定其嚴重程度[9]。CRP是這些炎癥標志物中的一種,它主要由肝臟細胞合成,反應組織損傷及系統炎癥嚴重程度。Gan等[10]研究發現,CRP在COPD穩定期吸煙者及肺功能降低者顯著升高,這與本研究結果相似。本研究發現,CRP與體質指數存在正向相關性,這與Marie-Kathrin Breyer等的研究相似,去除肥胖患者本身存在脂肪量的影響,脂肪細胞增加可使脂肪細胞因子分泌增加,進一步使肝細胞產生和分泌CRP增加,體質指數低者與高者比較,CRP增高的程度顯著減小[11],因此可出現CRP與體質指數負向相關性,這提示COPD可能存在脂肪誘導的全身炎癥。
SP-D主要由Ⅱ型肺泡細胞和呼吸性細支氣管上clara細胞分泌,屬于膠原凝集素亞族,具有調節免疫和炎癥的作用,有助于機體對病原體清除[12]。Sin等報道,SP-D是一種與肺特定相關,并可在血中檢測到的蛋白,血中SP-D變化與肺部病理變化存在相關性,SP-D可能是COPD的肺部特異標記[13]。敲除SP-D基因鼠肺部的巨噬細胞被激活、金屬蛋白酶產生增多、肺組織的肺氣腫改變[8],說明SP-D與COPD發病及病情進展關系密切。本研究發現SP-D與FEV1%預計值存在負相關性,Sin等的研究也顯示,重度和極重度COPD穩定期SP-D濃度與FEV1值呈負向相關,雖然肺部損傷嚴重者肺部合成SP-D降低,但肺損傷后,已合成存儲在肺內SP-D可入血,這使肺損傷嚴重者SP-D濃度反而高,另外,COPD可導致全身炎癥反應,可能存在其他部位分泌SP-D入血。本研究顯示COPD患者血清SP-D顯著高于健康人,這與Mutti等[14]的研究相似,COPD存在持續慢性肺部炎癥,可促使SP-D分泌增加,肺上皮滲漏作用增強,可能與SP-D濃度升高有關。
綜上所述,在COPD穩定期,CRP顯著升高,BMI與CRP呈正向相關,在COPD病程中可能存在脂肪細胞誘導的全身炎癥;SP-D顯著升高,且與FEV1%預計值呈負相關,SP-D可能是監測COPD嚴重程度的生物標記物。
1 中華醫學會呼吸病學分會慢性阻塞性肺疾病組.COPD診治指南(2007年修訂版)[J].繼續醫學教育,2007,21(2):31-41.
2 閆莉,劉春霞,平芬.慢性阻塞性肺疾病的非藥物治療[J].河北醫藥,2010,32(21):3064.
3 李瑞,王紅.慢性阻塞性肺疾病治療的研究進展[J].實用心腦肺血管病雜志,2008,16(6):80.
4 Black S,Kushner I,Samols D.C-reactive Protein [J].Biol Chem,2004,279(47):48487-48490.
5 Madsen J,Kliem A,Tornoe I,et al.Localization of lung surfactant protein D on mucosal surfaces in human tissues [J].Journal of Immunology,2000,164(11):5866-5870.
6 林云霞,胡華成.CRP在慢性阻塞性肺病急性加重期的臨床意義[J].中國誤診學雜志,2009,9(9):2077.
7 Koutsokera A,Kiropoulos TS,Nikoulis DJ,et al.Clinical functional and biochemical changes during recovery from COPD exacerbations[J].Respiration Medcine,2009,103(6):926.
8 Sorensen GL,Husby S,Holmskov U.Surfactant protein A and surfactant protein D variation in pulmonary disease [J].Immunobiology,2007,212(45):381-416.
9 Agusti AG,Noguera A,Sauleda J,et al.Systemic effects of chronic obstructive pulmonary disease [J].Eur Respir J,2003,21(2):347-360.
10 Gan WQ,Man SF,Sin DD.The interactions between cigarette smoking and reduced lung function on systemic inflammation [J].Chest,2005,127(2):558-564.
11 Fantuzzi G,Mazzone T.Adipose tissue and atherosclerosis:exploring the connection[J].Arterioscler Thromb Vasc Biol,2007,27(5):996-1003.
12 Takahashi H,Chiba H,Shirator IM,et al.Elevated serum surfactant protein A and D in pulmonary alveolar microlithiasis[J].Respirology,2006,11(3):330-333.
13 Dahl M.Biomarkers for chronic obstructive pulmonary disease-Surfactant protein D and C-reactive protein [J].American Journal of Respiratory and Critical Care Medicine,2008,177(11):1177-1178.
14 Mutti A,Corradi M,Goldoni M,et al.Exhaled metallic elements and serum pneumoproteins in asymptomatic smokers and patients with COPD or asthma [J].Chest,2006,129(5):1288-1297.

