熱破碎番茄漿貯藏期間非酶褐變動力學分析
劉鳳霞,張 燕,汪厚銀,廖小軍,*
(1.中國農業大學食品科學與營養工程學院,農業部果蔬加工重點開放實驗室,國家果蔬加工工程技術研究中心,北京 100083;2.中國標準化研究院,北京 100088)
熱破碎番茄漿貯藏期間非酶褐變動力學分析
劉鳳霞1,張 燕1,汪厚銀2,廖小軍1,*
(1.中國農業大學食品科學與營養工程學院,農業部果蔬加工重點開放實驗室,國家果蔬加工工程技術研究中心,北京 100083;2.中國標準化研究院,北京 100088)
探討熱破碎番茄漿在貯藏過程中非酶褐變的規律,以期為番茄漿的貯藏提供指導。在0、25℃和37 ℃條件對其進行了5個月的貯藏研究,并對產品中與非酶褐變相關的指標總氨基酸、總糖、維生素C(VC)、5-羥甲基糠醛(HMF)和褐變度(BD)的變化分別應用零級、一級、聯合動力學模型進行了擬合分析。結果表明:聯合動力學模型較零級、一級動力學模型能更好地解釋熱破碎番茄漿貯藏過程中非酶褐變的動態變化。25℃和37 ℃貯藏過程中,熱破碎番茄漿中HMF含量和BD的變化呈線性關系,同時顏色指標亮度L*、紅值a*、黃值b*是HMF的函數,可用聯合動力學方程表示。較高的貯藏溫度(25℃和37℃)對熱破番茄漿中總氨基酸、總糖、VC、HMF含量、BD以及顏色指標(亮度L*、紅值a*、黃值b*)影響顯著(P<0.05),較低溫度(0℃)貯藏條件下,HMF含量、褐變度BD及顏色指標變化不明顯(P>0.05)。表明高溫貯藏顯著降低熱破碎番茄漿的品質,而低溫貯藏可有效保護熱破碎番茄漿的品質。
貯藏;非酶褐變;動力學;熱破番茄漿
番茄是許多加工食品非常寶貴的原料,全球食品工業對于番茄的需求量一直居高不下,據FAO統計,全世界每年用于加工的番茄達3000多萬噸,而在番茄加工制品中產量最高的是番茄漿,占番茄制品總量的60%[1]。以番茄為原料加工成番茄漿,由于加工過程中脫除了大部分水分,與新鮮番茄和番茄汁相比,其貯藏、運輸、包裝等成本大大降低,因此具有明顯的優勢。破碎工藝是番茄漿加工中的重要步驟,其中熱破碎是一種常用的破碎方法,即將番茄破碎后迅速加熱到80℃以上保持15s,使其中的果膠酶失活,保證果膠不被破壞,因此熱破碎番茄漿有較高的黏度[2]。但是在熱破碎番茄漿加工和貯藏過程中,常由于化學及生理生化反應而發生褐變,使加工品變色,降低食品營養品質和風味。非酶褐變是番茄漿在加工及貯藏過程中變色的主要原因,其反應的機制一般包括焦糖化反應、美拉德(Maillard)反應、VC氧化分解等[3]。焦糖化反應需要在高溫150~200℃條件下才能發生,本研究的溫度(低于40℃)條件下其發生的可能性很小,因此,熱破碎番茄漿在貯藏過程中發生的非酶褐變主要是由糖和氨基酸之間的Maillard反應以及VC的氧化分解引起的。近年來有關果蔬制品在貯藏加工過程中非酶褐變的動力學研究在國內外報道較多[4-9],然而未見關于熱破碎番茄漿在貯藏過程中褐變動力學分析的研究報道,本實驗在0、25℃及37℃三種溫度條件下,對熱破碎番茄漿中與非酶褐變相關指標變化進行觀察研究,探討熱破碎番茄漿在貯藏期間發生褐變的主要原因,應用相關動力學模型分析熱破碎番茄漿貯藏過程中的非酶褐變,以指導番茄漿的貯藏、保證產品品質。
1 材料與方法
1.1 材料與處理
熱破番茄漿(36.8 °Brix) 中糧新疆屯河股份有限公司。番茄漿以鋁箔袋(100g/包)密封,分別置于0、25℃和37℃貯藏150d,各項指標每30d測定1次,每組3次重復。番茄漿在做指標檢測前,加超純水還原至4.0°Brix后于10000r/min離心30min,上清液經0.45μm的纖維素膜過濾,收集濾液待測。
1.2 試劑與儀器
氨基酸、蔗糖、葡萄糖、果糖、H M F、V C標樣(色譜純) 美國Sigma公司;甲醇、乙腈(色譜純) 德國Merck公司;其他試劑(均為分析純) 北京化學試劑公司。
高效液相色譜儀 德國諾爾儀器有限公司;SC-80C全自動色差儀 北京康光儀器廠;UV-762型分光光度計上海陵光有限公司;868型pH計 美國奧立龍公司;WAY-2S型數字阿貝折射儀 上海精密科學儀器有限公司;EY-300A分析天平 日本松下電器公司;TDL-5-A型高速離心機 上海一恒科技有限公司;恒溫水浴鍋 北京醫療設備廠。
1.3 方法
1.3.1 品質動力學理論
近年來有關食品在貯藏加工過程中的動力學研究在國內外報道了很多,大多都從動力學變化的角度研究食品品質的損失。品質因子C(如氨基酸、糖、VC、褐變度等)的變化速率可以表示為:

式中:C為測定指標在任意時間的值;t為時間;k為動力學常數;n為級數。從前人的研究來看,大多數食品的質量變化與時間關系表現出零級或一級的反應,即n=0或n=1。Garza等[4]對桃漿在熱加工過程中非酶褐變的研究、王素雅等[5]對香蕉汁、Burburlu等[6]對濃縮蘋果汁在貯藏過程非酶褐變的研究中,認為其非酶褐變都符合零級動力學模型;Johnson等[7]認為橙汁貯藏過程中的非酶褐變符合一級動力學模型。零級和一級動力學方程分別如下:


Wang等[9]用上述3種動力學模型比較分析了胡蘿卜濃縮汁在貯藏過程中褐變度(BD)、5-羥甲基糠醛(HMF)和氨基酸的變化,發現用聯合動力學模型分析時擬合程度最高。
式(2)~(4)中:C為測定指標在任意時間的值;C0為測定指標的起始值;t為時間;k、k1、k2為動力學常數。
1.3.2 指標測定方法
熱破番茄漿中HMF含量的測定:采用高效液相色譜法[10]進行;褐變度(brown degree,BD)的測定:采用分光光度法[11]進行;氨基酸的測定:采用高效液相色譜法[12]進行;總糖、蔗糖、果糖、葡萄糖的測定:采用高效液相色譜法[9]進行;VC的測定:采用高效液相色譜法[13]進行;色澤變化的測定:采用全自動色差儀,樣品搖勻后在反射模式下測定亮度L*、紅值a*、黃值b*(L*值表示亮度,范圍在0~100之間,L*值越高表明樣品表面越白,a*>0表示紅值、a*<0表示綠值,b*>0表示黃值、b*<0表示藍值);pH值測定:采用p H計進行測定;可滴定酸的測定:參照Rodrigod等[14]的方法,采用0.02mol/L NaOH溶液滴定至終點pH8.1;可溶性固形物含量:采用阿貝折射儀,連接水浴使設備溫度控制在(20±2)℃后測定;番茄紅素的測定:參照Athanasia等[15]的方法,用含有0.025% BHT的氯仿作為提取溶劑,在避光避氧的情況下,少量多次添加氯仿來提取番茄漿中的番茄紅素,直到番茄汁成無色為止,在505nm測定吸光度。
1.3.3 數據處理
試驗數據采用統計軟件 Microcal Origin 8.0(Microcal Software, Inc., Northampton USA)進行方差分析,顯著水平為0.05;同時對相關指標的變化進行動力學分析或回歸分析,并計算相關系數R2(R2范圍在0~1之間,R2越接近于1,表明擬合度越高),所有的指標做3個重復。
2 結果與分析
2.1 貯藏過程中總氨基酸、總糖、VC的變化及動力學分析
研究發現,熱破番茄漿中的主要氨基酸為天冬氨酸、谷氨酸、絲氨酸、脯氨酸、纈氨酸、亮氨酸和苯丙氨酸。貯藏過程中不同氨基酸的變化趨勢非常相似,即隨貯藏時間的延長不同氨基酸的含量均有一定程度的下降,因此引起總氨基酸含量的下降(圖1a)。番茄漿中氨基酸的損失主要是由貯藏過程中氨基酸與還原糖(如果糖等)發生美拉德反應造成的[16-17]。熱破番茄漿在37℃經5個月貯藏,總氨基酸損失約96.55%,其中谷氨酸、脯氨酸、天冬氨酸、苯丙氨酸、亮氨酸、絲氨酸、纈氨酸的損失率分別為99.46%、97.77%、92.70%、91.95%、99.13%、96.55%、87.76%。在貯藏過程中每種氨基酸的消耗量不同,其中谷氨酸的損失最大,但是不同氨基酸對番茄漿褐變的影響程度并不取決于其消耗量,因為不同的氨基酸在反應過程中會產生具有不同吸光特性的顯色物質[18]。
熱破番茄漿中的糖主要為蔗糖和果糖,而葡萄糖含量很少(小于100mg/kg),在貯藏過程中熱破番茄漿中的蔗糖、果糖和葡萄糖均呈下降趨勢,導致總糖含量的下降(圖1b)。在貯藏期間,與番茄漿中主要糖變化有關的反應主要有兩條途徑:一是低pH值條件下蔗糖易轉化為果糖和葡萄糖導致還原糖含量的升高;二是還原糖和氨基酸之間發生的Maillard反應導致還原糖含量的下降[9]。在本研究中果糖的含量在貯藏的過程中有不同程度的下降,表明果糖參與Maillard反應的速率略大于蔗糖轉化為果糖和葡萄糖的速率。
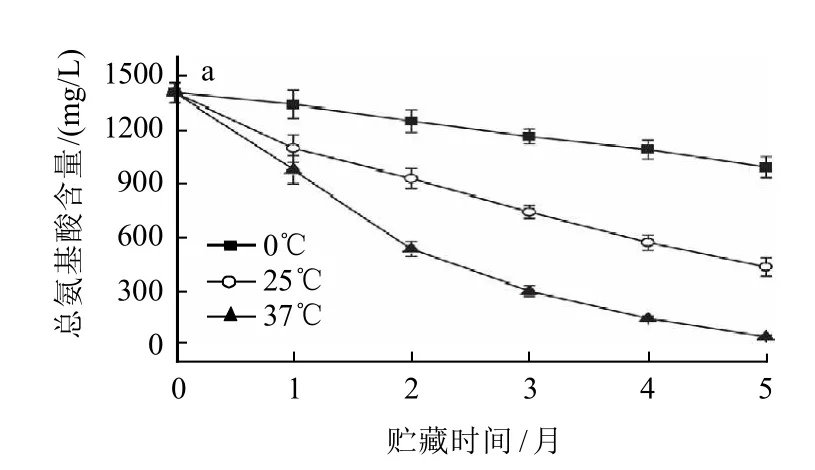

圖1 熱破番茄漿貯藏期間總氨基酸(a)、總糖(b)、VC(c)含量的變化Fig.1 Changes of total free amino acids (a), total sugar (b), and vitamin C content (c) in HBTP during storage
如圖1c所示,貯藏過程中,熱破番茄漿中的VC含量隨貯藏時間的延長顯著下降(P<0.05),同時VC的損耗具有很強的溫度依賴性,在0、25℃和37℃貯藏過程中,損失量分別為33.31%、60.97%、87.49%,即高溫條件會促進VC的氧化降解。VC的氧化在食品的非酶褐變中起著非常重要的作用,其氧化過程中首先形成脫氫抗壞血酸[19],后者易與氨基酸經過一系列的反應生成深色物質,貯藏過程中VC的氧化降解速率往往取決于加工形式、貯藏條件及包裝材料的不同[20]。
如前所述,食品的品質變化可以用零級動力學模型和一級動力學模型[4-7]以及聯合動力學模型[8-9]進行分析。圖1中的總氨基酸、總糖、VC含量變化趨勢用這三種模型進行擬合分析,其反應常數如表1所示。用零級反應模型分析所得的相關系數R2在0.556~0.997之間,用一級反應模型分析所得的相關系數R2在0.578~0.994之間,用聯合模型分析所得的相關系數R2在0.607~0.998之間,表明熱破碎番茄漿貯藏過程中的總氨基酸、總糖、VC含量變化可以用零級或一級或聯合模型進行擬合,且除了總糖外,聯合動力學模型的擬合程度均優于一級模型和零級模型,用聯合模型能更好解釋熱破碎番茄漿貯藏過程中總氨基酸、總糖、VC的動態變化。在零級和一級反應模型中,熱破番茄漿的總氨基酸、總糖、VC的反應常數隨著溫度的增加而增加,表明熱破番茄漿貯藏過程中總氨基酸、總糖、VC損失的速度與溫度有很大的相關性。

表1 熱破碎番茄漿貯藏過程中各指標變化的速率常數和相關系數Table 1 Reaction rate constants and correlation coefficients of different indices for HBTP during storage
2.2 HMF與BD的變化及動力學分析
圖2為熱破番茄漿在0、25℃和37℃貯藏5個月過程中HMF含量和BD的變化,0℃貯藏5個月過程中熱破碎番茄漿中HMF含量和BD沒有顯著變化(P>0.05),而25℃和37℃貯藏過程中HMF含量和BD隨著貯藏時間的延長而顯著增加(P<0.05),表明較高溫度能夠促進番茄漿HMF的形成及褐變反應。另外,Ajandouz等[21]報道,HMF的主要形成途徑發生在較低pH值條件,本研究發現,熱破番茄漿中可滴定酸含量隨貯藏時間的增加和貯藏溫度的升高有增加的趨勢,而pH值則有下降的趨勢,這種變化主要是由Maillard反應中糖和羰氨反應的中間產物分解為糖醛酸等酸性物質,以及Maillard反應引起氨基酸中堿性集團的消失導致其酸性增加[22],酸性增加對貯藏過程中HMF的形成起促進作用,這一點與本研究中番茄漿HMF含量的變化是相一致的。圖2中HMF和BD的變化趨勢分別用零級、一級、聯合動力學模型進行擬合分析,其反應常數如表1所示。用零級反應模型分析所得的相關系數R2在0.187~0.893之間,用一級反應模型分析所得的相關系數R2在0.411~0.959之間,用聯合模型分析所得的相關系數R2在0.706~0.999之間。從HMF和BD的模型擬合情況來看,相同條件下,聯合模型的擬合程度均優于一級模型和零級模型,表明用聯合模型能更好解釋熱破碎番茄漿貯藏過程中HMF和BD的動態變化。
HMF和BD是果蔬及其制品的兩個重要品質指標,同時HMF的含量可反映果蔬產品加工和貯藏過程中的褐變度。圖2中可見在貯藏過程中,熱破碎番茄漿中的HMF含量和BD隨貯藏時間和貯藏溫度的變化趨勢非常相似。25℃和37℃貯藏過程中,熱破碎番茄漿HMF和BD的變化存在線性關系,相應的線性回歸方程如表2所示,相關系數R2分別是0.802和0.992。Wang等[9]在研究胡蘿卜汁貯藏過程中非酶褐變時得出相同結論,即在25℃和37℃貯藏溫度下,HMF和BD的變化存在線性關系。
2.3 貯藏過程中顏色的變化
顏色是果蔬制品的重要品質指標,它通常能夠影響消費者對產品的可接受性。亮度L*、紅值a*、黃值b*是觀測果蔬制品顏色變化的常用參數。如前所述,在貯藏期間熱破番茄漿中的還原糖和氨基酸之間的Maillard反應及VC的氧化降解使番茄漿中褐變度增加,這必然導致產品顏色發生變化。熱破番茄漿在貯藏過程中的顏色的變化如圖3所示,從圖3可以看出,貯藏期間番茄漿的亮度L*、紅值a*、黃值b*呈下降趨勢,表明番茄漿在貯藏期間隨貯藏時間的延長顏色變暗。0℃貯藏5個月后,番茄漿的亮度L*、紅值a*、黃值b*均有下降,但變化不顯著(P>0.05),而25、37 ℃貯藏時各顏色指標值隨貯藏時間延長顯著下降(P<0.05),尤其以37℃時下降最為明顯,表明在較高溫度條件下番茄漿的顏色褐變加劇,這一結論和BD的變化趨勢是一致的。另外,在研究中發現,不同貯藏條件下,熱破碎番茄漿中的番茄紅素含量有一定波動,但變化不顯著(P>0.05),Ordonez-Santos等[23]也發現,貯藏6個月后的番茄漿番茄紅素的變化不明顯。顏色的變化不僅來自Maillard反應及VC的氧化降解,同時還受番茄紅素變化的影響[24],本研究中,番茄紅素變化不顯著(P>0.05),表明貯藏過程中的顏色變化主要是由Maillard反應及VC的氧化降解引起的,這一結論與氨基酸、糖及VC的變化相符的。
貯藏過程中產品顏色的變化與非酶褐變過程中產生的HMF有很大關系,本實驗研究發現,在較高的貯藏溫度25℃和37℃貯藏過程中番茄漿的顏色參數L*、a*、b*的變化是HMF的函數,可用表2中所示的聯合動力學方程表示,回歸方程的相關系數均在0.822以上,表明HMF與顏色指標亮度L*、紅值a*、黃值b*呈現很好的相關性,貯藏過程中可通過抑制HMF形成來防止產品顏色的褐變。

圖 3 熱破番茄漿貯藏過程中 L*(A)、a*(B)、b*(C)值的變化Fig.3 Changes of L*, a* and b* in HBTP during storage

表2 熱破碎番茄漿貯藏過程中HMF含量與BD、 L*、a*、 b*的相關性Table 2 Correlations between HMF and BD, L*, a*, b* for HBTP during storage
3 結 論
熱破碎番茄漿中的主要氨基酸為天冬氨酸、谷氨酸、絲氨酸、脯氨酸、纈氨酸、亮氨酸和苯丙氨酸;主要糖為蔗糖和果糖,葡萄糖含量很少。25℃和37℃貯藏5個月過程中,總氨基酸、總糖、VC含量、顏色指標(亮度L*、紅值a*、黃值b*)均顯著下降(P<0.05),HMF和BD顯著增加(P<0.05);0℃貯藏條件下,總氨基酸、總糖、VC含量亦明顯下降(P<0.05),但HMF、BD及顏色變化不明顯(P>0.05)。熱破碎番茄漿貯藏過程中的總氨基酸、總糖、VC、HMF、BD變化可以用零級或一級或聯合模型進行擬合,且除了總糖外,聯合模型的擬合程度均優于一級模型和零級模型,用聯合模型能更好解釋熱破碎番茄漿貯藏過程中非酶褐變的動態變化。25℃和37℃貯藏條件下,番茄漿的HMF與BD變化存在線性關系;同時感官顏色指標(亮度L*、紅值a*、黃值b*)和HMF也具有很好的相關性,可用聯合動力學方程表示,表明一定程度上可通過控制HMF的形成來防止番茄漿在貯藏過程中發生顏色的褐變,保護產品的品質。
另外,番茄漿在加工和貯藏過程中品質變化普遍存在,本實驗只研究了其貯藏過程中的品質變化,并未對加工過程中番茄漿的品質變化進行研究。盡管有關番茄漿的加工技術已較為成熟,但是加工因素對其品質的影響仍需要進一步具體研究,以指導番茄漿的生產。
[1] 司瑞敬. 關鍵工藝步驟對番茄汁品質的影響[D]. 北京: 中國農業大學, 2005.
[2] GOODMAN C L, FAWCETT S, BARRINGER S A. Flavor, viscosity,and color analyses of hot and cold break tomato juices[J]. Journal of Food Science, 2002, 67(1): 404-408.
[3] HUSEYIN B, FAHRETTIN G, SAMI E. Non-enzymic browning reactions in boiled grape juice and its models during storage[J]. Food Chemistry, 1999, 64 (2): 89-93.
[4] GARZA S, IBARZ A, PAGAN J, et al. Non-enzymatic browning in peach puree during heating[J]. Food research international, 1999, 32(5):335-343.
[5] 王素雅, 王璋. 香蕉汁儲藏過程中非酶褐變的研究[J]. 食品科學,2005, 26(12): 81-85.
[6] BURDURLU H S, KARADENIZ F. Effect of storage on non-enzymatic browning of apple juice concentrates[J]. Food Chemistry, 2003, 80(1):91-97.
[7] JOHNSON J R, BRADDOCK R J, CHEN C S. Kinetics of ascorbic acid loss and non-enzymatic browning in orange juice serum: Experimental rate constants [J]. Journal of Food Science, 1995, 60(2): 502-505.
[8] GONZALEZ C, IBARZ A, ESPLUGA S, et al. Cinética de pardeamiento no enzimático en zumos de frutas[J]. Alimentaria, 1988, 198(2): 53-60.
[9] WANG Houyin, HU Xiaosong, CHEN Fang, et al. Kinetic analysis of non-enzymatic browning in carrot juice concentrate during storage [J].European Food Research and Technology, 2006, 223(2): 282-289.
[10] RADA-MENDOZA M, OLANO A, VILLAMIEL M. Determination of hydroxymethylfurfural in commercial jams and in fruit-based infant foods[J]. Food Chemistry, 2002, 79(4): 513-516.
[11] LIU S C, CHANG H M, WU J S B. A study on the mechanism of browning in Mei liqueur using model solutions[J]. Food Research International, 2003, 36(6): 579-585.
[12] VAN EIJK H M H, SUYLEN D P L, DEJONG C H C, et al. Measurement of amino acid isotope enrichment by liquid chromatography mass spectroscopy after derivatization with 9-fluorenylmethylchloroformate[J]. Journal of Chromatography B, 2007, 856(1/2): 48-56.
[13] RODRIGUEZ-BERNALDO A, LOPEZ-HEMANDEZ J, SIRNAILOZANO J. Determination of Vitamin C in Sea Urchin: Comparison of Two HPLC Methods[J]. Chromatographia, 2001, 53(2): 246-249.
[14] RODRIGO D, ARRANZ J I, KOCH S, et al. Physico-chemical characteristics and quality of refrigerated Spanish orange-carrot juices and influence of storage conditions[J]. Journal of Food Science, 2003, 68(4):2111-2116.
[15] ATHANASIA M G, KONSTANTINOS G A, PARIS C C, et al. Prediction of lycopene degradation during a drying process of tomato pulp[J].Journal of Food Engineering, 2006, 74(1): 37-46.
[16] BUEDO A P, ELUSTONDO M P, URBICAIN M J. Amino acid loss in peach juice concentrate during storage[J]. Innovative Food Science and Emerging Technologies, 2001, 1(4): 255-260.
[17] WANG Houyin, NI Yuanying, HU Xiaosong, et al. Kinetics of amino acid loss in carrot juice concentrate during storage[J]. LWT-Food Science and Technology, 2007, 40(5): 785-792.
[18] GARCIA-BANOS J L, DEL CASTILLO M D, SANZ M L, et al.Maillard reaction during storage of powder enteral formulas[J]. Food Chemistry, 2005, 89(4): 555-560.
[19] CERNISEV S. Effects of conventional and multistage drying processing on non-enzymatic browning in tomato[J]. Journal of Food Engeering,2010, 96(1): 114-118.
[20] DAVEY M W, VAN MONTAGU M, INZE D, et al. Plant L-ascorbic:chemistry, function, metabolism, bioavailable and effects of processing[J]. Journal of Food Science and Agricultural, 2000, 80(2): 825-860.
[21] AJANDOUZ E H, DESSEAUX V, TAZI S, et al. Effects of temperature and pH on the kinetics of caramelisation, protein cross-linking and Maillard reactions in aqueous model systems[J]. Food Chemistry, 2008,107(3): 1244-1252.
[22] LIU S C, YANG D J, JIN S Y, et al. Kinetics of color development, pH decreasing, and anti-oxidative activity reduction of Maillard reaction in galactose/glycine model systems[J]. Food Chemistry, 2008, 108(2):533-541.
[23] ORDONEZ-SANTOS L E, VAZQUEZ-ODERIZ L, ARBONESMACINEIRA E, et al. The influence of storage time on micronutrients in bottled tomato pulp[J]. Food Chemistry, 2009, 112(1): 146-149.
[24] DAVOODI M G, VIJAYANAND P, KULKAMI S G, et al. Effect of different pre-treatments and dehydration methods on quality characteristics and storage stability of tomato powder[J]. LWT, 2007, 40(10):1832-1840.
Kinetic Analysis of Non-enzymatic Browning in Hot Break Tomato Paste during Storage
LIU Feng-xia1,ZHANG Yan1,WANG Hou-yin2,LIAO Xiao-jun1,*
(1. Key Laboratory of Fruit and Vegetable Processing, Ministry of Agriculture, National Research Centre for Fruits and Vegetable Processing Engineering and Technology, College of Food Science and Nutritional Engineering, China Agricultural University, Beijing 100083, China;2. China National Institute of Standardization, Beijing 100088, China)
Changes of qualities related to non-enzymatic browning in hot break tomato paste (HBTP) at different storage temperatures (0, 25 ℃ and 37 ℃) for 5 months were evaluated in this study, in order to guide the storage of HBTP. Changes of free amino acids, total sugar, vitamin C, 5-hydroxymethylfurfural (HMF) and browning degree (BD) were fitted with zero-,first-order and combined models, respectively, and it was found that the combined model could better explain the kinetic changes of non-enzymatic browning in HBTP during storage. At 25 ℃ or 37 ℃, a good correlation between HMF formation and BD was observed, and color parameters (lightness L*, redness a* and yellowness b*) could be expressed by combined equations as functions of HMF. Higher storage temperatures (25 ℃ and 37 ℃) had significant effects (P<0.05) on changes of total amino acids, total sugar, vitamin C, HMF, BD and color parameters in HBTP. When stored at 0 ℃, changes of HMF, BD and color parameters in HBTP were not significant (P >0.05). All the results indicated that the quality of HBTP was deteriorated significantly during higher temperature storage, but could be protected well during lower temperature storage.
storage;non-enzymatic browning;kinetics;hot break tomato paste (HBTP)
TS255.3;S641.2
A
1002-6630(2011)10-0260-06
2010-08-23
“十五”國家重大科技攻關項目(2001BA501A23)
劉鳳霞(1987—),女,博士研究生,研究方向為農產品加工與貯藏工程。E-mail:xia870529@163.com
*通信作者:廖小軍(1966—),男,教授,博士,研究方向為農產品加工與貯藏工程。 E-mail:liaoxjun@hotmail.com

