(Ca1-x-y Lu y)M oO4∶x Eu3+紅色熒光粉的化學共沉淀合成與光致發光
楊玉玲 黎學明*,, 馮文林 李武林 陶傳義
(1重慶大學化學化工學院,重慶 400044) (2重慶大學光電工程學院,光電技術及系統教育部重點實驗室,重慶 400044) (3重慶理工大學應用物理學院,重慶 400044)
(Ca1-x-yLuy)M oO4∶x Eu3+紅色熒光粉的化學共沉淀合成與光致發光
楊玉玲1黎學明*,1,2馮文林3李武林2陶傳義2
(1重慶大學化學化工學院,重慶 400044) (2重慶大學光電工程學院,光電技術及系統教育部重點實驗室,重慶 400044) (3重慶理工大學應用物理學院,重慶 400044)
使用NH4HCO3-NH3·H2O混合沉淀劑,采用化學共沉淀法合成(Ca1-x-yLuy)MoO4∶x Eu3+紅色熒光粉,通過XRD、EDS、熒光光譜和CIE色度圖研究該熒光粉的晶體結構、成分組成及發光性能。結果表明,實驗按照理論化學計量比成功合成了(Ca1-x-yLuy)MoO4∶x Eu3+紅色熒光粉,該熒光粉為CaMoO4白鎢礦結構;(Ca1-x-yLuy)MoO4∶x Eu3+具有7F0→5L6(394 nm)和7F0→5D2(465 nm)的強電子吸收,且在613 nm處可發射高強度紅光,其色坐標為(0.666 5,0.332 9),明顯優于傳統的Y2O2S∶Eu3+紅色熒光粉;此外,當Lu含量為30mol%時,熒光粉發光強度最佳。
(Ca1-x-yLuy)MoO4∶x Eu3+;化學共沉淀;發光;紅色熒光粉
熒光轉換型白光發射二極管(W-LED)具有高效節能、無污染、壽命長等優點,正逐漸取代傳統的白熾燈、熒光燈,將成為 21世紀的主要照明光源[1-3]。在白光LED的實現過程中,紅色熒光粉具有重要作用,它不僅可克服黃色熒光粉YAG∶Ce3+與藍光LED形成的白光因缺少紅光成分顯色性差的缺點,也是三基色熒光粉的重要組成。但是,目前廣泛應用于W-LED的紅色熒光粉(如Y2O2S∶Eu3+)發光效率低且化學性質不穩定[4],嚴重影響W-LED的應用性能。因此,研究出一種在近紫外光和藍光激發下具有高光輸出率、半峰寬小且低光衰的紅色熒光粉,對于改善W-LED的性能十分重要。
大量研究表明,化學性質穩定的白鎢礦鉬酸鹽體系是一種性能優異的基質材料[5-8]。Hu[9]等采用高溫固相法制備CaMoO4∶Eu3+紅色熒光粉。研究表明,該熒光粉在近紫外(394 nm)和藍光(464 nm)激發下可發射高純度紅光,發光強度為傳統紅色熒光粉Y2O2S∶Eu3+的5倍。與黃、綠、藍色熒光粉相比,該CaMoO4∶Eu3+紅色熒光粉的發光效率仍然較低。元素Y、La、Gd和Lu處于全充滿、半充滿或全空的穩定狀態,屬于光學惰性元素,因此特別適宜用作基質材料。高飛[10]通過對 Li3Ba2Ln3-xEux(MoO4)8(Ln=La,Gd,Y)的研究表明,該紅色熒光粉不僅具有很強的基質吸收帶,并且在616 nm處有強紅光發射;Haque[11]等也發現,光學惰性元素Y的引入,使NaCaY(MoO4)3∶Eu的發光強度為CaMoO4∶Eu,Na的1.6倍。但是,目前熒光粉主要采用傳統高溫固相法制備,合成的產品顆粒較大需進行后處理,嚴重影響熒光粉的發光性能。而化學共沉淀法由于操作簡單、合成的產品組分均勻且顆粒較小等優點而廣泛應用于無機材料的制備[12]。因此,實驗擬以NH4HCO3-NH3為沉淀劑,采用化學共沉淀法合成(Ca1-x-yLuy)MoO4∶x Eu3+紅色熒光粉,并討論Lu的引入對晶體結構及發光性能的影響。
1 實驗部分
1.1 (Ca0.85-x Lu x)M oO4∶0.15Eu3+的合成
按(Ca0.85-xLux)MoO4∶0.15Eu3+化學式物質的量比分別稱取Eu2O3(99.99%)、Ca(NO3)2·4H2O(A.R.)、Lu(NO3)3·4H2O(A.R.),用適量稀硝酸(HNO3∶H2O=1∶1,V/V)加熱溶解Eu2O3,用去離子水分別溶解Ca(NO3)2·4H2O、Lu(NO3)3·4H2O和(NH4)6Mo7O24·4H2O,將上述溶液混合均勻即為母液。配置一定濃度比的NH4HCO3-混合沉淀劑。在不斷劇烈攪拌下,使用蠕動泵(流量5 mL·min-1)將母液滴加到沉淀劑中,結束后繼續攪拌30 min,停止攪拌,陳化、抽濾后在110~120℃干燥12 h即得前驅體。將前驅體在500℃預燒,900℃煅燒后隨爐冷卻,得到分散均勻的熒光粉樣品。
1.2 實驗表征
使用XRD-6000型X射線衍射儀分析熒光粉的晶體結構,工作電壓和電流分別為40 kV和30 mA,掃描速度8°·min-1,步長0.02°,掃描范圍10°~70°;使用INCA-350型X射線能譜儀分析熒光粉的化學元素組成;利用RF-5301型分子熒光光度計測試熒光粉的激發與發射光譜,光源為氙燈,激發和發射狹縫均為3 nm;使用PMS-50(增強型)紫外-可見-近紅外光譜分析系統測定熒光粉的色度學參數,儀器掃描范圍300~800 nm,掃描間隔5 nm。
2 結果與討論
2.1 Lu摻雜對晶體結構的影響
圖1為使用混合沉淀劑制備的(Ca0.85-xLux)MoO4∶0.15Eu3+熒光粉的XRD圖,煅燒時間4 h。由圖可知,當元素Lu的摻雜量較少,即低于50mol%時,樣品的所有衍射峰均與CaMoO4標準卡JCPDS 29-0351一致,為單一的四方晶系白鎢礦結構,無任何雜質峰出現,表明適量Lu元素的引入不會破壞熒光粉的晶體結構。但當Lu元素摻雜量超過50mol%后,樣品XRD圖出現少量雜峰,且衍射峰強度明顯下降。在(Ca0.85-xLux)MoO4∶0.15Eu3+體系中,Eu3+和Lu3+分別取代CaMoO4晶體中的Ca2+而非Mo6+。這是因為Eu3+(0.094 7 nm)和Lu3+(0.084 8 nm)與Ca2+(0.099 nm)的離子半徑相差較小,而與Mo6+(0.065 nm)相差太大,如果取代Mo6+格位會使晶體體積發生較大的變化,從而將改變樣品的晶體結構,這與XRD的實驗結果不一致。但是,若Lu元素的摻雜量過多,大量Ca2+的取代導致晶體結構畸變程度加大[13],甚至破壞原有的鉬酸鈣白鎢礦結構,因而在XRD圖中出現了少量的雜峰。
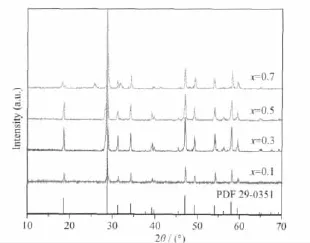
圖1 (Ca0.85-x Lu x)MoO4∶0.15Eu3+的XRD圖Fig.1 XRD patterns of(Ca0.85-x Lu x)MoO4∶0.15Eu3+ phosphors
在本實驗中,Ca2+存在兩種取代方式:2M3+(M= Eu或Lu)取代3Ca2+后,在晶格中形成一個Ca2+空位,或者1M3+取代1Ca2+后產生1個剩余電荷。雖然大量研究表明[14-15],使用堿金屬離子M+(M=Li,Na,K)等電荷補償劑可以有效改善在取代過程中的電荷不平衡情況。但王貴喜等[16]的研究表明,本實驗存在的兩種取代方式導致的缺陷有助于加強該熒光粉的發光強度并進一步改善其性能。
2.2 (Ca0.85-x Lu x)M oO4∶0.15Eu3+的元素分析
圖 2給出(Ca0.45Lu0.4)MoO4∶0.15Eu3+紅色熒光粉的EDS譜圖。由圖可知,(Ca0.45Lu0.4)MoO4∶0.15Eu3+中含有Ca、O、Mo、Eu和Lu元素。通過EDS表面組成分析可知,(Ca0.45Lu0.4)MoO4∶0.15Eu3+中 Ca、O、Mo、Eu和 Lu的重量百分比分別為 6.90%、23.11%、35.63%、9.11%和25.25%,與理論比6.66%、23.64%、35.43%、8.4%和25.85%相接近,表明實驗通過化學共沉淀法且按理論百分比成功合成了(Ca0.45Lu0.4) MoO4∶0.15Eu3+紅色熒光粉。
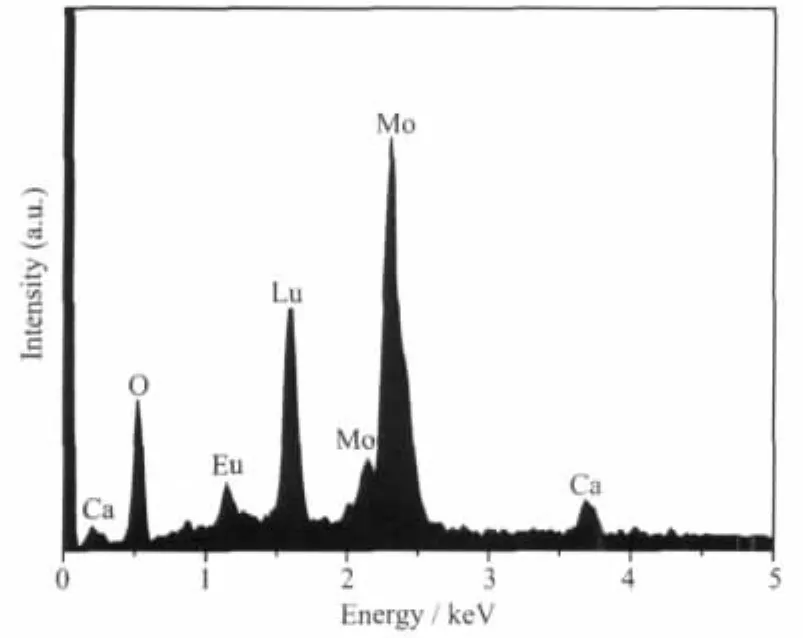
圖2 (Ca0.45Lu0.4)MoO4∶0.15Eu3+的EDS譜圖Fig.2 EDSof(Ca0.45Lu0.4)MoO4∶0.15Eu3+phosphors
2.3 (Ca0.85-x Lu x)MoO4∶0.15Eu3+發光性能
圖 3為 900℃下煅燒 4 h的 (Ca0.55Lu0.3)MoO4∶0.15Eu3+和CaMoO4∶0.15Eu3+的激發光譜圖,監測波長為613 nm。由圖可知,Lu元素的引入對熒光粉的激發光譜峰的位置和形狀沒有影響,(Ca0.55,Lu0.3) MoO4∶0.15Eu3+和CaMoO4∶0.15Eu3+的激發光譜均有一個300~350 nm寬電荷遷移帶,為電荷密度從配體O2-的2p軌道向金屬離子Mo6+和Eu3+的4d和4f分子軌道重新分配的結果[17]。該電荷遷移帶很弱,這是因為Eu3+、Lu3+取代了晶體中部分Ca2+的格位,從而使晶體結構產生微小的缺陷所致[16],但該缺陷可使MoO42-吸收的能量更有效傳遞給Eu3+,明顯增強了465 nm的7F0→5D2電子躍遷。此外,位于362、383、394、425、465和475 nm的窄峰均為Eu3+的4f7基態向激發態躍遷,分別對應于7F0→5D4、7F0→5L7、7F0→5L6、7F0→5D3、7F0→5D2和7F0→5D1躍遷。其中,7F0→5L6和7F0→5D2吸收遠強于其它峰,這有利于提高紅色熒光粉與紫外光和藍光LED芯片的匹性配,從而改善商業W-LED的顯色性能。
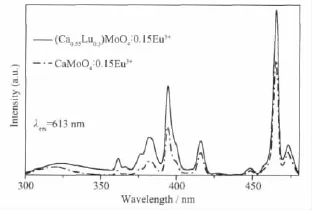
圖3 (Ca0.55Lu0.3)MoO4∶0.15Eu3+和CaMoO4∶0.15Eu3+的激發光譜圖Fig.3 Excitaion spectra of(Ca0.55Lu0.3)MoO4∶0.15Eu3+and CaMoO4∶0.15Eu3+phosphors
圖 4為 (Ca0.55Lu0.3)MoO4∶0.15Eu3+和 CaMoO4∶0.15Eu3+的發射光譜,激發波長為394 nm。由圖可知,(Ca0.55Lu0.3)MoO4∶0.15Eu3+和CaMoO4∶0.15Eu3+的峰形和峰位置均相同,主要由614 nm的5D0→7F2電偶極躍遷和590 nm的5D0→7F1磁偶極躍遷組成。但(Ca0.55Lu0.3)MoO4∶0.15Eu3+紅色熒光粉的發光強度明顯高于CaMoO4∶0.15Eu3+紅色熒光粉。這是因為Eu3+的f-f躍遷是f6組態內的躍遷,始態和終態的宇稱相同,因而電偶極躍遷是禁阻的。但在(Ca0.55Lu0.3) MoO4∶0.15Eu3+晶格中,Lu3+的引入使Eu3+周圍環境的對稱中心移動,宇稱相反的5d和5g組態與4f組態混合,從而使宇稱禁阻能更好的解除而產生5D0→7F2的電偶極躍遷[18],因而發射高強度紅光。此外,Hu[9]通過對比 CaMoO4∶Eu3+和傳統紅色熒光粉Y2O2S∶Eu3+的熒光光譜發現,在394和464 nm激發下,Y2O2S∶Eu3+的發射光譜均為一個600~700 nm寬帶,最大峰位于650 nm處,且其發光強度分別為CaMoO4∶Eu3+發光強度的 20%和 15%。因此,(Ca0.55Lu0.3)MoO4∶0.15Eu3+紅色熒光粉的發光性能不僅明顯優于傳統的紅色熒光粉,還改善了CaMoO4∶Eu3+紅色熒光粉的發光強度。
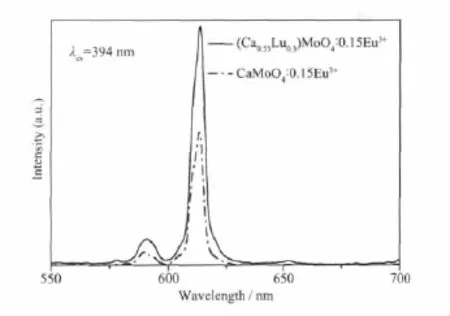
圖4 (Ca0.55Lu0.3)MoO4∶0.15Eu3+和CaMoO4∶0.15Eu3+的發射光譜Fig.4 Emission spectra of(Ca0.55Lu0.3)MoO4∶0.15Eu3+and CaMoO4∶0.15Eu3+phosphors
發光色度是表征發光材料特性的一個基本參數[19-20]。圖5為(Ca0.55Lu0.3)MoO4∶0.15Eu3+在近紫外光激發下的CIE色度圖。測量結果表明,樣品的色坐標值為(0.666 5,0.332 9),與傳統的紅色熒光粉Y2O2S∶Eu3+(0.631,0.350)相比,(Ca0.55Lu0.3)MoO4∶0.15Eu3+熒光粉的色坐標更接近規定的紅色色度坐標(0.67,0.33),具有高純度的紅光。因此,該紅色熒光粉有可能取代傳統商業紅色熒光粉并應用于WLED中,從而改善W-LED的顯色性和使用性能。
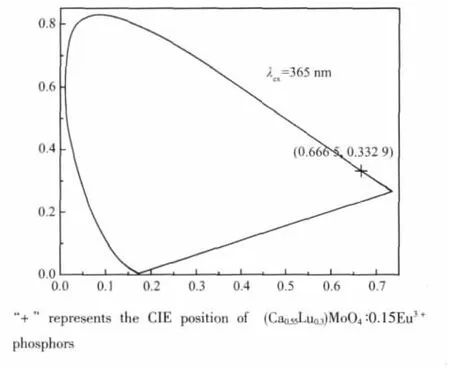
圖5 (Ca0.55Lu0.3)MoO4∶0.15Eu3+的CIE色度圖Fig.5 CIE of(Ca0.55Lu0.3)MoO4∶0.15Eu3+phosphors
2.4 Lu摻雜量對發光性能的影響
圖6給出在394 nm激發的不同Lu摻雜量對熒光粉發光性能的影響圖。由圖可知,隨Lu摻雜量的增加,熒光粉的發光強度明顯增強,但當Lu含量達到30mol%后,摻雜離子的再增加使發光強度下降。在CaMoO4∶Eu3+晶體中,Lu3+的引入主要取代Ca2+格位,少量摻雜可一定程度上破壞晶體完整性并在雜質格點上造成電荷失衡,使Eu3+受周圍晶格產生的晶體場作用更大,因此宇稱選律定則放寬,發光強度更高。但若摻雜量過高,會改變CaMoO4的白鎢礦晶體結構,引起發光性質突變[21],因而發光強度下降。
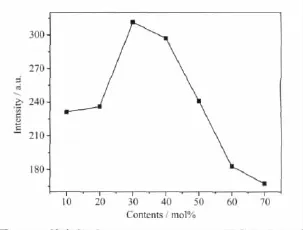
圖6 Lu摻雜量對(Ca1-x Lu x)MoO4∶0.15Eu3+的發光強度的影響Fig.6 Effectof concentration of Lu on the luminescent intensity of(Ca1-x Lu x)MoO4∶0.15Eu3+phosphors
3 結 論
采用NH4HCO3-NH3·H2O混合沉淀劑,通過化學共沉淀法且按理論百分比成功合成了 (Ca1-x-yLuy) MoO4∶x Eu3+紅色熒光粉。Lu的引入不會破壞鉬酸鈣的白鎢礦晶相結構,卻可有效提高7F0→5L6(394 nm)和7F0→5D2(465 nm)的電子吸收效率,增加與紫外光和藍光LED芯片的匹配性。與CaMoO4∶Eu3+紅色熒光粉相比,(Ca1-x-yLuy)MoO4∶x Eu3+的發光強度明顯提高,其色坐標為(0.666 5,0.332 9),優于傳統的紅色熒光粉Y2O2S∶Eu3+(0.631,0.350)。當Lu的摻雜量為30mol%時,熒光粉發光強度最佳。因此,使用化學共沉淀法制備的(Ca1-x-yLuy)MoO4∶x Eu3+熒光粉,有望取代傳統的紅色熒光粉并應用于白光LED中,從而改善W-LED的使用性能。
[1]Dong T T,Li ZH,Ding ZG,et al.Mater.Res.Bull.,2008, 43(7):1694-1701
[2]GAO Fei(高飛),LIANG Li-Fang(梁利芳),GUO Chong-Feng (郭崇峰).Chin.Rare Earths.(Xitu Xuebao),2010,31(1):7-10
[3]Yang Y L,Li X M,Feng W L.et al.J.Alloys Compd., 2010,505(1):239-242
[4]Wang Y G,Ma JF,Tao JT,et al.Ceram.Int.,2007,133(4): 693-695
[5]Nassau K,Levinstein H J,Loiaconon G M.J.Phys.Chem., 1965,26(12):1805-1806
[6]Hwang K S,Seung H,Kim J T.Ceram.Int.,2009,35(6): 2517-2519
[7]ZHOU Li-Ya(周立亞),WANG Lei(王雷),WEIJian-She(魏建設),et al.Chin.Chem.Res.Appl.(Huaxue Yanjiu Yu Yingyong),2008,20(8):952-956
[8]Chiu C H,Wang M F,Lee C S,et al.J.Solid State Chem., 2007,180(2):619-627
[9]Hu Y S,Zhuang W D,Ye H Q,et al.J.Alloys Compd., 2005,390(1/2):226-229
[10]GAO Fei(高飛),LIANG Li-Fang(梁利芳),GUO Chong-Feng (郭崇峰).Chin.J.Lumin.(Faguang Xuebao),2009,30(5):611 -615
[11]Haque M M,Lee H L,Kim D K.J.Alloys Compd.,2009, 481(1/2):792-796
[12]Yang P,Yao G Q,Lin JH.Inorg.Chem.Commun.,2004,7 (3):389-391
[13]XIE An(謝安),YUAN Xi-Ming(袁曦明),WANG Juan-Juan (王娟娟),et al.Chin.Sci.E(Zhongguo Kexue),2009,39(6): 1063-1068
[14]Liu J,Lian H Z,Shi C S.Opt.Mater.,2007,29(12):1591-1594
[15]Li X,Yang Z P,Guan L,et al.J.Alloys Compd.,2009,478 (1/2):684-686
[16]WANG Gui-Xi(王貴喜),BO Su-Ling(薄素玲),QIXia(齊霞), et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2009, 25(2):350-353
[17]Zhang Z J,Chen H H,Yang X X,etal.Mater.Sci.Eng.,B, 2007,145(1/2/3):34-40
[18]Yan B,Wu JH.Mater.Chem.Phys.,2009,116:67-71
[19]LIXue-Ming(黎學明),KONG Ling-Feng(孔令峰),LIWu-Lin(李武林),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2009,25(5):865-868
[20]ZHANGMei(張梅),HE Xin(何鑫),DINGWei-Jia(丁唯嘉), etal.Prog.Chem.(Huaxue Jinzhan),2010,22(2/3):376-382
[21]YAO Guang-Qing(姚光慶),FENG Yan-E(馮艷娥),DUAN Jie-Fei(段潔菲),et al.Acta Phys.-Chim.Sin.(Wuli Huaxue Xuebao),2003,19(3):226-229
Co-precipitation Synthesis and Photolum inescence of (Ca1-x-yLuy)M oO4∶x Eu3+Red Phosphors
YANG Yu-Ling1LIXue-Ming*,1,2FENGWen-Lin3LIWu-Lin2TAO Chuan-Yi2
(1College of Chemistry and Chemical Engineering,Chongqing University,Chongqing 400044,China) (2The Key Lab for Optoelectronic Technology&System of the Ministry of Education, College of Optoelectronic Engineering,Chongqing University,Chongqing 400044,China) (3Department of Applied Physics,Chongqing University of Technology,Chongqing 400044,China)
Using NH4HCO3-2O asmixed precipitator,(Ca1-x-yLuy)MoO4∶x Eu3+red phosphorswere synthesized by co-precipitationmethod.The phase formation,composition and luminescence propertiesof(Ca1-x-yLuy)MoO4∶x Eu3+were analyzed by XRD,EDS,PL and CIE.The results show that(Ca1-x-yLuy)MoO4∶x Eu3+red phosphors have been successfully prepared by co-precipitationmethod according to theoretic ratio,and the synthesized (Ca1-x-yLuy)MoO4∶x Eu3+have scheelite structure with pure phase.The phosphors have strong electron absorbability of7F0→5L6and7F0→5D2at394 nm and 465 nm and can emit red lightingwith high intensity.The CIE of(Ca1-x-yLuy)MoO4∶x Eu3+red phosphors is(0.666 5,0.3329),which isbetter than thatof traditional Y2O2S∶Eu3+red phosphors.In addition,when the concentration of Lu is30mol%,the luminescent intensity of(Ca0.55Lu0.3)MoO4∶0.15Eu3+ishighest.
(Ca1-x-yLuy)MoO4∶x Eu3+;co-precipitation;photoluminescence;red phosphors
O611.4
A
1001-4861(2011)02-0276-05
2010-07-27。收修改稿日期:2010-09-16。
重慶大學211工程三期創新人才培養計劃建設項目(No.S-09013),重慶市自然科學基金(No.2005BA4016),中國博士后基金(No.20100470810)項目資助。
*通訊聯系人。E-mail:xuemingli@cqu.edu.cn;會員登記號:S06N5027M1006。

