碳酸氫鈉浸提-鉬銻抗分光光度法測定土壤中的有效磷
沈志群,張 琪,劉琳娟,邱 燕
(南通市環境監測中心站,江蘇 南通 226006)
·監測技術·
碳酸氫鈉浸提-鉬銻抗分光光度法測定土壤中的有效磷
沈志群,張 琪,劉琳娟,邱 燕
(南通市環境監測中心站,江蘇 南通 226006)
用0.50 mol/L碳酸氫鈉溶液浸提中性和石灰性土壤中的有效磷。碳酸氫鈉可以抑制溶液中Ca2+的活度,使某些活性較大的磷酸鈣鹽被浸提出來,同時也可使活性磷酸鐵、鋁鹽水解而被浸出。浸提液與鉬銻抗顯色劑反應生成磷鉬藍,在波長880 nm處測量吸光度。當取樣量為2.50 g時,使用50 mL碳酸氫鈉溶液浸提,使用1 cm比色皿,檢出限為0.4 mg/kg,測定下限為1.6 mg/kg,滿足了土壤有效磷的監測要求。
土壤;有效磷;碳酸氫鈉浸提;分光光度法
土壤有效磷并不是指土壤中某一特定形態的磷,也不具有真正“數量”的概念,應用不同的測定方法在同一土壤樣品中可以得到不同的數量,因此土壤有效磷水平只是一個相對指標。它可以相對地說明土壤的供磷水平,可以作為一個指標判斷施用磷肥是否必要,亦可作為施肥(磷)的一個推薦方法[1]。近年來,由于連續大量施用磷肥導致磷礦資源的加速耗竭,農田土壤磷素作為非點源污染源造成的地表水富營養化和地下水污染,環境保護工作也越來越重視科學、合理地施用磷肥,因而對于土壤有效磷的測定方法也提出了新的要求,不僅需要準確測出土壤中的植物有效磷水平,而且應能夠反映出土壤磷對環境的潛在影響程度[2]。筆者通過試驗,建立了碳酸氫鈉浸提-鉬銻抗分光光度法測定中性和石灰性土壤中有效磷的方法,該方法的檢出限、精密度、準確度均較好,滿足了土壤有效磷測定的要求。
1 試驗
1.1 主要儀器和試劑
土壤樣品粉碎設備;分光光度計;恒溫往復振蕩器,頻率為50~500次/min;一般實驗室常用儀器和設備。
氫氧化鈉溶液:ω(NaOH)=10%;濃硫酸:ρ(H2SO4)=1.84 g/mL;濃硝酸:ρ(HNO3)=1.51 g/mL;碳酸氫鈉(NaHCO3);鉬酸銨[(NH4)6Mo7O24·4H2O];抗壞血酸(C6H8O6):左旋,比旋光度+21°~ +22°;浸提劑:C(NaHCO3)=0.50 mol/L,pH=8.5;酒石酸氧銻鉀溶液:ρ(KSbOC4H4O6)=5 g/L;鉬銻貯備液;抗壞血酸溶液:ω(C6H8O6)=10%;磷標準使用液:ρ(P)=5mg/L,用浸提劑稀釋至刻度;指示劑:2,4-二硝基酚或2,6-二硝基酚,稱取0.2 g 2,4-二硝基酚或2,6-二硝基酚溶于100 mL水中。
1.2 采樣及樣品制備
按照文獻[3]中有關規定進行土壤樣品的采集和保存。
將采集好的樣品置于風干盤中,攤成2~3 cm的薄層,適當地壓碎、翻動,揀出碎石、沙礫、植物殘體。用木棒研壓,然后去雜物,粉碎,充分混勻,通過1 mm土壤篩,裝入磨口瓶中備用,并進行干物質的測量。
1.3 實驗步驟
1.3.1 標準曲線的繪制
分別量取 0,1.00,2.00,3.00,4.00,5.00,6.00 mL磷標準使用液于50 mL容量瓶中,用浸提劑補足至10 mL。分別加水至15~20 mL左右,再加入1滴2,4-二硝基酚指示劑,然后逐滴加入硫酸溶液調至溶液近無色,加入0.75 mL抗壞血酸溶液,混勻,30 s后加5 mL鉬銻貯備液,并用水定容至50 mL,混勻。此標準系列溶液中磷質量濃度依次為 0,0.1,0.2,0.3,0.4,0.5,0.6 mg/L。(注:上述操作過程中,會有CO2氣泡產生,應緩慢搖動容量瓶,勿使氣泡溢出瓶口。)
將上述容量瓶置于室溫高于15℃處,放置30 min(若室溫低于15℃,可在20~30℃水浴顯色30 min)。用1 cm比色皿在880 nm波長處比色,以空白溶液為參比,分別測量吸光度。以吸光度為縱坐標,對應的磷濃度為橫坐標,繪制校準曲線。
1.3.2 試樣預處理
稱取通過1 mm孔徑篩的風干土樣2.50 g,置于干燥的150 mL錐形瓶中,加入50.0 mL浸提劑,用橡皮塞塞緊,置于恒溫往復振蕩機上,在(25±1)℃下以170 r/min的振蕩頻率振蕩(30±1)min,立即用無磷濾紙過濾入干燥的150 mL錐形瓶中。濾液必須當天分析。1.3.3 試樣的測定
量取10.0 mL經過預處理的樣品于干燥的50 mL容量瓶中,然后按照與校準曲線相同的操作步驟進行顯色和測量。不加土壤樣品,按上述步驟測定全過程空白,以下操作同標準曲線。校準曲線測定數據見表1。
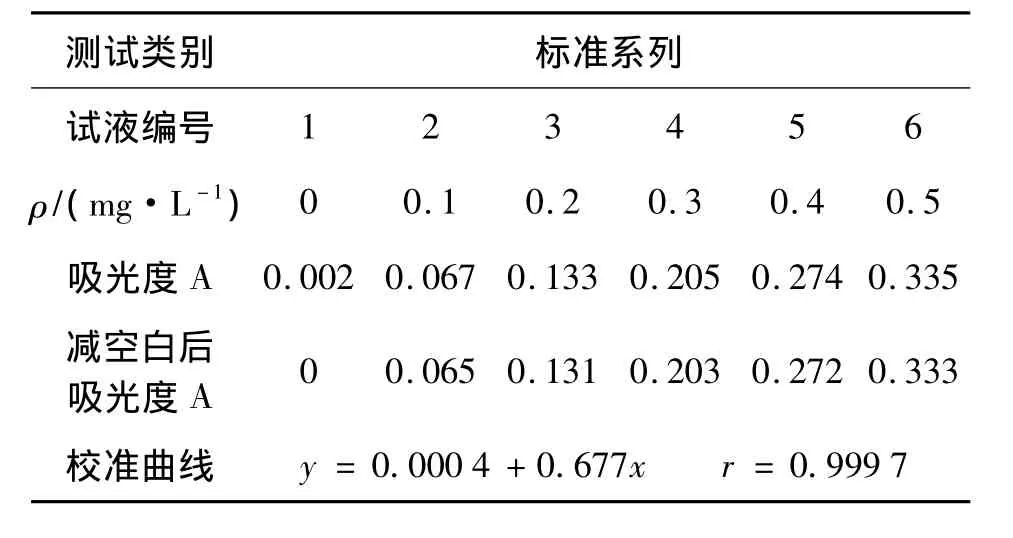
表1 校準曲線測定數據
2 結果與討論
2.1 浸提劑pH值的控制
NaHCO3的pH往往隨放置時間的延長而上升[4,5],將配置好的浸提劑放置3,5,8 和 12 d 后分別進行pH值測定,其結果見表2。
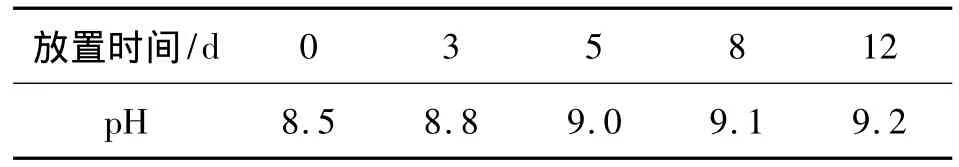
表2 浸提劑pH值的變化
從表2可知,0.5 mol/L NaHCO3存放3 d,pH值上升0.3,存放12 d,pH上升0.7。而有效磷的測定值會隨浸提劑pH的上升而增大,增大幅度取決于土壤類型,因此,浸提劑pH的變化是不可忽視的。NaHCO3應臨用現配,浸提前一定要將浸提劑的pH值調至8.5。
2.2 振蕩時間的選擇
對同一個土壤樣品進行不同時間的浸提,結果見表3。
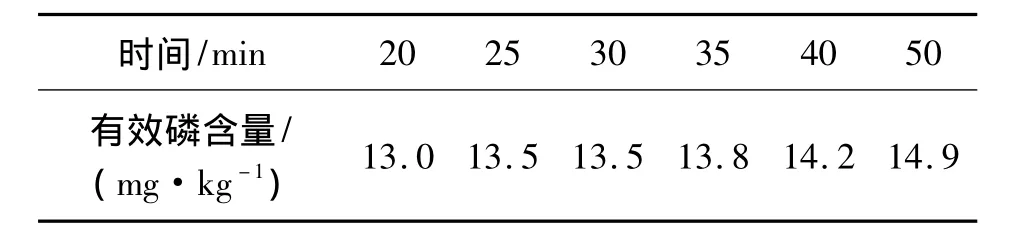
表3 不同浸提時間對同一土壤有效磷含量的影響
固相磷的溶解作用和交換作用都與作用時間有關,振蕩時間愈長,浸提出來的養分愈多。因此,參照文獻[4]和[5]中的規定,把振蕩時間30 min改為25~30 min更加容易控制。
2.3 振蕩頻率的選擇
對(13.8±2.3)mg/kg土壤有證樣品,分別使用100,130,150,170,200,250 r/min 的振蕩頻率進行處理,結果見表4。

表4 不同振蕩頻率對同一土壤有效磷含量的影響
由表4可知,振蕩頻率越快,浸提效率越高。但是,頻率過快會導致液體濺出,設備損壞,也超出了土壤樣品標準值。因此,振蕩頻率選擇170 r/min為宜。
2.4 浸提液適宜土壤的選擇
(1)1945年,BRAY和KURTZ提出用0.025 mol/L HCl+0.03 mol/L NH4F浸提土壤,可以方便地測定酸溶性磷和吸附磷,包括大部分磷酸鈣和一部分磷酸鋁和磷酸鐵,此方法為目前國際通用的測定酸性土壤有效磷的方法[6]。1954年,OLSEN等人提出用0.5 mol/L NaHCO3(pH=8.5)浸提,測定石灰性土壤和中性土壤中的有效磷[7]。
用本方法分別測定酸性土壤和堿性土壤有效磷含量,結果如表5所示。
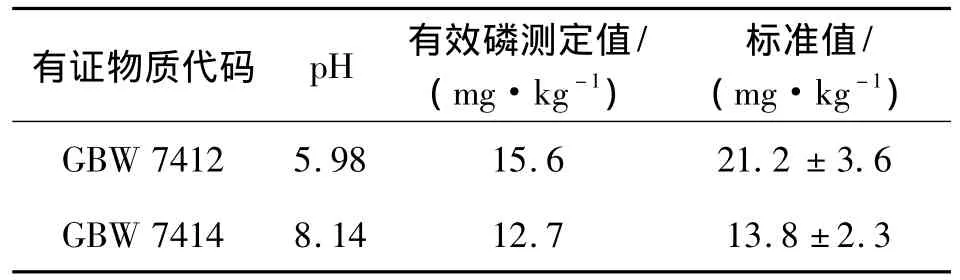
表5 浸提液對不同性質的土壤有效磷含量的影響
由表5可知,用該浸提方式測定酸性土壤中的有效磷,結果偏低,這是因為碳酸氫鈉溶液與土壤中的酸中和,導致浸提劑pH值降低而使結果偏低,因此,本方法適宜中性和石灰性土壤。
2.5 溫度的選擇
2.5.1 浸提溫度
OLSEN曾指出:在20~30℃提取溫度范圍內,以(25±1)℃為標準,溫度每升高1℃,土壤速效磷含量增加0.43 mg/kg[7]。筆者在實驗中發現,振蕩溫度在25℃時較為合理。溫度低于25℃,PO34-提取緩慢;溫度超過25℃,實際操作中比較困難,而且還將會增加非有效磷的溶解。因此,本方法采用《森林土壤有效磷的測定》(LY/T 1233—1999)中的浸提溫度。具體控制時,可采用恒溫振蕩器,保證浸提溫度為25℃。
2.5.2 顯色溫度
參照《森林土壤有效磷的測定》(LY/T 1233—1999)和《土壤質量 磷的測定 光譜法測定碳酸氫鈉溶液中可溶磷》(ISO 11263—1994)中的顯色溫度。溫度為15~25℃。實際樣品分析時,在恒溫振蕩機上進行提取,顯色溫度較易控制。
2.6 顯色劑的酸度的選擇
鉬藍顯色是在適宜的試劑濃度下進行的,磷鉬雜多酸需在一定酸度條件下生成,過酸與不足均會影響結果。因此,在磷的鉬藍比色測定中,酸度的控制最為重要。使用不同酸度的顯色劑對磷的曲線和土壤的浸提液進行比色測定,其結果見表6。

表6 不同方法的顯色劑對磷的曲線和土壤有效磷的影響
從表6可知,不同方法測定的標準曲線的吸光度沒有顯著差異。但是,對于浸提出來的土壤樣品,用不同方法的顯色劑,其吸光度差異很大,這主要與土壤本身的酸度有關。因此,在加入顯色劑前,需調節浸提液的pH值,即加1滴2,4-二硝基酚指示劑,用硫酸溶液調節pH至溶液呈現微黃色。
2.7 檢出限的測定
按照樣品分析的全部步驟,重復n(n≥7)次空白試驗,將各測定結果換算為樣品中的濃度,計算n次平行測定的標準偏差,按下列公式計算方法檢出限[8]:
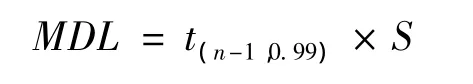
式中:n——樣品的平行測定次數;t——自由度為n-1,置信度為0.99時的t分布(單側),當n=7時,t=3.143;S——n次平行測定的標準偏差。以4倍檢出限作為方法測定下限,檢出限為0.4 mg/kg,檢出下限為1.6 mg/kg。
2.8 精密度的測定
實驗室采用高[含量為(23.3±1.4)mg/kg的有證標準樣品]、中[含量為(13.8±2.3)mg/kg的有證標準樣品]、低(含量為4.59 mg/kg的實際土壤)3種不同含量水平的土壤樣品,每個樣品平行測定6次,分別計算不同含量樣品的平均值、標準偏差、相對標準偏差等各項參數(表7)。
2.9 準確度的確定
使用2個不同含量水平的有證標準樣品進行測定。有證物質1的編號為GBW 07414,濃度為13.8 mg/kg;有證物質2的編號為ASA-2a,濃度為23.3 mg/kg。每個有證標準樣品平行測定6次,分別計算不同含量水平有證標準樣品的平均值、相對誤差等各項參數,結果見表8。
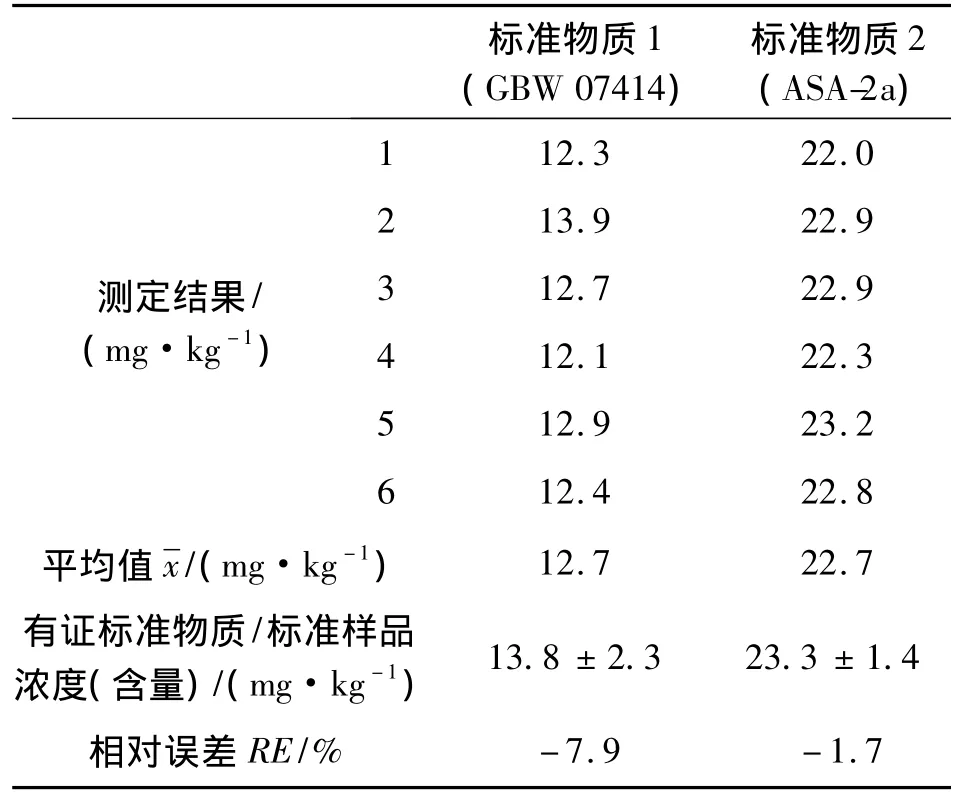
表8 有證標準物質/標準樣品測試數據
2.10 其他影響因素
所有的采樣儀器和設備、分析儀器和設備經處理后都不應含磷。試驗中使用的玻璃器皿可用(1+5)鹽酸溶液(鹽酸與蒸餾水體積比為1∶5)浸泡2 h,或用不含磷的洗滌劑清洗。比色皿用后應以稀硝酸或鉻酸洗液浸泡片刻,以除去吸附的鉬藍有色物質。
由于浸提出來的養分受浸提液濃度、水土比例、振蕩時間、溫度等影響,因此要嚴格控制好實驗室的溫度。浸提溫度和顯色溫度要嚴格控制在(25±1)℃,否則試驗誤差較大。
3 結語
采用碳酸氫鈉浸提-鉬銻抗分光光度法測定中性及石灰性土壤中有效磷,該方法干擾少,顯色范圍寬,實際土壤樣品測定RSD為1.92% ~5.04%,標準土壤樣品相對誤差分別為1.7%和7.9%,精密度和準確度均滿足要求。
[1] 魯如坤.土壤農業化學分析[M].北京:中國農業科技出版社,1999:179-181.
[2] 卜玉山,楊鳳仙,韓明正.土壤生物有效磷測定方法的發展及其在美國的研究動態[J].山西農業大學學報,2001,21(2):184-187.
[3] HJ/T 166 土壤環境監測技術規范[S].
[4] LY/T 1233—1999 森林土壤有效磷的測定[S].
[5] ISO 11263:1994 土壤質量 磷的測定 光譜法測定碳酸氫鈉溶液中可溶磷[S].
[6] BRAY R H,KURTZ L T.Determination of total,organic and available forms of phosphorus in soils[J].Soil Science,1945,59:39-45.
[7] OLSEN S R,COLE C V,WATANABE F S,et al.Estimation of available phosphorus in soils by extraction with sodium bicarbonate[R].1954.
[8] HJ 168—2010 環境監測分析方法標準制修訂技術導則[S].
Determination of Available Phosphorus in Soil by Sodium Bicarbonate Extraction Mo-Sb Anti-spectrophotometry Method
SHEN Zhi-qun,ZHANG Qi,LIU Lin-juan,QIU Yan
(Nantong Environmental Monitoring Central Station,Nantong ,Jiangsu 226006,China)
Theavailable phosphorus was extracted by 0.50 mol/L sodium bicarbonate solutionin neutral and calcareous soil.Sodium bicarbonate solution can inhibit the activity of Ca2+,so that the calcium phosphate of large activity were extracted;meanwhile active iron phosphate and aluminum salt was leached by hydrolysis.Molybdenum Blue reaction occurred by mixing elution and Mo-Sb anti-chromogenic reagent and the absorbance was measured at a wavelength of 880 nm.In this study,the method of measuring concentrations of available phosphorus in soil was developed.The sample volume was 2.50 g and sodium bicarbonate solution was 50 mL.The detection limit of this method was 0.4 mg/kg and lower limit was 1.6 mg/kg when 1 cm cuvette was used.
soil;available phosphorus;sodium bicarbonate extraction;spectrophotometery
X833
B
1674-6732(2011)-05-0012-04
10.3969/j.issn.1674-6732.2011.05.004
2011-06-09;
2011-07-13
2008年度環境保護標準制修訂項目(1013)。
沈志群(1963—),女,高級工程師,本科,從事環境監測與管理工作。

