一節“甜蜜”的課——滬教版“溶液組成的定量表示”教學設計
杜玉芬 李德前
(1 徐州市科技中學 江蘇 徐州 221008;2 徐州市西苑中學 江蘇 徐州 221002)
本節教材是上海教育出版社《義務教育課程標準實驗教科書·化學》第6 章第二節(溶液組成的表示)第2課時(溶液組成的定量表示)的內容。
【設計思想】
本節課屬于研究化學基本概念的理論課,內容較為枯燥。 為激發學生的學習興趣,體現“化學就在身邊”,同時便于回收實驗廢液、減少環境污染,筆者拒絕照本宣科,而是將有關的實驗和計算均利用糖溶液作為情景素材。
為提高學生的化學素養,筆者重視引導學生以化學原理為核心、 以數學計算為手段研究溶液的組成和變化;為培養學生的計算能力,筆者注重站在學生的思維角度分析解題思路、總結解題方法,對較難的計算題則采用化繁為簡的方法,將其分解為一組小問題,使學生“跳一跳就能摘到桃子”。
另外,筆者改進、調整了課本上的兩個學生活動內容:(1)在課本161 頁的“活動與探究”中,實驗1 所給數據是3g 蔗糖和20mL 水, 實驗2 所給數據是5g 蔗糖和50mL 水,這兩組數據在下一步計算“溶質質量與溶液質量的比” 時均不太方便(因為3/23 和5/55 均除不盡)。于是,筆者將水的體積分別更改為17mL 和45mL。(2)在課本163 頁的“觀察與思考”中,以“濃鹽酸配制稀鹽酸”為例,給出了“配制一定溶質質量分數的溶液”步驟,這樣沒有代表性;而且在涉及的溶液稀釋計算中,設問多、難度大、綜合性強。 于是,筆者將其中的溶液配制實驗進行改進,簡化為“利用固體溶質配制溶質質量分數一定的溶液”,將有關溶液體積與質量轉換的計算、溶液稀釋的計算提前安排。 這樣處理,分散了難點、突出了重點,更符合學生實際和課程標準的要求。
總之,本節課力爭用“一杯糖水”演繹“一節甜蜜的課”。
【教學目標】
知識與技能:理解溶質質量分數的概念;掌握有關溶質質量分數的簡單計算。
過程與方法: 培養分析問題和解決問題的能力,以及化學計算的能力;初步學會配制溶質(固體)質量分數一定的溶液。
情感態度與價值觀: 認識溶質質量分數的實際應用,體會生活中處處有化學。
【教學重難點】
重點:溶質質量分數的概念和計算;難點:有關溶質質量分數的計算。
【教學過程】
一、組織教學
教師面帶微笑、精神抖擻進入教室;師生互相問好。
二、溫故知新
[講評]上節課布置的課后作業中存在的問題。
[學生復習]說出下列溶液中的溶質和溶劑:碘酒;稀硫酸;蔗糖溶液;汽水;白磷的二硫化碳溶液。
三、探究新知
[引言]在生產、生活中,我們有時僅僅知道溶液是由哪些溶質、哪些溶劑組成的還不夠,往往還需要知道溶質、溶劑、溶液之間的定量關系。
[板書課題]溶液組成的定量表示
[過渡]下面,請同學們動手配制兩種紅糖溶液。
[學生實驗]分組配制兩種紅糖溶液。 實驗1:將3g紅糖溶于17mL 水中; 實驗2: 將5g 紅糖溶于45mL 水中。 教師巡視,并適時糾正學生在稱量、量取、溶解等操作中出現的錯誤。
[提問] 不用數學方法, 你能判斷出這兩杯紅糖溶液,哪個濃些嗎?
[學生回答]多數學生都知道“看顏色”、“嘗甜度”、“測密度”,少數學生還提出了“向溶液里再加紅糖”、“蒸干水分稱紅糖質量”等方法。
[討論]若利用數據比較兩種糖水的濃稀,你有哪些方法? 教師巡視、指導、參與、評價。
[學生匯報]提出的方法主要是:比較“溶質質量/溶劑質量”大小、比較“溶質質量/溶液質量”大小、比較“溶質體積/溶液體積”大小。
[講述]能定量表示溶液濃稀的方法確實很多,但為了統一、規范,化學上常采用“溶質質量”跟“溶液質量”之比,我們稱之為“溶質質量分數”。
[板書](一)溶質質量分數
[學生朗讀] 課本162 頁溶質質量分數的定義2~3遍。
[板書]1.定義:溶質質量與溶液質量之比。
[過渡] 由溶質質量分數的定義不難寫出其計算公式。
[學生填表] 算出剛才配制的兩杯紅糖溶液的溶質質量分數(分別是15%、10%),并把結果填入課本162 頁表6-7 中;教師巡視、釋疑。
[學生推導] 溶質質量分數計算式的另外兩個變形公式;教師巡視、指導。
[板書]溶質質量=溶液質量×溶質質量分數;溶液質量=溶質質量/溶質質量分數
[學生練習] 利用溶質質量分數的計算式及變形公式,完成下表中幾種蔗糖溶液的組成:
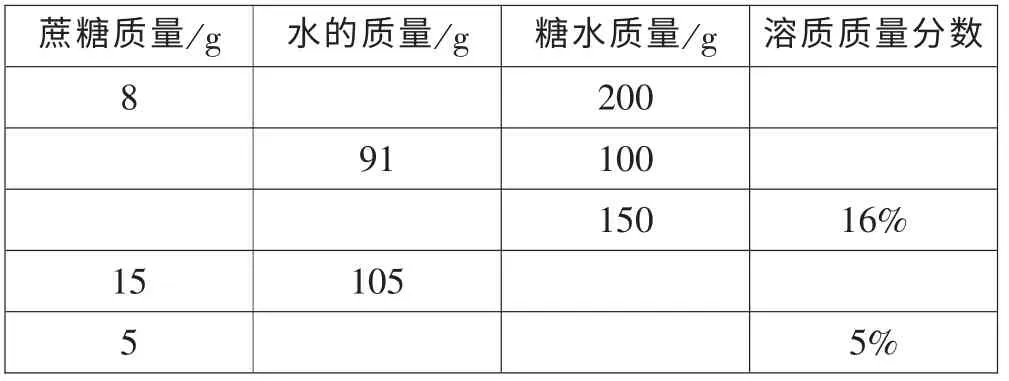
?
[小結并過渡]溶質質量分數不僅能準確、直觀的表示溶液組成,還能方便地比較不同溶液的濃稀,因此它在生產、生活有廣泛的應用。 下面我們就來學習有關溶質質量分數的幾種簡單計算。
[板書]3.有關溶質質量分數的計算
[例1]紅糖不僅營養豐富,而且具有造血、補氣、健脾、暖胃的功效。 小明同學為生病的媽媽配制紅糖水,他將150g 水加入45g 紅糖中, 并充分攪拌使紅糖完全溶解。 你知道小明配制的紅糖溶液中溶質質量分數是多少嗎?
[分析]首先根據“溶液質量=溶質質量+溶劑質量”,算出溶液質量;再把溶質、溶液質量代入溶質質量分數的計算式,即可算出結果(也可以把溶質、溶劑質量直接代入計算公式求解)。 計算過程要簡明扼要,解題格式要規范美觀, 數據單位要參與運算, 比例式后面要乘以100%,計算結果一般精確到0.1%等。
[板書]解:m(糖水)=150g+45g=195g
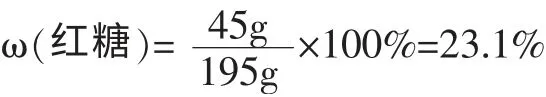
答:紅糖溶液中溶質質量分數是23.1%。
[例2]白糖具有潤肺、生津、解暑的作用。暑假里,小剛同學給工作繁忙的爸爸配制冰凍白糖水。 如果他配制2000mL 溶質質量分數為20%的白糖水 (糖水密度是1.08g/mL),那么需要白糖多少克?
[分析]進行溶質質量分數的計算時,如果溶液的量是體積單位,必須先用“密度公式”把溶液體積換算成質量,然后才能代入溶質質量分數的關系式進行解答。
[板書]解:m(白糖水)=1.08g/mL×2000mL=2160g
m(白糖)=2160g×20%=432g
答:需要白糖432g。
[例3] 低血糖患者早上喝一小杯葡萄糖口服液,就能有效改善低糖癥狀。 現用20g 溶質質量分數為50%的葡萄糖注射液,配制溶質質量分數為10%的葡萄糖口服液,需加水多少克?
[分析]為降低本題難度,可以先出示如下幾個小問題作為思維鋪墊:(1)20g 溶質質量分數為50%的葡萄糖注射液中含有多少克葡萄糖? (2)若設需要加水的質量為x, 那么10%的葡萄糖口服液中葡萄糖質量的代數式怎么寫? (3)濃葡萄糖溶液和稀葡萄糖溶液中葡萄糖質量是否相等? 這樣處理,學生就能抓住“溶液在稀釋前后溶質質量不變”的規律去建立等量關系,從而使問題迎刃而解。
[板書]解:設需要加水的質量為x。
根據“溶液在稀釋前后溶質質量不變”得:20g×50%=(20g+x)×10%,x=80g。
答:需要加水80g。
[過渡]前面同學們配制的是溶質、溶劑質量一定的溶液。 下面我們來看如何配制溶質質量分數一定的溶液。
[板書](二)配制溶質質量分數一定的溶液
[討論]如何配制50g 溶質質量分數為5%的白糖溶液。 教師巡視、參與、指導、小結。
[學生匯報]首先是計算,算出所需白糖是2.5g、水是47.5g;接下來就是配制溶質、溶劑質量一定的溶液了,涉及的操作主要是稱量、溶解。
[小結并扼要板書]
1.主要步驟:計算、稱量、溶解
[演示] 配制50g 溶質質量分數為5%的白糖溶液,并適時講述實驗操作和注意事項。
(因為配制溶液的稱量、 溶解等操作學生已經練習了,為節省時間,這里就不再安排學生實驗了)
[小結并扼要板書]
2.主要儀器:托盤天平、量筒、燒杯、玻璃棒、藥匙、膠頭滴管
四、整理桌面
學生整理桌上的實驗用品,并將糖溶液倒入指定容器(回收利用)。
五、總結評價
師生共同總結本節課的主要內容;教師對學生的學習表現和成果進行評價;學生自評互評。
六、布置作業
1.完成課本P164~165 習題2、3、4、5。
2.閱讀課本P163“無土栽培”的內容。

