U(Ⅵ)在Na-凹凸棒石黏土上的吸附
牛智偉,范橋輝,潘多強,許君政,吳王鎖
蘭州大學 放射化學與核環境研究所,甘肅 蘭州 730000
高放廢物地質處置是放射化學領域的前沿研究課題,也是世界各國面臨的涉及環境保護和核能可持續發展的重大問題。因此,研究放射性核素和重金屬離子在黏土表面的吸附/解吸和遷移,對高放廢物地質處置庫的性能評價和模型計算具有重要的理論和實際意義。
凹凸棒石黏土是一種鏈層狀的富鎂鋁納米級硅酸鹽粘土。其晶體結構屬2∶1型(圖1),分為3層,上下2層是Si—O四面體,中間1層是(Al,Mg,Fe)—O—OH八面體。凹凸棒石黏土含有大量的結構羥基,如Si—OH、Mg—OH和Al—OH等。由于其結構中存在著Al3+對Si4+,Fe2+、Mg2+對A13+或Si4+等產生同晶置換現象[1-3],形成鋁凹凸棒石和鐵凹凸棒石等變種,故晶體中含有不定量的Na+、Ca2+、Fe3+和Al3+等,各種離子替代的綜合結果使凹凸棒石常常帶少量的永久性的負電荷,因此凹凸棒石黏土具有很強的物理和化學吸附能力[3]。
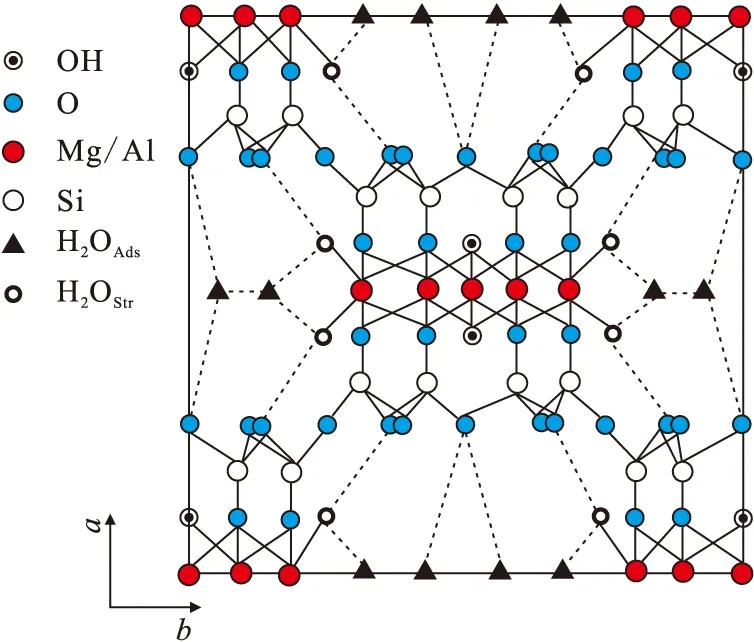
圖1 凹凸棒石粘土在001晶面結構示意圖
我國凹凸棒石黏土儲量豐富、價格低廉,其原土和活化改性產物在廢物、廢水處理及其它領域具有非常廣闊的應用前景。lvarez-Ayuso等[4]研究并發現凹凸棒石黏土對Pb2+、Cu2+、Zn2+和Cd2+均有較強的吸附能力,其順序為Cu>Pb>Zn>Cd,認為凹凸棒石黏土能有效富集污染水體中的重金屬離子。Fan等[5]研究了磁改性凹凸棒石黏土對的吸附,發現凹凸棒石黏土經磁改性后吸附能力明顯增強,且易于固液分離。殷竟洲等[6]發現經殼聚糖改性的凹凸棒石黏土對Pb2+和Cd2+的吸附性能優于凹凸棒石黏土,且經5次再生后凹凸棒石黏土仍具有很高的吸附容量。
雖然國內學者對凹凸棒石黏土的吸附性能做了一些研究,但仍有很多問題亟待解決,如對顯著影響吸附的重要因素的考察不夠細致,凹凸棒石黏土與重金屬離子的吸附機理還很模糊。本工作擬采用X射線衍射、掃描電鏡對天然和Na-凹凸棒石黏土的結構進行表征;重點研究離子強度、pH值、富里酸及溫度對U(Ⅵ)在Na-凹凸棒石黏土上吸附的影響。
1 實驗部分
1.1 主要實驗試劑
凹凸棒石黏土由蘭州凱西科技公司提供;富里酸(FA)由甘肅興隆山土壤中提取,組成分析見文獻[7];實驗中所用其它試劑均為分析純。
標準鈾溶液的配制:準確稱取1.179 2 g經850 ℃灼燒過的八氧化三鈾,用10 mL鹽酸和3 mL過氧化氫加熱溶解,蒸至近干。再加入20 mL水,使其完全溶解后轉入1 000 mL容量瓶中,加0.1 mol/L鹽酸溶液至刻度,搖勻,此溶液中鈾的濃度為1.00 g/L(即4.20 mmol/L)。
Na-凹凸棒石的制備:將原凹凸棒石黏土研磨、過140目篩,用0.500 mol/L NaCl配制成含凹凸棒石40.0 g/L的懸浮液,調節其pH值穩定在4.0左右,振蕩24 h,10 000 r/min下分離,重復2次;再用0.100 mol/L NaCl配成含凹凸棒石40.0 g/L的懸浮液,振蕩、10 000 r/min下分離,重復3次,第4次在1 500 r/min下分離,傾出上層凹凸棒石懸浮液,棄去殘渣,在10 000 r/min下分離,干燥、研磨過篩后置于干燥器中備用。
1.2 實驗儀器
V-1800型分光光度計,上海美譜達儀器有限公司;BS110S型電光分析天平,北京塞多利斯天平有限公司,感量0.1 mg;PHSJ-4A型精密pH計,上海精密科學儀器有限公司;H2050R-1型高速離心機,湖南湘儀實驗室儀器開發有限公司;微量可調移液槍(200 μL、1 mL、5 mL);聚乙烯試管(10 mL)。
1.3 實驗方法
(1)吸附實驗
依次向聚乙烯管中加入2.00 mL 12.0 g/L的Na-凹凸棒石懸浮液,1.00 mL 1.00 mol/L NaCl溶液,振蕩平衡24 h后繼續向體系中加入一定體積的鈾溶液和去離子水,使總體積為8.00 mL,用微量的HCl或NaOH調節pH至所需值。在25 ℃下振蕩48 h后12 000 r/min下離心分離,取上清液4.00 mL于25 mL容量瓶中,加入1.00 mL 0.500 mol/L HCl、5.00 mL 0.1%的偶氮胂Ⅲ,用去離子水定容,在波長650 nm處測吸光度。
(2)解吸實驗
將吸附實驗所得的懸浮液經離心后,移去4.00 mL上清液,向剩余懸浮液中加入4.00 mL相同濃度的NaCl溶液,調節pH值與吸附實驗時的相同,在25 ℃下振蕩48 h,12 000 r/min下離心分離,其它實驗方法與吸附實驗方法相同。所有實驗數據都是2次測量值的平均值,相對誤差小于5%。
吸附結果用吸附百分數(Y)和分配系數(Kd)表示:
(1)
(2)
式中:c0、ce分別為U(Ⅵ)的初始濃度(mol/L)和平衡濃度(mol/L),V為凹凸棒石懸浮液的體積;m為凹凸棒石的質量。
2 結果與討論
2.1 X射線衍射(XRD)分析
圖2是天然凹凸棒石與Na-凹凸棒石的XRD譜。由圖2可看出,凹凸棒石的主要峰(2θ=8.360°、19.740°、27.980°、34.580°和42.360°)沒有發生明顯的變化,說明二者的基本結構沒有發生顯著變化。根據布拉格公式:
2dsinθ=nλ
(3)
式中:θ為X光的入射角度(°),n為衍射級數,d為晶面間距(nm),λ為波長(nm)。可計算出天然凹凸棒石黏土在(001)晶面方向上的晶面間距d=1.062 nm,Na-凹凸棒石的d=1.052 nm,與文獻報道基本吻合[8]。
2.2 掃描電鏡(SEM)分析
圖3為凹凸棒石的SEM表征照片。由圖3可知,天然凹凸棒石和Na-凹凸棒石的基本形態相似,呈現一種長條狀粘結聚集起來的針棒狀和纖維狀致密有序的晶束,并互相交織形成“柴垛”狀結構。Na-凹凸棒石由于除去了碳酸鹽及其它雜質,呈現出更多孔隙,具有更強的吸附能力[9]。
2.3 接觸時間對吸附的影響
為了研究U(Ⅵ)在Na-凹凸棒石上的吸附動力學,引入假二級動力學方程[10]:
(4)
式中:qe和qt分別為平衡時刻和t時刻U(Ⅵ)在Na-凹凸棒石上的吸附量,mg/g;k為假二級動力學方程吸附速率常數,g/(mg·h)。
由圖4可知,U(Ⅵ)在Na-凹凸棒石上的吸附2~3 h達到平衡;3 h以后吸附百分數基本不變。圖5為U(Ⅵ)在Na-凹凸棒石上吸附的假二級動力學的線性擬合。利用其直線的斜率和截距求得吸附速率常數k=1.54 g/(mg·h),吸附達平衡后的吸附量qe=2.63 mg/g。線性相關系數(r=0.999 7)非常接近1,說明U(Ⅵ)在Na-凹凸棒石上的吸附符合假二級動力學模型。
2.4 Na-凹凸棒石用量(m/V)對吸附的影響
Na-凹凸棒石用量對吸附的影響示于圖6。由圖6可以看出,當m/V<15.0 g/L時,U(Ⅵ)在Na-凹凸棒石上的吸附百分數隨著Na-凹凸棒石用量的增大而迅速增大;當m/V>15.0 g/L時,吸附百分數達90%以上,且吸附百分數的增加非常緩慢。隨著Na-凹凸棒石用量增大,體系中Na-凹凸棒石提供吸附位的總量隨之增加,更多的表面位與U(Ⅵ)形成表面絡合物而促進U(Ⅵ)的吸附[11-12]。圖6還表明,當m/V<15.0 g/L時,U(Ⅵ)在Na-凹凸棒石黏土上的分配系數Kd隨用量的增大而增大;當m/V>15.0 g/L時,Kd值卻隨吸附劑用量的增大而略有減小。鑒于表觀分配系數Kd的物理化學意義,Kd通常不隨吸附劑用量的改變而發生變化。以上結果可能是因為在較低的m/V下,吸附在凹凸棒石黏土表面上的U(Ⅵ)繼續通過孔道和晶格擴散至凹凸棒石黏土顆粒的內部,空缺的表面可繼續吸附溶液中的U(Ⅵ),從而使得Kd增大;當m/V較高時,吸附劑顆粒之間相互作用增大而導致Kd略有減小。

圖3 凹凸棒石的SEM表征
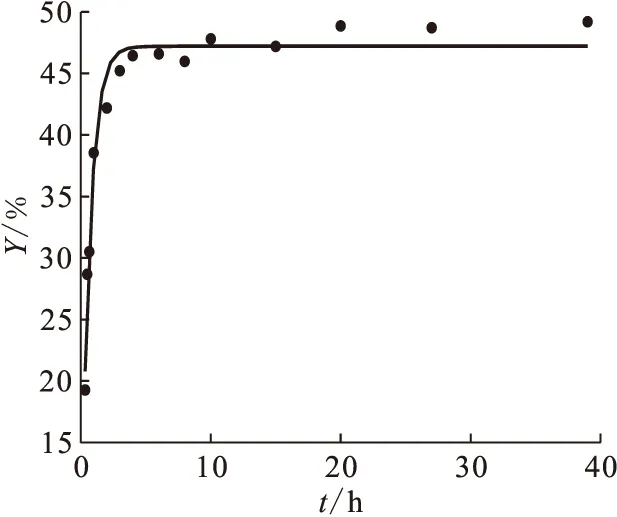
圖4 接觸時間對U(Ⅵ)在Na-凹凸棒石上吸附的影響
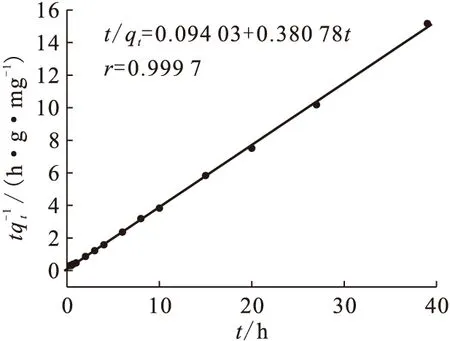
圖5 假二級反應動力學線性擬合
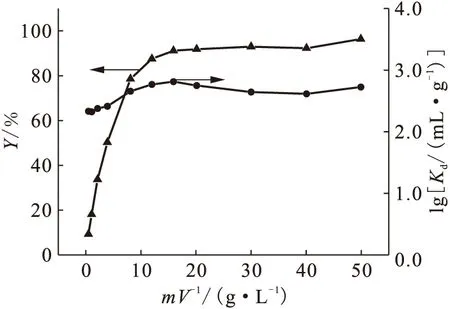
圖6 Na-凹凸棒石用量(m/V)對吸附的影響
2.5 pH值、離子強度對吸附的影響
圖7為不同濃度的背景電解質(NaCl)下pH對吸附的影響。由圖7可知,在酸性范圍內,U(Ⅵ)在Na-凹凸棒石上的吸附百分數隨pH的增大而增大,隨背景電解質濃度的增大而減小;而在堿性范圍內,吸附百分數隨pH的增大而減小,隨背景電解質濃度的增大而增大。
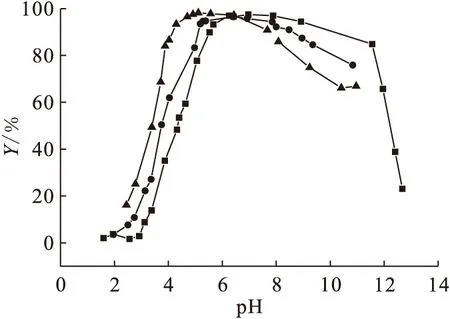
圖7 不同濃度背景電解質下pH對吸附的影響
在液相中,凹凸棒石黏土表面的羥基官能團在不同pH值下會發生質子化或去質子化可逆反應:
pH<7.0時,隨著NaCl濃度的增大,Na+對凹凸棒石表面位的吸附競爭效應增強,使得U(Ⅵ)的吸附下降;另外,離子強度增大,溶液的活度系數減小,導致U(Ⅵ)在溶液中的有效濃度減小[15]。所以,U(Ⅵ)在凹凸棒石上的吸附百分數隨NaCl濃度的增大而減小。而當pH>7.0時,U(Ⅵ)在凹凸棒石上的吸附百分數隨NaCl濃度的增大而增大,其原因有待進一步研究說明。
2.6 富里酸(FA)對吸附的影響
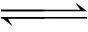
圖8為富里酸(FA)對U(Ⅵ)在Na-凹凸棒石上吸附的影響。由圖8可知,富里酸對吸附有明顯的促進作用,這是由于富里酸(FA)含大量可與金屬離子配位的羧基、醇羥基、酚羥基和酮羰基[16]。許多研究表明,在酸性條件下,吸附在黏土表面的FA可增加其表面的負電性,且提供大量的配位位點,因此FA可促進金屬離子在黏土表面的吸附;但是在堿性條件下,帶負電的黏土表面與FA產生靜電排斥,使FA游離在液相中,而液相中的FA與金屬離子可形成絡合物,從而降低黏土表面對金屬離子的吸附[17]。
圖8 FA對吸附的影響
2.7 溫度對吸附的影響
(1)吸附等溫線
采用Langmuir和Freundlich吸附模型對吸附等溫線進行擬合,表達式如下:
Langmuir模型:
(5)
式中,qe為U(Ⅵ)在Na-凹凸棒石上吸附達平衡后的吸附量,ce為U(Ⅵ)在液相中的平衡濃度,qmax為最大吸附量,KL為Langmuir吸附平衡常數。
Freundlich模型:
(6)
式中KF、n為Freundlich吸附平衡常數。
由圖9及表1可知,Langmuir和Freundlich的線性相關系數r均大于0.96,相對而言,Lang-muir模型能更好地擬合吸附結果,表明Na-凹凸棒石表面位點對U(Ⅵ)具有均一的吸附活性,且U(Ⅵ)在Na-凹凸棒石表面的吸附是單層吸附,已吸附的U(Ⅵ)不再與其他鈾物種相作用。另外,富里酸的加入使得qmax增大(無FA時,qmax=1.47×10-5mol/g;ρ(FA)=20 mg/L時,qmax=2.44×10-5mol/g),說明富里酸能夠促進Na-凹凸棒石對U(Ⅵ)的吸附。
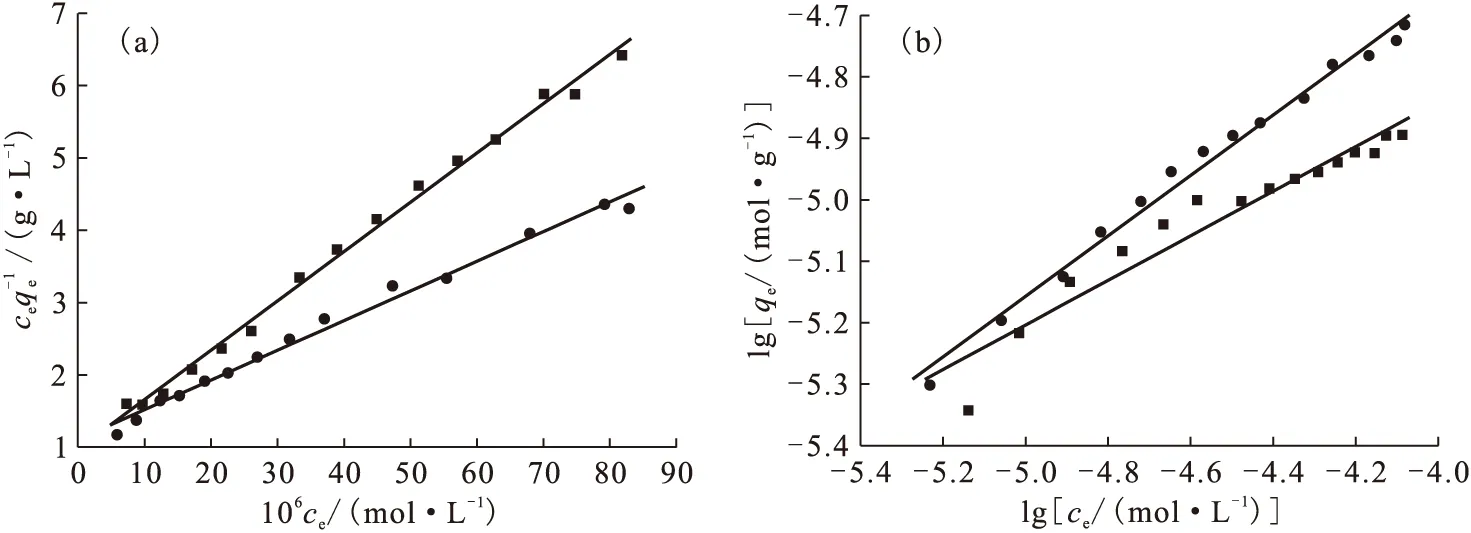
圖9 Langmuir(a)和Freundlich(b)吸附等溫線

表1 Langmuir和Freundlich模型相關參數
(2)吸附-解吸等溫線
(3)吸附熱力學

3個熱力學函數基本公式[19]如下:
(7)
(8)
(9)
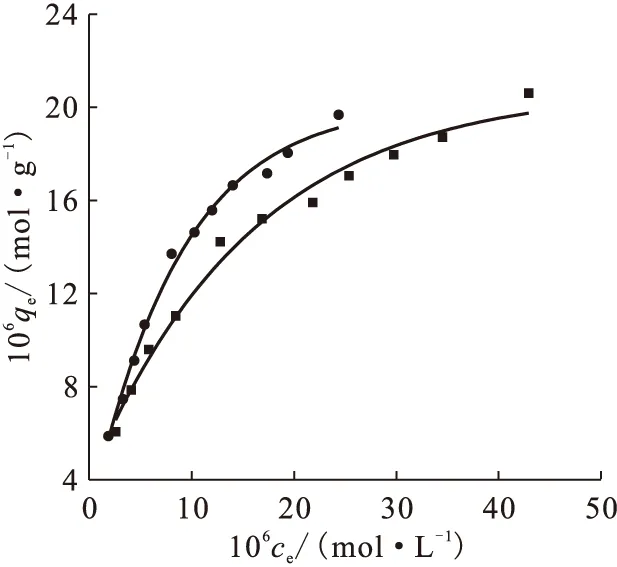
圖10 吸附-解吸等溫線

(10)
式中:qe為金屬離子在吸附劑上吸附達平衡后的吸附量,mol/g;ce為金屬離子在液相中的平衡濃度,mol/L。
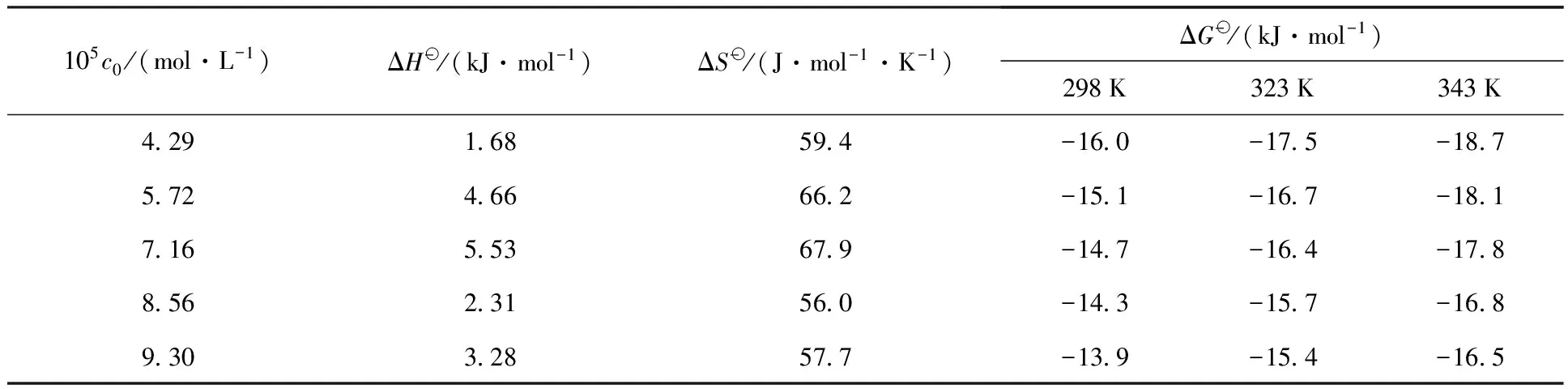
表2 U(Ⅵ)在Na-凹凸棒石粘土上的吸附熱力學參數
3 結 論
(1)U(Ⅵ)在Na-凹凸棒石粘土上的吸附速率較快,其吸附動力學符合假二級動力學方程。
(2)在酸性條件下,背景電解質(NaCl)對U(Ⅵ)在Na-凹凸棒石上的吸附有抑制作用;而在強堿性條件下,背景電解質(NaCl)促進U(Ⅵ)在Na-凹凸棒石上的吸附。
(3)pH對吸附的影響強烈。在較低pH范圍內,隨著pH增大,U(Ⅵ)在凹凸棒石上的吸附量增大,吸附主要為離子交換或外層絡合吸附;而在強堿性條件下,U(Ⅵ)在Na-凹凸棒石上的吸附隨著pH增大而減小,吸附以內層絡合及靜電作用為主。富里酸的存在能促進U(Ⅵ)的吸附。
(4)溫度的升高有利于Na-凹凸棒石對U(Ⅵ)的吸附,且該吸附過程是吸熱的、自發的不可逆過程。
[1]Chisholm J E.An X-Ray Powder-Diffraction Study of Palygorskite[J].Can Mineral,1990,28:329-339.
[2]Chiari G,Giustetto R,Ricchiardi G.Crystal Structure Refinements of Palygorskite and Maya Blue From Molecular Modelling and Powder Synchrotron Diffraction[J].Eur J Miner,2003,15:21-33.
[3]Fan Q H,Shao D D,Hu J,et al.Comparison of Ni2+Sorption to Bare and ACT-Graft Attapulgite:Effect of pH,Temperatures and Foreign Ions[J].Surf Sci,2008,602:778-785.
[4]Alvarez-Ayuso E,García-Snchez A.Palygorskite as a Feasible Amendment to Stabilize Heavy Metal Polluted Soils[J].Environ Pollut,2003,125:337-344.
[5]Fan Q H,Li P,Chen Y F,et al.Preparation and Application of Attapulgite/Iron Oxide Magnetic Composites for the Removal of U(Ⅵ)From Aqueous Solution[J].J Hazard Mater,2011,192(3):1 851-1 859.
[6]殷竟洲,楊文瀾,夏士朋.殼聚糖改性凹凸棒土對重金屬離子的吸附[J].化工環保,2007,27(3):276-279.
[7]Xu D,Wang X K,Chen C L,et al.Influence of Soil Humic Acid and Fulvic Acid on Sorption of Thorium(Ⅳ)on MX-80 Bentonite[J].Radiochim Acta,2006,94:429-434.
[8]Wu W S,Fan Q H,Xu J Z,et al.Sorption-Desorption of Th(Ⅳ)on Attapulgite:Effects of pH,Ionic Strength and Temperature[J].Appl Radiat Isot,2007,65:1 108-1 114.
[9]Pan B L,Yue Q F,Ren J F,et al.A Study on Attapulgite Reinforced PA6 Composites[J].Polym Test,2006,25:384-391.
[10] Ho Y S,McKay G.The Kinetics of Sorption of Divalent Metal Ions Onto Sphagnum Moss Peat[J].Water Res,2000,34:735-742.
[11] Anirudhan T S,Divya L,Suchithra P S.Kinetic and Equilibrium Characterization of Uranium(Ⅵ)Adsorption Onto Carboxylate-Functionalized Poly-Grafted Lignocellulosics[J].J Environ Manage,2009,90:549-560.
[12] Chang P P,Wang X K,Yu S M,et al.Sorption of Ni(Ⅱ)on Na-Rectorite From Aqueous Solution:Effect of pH,Ionic Strength and Temperature[J].Colloid Surf A,2007,302:75-81.
[13] Psareva T S,Zakutevrskgy O I,Chubar N I,et al.Uranium Sorption on Cork Biomass[J].Colloid Surf A,2005,252:231-236.
[14] Waite T D,Davis J A,Payne T E,et al.Uranium(Ⅵ)Adsorption to Ferrihydrite:Application of a Surface Complexation Model[J].Geochim Cosmochim Acta,1994,58:5 465-5 478.
[15] Han R P,Zou W H,Wang Y,et al.Removal of Uranium(Ⅵ)From Aqueous Solutions by Manganese Oxide Coated Zeolite:Discussion of Adsorption Isotherms and pH Effect[J].J Environ Radioact,2007,93:127-143.
[16] 吳景貴,席時權,姜巖.土壤腐殖質的分析化學研究進展[J].分析化學,1997,25:1221-1 227.
[17] 許君政,范橋輝,白洪彬,等.離子強度、溫度、pH和腐殖酸濃度對Th(Ⅳ)在凹凸棒石上吸附的影響[J].核化學與放射化學,2009,31(3):179-185.
[18] Businelli M,Casciari F,Businelli D,et al.Mechanisms of Pb(Ⅱ)Sorption and Desorption at Some Clays and Goethite-Water Interfaces[J].Agron J,2003,23:219-225.
[19] Shahawi M S,Othman M A,Abdel-Fadeel M A.Kinetics,Thermodynamic and Chromatographic Behaviour of the Uranyl Ions Sorption From Aqueous Thiocyanate Media Onto Polyurethane Foams[J].Anal Chim Acta,2005,546:221-228.
[20] Aksu Z.Determination of the Equilibrium,Kinetic and Thermodynamic Parameters of the Batch Biosorption of Nickel(Ⅱ)Ions Onto Chlorella Vulgaris[J].Process Biochem,2002,38:89-99.
[21] Namasivayam C,Ranganathan K.Waste Fe(Ⅲ)/Cr(Ⅲ)Hydroxide as Adsorbent for the Removal of Cr(Ⅵ)Fromaqueous Solution and Chromium Plating Industry Wastewater[J].Environ Pollut,1993,82:255-261.
[22] Chen C L,Wang X L.Adsorption of Ni(Ⅱ)From Aqueous Solution Using Oxidized Multi-Walled Carbon Nanotubes[J].Ind Eng Chem Res,2006,45:9 144-9 149.
[23] Genc-Fuhrman H,Tjell J C,Mcconchie D.Adsorption of Arsenic From Water Using Activated Neutralized Red Mud[J].Environ Sci Technol,2004,38:2 428-2 434.

