合成生物學在醫藥領域中的應用
馮嬌,何珣,陳怡露
(南京工業大學生物與制藥工程學院,江蘇南京 210009)
1 醫藥行業的發展現狀
中國是世界第一大原料藥生產國和出口國、世界第二大非處方(OTC)藥物市場[1]。國際知名醫藥健康咨詢公司 IMS Health Inc.的統計數據[2]顯示,目前我國已成為繼日本之后的全球第三大醫藥市場。
據統計,目前美國已有1 300多家的生物技術企業,約占世界總量的2/3;生物技術市場資本總額超過了400億美元,每年的科研經費超過了50億美元[3];已經成功研發出30多個重要的治療藥物,正式投放市場的藥物也達到了40多個;日本已有65%的生物技術公司從事于生物醫藥研究[4]。在我國生物醫藥產業近年來一直保持著較高的增長速度,從事生物技術產業和相關產品研發的公司、大學和科研院所達600余家,注冊的生物醫藥公司有200余家[5]。同時在我國生物制藥的利潤率達11%,超出行業平均利潤率 2%[1]。
醫藥制造產業是一個朝陽產業,現在醫藥的需要量越來越大,而醫藥制造的技術含量相當高,在醫藥企業的競爭較量中,科學技術實力往往是關鍵性因素,所以,對于醫藥企業而言,技術創新具有更特殊的意義。近年來,合成生物學這門學科的出現和發展可為醫藥產業的技術帶來新一輪的創新和提高。
2 合成生物學概況
2. 1 合成生物學概念及其研究內容
合成生物學是一門新興的交叉學科,2010年5月生物學家克雷格.文特爾、漢密爾頓.史密斯等在世界著名權威學術期刊《科學》上宣布他們通過化學合成方法成功合成了人類歷史上首個“人造細胞生物”——完整的細菌染色體 Mycoplasmamycoide,并將其成功轉移到了另一種與其親緣關系很近的,并且去除原基因組的山羊支原體細胞內[6]。這一研究成果使得合成生物學受到了前所未有的關注,成為現代生命科學的研究熱點。
合成生物學是以生命科學理論為指導,以工程學原理進行遺傳設計、基因組改造(重組染色體)和(或)合成(包括賦予各種復雜生物功能為單位的基因群模塊合成、模塊組裝)以及人造細胞合成,它們能在從分子到細胞、從組織到機體的多個水平上參與包括遺傳與進化在內的復雜生物學[7],這是一門涉及微生物學、分子生物學、遺傳工程、材料科學以及計算科學等多個領域的綜合性交叉學科[8]。
作為一門前沿學科,合成生物學不同于以往的代謝工程及系統生物學。代謝工程著眼于宿主細胞已有代謝途徑的敲除和(或)過量表達以實現代謝網絡的定向優化,以及對底物轉運蛋白和產物轉運過程的修飾。系統生物學是從基因組規模去全面理解細胞的代謝網絡,包括組成代謝途徑的結構基因、細胞代謝復雜的調節機制以及遺傳和環境擾動對細胞全局代謝的影響,從而建立組學規模的代謝模型,對可能的基因工程操作效果進行評價和預測,并通過對基因工程操作后獲得的菌株的代謝網絡進行分析[9]。而合成生物學則著眼于從頭設計全新的代謝途徑或全新的生命系統,同時也可以通過模塊的優化和重建改造原有的生命系統。可以說合成生物學需要在系統生物學了解到的生物的基礎上,應用以基因組技術為核心的生物技術,綜合多種學科來設計、改造、重建或制造生物分子、生物體部件、生物反應系統、代謝途徑與過程乃至整個生命活動的細胞和生物個體。
目前合成生物學主要有兩個基本方向:一個是創造簡單的生命形式,比如最簡單的病毒和細菌,利用非天然的分子再現自然生物體的天然特性;另一個是分離自然生物體中的一部分并將其重構到具有非天然機能的生物系統當中來改造生命的過程或形式。
合成生物學的基本研究思路是利用生物零件(parts),如啟動子、核糖體結合位點、核糖核酸(RNA)、酶編碼基因等組裝成裝置(devices),即代謝途徑或調解環路,并將裝置進一步組建成生命系統(systems),包括根據人類的意愿從頭設計合成新的生命過程或生命體,以及對現有生物體進行重新設計[10]。
2. 2 合成生物學發展進程
1911年7月8日,在著名醫學刊物《柳葉刀》發表的一篇書評中合成生物學一詞首次出現[11],而“合成生物學”作為一個新概念,是由波蘭遺傳學家Waclaw Szybalski在1974年首先提出的。他指出分子生物學的發展必將最終發展到合成生物學階段,屆時人們將可以設計新的控制元件,利用他們改造自然界的基因組,甚至可以從頭構建全新的基因組[12]。之后,在1980年第一次以“基因外科術:合成生物學的開始”為題的一篇長篇論文出現在德文刊物[13]。自從2000年Kool在美國化學學會年會上重新提出合成生物學概念,其定義為基于系統生物學的遺傳工程,從基因片段、人工堿基DNA分子、基因調控網絡與信號傳導路徑到細胞的人工設計與合成,類似于現代集成型建筑工程,將工程學原理與方法應用于遺傳工程與細胞工程等生物技術領域,合成生物學、計算生物學與化學生物學一同構成系統生物技術的方法基礎。有研究人員[14]以“合成生物學的初次登臺”為題對此作了長篇報道,自此以來,細胞信號傳導、基因調控網絡設計與轉基因研究開發迅速發展。
2000年1月《自然》上發表了2篇文章:Gardner等[15]在大腸桿菌中構建了基因開關(toggle switch),一個合成的雙穩態基因調控網絡;Elowitz等[16]構建了第一個合成的生物振蕩器——壓縮振蕩子(repressilator)。這兩篇論文標志著合成生物學作為一個新的領域正式產生。2002年,Wimmer小組[17]制造了歷史上第一個人工合成有生物活性的脊髓灰質炎病毒基因組,這一工作開創了以無生命的化合物合成感染性病毒的先河。2003年文特爾小組合成了φX174噬菌體基因組[18],2004年6月在美國麻省理工學院舉行了第一屆合成生物學國際會議。2005年8月,在美國舊金山舉行的合成生物學會議討論了生物合成這一領域對藥物發展、細胞重編程、生物機器人等方面的潛在意義。2005年在美國創建了Cellincon合成生物公司,同年麻省理工學院的Endy[19]明確提出工程中常用的“標準化”、“復雜系統解耦”、“概念抽象化”做法,并清楚地將合成生物學涉及的生物系統分成DNA、部件、裝置、系統4個層次。之后隨著合成生物學的發展及影響,美國學者Endy等人于2005年在國際遺傳工程機器大賽[20]中創立了標準化的生物模塊BioBrick登記處,收集各種標準化的生物零件,這充分證明了合成生物學在設計模塊中的發展。
2006年以來,合成生物學發展又進入了新階段,研究主流從單一生物部件的設計快速發展到對多種基本部件和模塊進行整合。通過設計多部件之間的協調運作建立復雜的系統,并對代謝網絡流量進行精細調控,從而構建人工細胞行為來實現藥物、功能材料與能源替代品的大規模生產。2007年,加州大學伯克利校園首創了合成生物學系。
2010年1月,《細胞》和《自然》[21-22]同時為合成生物學創建10周年發表專題社論。2010年5月,文特爾成功地將人工合成的支原體基因組轉入到除原基因組的山羊支原體細胞內,獲得了具有自我復制和生存能力的新菌株[6],制造出了第一個具有人造基因組的活細胞。這在合成生物學的發展史中具有里程碑的意義,顯示了合成生物學的可行性和應用性。
3 合成生物學在醫藥行業的應用
合成生物學在醫藥領域已具有很多應用,這些方面包括更有效疫苗的生產、新藥和改進的藥物、可以進行檢測的生物傳感器等。隨著合成生物學的逐漸成熟以及它在醫藥領域應用的深入,合成生物學也必將極大地促進整個生物醫藥領域的發展。
3. 1 合成生物學降低醫藥的成本
合成生物學在醫藥領域的應用最典型的例子莫過于Keasling合成抗瘧疾藥物青蒿素的經典工作。瘧疾每年大約會感染5億世界上最貧困的人,并且致使其中多達100萬人喪生,喪生者多數是5歲以下的兒童。幾個世紀以來,標準的治療方法是使用奎寧,或者是其衍生物氯喹,但因長期使用和病原體抗藥性的增強而使其療效一降再降。青蒿素由于可以高效殺死瘧疾寄生蟲,因此是目前最有效的抗瘧疾藥物之一。天然的青蒿素是在青蒿(artemisia annua)中提取,但是產量十分稀少,提取工藝復雜,提取成本極其昂貴——植物提取成本約為奎寧的10倍,供應量無法滿足世界各地患者的需要。目前使用青蒿素進行治療每個療程的費用是8美元到15美元,而大部分患者均處于世界上最貧困的地區,無法負擔昂貴的藥費。美國UCB化學工程系教授、勞倫斯國家實驗室合成生物學中心主任Keasling意識到如果合理利用合成生物學的工具,就可以完全不受自然條件控制,將每一個細胞當作微生物制藥工廠進行設計、加工、集成、組裝、控制等而生產出青蒿素,那么就不再需要繁復且成本很高的生產過程了。之后,Keasling[23-24]在大腸桿菌、酵母中對青蒿基因及其代謝途徑進行了設計組裝與精密調控的研究。
2003 年,Keasling[24]在大腸桿菌中生產青蒿素的思路主要如圖1。首先是將大腸桿菌中乙酰輔酶A轉化成甲羥戊酸;再將甲羥戊酸轉化成異戊烯焦磷酸酯(IPP)或者二甲(基)丙烯焦磷酸酯(DMAPP);之后將IPP或DMAPP轉化成法尼基環焦磷酸酯(FPP),最后利用青蒿中的ADS基因,將FPP轉化成青蒿酸合成前體amorphadiene。
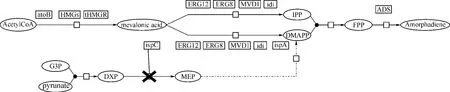
圖1 大腸桿菌生產青蒿素示意圖Fig 1 Producing artemisinic acid in Escherichia Coli
Keasling將大腸桿菌通過植物青蒿的amorphadiene合成酶(ADS)密碼子優化、共表達SOE4操縱子(編碼DXS、IPPHp、IspA)以及引入異源的酵母菌甲羥戊酸途徑,協調IPP有關的基因以平衡其合成與消耗,確保在其能夠殺傷大腸桿菌以前及時轉化為Amorphadiene,從而提高了amorphadiene的產量。
2006 年,keasling[25]在酵母菌中生產青蒿素的思路主要如圖2。通過優化FPP生物合成途徑提高FPP的產量;從青蒿中引入ADS基因,其表達的產物將FPP轉化為Amorphadiene;通過比較基因組學分析得到來自于青蒿的細胞色素P450氧化還原酶CYP71AV1/CPR,克隆表達后實現;Amorphadiene通過三步氧化還原反應得到青蒿素前體——青蒿酸。
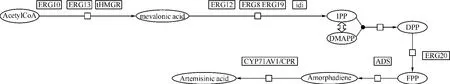
圖2 酵母菌生產青蒿素示意圖Fig 2 Producing artemisinic acid in Yeast
Keasling的主要工作是改造FPP合成途徑——過量表達tHMGR,有效限制FPP向固醇的轉化;通過甲硫氨酸可抑制啟動子(PMET3)下調ERG9編碼的角鯊烯(squalene)合成酶活性,阻斷FPP向下合成固醇的支路,避免FPP在其他方面的不必要消耗;引入植物青蒿的amorphadiene合成酶(ADS)基因,克隆青蒿類植物轉化amorphadiene為青蒿酸的細胞色素P450氧化還原酶等。他們利用酵母天然的甲羥戊酸途徑,該途徑在正常情況下通過糖類代謝產生乙酰輔酶A來合成甾醇;而在他們所合成的代謝途徑中,甲羥戊酸途徑被用來大量產生中間體FPP,而FPP接下來可被在酵母中表達的ADS和CYP71AV1催化產生青蒿素前體——青蒿酸。
Keasling利用合成生物學的手段,首先設計了一條在大腸桿菌或酵母中不存在的合成青蒿酸的途徑,在利用微生物自身已有的代謝途徑的前提下引入外源模塊,再將來自大腸桿菌、酵母、青蒿多種基因及其代謝途徑組裝與精密調控,最后執行所需功能的途徑生產出青蒿酸,最終實現了他將每一個細胞當作微生物制藥工廠進行設計、加工、集成、組裝、控制等,從而生產出青蒿素的想法。
通過上面的研究,利用大腸桿菌及酵母細胞合成青蒿素前體——青蒿酸的能力提高了100萬倍,使得每一劑量的藥品成本從10美元左右下降到了不到1美元。為表彰Keasling的杰出成就,Keasling被美國發現雜志評選為2006年最有影響的科學家[25],并獲得了Bill and Melinda Gates基金資助高達4 000萬美金的研究資金,用于產業化生產青蒿素。
3. 2 合成生物學治療疾病
通過合成生物學的手段對疾病治療也能起到幫助作用,主要是由于構建出能夠幫助基因治療的工程細胞。合成生物學還可以對細菌或者病毒的生物學特性進行改造,主要是改造對這些細菌或者病毒具有能夠識別和浸染特定的細胞可引發毒害作用的生物學特性,使其失去致病性并且具有能夠識別機體惡性細胞的新特性。之后利用這些改造后的細菌或者病毒來傳遞治療藥物,這對癌癥和其他相關疾病的治療會具有更好的作用。
一個殺死癌細胞的細菌應該能感覺到腫瘤環境,并能對其作出應答,一旦進入到腫瘤內,細菌必須滲入癌細胞,接著就開始產生殺腫瘤的毒素。美國加州大學的Voigt等[26]設計了一種可以侵入并殺死癌細胞的細菌,他們向細菌中引入了多個模塊化零件,包括兩個探測器、一個“與門”控制器、一個反應器,使得細菌可以探測外界的環境。當細菌處于低氧環境、且細菌的密度超過一定閾值時(這兩者都是只有在腫瘤細胞中才有的特征),細菌將表達透明質酸酶(invasin),從而殺死癌細胞。由于這些模塊可以與其他同類型零件進行替換,使得人們可以設計出針對特定癌細胞的特異性治療的細菌,這個充分顯示了合成生物學的靈活性。
3. 3 合成生物學生產醫用生物材料及檢測病毒
基于合成生物學的分子機器設計和合成,結合多種學科,通過設計、改造和合成獲得高活性和高穩定性等特殊要求的重要材料,可以進一步生產重要的以生物為基礎的產品,從而獲得滿足醫用的特殊性能材料。
除此之外,合成生物學可用于構建微生物或其他生物,對毒素、化學品、其他病原微生物進行監測,以使發現新傳染物及病毒,從而極大可能地幫助新發傳染病的早期監測及控制[27-28]。
通過以上一些應用可以看出,合成生物學可以通過合理的設計和構造代謝途徑來調節生物體內復雜的代謝、調控網絡,從而優化能源和資源的應用,以及提高目標產物。運用一些合成生物學的工具——如啟動子文庫、RNA控制元件、感應控制裝置、蛋白質降解標簽等[29-31]可以做到動態地改變代謝途徑中關鍵酶的水平;合成生物學的出現使我們可以將其他非傳統微生物中新型未發現的酶經過進化和設計改造后,篩選出性能優良的酶整合到設計的途徑中,從而優化代謝。由于合成生物學的優勢,在未來建構更多的合成生物學工具會被應用于醫藥的研究中。
4 結 語
合成生物學通過構筑人工生物系統來更好地理解和改造天然生物系統的工作原理,使它無論從科學或技術兩方面來看都占有重要的地位。隨著合成生物學的飛速發展,同樣也帶來了一些問題,如合成生物學高昂的研究費用、生物安全、倫理及知識產權等問題[32-35]。發展與問題一向是同在的,如何把握在于我們。相信隨著合成生物學的不斷成熟,一些問題將會迎刃而解。
醫藥行業雖說已經飛速發展,但仍存在許多阻礙,例如某些藥物生產成本高昂、某些疾病沒有治療方法、制藥企業帶來的嚴重的環境污染等。如今,合成生物學的發展使得我們可以以合成生物學相關技術方法為主體,結合已有的學術基礎和研究資源解決我國目前和未來面臨的嚴峻的醫藥問題,并帶動整個醫藥領域的發展。可以預見,合成生物學研究的不斷成熟,醫藥領域的更多方面將被涉及,更高效的生產宿主將成功構建,生物醫藥生產過程的經濟性也將得到明顯提高,從而使生物醫藥能得到更廣泛的生產和應用。
[1]孔學東,干榮富.中國醫藥產業的機遇、挑戰及相應對策[J].中國醫藥工業雜志,2011,42(1):76-80.
[2]http://www.imshealth.com/portal/site/imshealth.
[3]http://www.bio-soft.net/doc/shengwuyiyao.html.
[4]羅氏公司.生物醫藥市場統計數據(上卷).
[5]丁雪松,馮國忠.我國生物醫藥產業現狀及對策[J].經營管理者,2010,5:70-72.
[6]GIBSON D G,GLASS J I,LARTIGUE C,et al.Creation of a bacterial cell controlled by a chemically synthesized genome[J].Science,2010,329(5987):52-56.
[7]STAHLER P,BEIER M,GAO X L,et al.Another side of genomics:synthetic biology as a means for the exploitation of whole-genome sequence information[J].J Biotechnology,2006,124(1):206-212.
[8]KANEHISA M.Post-genome informatics[M].New York:Oxford University Press,2000:148.
[9]ZHAO X M,JIANG R,BAI F.Directed evolution of promoter and cellular transcription machinery and its application in microbial metabolic engineering—a review[J].Chin J Biotech,2009,25(9):1312-1315.
[10]WANG J,QI Q.Synthetic biology for metabolic engineering--a review[J].Chin J Biotech,2009,25(9):1296-1302.
[11]REGINALDA A.Reviews and notices of books[J].Lancet,1911,178(4584):97-99.
[12]http://www.efst.sh.cn/showKnowledge.do?id=547.
[13]HOBOM B.Gene surgery:on the threshold of synthetic biology[J].Med Klin,1980,75(24):834-841.
[14]RAWLS R L.‘Synthetic biology’makes its debut[J].Chem &Eng News,2000,78(17):49-53.
[15]GARDNER T S,CANTOR C R,COLLINS J J.Construction of a genetic toggle switch in Escherichia coli[J].Nature,2000,403(6767):339-342.
[16]ELOWITZ M B,LEIBLER S.A synthetic oscillatory network of transcriptional regulators[J].Nature,2000,403(6767):335-338.
[17]CELLO J,PAUL A V,WIMMER E.Chemical synthesis of poliovirus cDNA:generation of infectious virus in the absence of natural template[J].Science,2002,297(5583):1016-1018.
[18]SMITH H O,HUTCHISON C A,PFANNKOCH C,et al.Generating a synthetic genome by whole genome assembly:phiX174 bacteriophage from synthetic oligonucleotides[J].Proc Natl Acad Sci USA,2003,100(26):15440-15445.
[19]ENDY D.Foundations for engineering biology[J].Nature,2005,438(7067):449-453.
[20]International genetic engineering machine competition(iGEM)< http://parts.mit.edu/r/parts/igem/index.cgi> .
[21]Ten years of synergy[J].Nature,2010,463(7279):269-270.
[22]KRUGER R P.Synthetic biology select[J].Cell,2010,140(1):5-7.
[23]MARTIN V J,PITERA D J,WITHERS S T,et al.Engineering a mevalonate pathway in Escherichia coli for production of terpenoids[J].Nature Biotechnology,2003,21(7):796-802.
[24]RO D K,PARADISE E M,OUELLET M,et al.Production of the antimalarial drug precursor artemisinic acid in engineered yeast[J].Nature,2006,440(7086):940-943.
[25]http://discovermagazine.com/2006/dec/cover.
[26]LEVSKAYA A,CHEVALIER A A,TABOR J J,et al.Synthetic biology:engineering Escherichia coli to see light[J].Nature,2005,438(7067):441-442.
[27]WEBER W,FUSSENEGGER M.Emerging biomedical applications of synthetic biology[J].Nature Reviews Genetics,2012,13:21-35.
[28] KEASLING J D.Synthetic biology for synthetic chemistry[J].ACS Chem Biol,2008,3(1):64-76.
[29]LEE T S,KRUPA R A,ZHANG F,et al.BglBrick vectors and datasheets:a synthetic biology platform for gene expression[J].J Biol Eng,2011,5:12.
[30]JUNGMANN R,RENNER S,SIMMEI F C.From DNA nanotechnology to synthetic biology[J].HFSP J,2008,2(2):99-109.
[31]SKRLJ N,ERCULJ N,DOLINAR M.A versatile bacterial expression vector based on the synthetic biology plasmid pSB1[J].Protein Expr Purif,2009,64(2):198-204.
[32]BHUTKAR A.Synthetic biology:navigating the challenges ahead[J].J Biolaw Bus,2005,8(2):19-29.
[33]BUGL H,DANNER J P,MOLINARI R J,et al.DNA synthesis and biological security[J].Nature Biotechnology,2007,25(6):627-629.
[34]KUMAR S,RAI A.Synthetic biology:the intellectual property puzzle[J].Texas Law Reviews,2007,85:1745-1768.
[35]RAI A,BOYLE J.Synthetic biology:caught between property rights,the public domain,and the commons[J].PLoS Biology,2007,5(3):58.

