硫化物礦山尾礦緩釋抑菌劑滴丸的制備及性能測試
張 哲,楊 琛,黨 志,舒小華 (華南理工大學(xué)環(huán)境科學(xué)與工程學(xué)院,工業(yè)聚集區(qū)污染控制與生態(tài)修復(fù)教育部重點(diǎn)實(shí)驗(yàn)室,污染控制與生態(tài)修復(fù)廣東省教育廳重點(diǎn)實(shí)驗(yàn)室,廣東 廣州 510006)
金屬礦山尾礦在露天堆放過程中,其中所含的硫化物不斷被氧化,使尾礦中的金屬元素釋放出來,給周邊環(huán)境帶來嚴(yán)重的污染[1].在自然界中,相比化學(xué)氧化,氧化亞鐵硫桿菌(Acidthiobacillus ferroxidans,A.f)等氧化菌對尾礦中硫化物的生物氧化往往發(fā)揮更大的作用.研究表明,氧化亞鐵硫桿菌能使氧化反應(yīng)速率提高約106倍[2-3].因此,控制硫化物的生物氧化已成為金屬硫化物尾礦污染防治的重要途徑之一.20世紀(jì)80年代以來,國內(nèi)外學(xué)者在尾礦治理中采用殺菌劑抑制生物氧化和酸性廢水的產(chǎn)生,取得了一定的進(jìn)展[4-8].但由于在野外條件下直接投加殺菌劑,殺菌劑會隨雨水淋洗大量流失,同時在光照下失去殺菌活性,限制了殺菌劑在尾礦治理中的使用.近年來,隨著微膠囊技術(shù)在制藥領(lǐng)域的發(fā)展,以滴丸型緩釋技術(shù)為主的微膠囊技術(shù)已被廣泛應(yīng)用于藥物的緩釋和控釋等領(lǐng)域[9-12].由于該技術(shù)能減少物質(zhì)的損失,并可以根據(jù)需要,持續(xù)釋放物質(zhì)進(jìn)入外部環(huán)境,在很大程度上能有效解決殺菌劑在野外使用存在的問題.本研究擬采用微膠囊技術(shù),制備抑菌劑緩釋滴丸,控制抑菌劑的釋放,延長藥效,提高抑菌劑在尾礦露天堆放條件下的使用效率,從而實(shí)現(xiàn)對礦區(qū)生物氧化產(chǎn)酸的長期有效控制,為礦山尾礦污染治理提供新的途徑.
1 實(shí)驗(yàn)部分
1.1 材料與方法
材料:醋酸纖維素(CA) (分析純,康德科技有限公司),丙酮(分析純,康德科技有限公司),吐溫80(分析純)、液體石蠟、十二烷基磺酸鈉(SDS)(分析純)均購自北京化學(xué)試劑公司.
實(shí)驗(yàn)所用微生物為本課題組從廣東省韶關(guān)市大寶山多金屬硫化物礦山尾礦篩選出的氧化亞鐵硫桿菌(A.f)Z1(GenBank登錄號GQ984157).菌株的形態(tài)及生理特性見文獻(xiàn)[13].該菌在尾礦壩酸性礦坑水中培養(yǎng)5d后可達(dá)到對數(shù)生長期.
黃鐵礦取自廣東韶關(guān)大寶山礦區(qū),樣品取回后自然風(fēng)干.用瑪瑙研缽粉碎,過 80目篩,然后用無水乙醇浸泡 2h,去離子水清洗后,40℃烘干,真空干燥皿內(nèi)保存?zhèn)溆?經(jīng)X衍射分析顯示,FeS2的含量為93.33%.
緩釋滴丸制備采用文獻(xiàn)[14]的方法:將醋酸纖維素溶解于丙酮,加入 SDS,攪拌均勻,然后取適量,滴入不相溶的液體冷卻劑中,液滴由于表面張力的作用,收縮成球型,在水溶液中凝固成球形抑菌劑滴丸.抑菌劑滴丸的粒徑主要通過改變制備工藝進(jìn)行調(diào)整.
1.2 抑菌劑劑量的確定
SDS是典型陰離子型殺(抑)菌劑,生物降解性好,對人體刺激小,可通過使蛋白質(zhì)變性進(jìn)而破壞微生物的細(xì)胞膜,破壞細(xì)胞內(nèi)部環(huán)境,使微生物失活,已在很多領(lǐng)域被用作殺(抑)菌劑.于 100mL錐形瓶中添加 50mL 9K液體培養(yǎng)基,分別加入0,5,10,30,50,100mg/L抑菌劑,接種微生物,接種量為 10%,菌密度 108個/mL,置于 30℃搖床以150r/min的轉(zhuǎn)速培養(yǎng).每個濃度設(shè) 3個平行.每24h取樣,Fe2+的濃度用紫外-可見分光光度計(UV-2550,日本島津公司)以鄰菲羅啉分光光度法檢測.
1.3 緩釋滴丸的表征
1.3.1 緩釋滴丸的表面特征 用掃描電子顯微鏡 SEM(S-3700N型,日本日立公司)觀測緩釋滴丸的表面形態(tài)結(jié)構(gòu),并用能譜儀(Quantax400型,德國Bruker公司)分別對滴丸的表面和斷面進(jìn)行能譜分析.
1.3.2 緩釋滴丸的組成成分 用傅里葉變換紅外光譜儀(Nicolet 6700型,美國Thermo公司)對滴丸的結(jié)構(gòu)特征進(jìn)行分析.
元素組成用元素分析儀(Vario EL Ⅲ, 德國Elementar公司)測得.
1.3.3 緩釋滴丸中抑菌成分的緩釋性能 于100mL錐形瓶中添加50mL 9K液體培養(yǎng)基,緩釋滴丸的添加量為 0.1g,設(shè) 3個平行,一個不添加滴丸的空白對照,置于 30℃搖床浸溶,轉(zhuǎn)速為150r/min.每24h取樣檢測溶液中抑菌成分SDS的濃度,實(shí)驗(yàn)周期為15d,SDS濃度采用紫外-可見分光光度計(UV-2550,日本島津公司)進(jìn)行檢測.
1.3.4 緩釋抑菌劑對黃鐵礦生物氧化的抑制 選用Z1為目標(biāo)菌,在250mL錐形瓶中加入150mL的無鐵9K培養(yǎng)基,添加1%的黃鐵礦,接種10%的富集菌液,設(shè)置3個平行,同時設(shè)不加抑菌劑的空白對照.置于30℃搖床以150r/min培養(yǎng),實(shí)驗(yàn)周期為30d,間隔取樣,檢測浸礦溶液的pH值、Eh及相應(yīng)金屬(總鐵、Zn2+、Cd2+、Pb2+、Mn2+)的濃度變化.菌密度采用血球板計數(shù), pH值、Eh的測定采用pH計、電位計(6171C型,上海任氏電子有限公司);金屬濃度采用電感耦合等離子體發(fā)射光譜儀 ICP-OES(Optima 5300DV型,Perkin Elmer公司)測定.
2 結(jié)果與討論
2.1 抑菌劑劑量確定
菌株 Z1為好氧化自養(yǎng)微生物,將基質(zhì)中的Fe2+氧化為 Fe3+而獲得生物生長所需的能量,其生長與 Fe2+的氧化情況密切相關(guān).通過測量溶液中ρ(Fe2+)隨時間的變化可以判斷Z1菌的氧化活性,從而確定抑菌劑的劑量.在初始ρ(Fe2+)相同的情況下,溶液中 ρ(Fe2+)愈低,ρ(Fe3+)濃度愈高,說明Z1菌將Fe2+氧化為Fe3+的能力愈強(qiáng),即氧化活性愈好.Z1菌對Fe2+的累積氧化率隨時間變化情況如圖 1所示.在空白和 SDS濃度為 5mg/L時,Fe2+累積氧化率較高,36h 左右基本氧化完全;SDS濃度為10mg/L時,前24h出現(xiàn)了Fe2+氧化的遲滯期,而后基本以恒定的速率被氧化,直至120h氧化完全;而在SDS為30mg/L及更高濃度的處理中,Fe2+只在前 12h內(nèi)有緩慢氧化,而后基本不再變化,在整個實(shí)驗(yàn)周期內(nèi)只有不到10%[初始 ρ(Fe2+)為 5.65mg/L]累積氧化率.添加抑菌劑濃度為 30mg/L以上時,可以有效抑制 Z1菌對Fe2+氧化,抑制率達(dá) 80%以上.故后續(xù)實(shí)驗(yàn)選取30mg/L為SDS的最低有效濃度.

圖1 不同濃度SDS對Z1菌氧化Fe2+的影響Fig.1 Effects of SDS on the oxidation of ferrous iron by strain Z1
2.2 緩釋滴丸的形態(tài)結(jié)構(gòu)特征
本研究制得的抑菌劑緩釋滴丸為白色球狀顆粒,具有一定的光澤,其表面形態(tài)見圖2.

圖2 緩釋滴丸SEM圖Fig.2 SEM micrograph of sustained-release pills A:表面,×800; B:斷面,×1500
從圖2可以看出,滴丸表面比較平整,有大量微孔存在,這種結(jié)構(gòu)有利于滴丸內(nèi)部的SDS溶出.從滴丸斷面的SEM圖可以看出,滴丸內(nèi)部結(jié)構(gòu)疏松,有大量的孔隙,也有利于其中 SDS的溶出.圖3A和3B分別是對應(yīng)表面和斷面的能譜圖.斷面能譜圖中硫和鈉 2個元素的峰值是表面能譜圖的2~3倍,說明抑菌劑滴丸負(fù)載了SDS,且滴丸內(nèi)部含有比表面更豐富的SDS.可見,采用滴制法制備醋酸纖維素為骨架的SDS緩釋滴丸,可以把其均勻地包裹在滴丸內(nèi)部.
2.3 抑菌劑緩釋滴丸的結(jié)構(gòu)組成分析
滴丸、SDS及載體CA的紅外光譜圖如圖4所示.從圖4可以看出,滴丸和SDS的紅外譜圖中同時出現(xiàn)以下 SDS的特征峰:S(=O)2反對稱伸縮峰、S(=O)2對稱伸縮峰和多個強(qiáng)的S-O-C伸縮峰;CA的紅外譜圖中特征峰出現(xiàn)在 1751,1390,1210,1090cm-1,依次為 C=O 伸縮振動、C-H彎曲振動、C(=O)-O伸縮振動和C-N伸縮振動.另外,由于磺酸基吸水性強(qiáng),易形成水合物(SO3+·H3O+), 1200~1100cm-1之間出現(xiàn)的特征峰,可顯示磺酸基的存在.上述結(jié)果說明,本研究制備的抑菌劑滴丸中,SDS的化學(xué)組成沒有改變,仍然以抑菌劑有效成分分布在滴丸中.

圖3 緩釋滴丸能譜圖Fig.3 Energy dispersive X-Ray spectraof sustainedrelease pills
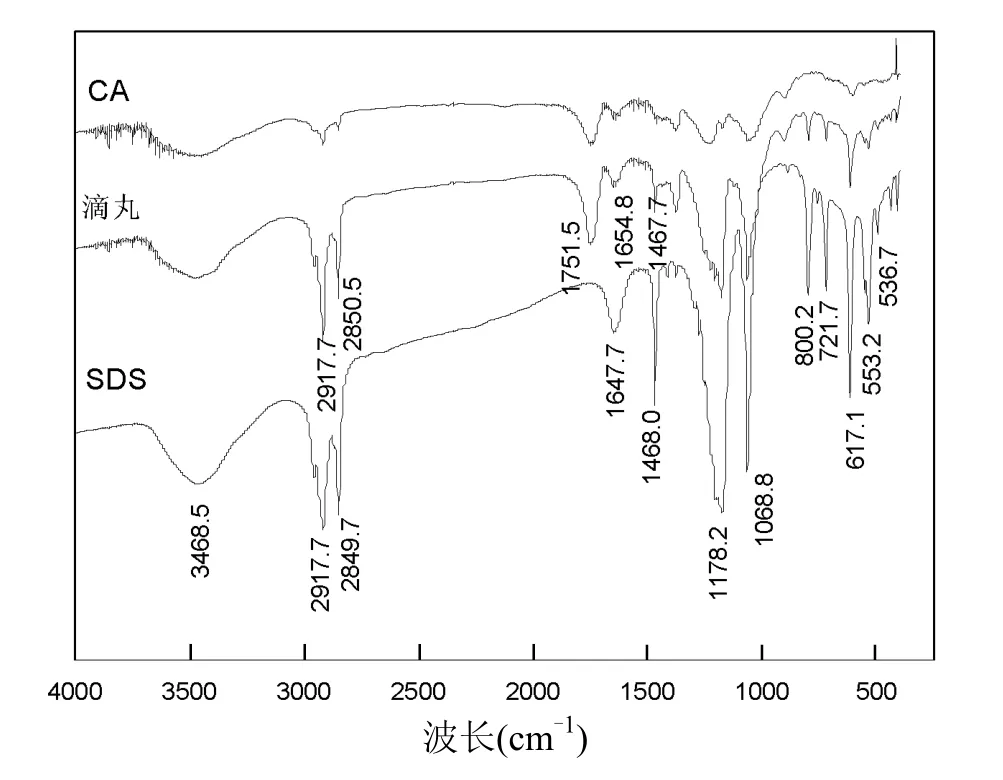
圖4 緩釋滴丸紅外譜圖Fig.4 FTIR spectra of sustained-release pills
2.4 載藥率
滴丸的載藥率是衡量滴丸質(zhì)量的重要指標(biāo),這里用 SDS、醋酸纖維素以及緩釋滴丸中硫的含量依據(jù)下式計算[15].
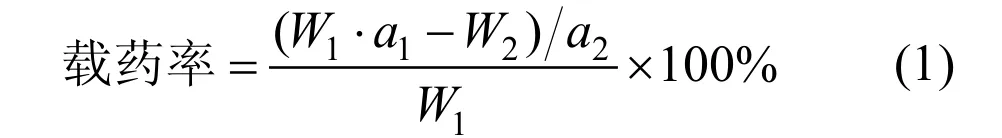
式中:W1為滴丸質(zhì)量, mg;a1為滴丸中硫的質(zhì)量百分?jǐn)?shù);W2為CA中所含 S元素的質(zhì)量,mg;a2為SDS中硫的質(zhì)量百分?jǐn)?shù).
樣品的元素組成如表1所示,結(jié)合表1數(shù)據(jù)算得,本研究制備的緩釋滴丸中SDS的載藥率為34.8%.

表1 緩釋滴丸的元素組成Table 1 Compositions of sustained-release pills
2.5 緩釋滴丸在酸性條件下的緩釋性能
由于抑菌劑組分與聚合物載體之間的結(jié)合方式與活性組分的釋放機(jī)理十分復(fù)雜,聚合物骨架的親水、親油性以及聚合物-抑菌劑結(jié)合體的交聯(lián)程度、立體結(jié)構(gòu)、顆粒大小等都可影響抑菌劑的釋放[4].為抑制尾礦的生物氧化作用,滴丸中的SDS需被逐漸釋放.結(jié)合投加量和載藥率,可了解滴丸中SDS的釋放隨時間的變化情況(圖5).

圖5 滴丸中SDS的釋放速率Fig.5 Released rate of ρ(SDS) in pills
前2d滴丸中SDS的釋放較多,平均每天釋放量達(dá)20.46%;之后2d,每天釋放量為12.4%;隨著時間的增加,釋放量明顯降低,每天只有1.12%的釋放量,15d時SDS溶出量為31mg左右,累積釋放量為89%,這說明所采用的高分子載體可滿足滴丸中SDS持續(xù)緩慢釋放的要求.另外,由于所采用的高分子材料可生物降解,因此滴丸中有效成分最終可全部釋放.
2.6 緩釋滴丸對黃鐵礦生物氧化的抑制效果
由于黃鐵礦氧化率主要受細(xì)菌濃度的影響,通過黃鐵礦的生物浸礦實(shí)驗(yàn)可直接反映其生物氧化效果.選擇黃鐵礦測試緩釋滴丸抑制礦物生物氧化的效果,結(jié)果如圖6和圖7所示.
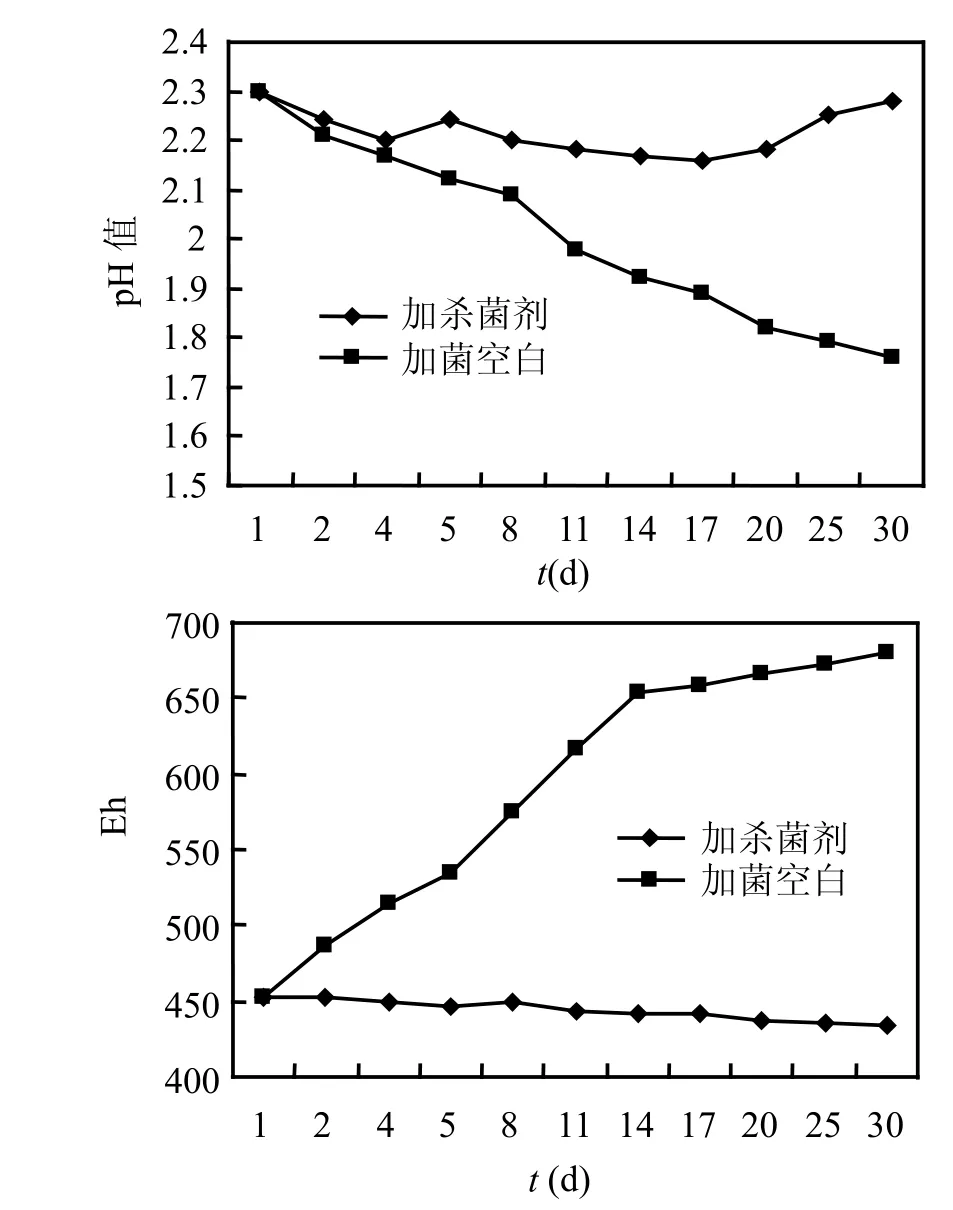
圖6 浸出液的pH值和Eh變化Fig.6 Variation of pH and Eh of solution
在未添加緩釋滴丸的情況下,實(shí)驗(yàn)初期,由于Z1菌的菌密度相對較低,黃鐵礦的氧化速度較慢,浸出液中金屬離子濃度較低,經(jīng)過適應(yīng)期后,Z1菌大量繁殖,加速黃鐵礦的氧化產(chǎn)酸,pH值降低,浸出液中Zn2+、Fe2+濃度及Eh迅速升高,氧化一段時間后,溶液Eh、pH值基本趨于穩(wěn)定.而添加了抑菌劑滴丸后,由于在實(shí)驗(yàn)過程中不斷有SDS從滴丸中釋放出來,抑制了 Z1菌的生長繁殖,在實(shí)驗(yàn)周期內(nèi),Eh、pH 值基本趨于恒定,浸出液中Zn2+和Fe2+濃度也遠(yuǎn)遠(yuǎn)低于未添加緩釋滴丸時的濃度.由此可知,所研制的抑菌劑緩釋滴丸可以有效抑制 Z1菌的生長,進(jìn)而抑制黃鐵礦的氧化產(chǎn)酸及重金屬溶出,具有良好的抑制礦物生物氧化的作用.

圖7 浸出液中金屬濃度的變化Fig.7 Concentrations of Zn2+ and total Fe2+ in solution
3 結(jié)論
3.1 十二烷基磺酸鈉可以作為所篩菌種的抑菌劑,以Fe2+氧化率作抑制指標(biāo),添加量為30mg/L時,對亞鐵氧化的抑制率可以達(dá)到80%以上,抑制了所選菌株的生長,進(jìn)而抑制了Fe2+的生物氧化.
3.2 采用滴制法制備出醋酸纖維素抑菌劑緩釋滴丸,SDS載藥率為34.8%,通過表征發(fā)現(xiàn),SDS以特征基團(tuán)的形式均勻分散于醋酸纖維素骨架中.
3.3 酸性介質(zhì)中緩釋實(shí)驗(yàn)結(jié)果顯示,緩釋滴丸中的SDS經(jīng)過快速釋放階段之后,釋放速度減慢,經(jīng)過15d的持續(xù)釋放,累積釋放率為89%.
3.4 生物浸礦實(shí)驗(yàn)結(jié)果顯示,添加抑菌劑緩釋滴丸,黃鐵礦生物浸出液的pH值、Eh變化幅度較小,同時重金屬的溶出下降,表明使用抑菌劑緩釋滴丸可有效抑制黃鐵礦的氧化產(chǎn)酸和金屬溶出.
[1]藍(lán)崇鈺,束文圣,張志權(quán).酸性淋溶對鉛鋅尾礦金屬行為的影響及植物毒性 [J]. 中國環(huán)境科學(xué), 1996,16(6):461-465.
[2]Crundwell F K. How do bacteria interact with minerals [J].Hydrometallurgy, 2003,71:75-81.
[3]蔣 磊,周懷陽,彭曉彤.黃鐵礦生物氧化過程的階段性 [J]. 金屬礦山, 2007,376:59-63.
[4]Peppas A K, Komnitsas H. Use of organic covers for acid mine drainage control [J]. Minerals Engineering, 2000,13(5):563-574.
[5]Dugan P R. Prevention of formation of acid drainage from high-sulfur coal refuse by inhibition of iron and sulfur-oxidizing microorganisms. II. Inhibition in run of mine refuse under simulated field conditions [J]. Biotechnology and Bioengineering,2004,29(1):49-54.
[6]Kleinmann R, Crerar D A, Pacelli R R, et al. Biogeochemistry of acid mine drainage and a method to control acid formation [J].Minerals Engineering, 1981,33(3):300-305.
[7]胡振琪,張明亮,馬保國,等.利用專性殺菌劑進(jìn)行煤矸石山酸化污染原位控制試驗(yàn) [J]. 環(huán)境科學(xué)研究, 2008,21(5):23-26.
[8]周科平,程 成.殺菌劑在礦山污水處理和復(fù)墾中的應(yīng)用 [J].采礦技術(shù),1996,15:15-17.
[9]Nixon J R. Preparation of microcapsules with possible pharmaceutical use [J]. Endeavour, 1985,9(3):123-128.
[10]Hari P R, Thomas C, Chandra P S. Chitosan/calcium alginate beads for oral delivery of insulin [J]. Journal of Applied Polymer Science, 1996,59(11):1795-1801.
[11]Edding T W, Schally A V, Tice T R et al. Long-acting delivery systems for peptides: inhibition of rat prostate tumors by controlled release of [D-Trp6]luteinizing hormone-releasing hormone from injectable microcapsules [J]. Proceedings of the National Academy of Sciences of the United States of America,1984,81(18):5845-5848.
[12]Peters M C, Isenberg B C, Rowley J A. Release from alginate enhances the biological activity of vascular endothelial growth factor [J]. Biomaterials Science, 1998,9(12):1267-1278.
[13]張 哲,金屬硫化物礦山尾礦生物氧化的抑制研究—以廣東大寶山多金屬硫化物礦山為例 [D]. 廣州:華南理工大學(xué), 2010.
[14]代瑞華,劉會娟,曲久輝,等.醋酸纖維素吸附劑的制備及其性能表征 [J]. 環(huán)境科學(xué), 2005,26(4):111-113.
[15]賈 偉.藥物控釋新劑型 [M]. 北京:化學(xué)工業(yè)出版社, 2005:49-69.

