牛磺酸的制備工藝優化及樹脂提純法初探
伍麗娜,孫 皓
(天津渤海職業技術學院,天津 300402)
牛磺酸(taurine),分子結構為H2NCH2CH2SO3H,化學名稱:2-氨基乙磺酸[1]。牛磺酸是機體細胞內含量最豐富的含硫自由氨基酸[2]。長期以來人們一直認為它是含硫氨基酸的一種無功能終末代謝產物,未被重視;直到1975年Hayes等報道貓缺乏牛磺酸可導致失明,Raiha等提出人工喂養的嬰兒因缺乏牛磺酸而血漿及尿中的牛磺酸水平不能維持正常后,方引起人們對牛磺酸的極大興趣[3]。
牛磺酸主要分布在人體內的中樞神經系統、視網膜、肝、心臟、骨骼肌等組織中。其生理作用主要表現在以下幾個方面:(1)促進大腦發育;(2)增強視力;(3)調節神經傳導;(4)促進吸收、消化脂肪,參與膽汁酸鹽的代謝;(5)對心臟、肝臟、內分泌機能也具有生理功能[4]。
現代研究表明[1]牛磺酸對嬰幼兒的健康和正常發育起著至關重要的作用。所以為保證嬰幼兒的健康發育,目前,世界上很多國家在供給嬰幼兒的牛奶和奶粉中已加入了牛磺酸。由此可見該產品的發展前途,它將產生巨大的經濟效益和社會效益。
本文研究用H2SO4、乙醇胺、Na2SO3等低成本的原料制備牛磺酸,并探索樹脂法分離提純牛磺酸的工藝。
1 實驗及部分
1.1 儀器及原料
樹脂(樹脂 D3520、樹脂 D4020、樹脂 X-5、樹脂S-8、樹脂 NKA-2)(南開大學化工廠);乙醇胺(A.R.天津北辰驊躍化學試劑廠);其它試劑均為分析純。
WH8401/7401攪拌器;電光分析天平(上海儀表電機廠);SHB-Ⅲ型真空泵(鄭州長城科工貿有限公司)。
1.2 基本原理
第一步:氨基乙醇硫酸酯的制備。

第二步:Na2SO3作為還原劑,將氨基乙醇硫酸酯還原為2-氨基乙磺酸(牛磺酸)。
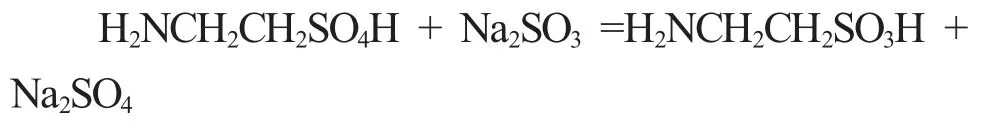
1.3 方法及過程
1.3.1 牛磺酸的制備
1.3.1.1 牛磺酸粗品的合成 先將一定量濃H2SO4加入到干燥的反應瓶中。再在攪拌和冷水浴冷卻下(溫度控制10℃左右,一定不能超過40℃),將一定量乙醇胺緩緩滴入反應瓶中。乙醇胺滴加完畢,減壓蒸餾。當得到計算量水后,停止蒸餾,冷卻后,得類白色固體,過濾,濾渣研細,干燥即得氨基乙醇硫酸酯的粗產品。
將若干Na2SO3和300mL水加入三口燒瓶中,緩慢升溫,加熱溶解,然后將氨基乙醇硫酸酯粗品緩慢加入,加完后回流反應18h后待用。
1.3.1.2 牛磺酸粗品的結晶 用30mLH2O和CaCl2配置CaCl2溶液,緩慢加入冷卻至80℃的上步反應液,加畢,繼續加熱回流2h。到時間后趁熱過濾,用熱水50mL洗滌濾餅兩次。合并濾液和洗液,蒸餾濃縮至大量NaCl晶體析出,趁熱過濾,收集濾液,濃縮,降溫后加入一定濃度的乙醇,冷卻至0℃,析出結晶,過濾,用乙醇洗滌,得牛磺酸粗品。
1.3.2 樹脂提純牛磺酸
1.3.2.1 樹脂吸附的靜態實驗 稱取經過預處理好的大孔吸附樹脂,用蒸餾水洗凈,瀝干水分后,放入250mL具塞磨口錐形瓶中,再加入牛磺酸水溶液,在間歇振蕩下靜態吸附,靜置8h,待達到飽和吸附后過濾,離心分離,定量移取清液,分析吸附后溶液中牛磺酸溶液的濃度。
1.3.2.2 吸附樹脂的動態實驗測定 稱取經過預處理好的大孔吸附樹脂,用蒸餾水洗凈,瀝干水分后,填充入吸附柱。在室溫下以1BV·h-1的流速從柱上口滴加配好的牛磺酸溶液。每10mL接收一次樹脂柱下的流出液,測牛磺酸的濃度,直到濃度不再變化為止。
將充分吸附后的大孔樹脂過濾,去除上清液,再加入裝水的錐形瓶中,封口,置于80℃水浴搖床中振搖2h,待解吸充分后,離心分離,過濾后取濾液測牛磺酸的濃度。蒸餾除去濾液中的溶劑,冷卻,析出結晶,干燥后得牛磺酸精品。
2 牛磺酸的檢驗[5]
2.1 鑒別
稱取樣品1g,加水20mL使之溶解,量取5mL,加入稀鹽酸(GB 622)5D及 Na2SO3試液(GB-633)(100g·L-1)5D,則產生無色氣泡。
2.2 含量測定
方法:精確稱取本品0.2左右(精確到0.0001g),加水50mL,使之溶解,再加5mL甲醛(GB-682)及4D酚酞,用 0.1mol·L-1NaOH 溶液(GB-629)滴定到終點。并用同樣方法進行空白校正試驗。
分析結果的表述:牛磺酸含量(X)以質量百分數計,按下式計算:
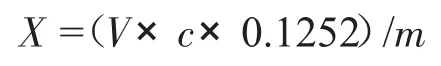
式中 V:NaOH標準滴定溶液的體積,mL;c:NaOH標準滴定溶液的摩爾濃度,mol/L;m:樣品的質量,g;0.1252 與 1.00mL NaOH 標準滴定溶液[c(NaOH)=1.000 mol·L-1]相當的以克表示的牛磺酸的質量。
所得結果取兩次平行測定的算術平均值。兩次平行測定的結果差值不大于0.3%。
3 結果與討論
3.1 牛磺酸制備工藝條件優化
3.1.1 牛磺酸制備工藝條件優化方案
3.1.1.1 氨基乙醇硫酸酯制備 此步操作,加料時乙醇胺和濃H2SO4的混合過程是一個大量放熱的過程。而乙醇胺和H2SO4在140℃發生分子間脫水生成醚,在170℃時則發生分子內脫水而生成烯烴。所以本步酯化反應的溫度必須小于100℃。
故本研究所采用的具體優化方法是:(1)改變反應物配料比,少量增加反應物濃H2SO4的用量;(2)加料時我們用冰水浴,在劇烈攪拌下將乙醇胺緩緩滴加入濃H2SO4中,使溫度保持在40℃以下;(3)在反應過程中用減壓蒸餾的方法,把反應中產生的水蒸出,產物生成量增加。
3.1.1.2 牛磺酸制備 此步反應是弱還原劑Na2SO3參與的氧化還原反應,需要高溫、長時的反應過程,而且此步反應的轉化率很低,控制著整個反應的反應產率。為了使產物生成量增加,本研究所采用的優化條件是:(1)改變反應物配料比,少量增加反應物 Na2SO3的用量;(2)分步加入中間體,攪拌;(3)通入 N2,保護Na2SO3,防止被空氣中的O2氧化為Na2SO4,滿足長時、高溫的需要。
3.1.2 牛磺酸制備工藝條件優化結果討論 通過實驗優化牛磺酸制備條件具體數據見表1。

表1 工藝條件變化對牛磺酸收率的影響Tab.1 Effect of change of process conditions to taurine yield
從表1上數據可以得出反應的最佳條件:濃H2SO4和乙醇胺的摩爾比是1.15∶1,Na2SO3和氨基乙醇硫酸酯的摩爾比是1.2∶1,通入N2,分批加料。
3.2 牛磺酸粗產品分離條件的優化
3.2.1 蒸發水量與牛磺酸產量的關系 為了使溶液中的牛磺酸析出,本研究應用牛磺酸在水中的溶解度隨溫度的升高而升高變化顯著,NaCl的溶解度隨溫度升高而變化不顯著的特性,用加熱濃縮使牛磺酸和NaCl都達到飽和,再降溫使牛磺酸充分析出NaCl少量析出,而達到提純分離牛磺酸的作用。
研究重點是通過實驗找到其最佳蒸發量。以牛磺酸含量為8.75g的100mL水溶液(0.7mol·L-1)為基準。下面就是本實驗在尋找最佳蒸發量時得出的數據:
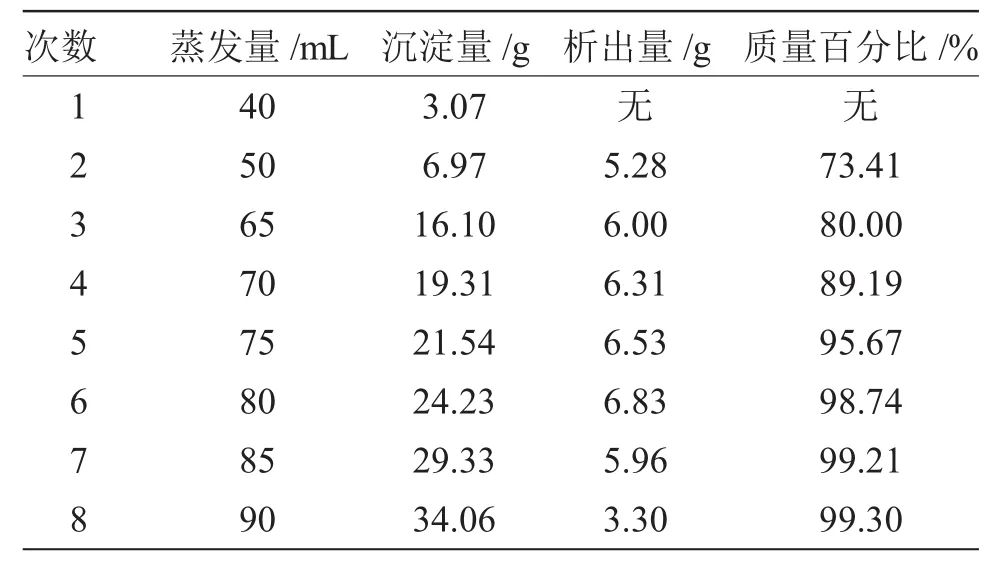
表2 蒸發量的測定Tab.2 Determination of evaporation capacity
從表上數據可以看出:蒸水量越多則牛磺酸的純度越高,但是牛磺酸的產率卻越低。所以并不是蒸水越多越好,應保證純度和產率都達到要求。故選擇最佳蒸水量是80mL。此時剩余的溶液量20mL正好略低于溶液中所含8.75g牛磺酸在92℃最大溶解度時的溶劑的量。因此可以得出:最佳蒸水量應達到使溶液中的牛磺酸在92℃時剛好達到飽和。
3.2.2 乙醇用量與牛磺酸產量的關系 加入CaCl2后的溶液中主要成分是牛磺酸和NaCl及其他少量雜質,為了使牛磺酸精品中的雜質含量及種類進一步減少,可用乙醇將溶液中的牛磺酸和NaCl先一步析出。經過多次試驗,進一步研究了乙醇用量與牛磺酸產量、純度的關系。具體數據見表3。
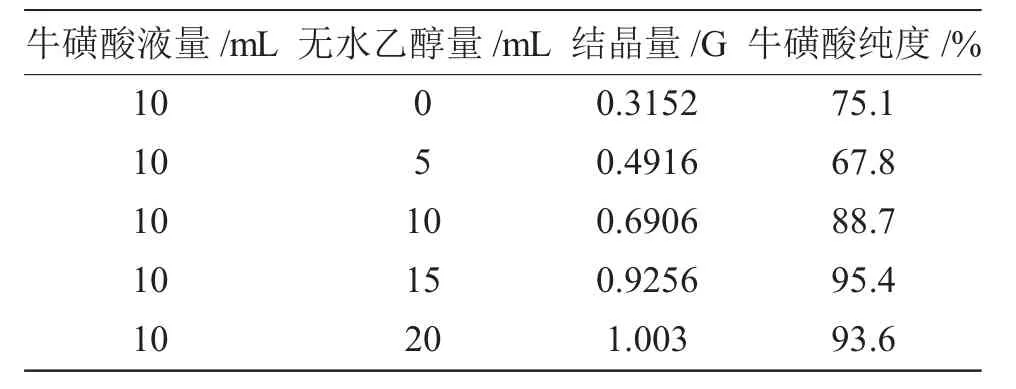
表3 乙醇用量與結晶純度Tab.3 Alcohol dosage and crystallization purity
從表3中數據可知,當乙醇∶牛磺酸液量=2∶1時得到的牛磺酸純度最高。牛磺酸的純度隨乙醇用量的增加而增加。但是考慮到成本的問題,建議在提純時,乙醇用量最好不要超過2∶1。
3.3 用樹脂精制牛磺酸的初探
3.3.1 樹脂的選擇 本實驗室用5種大孔吸附樹脂:NKA-2、X-5、S-8、D3520、D4020。牛磺酸在這幾種樹脂上的靜態吸附量見表4。

表4 樹脂吸附量Tab.4 Absorption of resin
實驗結果表明:牛磺酸在樹脂上的吸附性能與樹脂極性間的關聯性不是很強。牛磺酸在NKA-2和D3520上的吸附容量較大。估計與NKA-2具有較大的含水量和D3520具有較大的表面有一定關系。牛磺酸在大孔樹脂上的吸附機理需要進一步深入研究。
下面選擇吸附力較強的D3520和吸附力較弱的S-8兩種樹脂進行比較實驗。
3.3.2 溶液濃度與吸附量的關系 本研究在室溫(32℃),動態吸附,吸附時間均為4h,牛磺酸溶液量100mL,樹脂5mL的吸附環境下,逐步改變溶質濃度配合,觀察吸附效果。具體數據見表5。
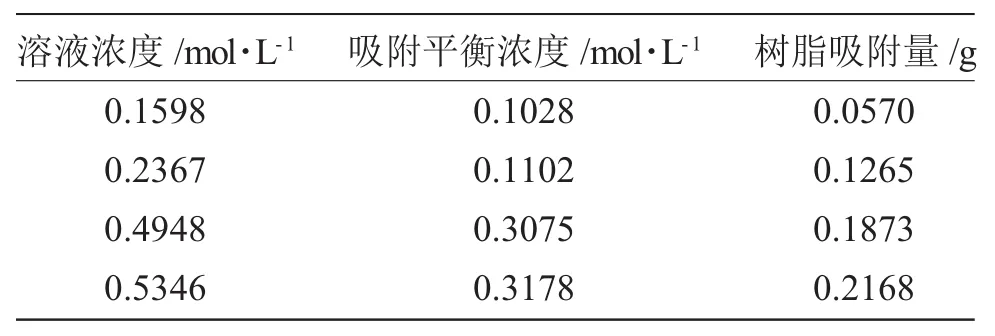
表5 D3520樹脂吸附受濃度影響Tab.5 Effect of concentration to D3520 resin adsorption
從表5數據可以得出,濃度對樹脂吸附量的影響結論:增加溶液的濃度可提高樹脂的吸附濃度,但是并不是溶液濃度與樹脂吸附效果呈直線關系,即達到一定程度后,溶液濃度對樹脂吸附效果的影響將越來越小。
3.3.3 溫度對樹脂吸附和脫附的影響 一般情況下,低溫有利于吸附,高溫有利于脫附。所以,本實驗擬用變溫的方法對吸附在樹脂上的牛磺酸進行解析。具體數據見表6。
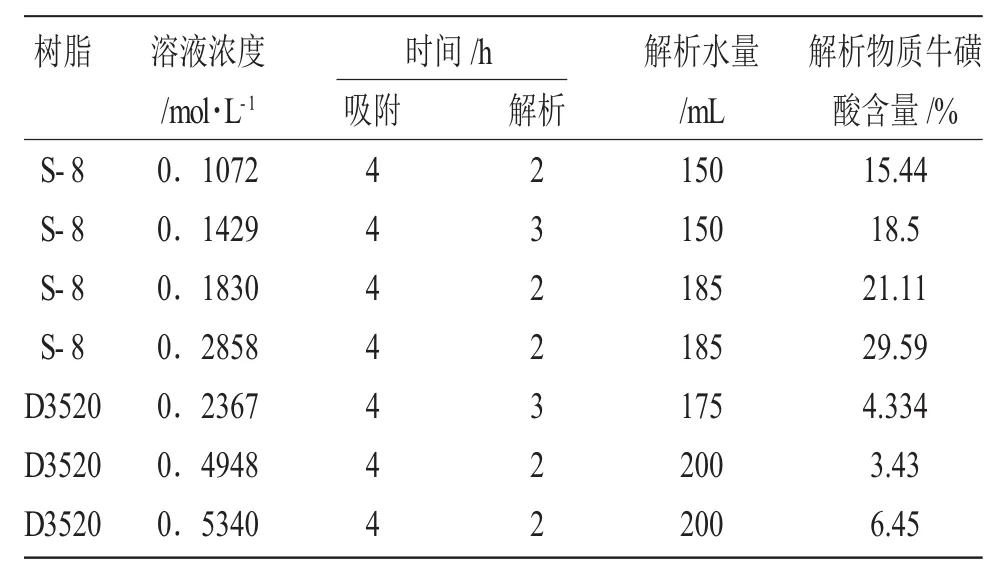
表6 解析結果Tab.6 Resolution results
從表6數據可知,不管在低溫還是在高溫環境,解析下來的牛磺酸粗品的純度都不高。估計不只有牛磺酸吸附在樹脂上,而且NaCl雜質也可能被樹脂所吸附。這與樹脂只吸附大分子量有機分子的理論相矛盾。
初步懷疑是NaCl粘附在樹脂外表面上,而不是真正為樹脂所吸附,是因為沒有沖凈樹脂表面而在解析時混入溶液。
3.3.4 增加沖洗工序對樹脂脫附的影響 增加一步沖洗樹脂的步驟,分別用0℃去離子水和0℃乙醇與去離子水的混合溶液沖洗。數據見表7。

表7 牛磺酸純度Tab.7 Taurine purity
實驗其它條件恒定為:吸附時間5h,溶液pH值7,解析時間2h,解析溫度80~90℃。
從表7數據可見,牛磺酸和NaCl均沒有樹脂所吸附,或是牛磺酸在樹脂上的吸附條件與解析條件非常接近,使得牛磺酸在樹脂上吸附非常不穩定,很容易就可以解析。可見,要使樹脂對牛磺酸達到吸附樹脂分離的效果,需要進一步研究牛磺酸在樹脂上的吸附行為,找到牛磺酸的準確吸附和解析條件,確定牛磺酸在樹脂上吸附的解析機理。
4 結論
(1)研究表明,當酯化反應,加料混合溫度為10℃,酸醇摩爾比為1.15∶1時,反應的結果最佳。而磺化反應中,需要在鹽Na2SO4加熱溶解與水時就通入N2,以防止鹽Na2SO4被空氣中的O2氧化。加料次數為4次,間隔2h。Na2SO4與酯的摩爾比是1.2∶1,反應溫度100~104℃,反應8h。反應總收率70.1%。
(2)初步研究了大孔吸附樹脂在牛磺酸提純方面的可行性。得出了大孔吸附樹脂對牛磺酸的吸附效果并不理想的結論。
[1]歐陽平凱,張贛道,祁嘉義,等.化工產品手冊[M].北京:化學工業出版社,1999.
[2]趙建偉,金征宇.牛磺酸在飼料中的應用[J].中國飼料,1999,(10):10-12.
[3]周建偉.牛磺酸與肝臟關系的研究進展[J].國外醫學(衛生學分冊),1995,(2):97-100.
[4]壟盛昭.牛磺酸的功能和合成新工藝研究[J].廣州食品工業科技,2000,(3.):12-13.
[5]伍麗娜.牛磺酸的合成及分離提純[J].天津化工,2008,(3):51-53.

