磷石膏還原分解過程的熱力學模擬*
(昆明理工大學環境科學與工程學院 昆明 650093)
磷石膏是濕法磷酸生產過程中產生的固體廢物,其主要成分是CaSO4.磷石膏具有產量巨大、利用率低、環境危害性大等特點,已成為一種嚴重的污染源且嚴重制約了磷肥工業的發展[1-2].目前,磷石膏的綜合利用已成為亟待解決的問題.隨著高溫熱分解技術的發展,多數學者傾向利用該技術回收磷石膏中的硫并替代石灰生產出大量的水泥[3-4].但因磷石膏成分極為復雜且受操作條件等的影響致使其分解機理極為復雜且副產物較多,嚴重制約了該工藝的工業化應用和發展.然而對磷石膏高溫熱分解的機理至今仍無確切定論,急需通過理論計算為磷石膏分解制酸聯產水泥熟料工藝的研究提供有效的理論指導.FactSage6.1計算軟件具有方便快捷、準確性高等特點,可以通過化學熱力學反應平衡分析方法對物料進行模擬計算以獲取物相組成、含量及動力學等基礎信息[5].因此,可以通過該軟件對反應物進行計算,為磷石膏分解反應特性的研究提供更多的基礎信息和有效指導.
本文所用符號說明如下:m為質量,g;Ai為加入量,g;φ為分解率,%;φ為脫硫率,%;V為揮發分;FC為固定碳;A為灰分.
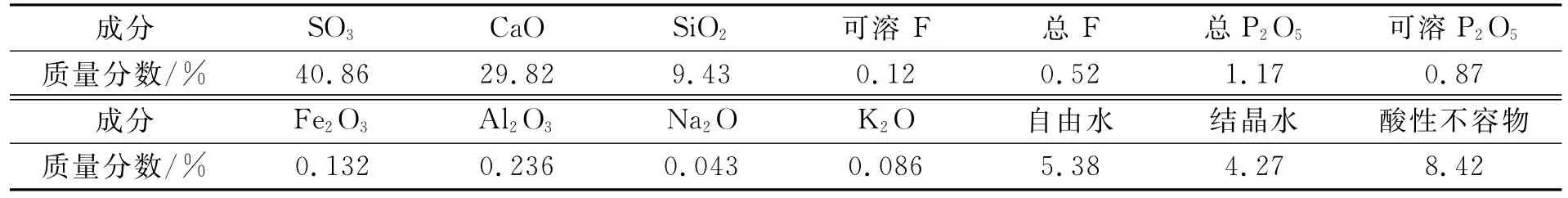
表1 磷石膏主要化學成分
1 原料與試驗方法
1.1 試驗原料
磷石膏采自云天化集團下屬富瑞化工廠,樣品經自然風干,過篩除去雜質備用.高硫煤采自云南楚雄,經風干后破碎,制成所需粒度的煤樣備用,其化學組成見表1.
1.2 試驗方法
試驗采用高溫熱分解的方法對高硫煤還原分解磷石膏的分解反應特性進行研究.試驗過程中將磷石膏與過100目篩的高硫煤按CaSO4/C摩爾比(β)為2混合備用.每次稱取物料1.1g送入管式爐內進行熱分解,反應溫度分別為1 000,1 100和1 200℃.試驗過程中0~800℃溫度段升溫速率(е)為8 ℃/min,800 ℃后е為5 ℃/min.99.9%的高純氮為保護氣,流量為250mL/min.通過XRD檢測固相產物物相組成,組分含量通過化學分析方法測定.
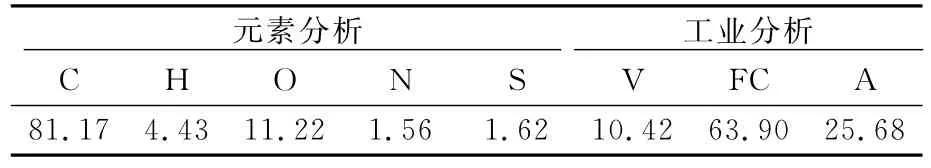
表2 高硫煤元素分析與工業分析數據 ω/%
2 理論計算
2.1 計算方法
FactSage軟件是在最小吉布斯函數原的基礎上建立的包括FACT-Win和ChemSage 2個計算熱化學軟件在內的功能強大的計算軟件.Fact-Sage擁有一個龐大的化學反應和熱力學數據庫,可對多種條件下的化學反應平衡及相圖進行有效計算與處理.
計算采用FactSage 6.1熱力學軟件中Equilib模型open算法對N2和CO下的磷石膏與高硫煤模擬體系分別進行計算.初始計算量如表3(β=2).采用 Phase Diagram 模型對 CaSO4-C 和CaSO4-C-CO體系的相圖變化進行了計算.計算條件:壓力為1.01×105Pa、反應溫度分別為1 000,1 100和1 200℃;N2加入量A=0.8g,CO 加入量Ai=0.3,0.8,1.0,1.5g.
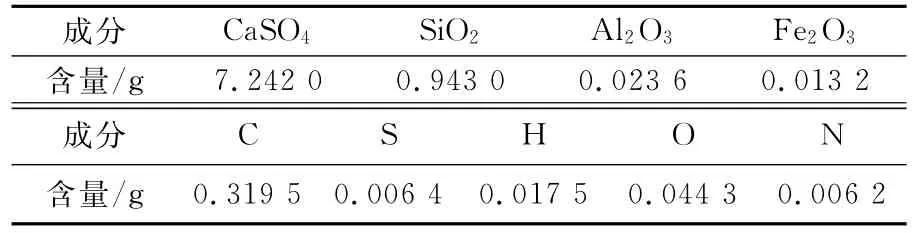
表3 磷石膏與高硫煤反應體系的模擬組成及含量
磷石膏分解反應的進行程度可以通過磷石膏的分解率和脫硫率2個轉化率來表示.

2.2 計算結果與分析
通過對N2下磷石膏與高硫煤模擬組分在不同反應溫度和CO不同加入量條件下(1 100℃)的物料進行平衡計算,結果如表4,5.表4,5的結果表明,N2和CO下磷石膏的分解產物為CaS,CaO,Ca3Al2O6,Ca2Fe2O5,SO2,CO 和 CO2等.表4表明,N2下隨著反應溫度的提高磷石膏的分解率和脫硫率呈逐漸增長趨勢直至達到最大值.這種變化趨勢表明反應溫度是影響磷石膏分解的重要因素,且結果顯示1 100℃即可達到最佳反應效果.在CO中(見表5),1 100℃時磷石膏的分解率隨CO加入量的增大呈現逐漸增長趨勢并直至最大值,而脫硫率卻呈類似正態分布的態勢.這表明一定質量濃度的CO對改善磷石膏的分解效果有重要貢獻.
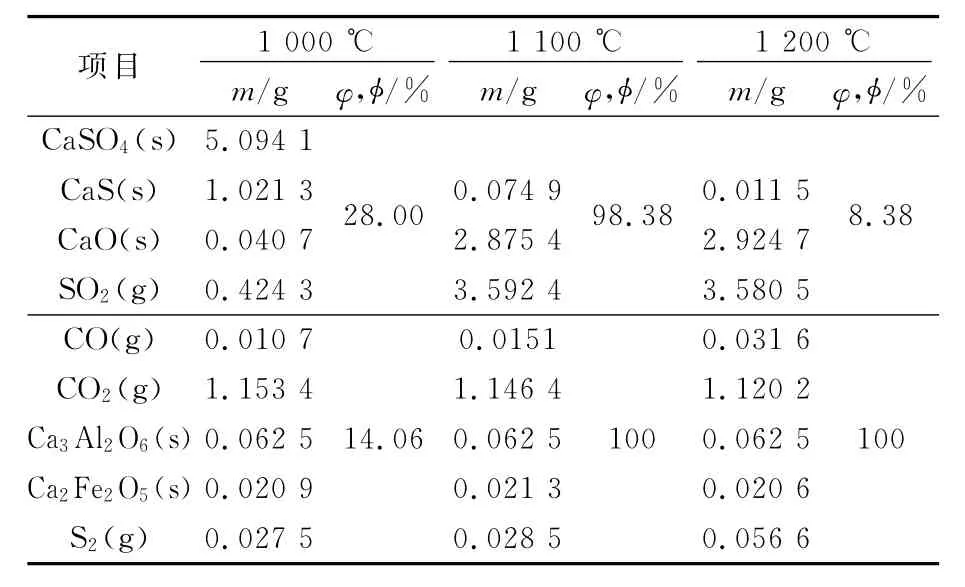
表4 不同溫度條件下磷石膏與高硫煤模擬反應體系的化學熱力學反應平衡計算結果

表5 CO氣氛下磷石膏與高硫煤模擬反應體系的化學熱力學反應平衡計算結果(1 100℃)
圖 1,2是 CaSO4-C 和 CaSO4-C-CO 體系物相組成圖.圖1表明CaSO4分解后的產物主要是CaS,CaO及氣相產物且在β=1~2時CaS與CaO區隨反應溫度升高而不斷增大,這表明溫度是影響CaSO4分解效果的重要因素.當溫度為1 130~1 200℃、β=1.7~2時固相產物只有CaO,推測此條件內CaSO4分解效果最佳.圖2表明1 000~1 200℃溫度段內,分解產物的物相組成與圖1中β=1~2時的變化趨勢相似,但1 130~1 200℃時主產物CaO區較同條件下CaSO4-C體系中CaO區略有增大,這表明微量的CO對獲取CaO有重要貢獻,而當CO/C大于0.18時則會產生CaS而不利于CaO的生成.由CaSO4-C和 CaSO4-C-CO體系相圖所確定的最佳反應條件與馬麗萍等[6]研究確定的高硫煤還原分解磷石膏的最佳β為1~2、反應溫度1 000~1 150℃等條件基本一致,這表明通過簡化反應體系的相圖可對部分反應條件予以預測從而為試驗研究提供基礎信息.

圖1 不同溫度下的CaSO4-C體系的物相變化圖
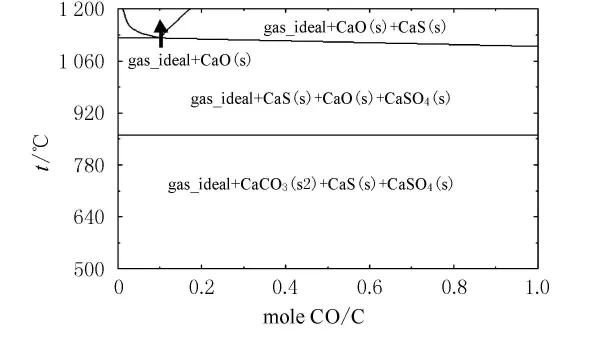
圖2 不同溫度下的CaSO4-C-CO體系的物相變化圖
3 結果分析與討論
圖3,4是不同溫度下磷石膏分解固相產物XRD圖及氣相產物析出速率曲線.圖3,4表明磷石膏分解后的產物與計算結果基本相同,分別是固相產物CaS,CaO及未反應的CaSO4和氣相產物CO,SO2等.鈣基化合物的定量化結果(見圖5)表明磷石膏分解后的固相產物的組分含量受反應溫度影響很大.隨著反應溫度的升高,CaSO4迅速減少,副產物CaS也呈減少趨勢,而CaO的含量恰好相反.
1 000℃時,計算結果表明反應后的固體物相組成為CaSO4,CaS與CaO,此結果恰與同溫度下的相圖和試驗結果的物相組成一致,推測化學熱力學反應平衡分析方法對磷石膏分解特性研究具有一定的指導作用.計算結果中CaSO4的分解率僅為28.00%且有大量的CaS產生而主產物CaO僅有微量生成,而試驗結果的磷石膏分解率為59.16%,高出計算結果約31%且CaS與CaO含量基本相同.這種分解率間的差異是因試驗反應體系中部分高硫煤經汽化生成CO后與煤粉共同作用于磷石膏,使得分解率大為提高.圖3中SO2及CO析出速率曲線也表明,反應過程中SO2與CO呈相同的變化趨勢但SO2析出略顯延后,推測磷石膏的分解主要是通過CaSO4與中間產物CO反應而實現.CaS與CaO的含量基本相同則是因CaSO4分解產生CaS與CaO的平行競爭現象所致.隨著CO濃度的變化,高濃度CO與CaSO4反應生成CaS而低濃度時則以生成CaO為主.肖海平等[7-8]研究也證實在 CO 還原分解CaSO4過程中CaS與CaO的生成的確存在平行競爭現象.
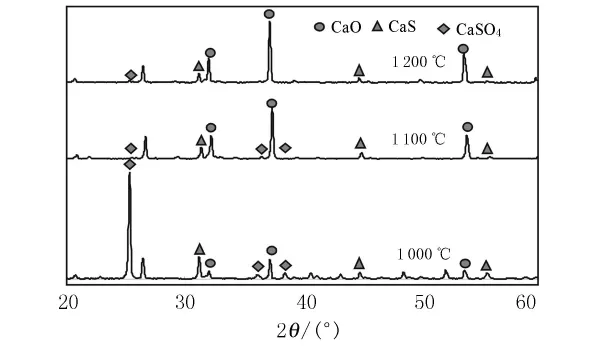
圖3 不同溫度條件下磷石膏分解固相產物的XRD曲線
隨著反應溫度提高到1 100℃,計算結果表明CaSO4分解率已達98.38%,比試驗結果的分解率高出約3.5%且CaS僅有微量殘余.磷石膏與高硫煤的反應體系極其復雜且磷石膏中的某些雜質(如:Al2O3,Fe2O3)對其分解具有催化作用,使得分解溫度降低而更利于分解.圖3中SO2析出速率曲線表明,SO2的析出速率在900℃即迅速增大且在1 050℃左右達到峰值濃度,推測磷石膏在900℃開始發生劇烈分解到1 050℃反應速率達到最快.肖海平等[8]研究證實N2氛下純CaSO4的起始分解在1 160℃以上,比磷石膏最佳分解溫度高出近100℃.綜合分析并推測試驗體系的分解效應高于理論結果,但結果卻恰好相反.原因是理論計算所獲取的是平衡條件下的結果而對反應時間等影響因素未加考慮,使得反應在長時間恒溫條件下反應更為完全所致.
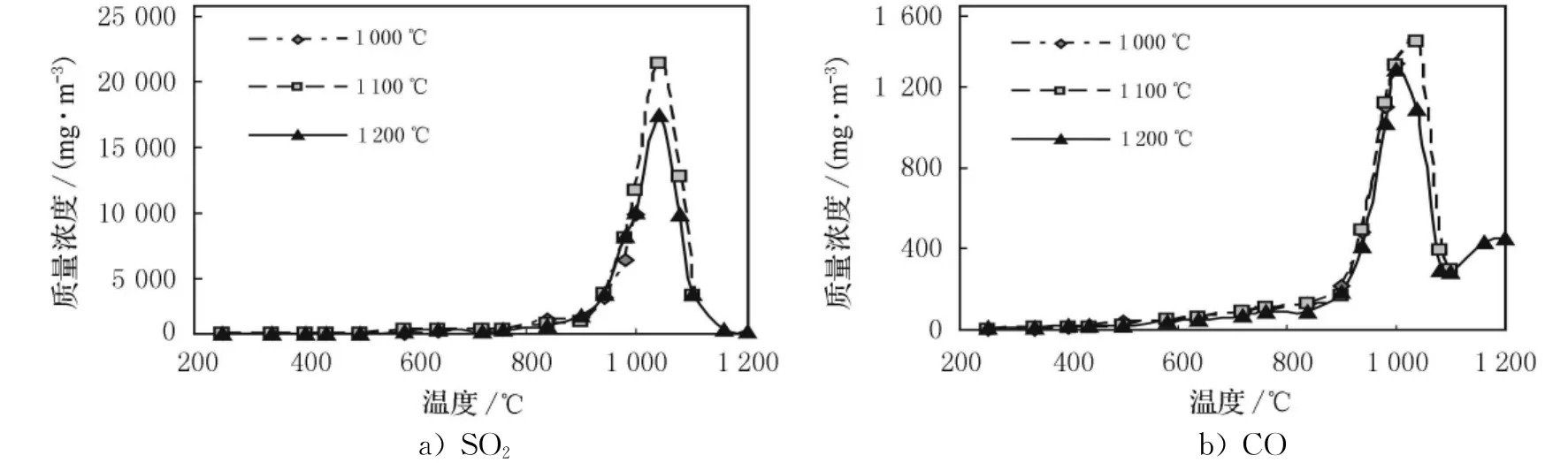
圖4 不同溫度條件下SO2及CO析出速率變化曲線
1 200℃時,試驗產物XRD結果表明CaSO4的特征峰基本消失,CaS特征峰也很微弱,圖5也表明CaSO4及CaS的含量分別不足2%和9%,這種變化趨勢與計算結果基本一致.但計算及試驗結果表明,在1 100℃即可獲得較高的分解率和脫硫率且綜合試驗及計算結果證實溫度進一步升高對分解率及CaS消除并無明顯作用,從節能及降低設備要求等考慮高硫煤還原分解磷石膏制取硫酸聯產水泥熟料工藝的最佳反應溫度為1 100℃.
CaSO4-C-CO體系的物相組成與同等配比和溫度下的CaSO4-C體系及實物體系物相組成基本一致,可以推斷磷石膏的分解在煤粉或煤粉與CO共同作用下均可完成.圖4中CO析出速率曲線表明在900~1 100℃溫度段內,CO的變化程度較大,反應溫度達到1 200℃時,CO仍不斷析出,且SO2與CO相似的變化趨勢也證實CO是磷石膏與高硫煤反應體系中重要的參與組分.綜合分析表明高硫煤還原分解磷石膏的反應過程更近似于CaSO4-C-CO體系的反應.
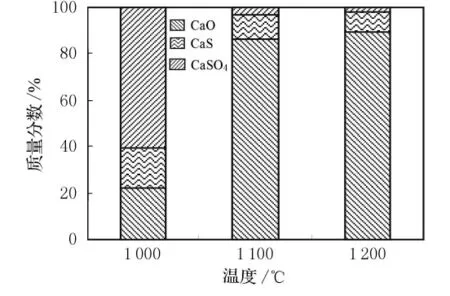
圖5 不同溫度下磷石膏分解固相產物的含量圖
化學熱力學反應平衡分析方法及相圖分析可在一定程度上對高硫煤還原分解磷石膏反應特性的研究提供指導但仍有很多不足,如其對高硫煤粒度、反應時間和升溫速率等因素對分解反應特性的影響無法提供有效的信息且具體成分含量及條件范圍確定上存有一定差異,因而需要結合試驗研究對分解反應過程進行深入研究以獲取最佳的結果.
4 結 論
1)理論計算與試驗結果的物相組成基本一致,主要為CaS,CaO,SO2等,但具體組分含量存有一定差異.原因是理論計算在假定反應平衡基礎上對模擬成分進行理論計算而并未對真實體系進行整體性計算.
2)綜合分析表明反應溫度對磷石膏分解產物有重要影響.高硫煤還原分解磷石膏制取硫酸聯產水泥熟料工藝的最佳反應溫度為1 100℃.
3)研究表明,磷石膏與高硫煤反應體系不是簡單的CaSO4-C的反應過程而更接近CaSO4-CCO體系.
4)化學熱力學反應平衡分析方法在研究磷石膏高溫分解反應特性時雖在確定組分含量方面存在一定差異,但整體變化趨勢與實際相似,因此該方法極具指導意義.
[1]Taher M A.Influence of thermally treated phosphogypsumon the properties of Portland slag cement[J].Resources Conservation and Recycling,2007,52(1):28-38.
[2]Yang J,Liu W,Zhang L,et al.Preparation of loadbearing building materials from autoclaved phosphogypsum[J].Construction and Building Materials,2009,23:687-693.
[3]van der Merwe E M,Strydom C A,Potgieter J H.Thermogravimetric analysis of the reaction between carbon and CaSO4.2H2O,gypsum and phosphogypusum in an inert atmosphere[J].Thermochimica Acta,1999(340-341):431-437.
[4]Elafifi E M,Hilal M A,Attallah M F,et al.Characterization of phosphogypsum wastes associated with phosphoric acid and fertilizers production[J].Journal of Environmental Radioactivity,2009,100(5):407-412.
[5]曹戰民,宋曉艷,喬芝郁.熱力學模擬計算軟件Fact-Sage及其應用[J].稀有金屬,2008,32(2):216-219.
[6]Ma Liping,Ning Ping,Zheng Shaocong,et al.Reaction mechanism and kinetic analysis of the decomposition of Phosphogypsum via a Solid-State reaction[J].Industrial and Engineering Chemistry Research,2010,49(8):3 597-3 602.
[7]肖海平,周俊虎,曹欣玉,等.CaSO4在CO氣氛下的平行競爭反應實驗與模型研究[J].燃料化學學報,2005,33(2):150-154.
[8]肖海平,周俊虎,曹欣玉,等.CaSO4在不同氣氛下分解特性的實驗研究[J].動力工程,2004,24(6):889-892.

