紫杉醇脂質體聯合順鉑治療晚期食管癌的臨床療效研究
丁令池,張曉東,姚衛東,陸俊國
(江蘇省南通市腫瘤醫院腫瘤科,江蘇南通,226361)
食管癌的發病率占全世界惡性腫瘤的第九位,其發病率具有明顯的區域性。在我國,食管癌的發病率與病死率位居第四位,高發區為河南林縣、太行山區、蘇北地區等,嚴重威脅人民健康,是我國確定的重點癌癥防治之一[1-2]。食管癌的早期癥狀不明顯,明確診斷時多為中晚期,約50%食管癌患者在就診時已為晚期,因而失去手術機會。化療是晚期食管癌的主要治療手段,可延長生存期,改善癥狀,提高生活質量。本科自2010年6月—2011年6月采用紫杉醇脂質體聯合順鉑(DDP)與順鉑聯合氟尿嘧啶(5-Fu)治療38例晚期食管癌患者,現匯報如下。
1 資料與方法
1.1 一般資料
2010年6月—2011年6月收治的食管癌患者38例,其中男 28例,女10例,年齡43~72歲,中位年齡62歲。肺轉移13例,肝轉移10例,鎖骨上淋巴結轉移17例,縱隔淋巴結轉移29例,腹腔淋巴結轉移16例,骨轉移8例。鱗癌32例,腺癌6例;初治患者26例,復治患者12例。入選標準:①均經病理學和影像學證實為晚期食管癌;②均有可測量的病灶;③無嚴重臟器功能障礙;④肝、腎功能及血常規正常;⑤一般情況良好,無嚴重營養不良;⑥預計生存期>3個月。所有患者隨機分為2組:其中試驗組19例,對照組19例,2組患者年齡、性別、分期均無統計學差異,具有可比性(P>0.05)。
1.2 方法
試驗組:紫杉醇脂質體135 mg/m2靜脈滴注,第1天;順鉑 25 mg/m2靜脈滴注,第1~3天,紫杉醇脂質體先于DDP使用,紫杉醇脂質體(商品名:力撲素,南京思科藥業有限公司生產)。對照組:5-Fu 0.75 mg/m2靜脈滴注,第1~5天;順鉑25 mg/m2靜脈滴注,第1~3天。2組均 21 d為1周期。初次使用紫杉醇脂質體化療前30 min分別給予地塞米松10 mg、西咪替丁400 mg靜脈注射,苯海拉明40 mg肌注預防過敏治療,初次用藥無過敏反應則第2次以后使用紫杉醇脂質體地塞米松可改為5 mg靜脈注射或不用。化療前血常規、肝腎功能、心電圖均正常,體力活動狀態(PS)評分<2分,且預計生存期>3個月。每2周期化療后評價療效。
1.3 評價標準
參照RECIST實體瘤療效評定標準,完全緩解(CR):所有目標病灶消失;部分緩解(PR):基線病灶最大徑之和至少減少30%;病變進展(PD):基線病灶最大徑之和至少增加20%或出現新病灶;病變穩定(SD):基線病灶最大徑之和有減少但未達PR或有增加但未達PD;有效率(RR)=CR+PR。毒性反按NCI-CTC毒性標準分0~4級。
1.4 隨訪
隨訪時間自化療結束時開始計算至死亡或隨診結束。疾病進展時間(TTP)從開始本方案治療的第1天至疾病進展,總生存時間(OS)從開始治療的第1天至死亡。采用電話隨訪,每月1次,所有入組病例均未失訪。
2 結 果
2.1 療效
全部共完成126個周期,其中治療組完成74個周期,對照組完成52個周期。試驗組CR 2例,PR 8例,SD 5例,PD 4例,總有效率為 49.65%;試驗組CR 0例,PR 5例,SD 6例,PD 8例,總有效率為26.31%。2組組間療效差異存在統計學意義(P<0.05),見表1。
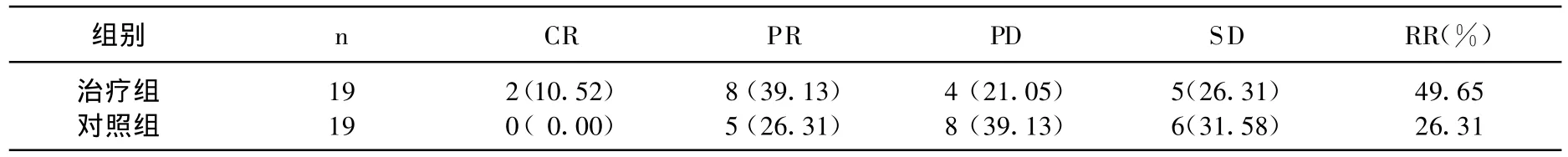
表1 2組療效比較[n(%)]
2.2 生存期和疾病進展
試驗組中位疾病進展時間(mTTP)4.6個月,中位生存期(mOS)10.3個月;對照組mTTP 3.7個月,mOS 9.2個月。2組生存期無顯著統計學意義。
2.3 毒性反應
所有患者均未出現水鈉潴留、過敏性休克、心臟損害等嚴重不良反應,無治療相關性死亡。出現的主要不良反應為骨髓抑制、胃腸道反應、周圍神經毒性及脫發,試驗組與對照組相比,2組不良反應無明顯差異(P>0.05),見表2。2組患者血清中CA125和CEA含量治療前差異無統計學意義(P>0.05),治療后均顯著下降(P<0.01),且治療后觀察組的CA125和CEA含量顯著低于對照組(P<0.01),見表2。
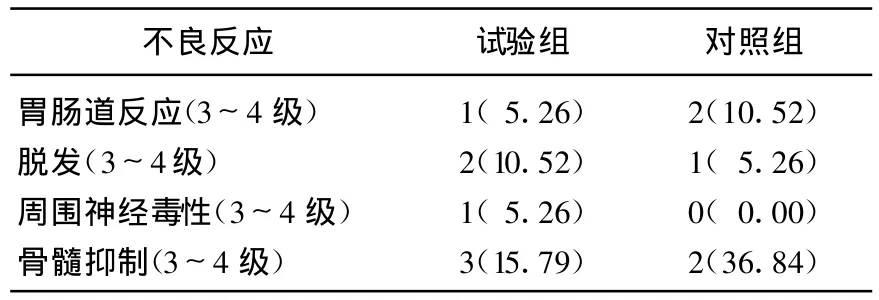
表2 2組不良反應比較[n(%)]
3 討 論
隨著腫瘤基礎理論研究的進展,抗癌新藥的問世,經過臨床研究工作者的不懈努力,使食管癌的臨床療效有了顯著的提高,生存時間明顯延長。20世紀70年代,食管癌化療以單藥為主,有效率較高的藥物有5-Fu、甲氨蝶呤(MTX)、絲裂霉素(MMC)、博來霉素(BLM)、長春堿性類(VDS)等。80年代以DDP+5-Fu的聯合方案成為食管癌的標準治療方案,有效率約25%~35%[3]。DDP和5-Fu聯合新藥是目前研究的主要方向,紫杉醇(PTX)顯示出了良好的單藥療效18%,無論是輔助化療、同步放化療,還是晚期姑息化療,PTX聯合DDP/5-Fu方案都是大家公認的療效較好的方案,有效率在 30%~50%。Zhang等[4]采用PTX、DDP化療方案治療食管癌和賁門癌,有效率腺癌為46%,鱗癌為25%。Huang等[5]在晚期食管鱗癌Ⅱ期研究中,方案為PTX+DDP,結果有效率59.3%,中位疾病進展時間5個月,中位生存期9.7個月,Ⅲ、Ⅳ度粒細胞減少在17.9%。國內黃鏡等[5]綜合分析了國外學者的臨床研究結果,認為三藥聯合(PTX+DDP+5-FU)的療效并不高于兩藥聯合(PTX+DDP),且毒性反應大,耐受性差。
紫杉醇(PTX)為從紫杉皮中提取后人工半合成,通過促進微管蛋白的集聚,抑制有絲分裂。但紫杉醇在水中幾乎不溶,因此其注射劑處方中加入助溶劑聚氧乙基蓖麻油和無水乙醇。助溶劑在體內降解時會引起嚴重的變態反應。近年來發現,脂質體能夠提高難溶藥物的水溶性,特別是還能減輕過敏反應的發生,并提高藥物穿透腫瘤血管的能力[7]。紫杉醇脂質體靜脈給藥最大耐受劑量可達200 mg/kg,而其注射制劑的最大耐受劑量僅為30 mg/kg[8]。另外脂質體可延長藥物在體內的循環時間[9],同時由于脂質體與細胞膜有類似的磷脂結構[10-11],可增加藥物與癌細胞的親和力,選擇性殺傷癌細胞。
本治療組采用紫杉醇脂質體聯合順鉑治療晚期食管癌,CR10.52%,PR39.13%,RR 49.65%;mT TP 4.6個月,mOS 10.3個月。與Zhang等[4]及Huang等[5]運用紫杉醇聯合順鉑治療晚期食管癌結果相近。紫杉醇脂質體與順鉑聯合方案的主要毒性反應是劑量限制性骨髓抑制和脫發、胃腸道反應,其中骨髓抑制以白細胞減少為主,Ⅲ~Ⅳ度骨髓發生率較低,經用粒細胞集落刺激因子治療后均能恢復正常,不影響下一周期的治療。紫杉醇脂質體過敏反應少,可減少激素的使用或不需激素預處理,在不降低療效的前提下副反應相對更少甚至有增加療效的作用,其臨床使用前景更廣泛,值得臨床進一步推廣。
[1]Bader F G,Lordick F,Fink U,et al.Paclitaxel in the neoadjuvant treatment for adeno carcinoma of the distal esophagus(AEG I).A comparison of two phase II trials with long-term follow-up[J].Onkologie,2008,31(7):366.
[2]蘇麗,張緯建,洪金省,等.食管癌三種放療技術的劑量學比較[J].實用臨床醫藥雜志,2010,14(9):37.
[3]Vashi P G,Gupta D,Tan B.Colon Carcinoma with Unusual Metastasis to the Esophagus Manifesting asM ultiple Nodules and Dysphagia:Management with Systemic Chemotherapy[J].Case Rep Gastroenterol,2012,6(2):484.
[4]Zhang X,Shen L,Li J,et al.A phase II trial of paclitaxel and cisplatin in patients with advanced squamous-cell carcinomaof the esophagus[J].Am J Clin Oncol,2008,31(1):29.
[5]Huang J,Cai R G,Meng P J,et al.PhaseⅡ study of paclitaxel and cisplatin for advanced squamous cell carcinoma of esophagus[J].Zhonghua Zhong Liu Za Zhi,2004,26(12):753.
[6]黃鏡,蔡銳剛,孟平均,等.紫杉醇聯合順鉑治療晚期食管鱗癌[J].中華腫瘤雜志,2004,26(12):753.
[7]Chen Q,Krol A,Wright A,et al.Tumormicrovascularpermeability is a key determinant for antivascular effects of doxorubicin encapsulated in a temperature sensitive liposome[J].Int J Hyperthermia,2008,24(6):475.
[8]Holvoet C,Vander H Y,Lories G,et al.Preparation and evaluation of paclitaxel-containing liposomes[J].Pharmazie,2007,62(2):126.
[9]趙銳,趙瑋瑋.抗癌植物藥紫杉醇研究進展與動態[J].中草藥,2009,7(7):1172.
[10]Strieth S,Eichhorn M E,WernerA,et al.Paclitaxel encapsulated in cationic liposomes increases tumor microvessel leakiness and improves therapeutic efficacy in combination with Cisplatin[J].Clin Cancer Res,2008,14(14):4603.
[11]Campbell R B,Ying B,Kuesters G M,et al.Fighting cancer:from the bench to bedside using second generation cationic liposomal therapeutics[J].J Pharm Sci,2009,98(2):411.

