層間水分子含量對銅鐵水滑石超分子作用力的影響
施 煒 胡 軍 倪哲明 李 遠 劉 嬌
(浙江工業大學化學工程與材料學院,先進催化材料實驗室,杭州310032)
層間水分子含量對銅鐵水滑石超分子作用力的影響
施 煒 胡 軍 倪哲明*李 遠 劉 嬌
(浙江工業大學化學工程與材料學院,先進催化材料實驗室,杭州310032)
構建銅鐵水滑石[Cu3Fe-LDHs-yH2O(y=0-2)]周期性計算模型,采用密度泛函理論(DFT),選取CASTEP程序模塊,對體系進行幾何全優化.從結構參數、氫鍵、Mulliken電荷布居、逐級水合能等角度研究了層間NO3-和H2O的分布形態及其與水滑石(LDHs)層板的超分子作用,探究了水分子數目對體系姜-泰勒效應的影響.結果表明:Cu3Fe-LDHs-yH2O主客體間存在著較強的超分子作用力,主要包括氫鍵和靜電作用,其中氫鍵作用在水合過程中起主導作用,氫鍵強度的順序是層板-陰離子(L-A)型>陰離子-水(A-W)型>層板-水(L-W)型>水-水(W-W)型;隨著層間水分子數的增加,層間距先略微降低后顯著升高,Cu3Fe-LDHs體系的Cu―O八面體被逐漸拉長,層板Cu2+的姜-泰勒畸變程度逐漸增大,體系的逐級水合能絕對值逐漸降低,說明Cu3Fe-LDHs的水合程度不會無限增加,而是具有一個飽和值.Cu3Fe-LDHs-1H2O構型接近理想六方晶胞,層板金屬畸變程度最小,穩定性最高,層間距與實驗值較吻合,推測其為實驗上合成的Cu3Fe-LDHs較穩定的構型.
密度泛函理論;銅鐵水滑石;超分子作用力;姜-泰勒效應;逐級水合能
1 引言
層狀雙羥基復合金屬氫氧化物俗稱水滑石(LDHs),由于它具有獨特的層狀構型,使得其層板金屬離子和層間陰離子具有可調變性.1,2人們可以將具有催化活性的二價(Zn2+、Ni2+、Mn2+、Cu2+等)或三價(Co3+、Fe3+、Cr3+等)金屬離子替換進LDHs層板,使其具有良好的催化性能.
銅、鐵是常見的催化活性組元,二者可被同時替換進LDHs層板,協同發揮催化作用.故銅鐵水滑石被廣泛應用于各種催化反應中,如糠醛合成、3安息香異丙醚合成、4,5高氯酸鹽分解、6胺的芳基化反應7等.但實際上,銅鐵水滑石的實驗合成比較困難,一方面Cu2+具有姜-泰勒效應,較難進入LDHs層板;1,5,8另一方面,銅鐵水滑石的層間含有不同數目的水分子,水分子的存在也會影響銅鐵水滑石的結構性質和催化性能.因此,研究銅鐵水滑石的微觀結構具有重要意義,為了從本質上解釋水分子對銅鐵水滑石微觀結構及穩定性的影響,有必要引入計算機模擬技術.
近年來,密度泛函理論(DFT)9,10作為計算機模擬技術中的一種常用方法,被廣泛用于研究LDHs材料的微觀結構,它是一種研究多電子體系電子結構的量子力學方法,可以用來計算LDHs體系的結構參數、成鍵狀況、作用能、電子密度,以及分子間交互作用的電子性質等.Deyse等11通過從頭算法模擬了ZnAl-LDHs在脫水過程中結構參數、電子性質以及吉布斯自由能的變化規律;Vinuthaa等12以MgAl-LDHs為基礎,采用分子動力學模擬和密度泛函理論,將CrO42-和VO43-插入層間并加入不同數目的水分子,探究了LDHs的結構參數、氫鍵、水合能,以及不同陰離子插層LDHs的自擴散系數.本課題組曾采用密度泛函理論搭建了Mg3Al-LDHs-yH2O模型,13探討了主客體間的超分子作用.此外,還搭建了Mg3Sn-LDHs-yH2O模型,14并對其進行幾何全優化,研究了層間陰離子和H2O的分布形態及其與主體層板的超分子作用.以上這些研究均只改變了LDHs層板中的一種二價或三價金屬離子,并沒有將LDHs中的二價和三價金屬離子全部進行替換.
基于以上基礎,本文采用密度泛函理論,運用Materials Studio 5.5構建了NO3-插層的Cu3Fe-LDHs雙層周期性計算模型,選取NO3-位于hcp-Fe位的構型(Fe正對)為模型,加入不同數目的水分子,探求客體NO3-與H2O在Cu3Fe-LDHs主體層板間的分布形態,研究了層間水分子含量對體系主客體作用力以及姜-泰勒效應的影響.
2 計算模型和方法
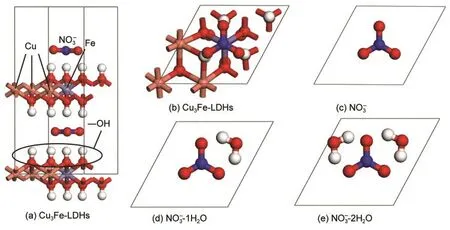
圖1 Cu3Fe-LDHs-yH2O(y=0-2)主客體計算模型Fig.1 Host-guest calculation models of Cu3Fe-LDHs-yH2O(y=0-2)
本文以2H堆積模式1構建了銅鐵水滑石的主體層板[Cu6Fe2(OH)16]2+,選取NO3-處于hcp-Fe位且平行地置于兩層板的中間位置(俯視時,NO3-上的三個氧原子所形成的三角形處于層板Fe原子上的三個羥基氫所形成的三角形的內部)的構型為模型,如圖1(a,b)所示.采用先前工作中證實對水滑石體系較適用的計算方法,13,15即選用CASTEP程序模塊,16在LDA-CA-PZ22基組17水平對模型進行幾何全優化,原子電子采用超軟贗勢,18截止能量為330.0 eV,自洽場計算的誤差為2×10-6eV·atom-1,能帶結構在布里淵區k矢量的選取為4×4×1,基態能量選用Pulay密度混合算法,19整體電荷數為0,同時優化晶胞,其它參數設置為程序的默認值.優化后的微觀結構及氫鍵作用模型如圖2(a)所示.在此基礎上,根據原子的電負性,選取在LDHs層板的中間位置加入yH2O(y=1-2),且H2O上的θHOH與NO3-上的θONO相對(客體初始位置見圖1(c,d,e)),并對其進行幾何全優化,得到的結構如圖2(b,c)所示,圖2(a?-c?)為優化所得的層間客體的分布形態.
3 結果與討論
3.1 結構參數分析
將優化得到的Cu3Fe-LDHs-yH2O(y=0-2)的結構參數列于表1,從圖2可以看出,當y=0,1時,NO3-和H2O與層板保持平行,并且二者均處于上下層板的中間位置,與上下層板的距離基本相等,氫鍵排布較為對稱;當y=2時,層間距顯著增大,為了維持LDHs體系的整體穩定性,NO3-和H2O不再與層板保持平行,而是以偏向某一層板的方式隨機地位于LDHs層間,以獲得最大的主客體作用力.

圖2 Cu3Fe-LDHs-yH2O(y=0-2)優化構型和層間氫鍵分布情況Fig.2 Optimized structures and distribution of hydrogen-bonding between layers of Cu3Fe-LDHs-yH2O(y=0-2)

表1 Cu3Fe-LDHs-yH2O(y=0-2)的晶胞參數Table 1 Lattice parameters of Cu3Fe-LDHs-yH2O(y=0-2)
從表1可以看出,隨著層間水分子數目的增多, c值先略微降低后顯著升高,這主要是由于晶胞參數c值(層間距dc=0.5c)不僅受到層板金屬離子半徑的影響,還受到主客體間作用力大小的影響.2當y=1時,Cu3Fe-LDHs的層間距dc=0.7416 nm,與實驗4合成的Cu3Fe-LDHs層間距dc=0.7247 nm相接近.從各體系的α、β、γ值與理想六方晶胞角度(α=90°、β=90°、γ=120°)的偏離值之和Δθα+β+γ中可以看出,Cu3Fe-LDHs-1H2O體系的角度畸變最小,說明其晶型較符合理想六方晶胞,實驗3證明,Cu3Fe-LDHs的結構越規整,其催化合成糠醛1,2-丙二醇縮醛的效果越好;Cu3Fe-LDHs-2H2O體系晶型偏離理想六方晶型較大,這可能與層間客體的對稱性最差有關.
3.2 氫鍵分析
氫鍵會對水滑石材料的微觀結構造成較大的影響,它是一種廣泛存在的分子間的弱作用力,是特殊的分子間或分子內作用.它是由氫原子與另一個電負性很強、原子半徑較小的Y原子(如F、N、O等)的孤對電子之間相互吸引而成的一種鍵(用X―H…Y表示).20-22一般情況下,氫鍵具有方向性和飽和性,氫鍵的鍵長越短,鍵角越接近180°,氫鍵的強度越強.
從圖2和表2可以看出,Cu3Fe-LDHs-yH2O體系存在復雜的氫鍵網絡,具有多重氫鍵.它與一般的氫鍵性質不同,層間NO3-并不只與層板上一個羥基中的氫或層間水分子中的氫、氧形成氫鍵,而是與多個羥基上的氫原子以及多個水分子形成多重氫鍵.當y=0-2時,Cu3Fe-LDHs體系的氫鍵數目分別為23、36、30.可將這些氫鍵劃分為四類:層板-陰離子(L-A)型、陰離子-水(A-W)型、層板-水(L-W)型、水-水(W-W)型,其中L-A型和A-W型氫鍵又可進一步分為O型和N型氫鍵.結合表2數據和圖3可以看出以下幾個特征:(1)L-A型氫鍵和A-W型氫鍵均分布于圖的左上角和右下角,且L-A型氫鍵的數目較A-W型氫鍵多.L-W型氫鍵在圖中較分散,且數目較少.W-W型氫鍵數目最少,故Cu3Fe-LDHsyH2O(y=0-2)體系中四種類型氫鍵的強弱關系為: L-A型>A-W型>L-W型>W-W型;(2)N型氫鍵均位于圖的右下角,氫鍵強度相對較弱,O型氫鍵絕大多數位于圖的左上角,氫鍵強度相對較強,說明N型氫鍵的強度要小于O型氫鍵,結果與N、O電負性大小相一致;(3)對比其他體系,Cu3Fe-LDHs-1H2O體系的氫鍵強度是最強的,原因是其氫鍵數目最多且層間距最小,NO3-和H2O與上下層板更接近,導致其受到靜電的協同效應變大,從而使其氫鍵強度最強;(4)對于不同的氫鍵類型,Cu3Fe-LDHs-yH2O(y= 0-2)的L-A型氫鍵強度呈先增大后減小趨勢,A-W型、L-A型、W-W型氫鍵強度均隨體系水分子數目的增多而增加,由于Cu3Fe-LDHs-yH2O的層間距先降低后升高,主客體作用力先增大后減小,故L-A型氫鍵在四種氫鍵類型中占主導作用;(5)從計算得到的氫鍵鍵長結果來看,所形成的O型氫鍵鍵長和N型氫鍵鍵長比一般的O―H…O型氫鍵鍵長(0.240-0.276 nm)和O―H…N型氫鍵鍵長(0.280-0.300 nm)均略短,氫鍵強度更強,這主要是LDHs主客體間靜電與氫鍵協同效應的結果.

表2 Cu3Fe-LDHs-yH2O(y=0-2)的氫鍵參數Table 2 Hydrogen bond parameters of Cu3Fe-LDHs-yH2O(y=0-2)

圖3 Cu3Fe-LDHs-yH2O(y=0-2)中氫鍵鍵角(θ)與鍵長(l)的關系Fig.3 Relationship between bond angle(θ)and bond length(l)of hydrogen-bonding in Cu3Fe-LDHs-yH2O(y=0-2)■Cu3Fe-LDHs,●Cu3Fe-LDHs-1H2O,▲Cu3Fe-LDHs-2H2O
3.3 Mulliken電荷布居分析
Mulliken布居是Mulliken23提出的表示電荷在各組原子之間分布情況的方法,它可以間接地討論分子內相互作用力的強弱,尤其對同一系列的分子十分奏效.因此,為了進一步研究Cu3Fe-LDHs-yH2O體系的主客體間相互作用力,對其進行了電子分析,得到的Mulliken電荷布居(對上下層板、客體陰離子及水分子的電荷布居作了平均化處理)列入表3中.從表中數據可以看出,當NO3-插層后,其電荷布居由-1.000e變為-0.730e,而層板的電荷布居由1.000e變為0.750e,表明兩者發生了靜電作用和氫鍵作用,且靜電作用總體表現為靜電吸引,大部分電荷由客體陰離子向主體層板發生了轉移.隨著Cu3Fe-LDHs層間水分子數目不斷增加,層間距先降低后升高,主客體作用力先增大后減小,而Cu3Fe-LDHs層板的電荷布居及層間NO3-的電荷布居的絕對值卻呈降低趨勢,分別為0.750e、0.680e、0.695e和0.730e、0.685e、0.665e.當y=1時,層板的電荷布居出現了一個最低值,這主要是由于該體系的層間距最小,體系中的客體NO3-和H2O較靠近主體層板使得其氫鍵作用占優勢所造成的,與前面的氫鍵布居分析結果相一致.
從表3中水分子的電荷數可以看出,當水分子插入Cu3Fe-LDHs層間,水分子上的電荷布居由0e變為-0.005e到-0.015e,發生了不同程度的降低,這主要是由于水分子既是氫鍵供體又是氫鍵受體的緣故,兩者相互作用平衡了部分電荷,導致水分子所帶的電荷數較小.隨著水分子加入的增多,水分子的電荷布居逐漸變大趨向于零,由此可知水分子作為氫鍵受體的優勢逐漸減弱,并逐漸被氫鍵供體作用所平衡,使兩種作用強度相當,單個水分子受到的超分子作用力逐漸趨向平衡.層間水與層板和層間陰離子的作用力隨著水分子數目的增多而減弱,說明Cu3Fe-LDHs的水合程度不會無限增加而是具有一定的飽和度.

表3 Cu3Fe-LDHs-yH2O(y=0-2)的電荷布居Table 3 Mulliken charge population of Cu3Fe-LDHs-yH2O(y=0-2)
3.4 姜-泰勒效應分析
1937年,姜(Jahn,H.A.)和泰勒(Teller,E.)指出:在對稱的非線性分子中,如果有一個體系的基態有幾個簡并能級,則是不穩定的,體系會發生畸變,使能級發生改變,以消除簡并性,這就是姜-泰勒效應.24水滑石層板類似于水鎂石Mg(OH)2結構,它是由MO6八面體共用棱邊所形成的,當其層板上的鎂被銅等一些金屬替換時,水滑石就會由于姜-泰勒效應發生畸變.對于Cu3Fe-LDHs-yH2O體系中的Cu2+, d軌道電子數理論上為9,則有可能失去dz2或dx2-y2
上的部分電子.若失去的是dz2上的電子,則會變成壓扁的八面體構型;若失去的是dx2-y2上的電子,則會變成拉長的八面體構型.表4列出了Cu3Fe-LDHsyH2O體系中的金屬-氧鍵成鍵布居及其鍵長分布,結合表4數據可以看出,Cu3Fe-LDHs中的6個Cu―O鍵均出現了4短鍵2長鍵的分化,為典型的拉長的八面體構型.隨著層間水分子數目的增多, Cu3Fe-LDHs中的Cu―O短鍵鍵長逐漸減小,長鍵鍵長逐漸增大,八面體體型被逐漸拉長,姜-泰勒畸變逐漸增大.實驗證明,銅的六配位配合物以拉長的八面體形式穩定存在,這是因為在無其它能量因素影響時,形成兩條長鍵四條短鍵比形成兩條短鍵四條長鍵的總鍵能要大.24
對于金屬離子的角度畸變程度,可用ΔθOMO(M為Cu、Mg、Al)來衡量,即層板中每一個金屬原子與其相配位的氧原子所形成的共12個角θOMO跟理想六配位角度(90°)的絕對差值的平均值.從表5數據可以看出,在Cu3Fe-LDHs-yH2O體系中,ΔθOCuO值大于ΔθOFeO,且隨著層間水分子數目的增多,ΔθOCuO值逐漸增加,說明層板Cu2+的畸變程度逐漸增大,與鍵布居分析結果一致.Cu3Fe-LDHs-1H2O的ΔθOMO最小,說明其金屬離子的畸變程度最小,層板穩定性最高.
此外,在Cu3Fe-LDHs-yH2O體系中,Fe的原始電子組態為3d64s2,Fe3+的電子組態理論上應為3d5, LDHs體系中OH為弱場環境,Fe3+的電子應為高自旋排布,理論上不會出現畸變.但從表5數據可以看出,Fe3+的配合物也存在一定程度的金屬畸變,這可能是由于Fe3+與Cu2+八面體共用棱邊,Fe3+電子組態受到Cu2+影響所造成的.
3.5 逐級水合能分析
用逐級水合能ΔEH(y)估算Cu3Fe-LDHs-yH2O隨水分子增加引起的勢能增加量.EH(y)的計算公式如下:

其中,E(Cu3Fe-LDHs-yH2O)為Cu3Fe-LDHs-yH2O體系的總能量;E(Cu3Fe-LDHs-(y-1)H2O)為Cu3Fe-LDHs-(y-1)H2O體系的總能量;E(H2O)為水分子的能量;y為水分子數目.計算結果列于表6.
從表6可以看出,單個水分子的逐級水合能的絕對值由140.802 kJ·mol-1降為75.5314 kJ·mol-1,這主要是由于隨著水分子數目的增加,水滑石的層間體積和層間距呈增大趨勢,從而導致了體系主客體間作用力呈降低趨勢,而水滑石的層柱結構具有一定的飽和性,無法無限膨脹.此外,文獻25報道的體相水(bulk water)的勢能約為-41.84 kJ·mol-1,而Cu3Fe-LDHs-2H2O的水合能為-75.53 kJ·mol-1,低于體相水勢能.從Cu3Fe-LDHs的逐級水合能逐漸降低的趨勢來看,Cu3Fe-LDHs的水合程度是不會無限增加的,而是具有一定的飽和程度,與先前Mulliken電荷布居分析結果相一致.
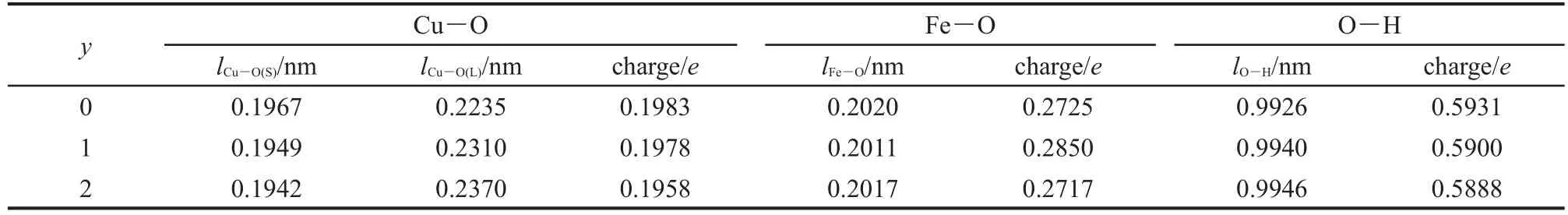
表4 Cu3Fe-LDHs-yH2O(y=0-2)體系中的Cu―O鍵長及成鍵布居Table 4 Cu―O bond length and bond population of Cu3Fe-LDHs-yH2O(y=0-2)

表5 Cu3Fe-LDHs-yH2O(y=0-2)體系中的金屬畸變角Table 5 Distortion angle in Cu3Fe-LDHs-yH2O(y=0-2)
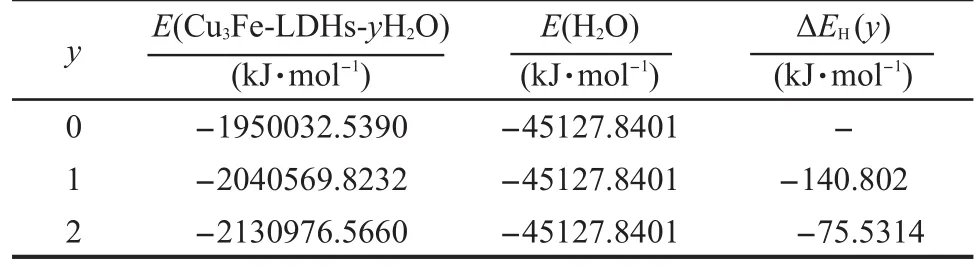
表6 Cu3Fe-LDHs-yH2O(y=0-2)的逐級水合能Table 6 Stepwise hydration energy ofCu3Fe-LDHs-yH2O(y=0-2)
4 結論
采用贗勢平面波法計算了Cu3Fe-LDHs-yH2O (y=0-2)的結構性質,研究了層間水分子含量對體系主客體作用力以及姜-泰勒效應的影響,結論如下:
(1)隨著水分子數目的增加,層間距先略微降低后顯著升高.當y=0,1時,NO3-和H2O與層板保持平行,并且二者均處于上下層板的中間位置.當y=2時,NO3-和H2O以偏向某一層板的方式隨機地位于水滑石層間.Cu3Fe-LDHs-yH2O(y=0-2)體系主客體間除了靜電作用外,還以多重氫鍵的形式維持著體系的穩定性,其水合過程引起了靜電作用及氫鍵的變化,且氫鍵作用更占優勢.對于不同水分子數目的體系,其氫鍵強度分布為:L-A型>A-W型>L-W型>W-W型.
(2)Cu3Fe-LDHs-yH2O(y=0-2)體系中的銅原子的六個Cu―O鍵均出現了四短鍵二長鍵的分化,為拉長的穩定的八面體形式.隨著層間水分子的增加,短鍵進一步縮短,長鍵進一步增長,八面體構型被逐漸拉長,畸變程度逐漸變大,說明水分子的加入會加劇層板Cu2+的姜-泰勒效應.
(3)隨著層間水分子的增加,Cu3Fe-LDHs-yH2O (y=0-2)體系的逐級水合能逐漸降低,低于體相水勢能,說明Cu3Fe-LDHs的水合程度不會無限增加,具有一個飽和量.
(4)對于Cu3Fe-LDHs-yH2O(y=0-2)體系,當y=1時,其構型接近六方晶胞,層板金屬畸變程度最小,穩定性最高,層間距與實驗值較吻合,據此推測Cu3Fe-LDHs-1H2O是實驗上合成的Cu3Fe-LDHs中較穩定的構型.
(1) Cavani,F.;Trifiro,F.;Vaccari,A.Catal.Today 1991,11,173. doi:10.1016/0920-5861(91)80068-K
(2) Duan,X.;Zhang,F.Z.Intercalation and Assembly Chemistry of Inorganic Supramolecular Materials;Science Press:Beijing, 2009.[段 雪,張法智.無機超分子材料的插層組裝化學.北京:科學出版社,2009.]
(3)Liao,J.Y.;Xie,X.M.;Cheng,S.Y.;Wu,X.;An,X. Petrochemical Technology 2009,38,1101.[廖家友,謝鮮梅,程淑艷,吳 旭,安 霞.石油化工,2009,38,1101.]
(4)Xie,X.M.;An,X.;Yan,K.;Wu,X.;Song,J.L.;Wang,Z.Z. J.Nat.Gas Chem.2010,19,77.doi:10.1016/S1003-9953(09) 60038-4
(5) Xie,X.M.;Yan,K.;Hu,Q.X.;Song,J.L.;Wang,Z.Z.Chin.J. Inorg.Chem.2008,24,32.[謝鮮梅,嚴 凱,胡秋霞,宋健玲,王志忠.無機化學學報,2008,24,32.]
(6) Liu,H.B.;Jiao,Q.Z.;Zhao,Y.;Li,H.S.;Sun,C.B.;Li,X.F.; Wu,H.Y.Mater.Lett.2010,64,1698.doi:10.1016/j.matlet. 2010.04.061
(7)Vinod,H.J.;Deepa,K.D.;Vilas,B.P.;Hanumant,B.B.; Radhika,D.W.Catal Commun.2007,8,65.doi:10.1016/ j.catcom.2006.05.030
(8) Xie,X.M.;Liu,J.X.;Song,J.L.;Wang,Z.Z.Chin.J.Catal. 2003,24,569.[謝鮮梅,劉潔翔,宋健玲,王志忠.無機化學學報,2003,24,569.]
(9)Heermann,D.W.Computer Simulation Methods in Theoretical Physics;Springer-Verlag Press:Heidelberg,1990;pp 387-439.
(10) Leach,A.R.Molecular Modelling:Principles and Applications; Addison Wesley Longman Limitted Press:Essex,2001;pp 26-454.
(11) Deyse,G.C.;Alexandre,B.R.;Wladmir,F.S.;Sandra,S.X. C.;Alexandre,A.L.J.Phys.Chem.B 2011,115,3531.doi: 10.1021/jp110668s
(12)Vinuthaa,M.;Howard,D.S.;Zhang,H.;Sean,C.S.J.Phys. Chem.A 2011,115,13673.doi:10.1021/jp2079499
(13)Xu,Q.;Ni,Z.M.;Pan,G.X.;Chen,L.T.;Liu,T.Acta Phys.-Chim.Sin.2008,24,601.[胥 倩,倪哲明,潘國祥,陳麗濤,劉 婷.物理化學學報,2008,24,601.]doi:10.1016/ S1872-1508(08)60026-1
(14)Yao,P.;Ni,Z.M.;Xu,Q.;Mao,J.H.;Liu,X.M.;Wang,Q.Q. Acta Phys.-Chim.Sin.2010,26,175.[姚 萍,倪哲明,胥倩,毛江洪,劉曉明,王巧巧.物理化學學報,2010,26,175.]
(15) Xu,Q.;Ni,Z.M.;Mao,J.H.J.Mol.Struct-Theochem 2009, 915,122.doi:10.1016/j.theochem.2009.08.033
(16) Segall,M.D.;Linda,P.;Probert,M.;Pickard,C.;Hasnip,P.; Clark,S.;Payne,M.J.Phys.-Condes.Matter 2002,14,2717. doi:10.1088/0953-8984/14/11/301
(17) Ceperley,D.M.;Aider,B.J.Phys.Rev.Lett.1980,45,566.doi: 10.1103/PhysRevLett.45.566
(18) Vanderbilt,D.Phys.Rev.B 1990,41,7892.doi:10.1103/ PhysRevB.41.7892
(19) Kresse,G.;Furthmiiller,J.Phys.Rev.B 1996,54,11169.doi: 10.1103/PhysRevB.54.11169
(20) Scheiner,S.Hydrogen Bonding;Oxford University Press:New York,1997.
(21) Jeffrey,G.A.An Introduction to Hydrogen Bond;Oxford University Press:New York,1997.
(22) Desiraju,G.;Steiner,T.The Weak Hydrogen Bond;Oxford University Press:New York,1999.
(23) Mulliken,R.S.J.Chem.Phys.1955,23,1833.doi:10.1063/ 1.1740588
(24) Pan,D.K.;Zhao,C.D.;Zheng,Z.X.The Structure of Matter; Higher Education Press:Beijing,1989;pp 329-330. [潘道皚,趙成大,鄭載興.物質結構.北京:高等教育出版社,1989: 329-330.]
(25) Kumar,P.P.;Kalinichev,A.G.;Kirkpatrick,R.J.J.Phys. Chem.C 2007,111,13517.doi:10.1021/jp0732054
January 20,2012;Revised:May 21,2012;Published on Web:May 21,2012.
Influence of Interlayer Water Content on Supermolecular Interaction of Copper-Iron Layered Double Hydroxides
SHI Wei HU Jun NI Zhe-Ming*LI Yuan LIU Jiao
(Laboratory of Advanced Catalytic Materials,College of Chemical Engineering and Materials Science, Zhejiang University of Technology,Hangzhou 310032,P.R.China)
A periodic interaction model was proposed for the copper-iron layered double hydroxides, Cu3Fe-LDHs-yH2O(y=0-2).Based on density functional theory,the geometry of Cu3Fe-LDHs-yH2O was optimized using the CASTEP program.The distribution of NO-3and H2O in the interlayer and the supermolecular interaction between host and guest was investigated by analyzing the geometric parameters,hydrogen-bonding,charge populations and stepwise hydration energy.Results indicated that when NO-3and H2O were inserted into the layers of the Cu3Fe-LDHs,there was a strong supramolecular interaction between the host layer and the guest,including hydrogen-bonding and electrostatic interaction. Hydrogen-bonding was superior to the electrostatic interaction in the hydration process.The strength of hydrogen bonding was ordered as Layer-Anion(L-A)>Anion-Water(A-W)>Layer-Water(L-W)>Water–Water(W-W).In Cu3Fe-LDHs-yH2O,the interlayer distance decreased slightly and then increased significantly with an increase in the number of interlayer water molecules.The Cu―O octahedral forms were stretched gradually because of the increased Jahn–Teller effect of Cu2+.The absolute value of the hydration energy decreased gradually with an increase in the number of water molecules.This suggested that the hydration of Cu3Fe-LDHs reached a saturation state.The geometry of Cu3Fe-LDHs-1H2O is close to hexagonal where the metal distortion of the layer is weakest and the stability is strongest;the interlayer distance agrees the experimental value,therefore Cu3Fe-LDHs-1H2O is a stable configuration.
Density functional theory;Copper-iron layered double hydroxides;Supramolecular interaction;Jahn-Teller effect;Stepwise hydration energy
10.3866/PKU.WHXB201205212
O641
?Corresponding author.Email:jchx@zjut.edu.cn;Tel:+86-13858123256