聚合鋁對鈾(Ⅵ)的吸附
杜興勝,張麟熹,梁 波,謝冬香,時燕華,劉 念
江西省核工業地質局 測試研究中心,江西 南昌 330002
核電的大力發展有利于國民經濟建設,核廢物的安全處置將直接影響核電發展[1-5]。在核能利用循環前端鈾礦開采和冶煉過程中,會產生大量的廢石和尾礦,它們的平均含鈾量是天然土壤的5~10倍,輻射劑量是一般土壤的6~70倍[2,6]。如果這些放射性廢物沒有進行適當的處理,在風吹、沖刷等外界作用下游離于自然界,無疑會對周圍環境造成污染;如在雨季,雨水浸入尾礦后最終滲入地下水,整個地下水系都將受到輻射和重金屬的污染,將對地下水系周邊的居民生活、生物生長造成巨大的影響[6-8]。
諸多放射性廢物中,放射性廢液危害最大、處理最難、花費高,它的安全處理受到國際普遍關注。放射廢液罐貯長途運輸存在嚴重的安全隱患,因此放射性廢液減容固化意義重大[9-13]。化學沉淀法是放射性廢水處理的重要方法之一,其原理為:采用絮凝劑通過沉淀法去除廢水中的放射性核素,以達到較高的去除率。絮凝劑主要是應用在城市、工業給水凈化方面,它不僅可去除廢水中細微懸浮顆粒物,而且可有效去除水中的各種油分、色度、化學需氧量(COD),去除率可達70%~90%以上。對水中微生物、細菌、藻類去除率達90%,對含有Pb2+和Cr3+等重金屬污水凈化率達90%,放射性物質去除率達80%[14]。絮凝法處理放射性廢水工藝簡單,成本較低,對大多數放射性核素具有良好的去除效果,其中無機絮凝劑以鋁鹽和鐵鹽兩種系列為主[12]。聚合鋁有多種形態,有二聚鋁、五聚鋁、九聚鋁、十三聚鋁、三十聚鋁[15-20]等。基于絮凝劑對重金屬和放射性元素的優異的吸附性能,本工作擬研究聚合鋁對鈾的吸附情況,由于吸附體系呈固體狀易于過濾達到有效減容目的,后期處理也較為方便,且原料簡單易得,開展該項研究將為實現鈾的減容和分離富集開啟新的研究思路,并為尋找應用性強的絮凝劑拓展新的視野。
1 實驗方法
本實驗所用的鈾標準溶液是用黃餅(撫州金安鈾業有限公司,分析純)經高溫煅燒成八氧化三鈾,然后稱取一定量八氧化三鈾溶于硝酸介質制備的。其它的化學試劑都是市售分析純。721型可見分光光度計,日本島津儀器公司。
溶液配制:配制好0.25mol/L的氫氧化鈉溶液、0.25mol/L的AlCl3溶 液、0.10mol/L的Na2SO4溶液、鈾 標準溶液(1g/L,100mg/L)、0.05%偶氮胂Ⅲ、1∶1(體積比,下同)鹽酸備用。
1.1 偶氮胂Ⅲ法測定鹽酸體系中鈾
董靈英[21]的研究表明,偶氮胂Ⅲ體系以乙酸鈉-氯乙酸作為緩沖溶液測鈾時,Al3+對鈾的測定會產生正誤差干擾,但是在4~8mol/L的鹽酸介質中,用偶氮胂Ⅲ測定鈾可以消除Al3+的干擾,靈敏度達到104L/(mol·cm),所以采用在1∶1的鹽酸介質中進行鈾的測定,以消除鋁的干擾。方法如下:分別準確移取不同體積的100mg/L鈾標準溶液或待測過濾液于25mL容量瓶中,加入0.05%的偶氮胂Ⅲ2mL,加入12.5mL濃鹽酸(12mol/L),最后用蒸餾水定容,搖勻,靜置20min,用不加鈾的鹽酸加偶氮胂Ⅲ體系做空白,在1cm比色皿中于655nm處用可見分光光度計測定其吸光度。
1.2 聚合鋁對鈾的吸附
1.2.1 不同羥鋁比對鈾的吸附 聚合鋁硫酸鹽的制備[12],移取25mL 0.25mol/L的AlCl3溶液于250mL燒杯中,用恒溫水浴加熱溶液至80℃,在不斷攪拌下,慢慢滴加一定體積(調節羥鋁比)0.25mol/L的NaOH溶液,保持燒杯在80℃水浴體系中,加入1mL鈾標準溶液,再加入62.5mL 0.10mol/L的Na2SO4溶液,攪拌,靜置一定時間(考察時間對鈾吸附的影響),將溶液進行過濾,移取上清液,用光度法測定溶液中鈾的濃度。
1.2.2 不同鋁濃度對鈾的吸附 分別移取25mL 0.800、0.500、0.250、0.120、0.060、0.030、0.015、0mol/L的AlCl3溶液于8個250mL燒杯中,用恒溫水浴加熱溶液至80℃,在不斷攪拌下,慢慢滴加50mL不同濃度的NaOH溶液,使聚合鋁的羥鋁比為2,保持燒杯在80℃水浴體系中,加入1mL鈾標準溶液,再加入62.5mL的0.320、0.200、0.100、0.050、0.025、0.012、0.006、0mol/L Na2SO4溶液,攪拌后靜置一定時間(時間對鈾吸附的影響),將溶液過濾后取濾液,用光度法測定溶液中鈾的濃度。
1.2.3 不同放置時間對鈾的吸附 平行配制8份如下溶液:移取25mL 0.030mol/L的AlCl3溶液于250mL燒杯中,用恒溫水浴加熱溶液至80℃,在不斷攪拌下,慢慢滴加一定體積(調節羥鋁比)0.25mol/L的NaOH溶液,保持燒杯在80℃水浴體系中,加入1mL鈾標準溶液,再加入62.5mL 0.012mol/L的Na2SO4溶液,攪拌,分別靜置2、4、5、6、7、8、9、12d,將溶液進行過濾,移取上清液,用光度法測定溶液中鈾的濃度。
1.2.4 不同鈾濃度對鈾的吸附 分別移取25mL 0.030mol/L的AlCl3溶液于8個250mL燒杯中,用恒溫水浴加熱溶液至80℃,在不斷攪拌下,慢慢滴加12.5mL 0.12mol/L的NaOH溶液,使聚合鋁的羥鋁比為2,保持燒杯在80℃水浴體系中,分別加入0.5、1、1.5、2、3、4、6、8mL鈾標準溶液,然后加入62.5mL 0.0125mol/L Na2SO4溶液,再加入一定量的蒸餾水使溶液總體積為138.5mL,攪拌后靜置9d,將溶液進行過濾,移取上清液,用光度法測定溶液中鈾的濃度。
2 結果與討論
2.1 鹽酸體系中偶氮胂Ⅲ法測定鈾的條件選擇
2.1.1 最大吸收波長的確定 加1mL 10mg/L鈾標準溶液、2mL 0.05%偶氮胂Ⅲ和12.5mL濃鹽酸,定容于25mL容量瓶中,然后進行顯色來確定最大吸收波長,結果示于圖1。由圖1可知:在鹽酸體系中絡合物的最大吸收波長為655nm,而試劑的最大吸收波長為540nm,此條件(大于50nm)滿足分光光度法的測定要求。
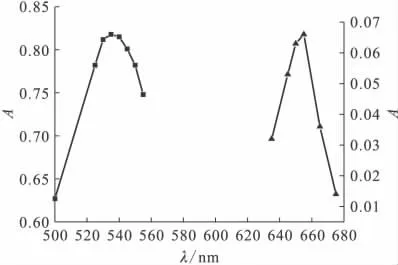
圖1 偶氮胂Ⅲ及其鈾(Ⅵ)絡合物的吸收峰Fig.1 Absorption peaks of ArsenazoⅢand its uranium(Ⅵ)complex
2.1.2 顯色體系的穩定性 鋁對鈾絡合物吸光度隨時間的影響列入表1。由表1可知:在加鋁溶液中絡合物顯色在15~20min比較穩定,所以在含有鋁的溶液中顯色時間選擇15~20min較好。
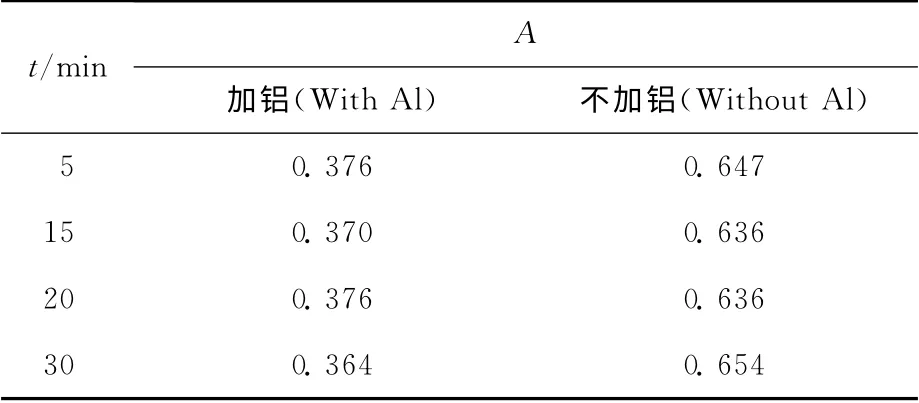
表1 鋁對鈾絡合物吸光度隨時間的影響Table 1 Effect of developing time on the absorbance of ArsenazoⅢ-uranium complex in the presence and absence of aluminum
2.1.3 鋁濃度對絡合物吸光度的影響 在鈾質量濃度為20.14mg/L溶液中加入不同量的三氯化鋁來研究鋁濃度對絡合物吸光度的影響,結果列入表2。由表2可知:當鋁濃度小于0.03mol/L時U的相對測量誤差均小于5%,而待測溶液中鋁的最大濃度為0.018mol/L,所以在鋁濃度小于0.018mol/L范圍內,該方法可用,并且相對誤差小于5%。
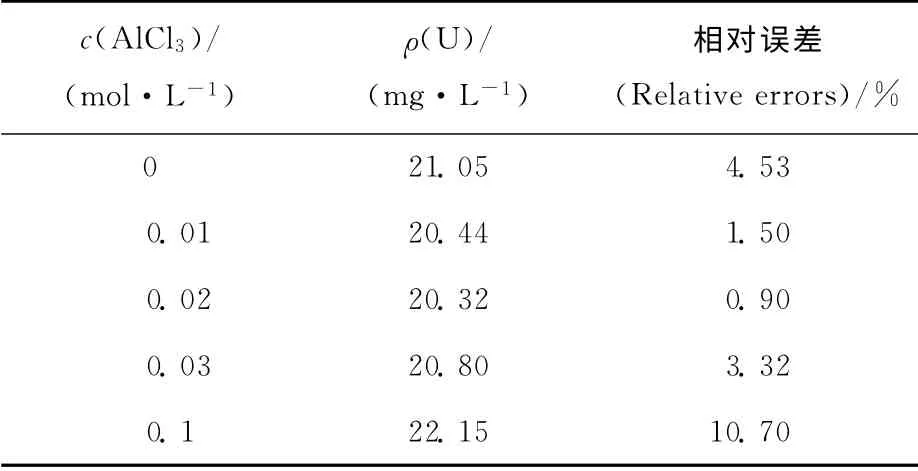
表2 不同鋁濃度時方法的測量相對誤差Table 2 Relative errors of the present method under different aluminum concentrations
2.2 不同羥鋁比對鈾吸附的影響
根據羅明標等[12]的研究,不同羥鋁比對聚合鋁的硫酸鹽晶形有重要影響。本實驗首先對不同羥鋁比對鈾的吸附進行研究。加入不同量NaOH,使羥鋁比R=n(OH-)/n(Al3+)分別為0、0.5、1.0、1.5、2.0、2.5,不同羥鋁比對鈾的吸附量關系示于圖2,圖中吸附率Y=(m/m0)×100%,m為吸附鈾的質量,μg;m0為加入鈾的總質量,μg。從圖2可以看出:聚合鋁對鈾吸附5d和吸附2d后過濾,吸附率隨著羥鋁比增加先增加后減少,并且都在羥鋁比R=2時達最大值,因此以下實驗以R=2進行。由此可知,不同羥鋁比對鈾吸附有重要影響。由于羥鋁比大于3時,溶液呈堿性,會有氫氧化鋁沉淀析出,鈾發生水解和被氫氧化鋁沉淀下來從而不能正確反映聚合鋁對鈾的吸附性能,所以沒進行R≥3的實驗。從圖2還可得出,吸附5d后過濾吸附率大于吸附2d的吸附率,這可得出,時間對聚合鋁吸附鈾具有一定的影響。根據聚合鋁生長特性,該吸附有可能是由于聚合鋁在形成結晶時,鈾酰離子取代一部分鋁參與到結晶過程中去,被包夾到聚合鋁的晶核內達到去除溶液中鈾的效果,隨著晶體成長成熟的聚合鋁表面會形成一層負電層繼續牢固吸附帶正電荷的鈾酰離子使其共沉淀下來。
2.3 不同鋁濃度對鈾吸附的影響

圖2 不同羥鋁比對鈾吸附的影響Fig.2 Adsorption of uranium with different ratio of OH-and aluminium
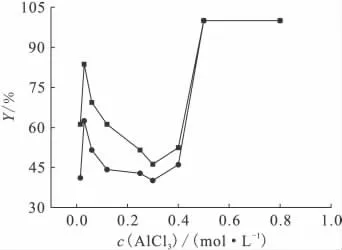
圖3 不同鋁濃度對鈾的吸附Fig.3 Adsorption of uranium with different concentration of aluminum
不同鋁濃度對鈾的吸附影響示于圖3。從圖3可看出:2d的吸附趨勢和5d的吸附趨勢相同,隨著鋁濃度增加,聚合鋁對鈾的吸附能力呈現先增加后減小、然后再增加的趨勢。這有可能是:首先,鋁濃度增加,聚合鋁的溶液中形成聚合鋁的初始速度也增加;另一方面,形成聚合鋁的總量也增加,從而導致隨鋁濃度的增加首先對鈾的吸附增加,但是當鋁濃度達到一定時,溶液接近飽和,過多的硫酸根離子起到抗衡作用,導致鈾酰離子不能和聚合鋁結合,接著鋁的濃度(大于0.5mol/L)繼續增加,溶液中開始有氫氧化鋁析出,溶液呈堿性,因此鈾會水解沉淀下來或者被氫氧化鋁吸附下來,從而使鈾的吸附率為100%,但是這種水解沉淀顆粒度小,通過過濾無法分離,因此用大于0.5mol/L的AlCl3制備聚合鋁不能實現吸附分離鈾。而且從圖上還可得出放置的時間越長聚合鋁對鈾的吸附也增加。因此,用c(AlCl3)=0.030mol/L合成聚合鋁時(實際體系中鋁的濃度為5.64×10-3mol/L),可實現聚合鋁吸附鈾性能最佳。
2.4 不同放置時間對鈾吸附的影響
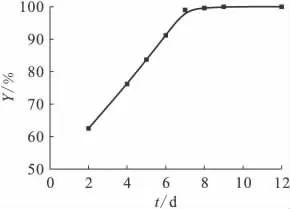
圖4 放置時間對鈾吸附的影響Fig.4 Effect of standing time on the adsorption of uranium
放置時間對鈾吸附的影響結果示于圖4。由圖4可知:在鈾總量為1mg時,聚合鋁對鈾的吸附在8d后就達到99%,溶液中幾乎所有鈾都被吸附到聚合鋁上。確定放置9d為最佳條件,這樣既能保證吸附足夠的鈾,又能減少時間。
2.5 不同鈾濃度對鈾吸附的影響
根據前面的研究數據,放置5d不能實現完全吸附鈾,因此在研究鈾濃度對聚合鋁的吸附鈾影響時采用吸附9d,結果示于圖5。由圖5可知:隨鈾加入量的不斷增加,開始聚合鋁還能很好的吸附鈾,但當鈾的加入量約為3mL(質量濃度約為29mg/L)時,聚合鋁對鈾的吸附能力下降。這是由于鈾濃度太高在該加入量時高聚合鋁吸附體系達到了飽和,使其吸附率下降,所以鈾濃度對聚合鋁吸附鈾具有重要影響。當鈾加入量約為0~3mL(ρ(U)<20mg/L)時,鈾的吸附率在96%~100%,證明聚合鋁具有很好的吸鈾效果;當鈾濃度增加時,吸附率在75%左右,這是因為鈾酰離子帶正電荷取代部分的鋁,當鈾酰離子濃度增加,包裹到晶體的表面上形成抗衡電荷使得晶體的顆粒度變小,顆粒數增加,表面積升高,所以在鈾濃度升高時會出現一個吸附平臺,吸附率維持在75%。
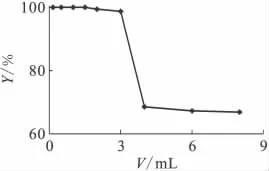
圖5 鈾不同加入量對吸附的影響Fig.5 Effect of different concentration of uranium on the adsorption of uranium t=9d
2.6 聚合鋁吸附鈾狀態研究
使用乙醇和蒸餾水分別對吸附鈾的聚合鋁進行淋洗,移取上清液,經測定其吸光度接近于零,即被吸附的鈾不能被乙醇和蒸餾水洗脫,鈾有可能被包裹在里面或者參與了結晶。再用1∶1鹽酸溶解,移取溶液進行測定,測定表明有鈾的存在,但由于洗脫鈾液過濾時濾紙對鈾的部分粘帶吸附,損失了一部分鈾,所以其回收率只有67.41%;當未沖洗直接測定時,鈾的回收率可達90%以上。
3 結 論
(1)在1∶1的鹽酸體系中用偶氮胂Ⅲ測定鈾,當鋁的濃度小于0.03mol/L時,該法可不受鋁影響(相對誤差小于5%),并且最大吸收波長為655nm。
(2)聚合鋁能作為一種良好的吸附和富集鈾材料,在一定鈾濃度范圍內其吸附率可達90%以上,并且用1∶1的鹽酸可將聚合鋁溶解,從而實現鈾的富集。
(3)鈾被吸附在聚合鋁上比較牢固,不易被洗脫下來,證明鈾有可能進入晶格內。
[1]梁惠碧.鈾元素在地殼中的富存狀態及應用[J].梧州學院學報,2009,19(3):34-39.
[2]陳偉,張軍,李桂菊.核電技術現狀與研究發展[J].世界科技研究與發展,2007,29(5):81-86.
[3]閆強,王安建,王高商.核電發展戰略研究[J].中國科技論壇,2009(9):18-22.
[4]胡興軍,周浩,屈平.我國核電發展進入新時代[J].上海電力,2008,21(5):470-474.
[5]李合蓮,鄧家軍.鈾尾礦對地下水環境影響研究[J].環境污染治理技術與設備,2000(3):198-203.
[6]商照榮.貧化鈾的環境污染影響及其對人體健康的危害[J].輻射防護,2005,25(1):56-61.
[7]常陽,張麟熹,羅明標.鈦納米管的制備與表征及吸附鈾研究[J].材料研究學報,2010,24(4):424-428.
[8]張麟熹,孫玉珍,羅明標,等.磷酸三丁酯修飾Ti納米晶須應用于吸附鈾酰離子[J].復合材料學報,2011,28(3):96-102.
[9]王翠蘋,孫紅文,徐樣昌.生物對鈾的吸附研究[J].環境科學與技術,2008,31(3):23-25.
[10]曹小紅,劉云海,朱政.殼聚糖及其衍生物對鈾的吸附研究[J].化學研究與應用,2006,18(7):878-880.
[11]劉淑娟,李金英,羅明標,等.純化及羧化多壁碳納米管吸附鈾的研究[J].核化學與放射化學,2011,33(5):285-290.
[12]羅明標,王趁義,劉淑娟.聚合Al13的制備及表征[J].無機化學學報,2004,20(1):69-73.
[13]薛彥輝,薛大兵,張琳.聚合硫酸鋁制備條件的研究及應用[J].能源環境保護,2008,22(2):24-25.
[14]郭榮杰.新型絮凝劑聚合鋁鹽的研制[J].質量天地,2002(2):61-61.
[15]Takayoshi S,Fathi K,Masaki L,et al.A Mixed Alkali Titanate With the Lepidocrocite-Like Layered Structure:Preparation,Crystal Structure,Protonic Form,and Acid-Base Intercalation Properties[J].J Mater Chem,1998(10):4 123-4 128.
[16]王瑞芬,孫忠,張胤.Al(Ⅲ)鹽水解聚合過程中Al5和Al9的制備及初步表征[J].應用化學,2009,26(7):878-880.
[17]陳進陽,欒兆坤,范彬.水解聚合鋁陽離子Al13和Al30的27Al核磁共振定量研究[J].分析化學,2006,34(1):38-42.
[18]Chen Z,Liu C,Luan Z,et al.Effect of Total Aluminum Concentration on the Formation and Transformation of Nanosized Al13and Al30in Hydrolytic Polymeric Aluminum Aqueous Solutions[J].Chinese Science Bulletin,2005,50(18):2 010-2 015.
[19]Rowsell J,Nazar L F.Speciation and Thermal Transformation in Alumina Sols:Structures of the Polyhydroxyoxoaluminum Cluster[Al30O8(OH)55(H2O)26]18+and Itsδ-Keggin Moiete[J].J Am Chem Soci,2000,122(15):3 777-3 778.
[20]Allouche L,Gerardin C,Loiseau T,et al.Al30:a Giant Aluminum Polycation[J].Angewandte Chemie International Edition,2000,39:511-514.
[21]董靈英.鈾的分析化學[M].北京:原子能出版社,1982:155-156.

