利用傳感技術(shù)探究次氯酸光照分解的實(shí)驗(yàn)
朱衛(wèi)華
利用傳感技術(shù)探究次氯酸光照分解的實(shí)驗(yàn)
朱衛(wèi)華
(無錫市第一中學(xué)江蘇無錫214031)
采用傳感技術(shù),通過pH傳感器和導(dǎo)電率傳感器實(shí)時(shí)監(jiān)測次氯酸光照分解過程中溶液的pH和導(dǎo)電率,借助計(jì)算機(jī)直接繪制出相應(yīng)的變化曲線,同時(shí)結(jié)合理論計(jì)算,對次氯酸光照分解實(shí)驗(yàn)進(jìn)行了初步研究。
傳感技術(shù);氯水;次氯酸;光照分解
一、問題的提出
氯水中的次氯酸不穩(wěn)定,容易分解放出氧氣,在陽光的照射下,次氯酸分解加快。傳統(tǒng)做這個(gè)實(shí)驗(yàn),可以在圓底燒瓶中裝滿氯水,將燒瓶倒放在裝有水的水槽中,用光線照射,在燒瓶中收集到氧氣。該實(shí)驗(yàn)出現(xiàn)明顯的現(xiàn)象所需的時(shí)間較長,一般要十天左右,所以教材中一般沒有這個(gè)實(shí)驗(yàn)。全日制普通高級(jí)中學(xué)教科書(必修)《化學(xué)》第一冊中只是在正文旁邊放了一張?jiān)搶?shí)驗(yàn)的裝置示意圖(圖1),而如今的普通高中課程標(biāo)準(zhǔn)實(shí)驗(yàn)教科書,不管是蘇教版、人教版還是魯科版,連這張圖都沒有,直接是作為一個(gè)信息告訴學(xué)生讓學(xué)生記憶,很難讓學(xué)生直觀地感受次氯酸光照分解的過程。

圖1 氯水受光照的實(shí)驗(yàn)
在多年的教學(xué)過程中,筆者也感覺到要想做好這一實(shí)驗(yàn)有時(shí)間長、現(xiàn)象不明顯、合適的光源難找等較多的難點(diǎn)。而傳感技術(shù)能夠?qū)崟r(shí)直接監(jiān)測實(shí)驗(yàn)過程中曲線的變化,不同的傳感器能夠檢測傳統(tǒng)實(shí)驗(yàn)手段無法檢測的物理量,有力地彌補(bǔ)了傳統(tǒng)實(shí)驗(yàn)手段的不足。由于氯水中的次氯酸光照分解生成鹽酸,溶液的pH會(huì)降低、導(dǎo)電率會(huì)增強(qiáng),所以我們嘗試?yán)胮H傳感器和導(dǎo)電率傳感器實(shí)時(shí)監(jiān)測光照條件下氯水的pH和導(dǎo)電率的變化,通過相應(yīng)的曲線引起學(xué)生的思考,進(jìn)而探索出分解的產(chǎn)物。
二、實(shí)驗(yàn)過程
所需用到的儀器與用品有:pH傳感器(pHBTA)、導(dǎo)電率傳感器(C0N-BTA)、數(shù)據(jù)采集器(VENIERLabPro)、計(jì)算機(jī)及其相配套的軟件(Logger Pro)、大功率冷光源臺(tái)燈、燒杯、氯水。
1.實(shí)驗(yàn)步驟
(1)組裝實(shí)驗(yàn)裝置,將pH傳感器、數(shù)據(jù)采集器、計(jì)算機(jī)三者相連接。
(2)在燒杯中加入少量氯水,插入pH傳感器,打開臺(tái)燈光照氯水,對氯水的pH變化進(jìn)行測定。
(3)組裝實(shí)驗(yàn)裝置,將導(dǎo)電率傳感器、數(shù)據(jù)采集器、計(jì)算機(jī)三者相連接。
(4)在燒杯中加入少量氯水,插入導(dǎo)電率傳感器,打開臺(tái)燈光照氯水,對氯水的導(dǎo)電率變化進(jìn)行測定。
2.實(shí)驗(yàn)現(xiàn)象記錄

表1 實(shí)驗(yàn)現(xiàn)象記錄
3.實(shí)驗(yàn)數(shù)據(jù)記錄

圖2 反應(yīng)過程中的pH變化示意圖

圖3 反應(yīng)過程中導(dǎo)電率變化示意圖
4.實(shí)驗(yàn)現(xiàn)象的分析和理論計(jì)算
圖2和圖3中顯示,氯水光照的過程中,pH不斷降低,導(dǎo)電率不斷增強(qiáng),這說明次氯酸見光分解產(chǎn)生了強(qiáng)酸,學(xué)生會(huì)聯(lián)想到光照分解的產(chǎn)物——鹽酸以及氧氣。實(shí)驗(yàn)起始時(shí)pH和導(dǎo)電率變化很快,后來較慢,與次氯酸的濃度變化有關(guān)。隨著次氯酸的分解,次氯酸的濃度不斷降低,分解速率就不斷減慢。
氯氣溶于水,1L水溶解2L氯氣達(dá)到飽和,粗略計(jì)算氯水的物質(zhì)的量濃度是0.0921mol/L。但是氯氣溶于水會(huì)跟水發(fā)生反應(yīng),并很快達(dá)到平衡:
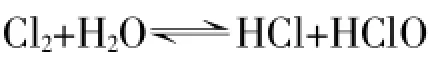
此反應(yīng)的平衡常數(shù)為K=4.2×10-4,由此計(jì)算各物質(zhì)的平衡濃度:
c(Cl2)=0.062mol/L
c(HCl0)=0.030mol/L
c(HCl)=0.030mol/L
考慮到HCl0的電離平衡常數(shù)較小(查閱文獻(xiàn)4為3.0×10-8),所以HCl0電離出的H+可以忽略,由此可以求出飽和氯水的pH為1.52。但是,氯氣溶于水需要較長的時(shí)間才能達(dá)到飽和,而且濃度越大的氯水,氯氣的擴(kuò)散越慢,氯氣的溶解能力越差。因此通常所用的氯水實(shí)際上是不飽和的,各成分的實(shí)際濃度比上面的理論值要低。比如:圖2顯示,實(shí)驗(yàn)前氯水的pH約為1.72左右。
通過采集的數(shù)據(jù),可以估算出次氯酸的分解率。實(shí)驗(yàn)開始時(shí)氯水的pH為1.72,c(H+)=0.01905mol/L,忽略HCl0的電離,c(HCl)=0.01905mol/L,則此時(shí)的c(HCl0)=0.01905mol/L;實(shí)驗(yàn)開始后,pH減小,c(H+)增大,新增的H+就是HCl0分解產(chǎn)生的。由此可以計(jì)算出次氯酸的分解率(見表2)。可以清楚地發(fā)現(xiàn),光照少量的氯水,80分鐘后次氯酸幾乎全分解,40分鐘就能分解了一大半,在圖像上已經(jīng)能清楚地看到pH的變化,可用于課堂演示使用。至于導(dǎo)電率的變化,10分鐘左右就能看到明顯的變化,更有力地說明了次氯酸的分解。

表2 次氯酸的分解率
三、實(shí)驗(yàn)后的反思
新制的飽和氯水不適合做氯水的光分解實(shí)驗(yàn),因?yàn)樾轮频穆人校葰夂退姆磻?yīng)并不充分,次氯酸的數(shù)量小、濃度低。可以把新制的飽和氯水,在暗處放置1-2周(10天左右)之后,再把它用來做氯水的光分解實(shí)驗(yàn),效果就要好一點(diǎn)。
本實(shí)驗(yàn)主要探究次氯酸光分解的產(chǎn)物,采用pH傳感器和導(dǎo)電率傳感器跟蹤其隨時(shí)間的變化,可以克服傳統(tǒng)實(shí)驗(yàn)所需時(shí)間太長、現(xiàn)象不明顯的缺陷。其他實(shí)驗(yàn)如果也存在類似的難點(diǎn),也可以考慮采用傳感技術(shù),檢測出傳統(tǒng)實(shí)驗(yàn)無法檢測的物理量,從而達(dá)到實(shí)驗(yàn)?zāi)康摹?/p>
盡管本實(shí)驗(yàn)取得了不錯(cuò)的效果,但仍存在實(shí)驗(yàn)過程中敞開體系可能有污染、尋找恰當(dāng)?shù)墓庠词箤?shí)驗(yàn)效果更明顯等問題,將在以后的研究中繼續(xù)不斷的探索。
[1]人教社化學(xué)室.全日制普通高級(jí)中學(xué)教科書(必修)化學(xué)(第一冊)[M].北京:人民教育出版社,2003:66
[2]王祖浩.普通高中課程標(biāo)準(zhǔn)實(shí)驗(yàn)教科書化學(xué)1(必修)[M].南京:江蘇教育出版社,2009:43
[3]劉懷樂.中學(xué)化學(xué)教學(xué)思維[M].重慶:重慶出版社,2009:176-179
[4]北京師范大學(xué)無機(jī)化學(xué)教研室等.無機(jī)化學(xué)(上冊)[M].北京:高等教育出版社,2002:409
1008-0546(2013)11-0087-02
G632.41
B
10.3969/j.issn.1008-0546.2013.11.034
- 化學(xué)教與學(xué)的其它文章
- 激活復(fù)習(xí)課堂 提高復(fù)習(xí)效率——以“《復(fù)分解反應(yīng)的條件及簡單應(yīng)用》復(fù)習(xí)”為例
- 普通高中化學(xué)職業(yè)技能類校本選修課程開發(fā)的實(shí)踐——以“金屬冶煉與玉環(huán)冶金工業(yè)”課程實(shí)踐為例
- “問題驅(qū)動(dòng)”教學(xué)模式在高三化學(xué)復(fù)習(xí)中的實(shí)踐研究——以“鋁及其化合物”的復(fù)習(xí)為例
- 淺議初中化學(xué)紙筆測評的階段層次性——以“單質(zhì)與化合物”的測評設(shè)計(jì)為例
- 淺談制約農(nóng)村初中化學(xué)實(shí)驗(yàn)教學(xué)的因素和對策——由初中化學(xué)實(shí)驗(yàn)教學(xué)技能培訓(xùn)考核引發(fā)的思考
- “吹”出來的銀鏡反應(yīng)

