銀納米粒子構筑樹枝狀微納結構用于表面增強拉曼散射的研究
胡成龍,劉繼延,彭湘紅,劉學清,蔡少君
(江漢大學 光電化學材料與器件省部共建教育部重點實驗室,化學與環境工程學院,湖北 武漢 430056)
0 引言
1974年Fleischmann發現吸附在粗糙的銀電極上吡啶分子具有很強的拉曼散射效應,這種效應被稱之為“表面增強拉曼散射”(Surface enhanced Raman scattering,SERS)[1]。由于 SERS 具有檢測靈敏度高、分辨率高及超低濃度檢測限等優點,對拉曼光譜學的應用及其發展具有重要的實際意義。近年來許多研究者致力于研究SERS效應的本質現象及其新的應用研究,涉及到電化學、分析化學、物理學、生物醫學、納米科學和考古學等多個學科領域[2-6],具體應用于單分子檢測、痕量分析、分子間的相互作用、分子的結構和構象、聚合物/金屬納米材料的表面與界面和生物傳感等。如S.Nie等[7]利用單個銀納米粒子研究單分子檢測,發現在銀基體的作用下羅丹明拉曼信號的增強因子高達 1014~1015;Xue G.等[8]研究了聚丙烯腈分子鏈在銀基體上的構象結構,通過SERS研究發現,聚丙烯腈中的N原子能垂直排列在銀基體表面,當將所制備的樣品置于200℃退火時,N原子能通過未共用的電子對結合在一起,環化成有序的芳環結構,在SERS光譜中表現出石墨的結構特性;國內學者田中群等[9]利用一種惰性殼層材料把作為拉曼信號放大器的金屬納米粒子隔絕起來,使金屬粒子與待測物分離,該技術突破了以往使用裸金屬粒子的局限性,使得SERS技術變得更加通用和實用。
盡管SERS技術取得很好的發展,金屬基體制備也日趨成熟,但是也存在一個問題:一般高增強因子的金屬基體的制備過程比較復雜,實驗條件不易操作與調控,在普通實驗室難以合成高質量的金屬納米結構,因此對于通用性金屬基體的制備仍備受關注。迄今為止,作為SERS基體的金屬銀(Ag)的納米結構,如銀納米粒子[10]、銀納米團簇[11]、立方納米 Ag[12]、銀納米線[13]、銀納米棒[14]和圓環狀納米 Ag[15]都取得了較好的發展與應用。近年來,樹枝狀納米結構的Ag引起了研究者的關注,原因在于樹枝狀Ag不僅具有大的比表面積,而且具有不規整生長蔓延的層級結構,這一結構特點導致樹枝狀Ag具有表觀自相似性[16],這就賦予樹枝狀Ag優異的SERS效應,對于單分子的檢測和痕量檢測具有重要的應用價值。對于樹枝狀納米Ag的制備,一般用采用:(1)腐蝕法,如以Si基體作為襯底,先將金屬Ag還原至Si基體上制備成金屬膜,然后控制反應條件,用HF酸進行刻蝕;(2)化學合成法,利用聚乙烯基吡咯(PVP)或十二烷基磺酸鹽作為穩定劑,在相應的溶劑中合成層級結構不同的樹枝狀Ag;(3)電化學沉積法,利用傳統的三電極在適宜的AgNO3電解質溶液中,調節電解液的性質、輸出電壓及電流,合成具有不同結構特點的樹枝狀Ag。
為了降低實驗過程中的成本及制備工藝條件的復雜性,本實驗采用兩電極法,以AgNO3和檸檬酸的復合水溶液作為電解質,導電玻璃分別作為工作電極和對電極進行Ag的電化學沉積,研究了所制備銀微納結構的形貌結構、生長機制及其SERS效應。
1 實驗部分
1.1 主要原料
AgNO3,分析純,阿拉丁試劑;檸檬酸(分析純),北京華業寰宇化工有限公司;KCl,分析純,國藥集團化學試劑有限公司;Rhodamine 6G(R6G),分析純,阿拉丁試劑;二次蒸餾水,自制。
1.2 主要設備
顯微共焦拉曼光譜儀(Via Laser),英國雷尼紹公司;掃描電子顯微鏡(S-4800),日本日立公司;X射線衍射儀(D-MAX 2200),德國布魯克公司;直流電源,香港龍威電源。
1.3 實驗步驟
采用導電玻璃(ITO)為工作電極和對電極組成的兩電極體系。每次實驗之前,導電玻璃電極先用丙酮和乙醇依次清洗,然后用二次蒸餾水沖洗和超聲波清洗,導電玻璃的工作面積為(0.6±0.04)cm2;電解液為2 mg/mL的AgNO3和5 mg/mL的檸檬酸復合水溶液,工作電壓為3 V,反應溫度25℃,電鍍時間60 min。沉積后的樹枝狀Ag依次用乙腈和乙醇沖洗,然后在1M的KCl溶液中浸泡30 min,二次蒸餾水清洗后,N2吹干。
2 結果與討論
2.1 樹枝狀銀的結構分析
圖1所示是樹枝狀銀的SEM圖,從圖1可知電化學沉積60 min后,銀晶體呈現出完整的樹枝狀結構,形狀美觀的樹干、對稱性的樹枝及樹葉清晰可見。值得注意的是,除了樹枝狀的Ag之外,導電玻璃基體上仍有許多銀納米顆粒,這是樹枝狀Ag在其生長過程中消耗了大量的銀納米粒子或銀納米團簇,隨著還原劑的消耗,一方面銀納米粒子沉積在ITO上,另一方面晶體后期的生長主要是依賴于銀納米顆粒表面能的作用,促使銀晶體進一步生長成樹枝狀結構。為了進一步確定樹枝狀Ag的結構,產物的X射線衍射(XRD)分析如圖2所示。結果與Ag的粉末衍射卡(JCPDS,04-0783)完全吻合,在 θ=38.12°,44.28°,65.43°和81.24°處的4個衍射峰分別對應于面心立方(FCC)Ag的(111)、(200)、(220)和(311)面。此外,產物(111)面的衍射峰明顯比其他峰高。所有的衍射峰都非常尖銳,表明產物具有非常高的結晶度。

圖1 具有樹干、樹枝和樹葉結構的樹枝狀銀的SEM圖
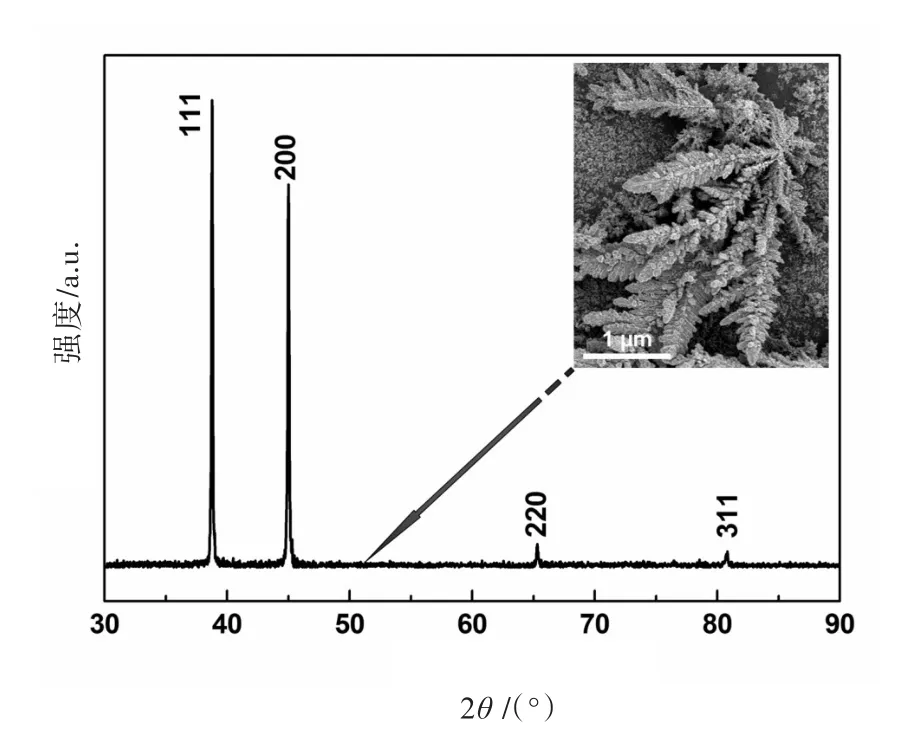
圖2 具有樹干、樹枝和樹葉結構的樹枝狀銀的XRD圖
2.2 樹枝狀銀的生長機制研究
樹枝狀Ag的生長機制如圖3所示,樹枝狀Ag的形成一般解釋為Ag+在電極上的電化學還原過程,氧化還原過程中的電子是通過陽極和陰極進行交換的。起初沉積在導電玻璃的導電層上的銀原子形成納米團簇作為局部陰極,而周圍“漂浮”的銀納米團簇可以看作是陽極,因此眾多的納米原電池能在ITO的表面進行自組裝。高濃度的AgNO3溶液和還原劑致使生長過程的納米銀晶核分布各個位置,形成鏈狀的網絡結構。隨著反應的進一步進行,還原劑的含量下降,晶體銀生長的動力主要來源于逐漸下降的表面能,并最終形成樹枝狀的Ag[17]。其可控的形貌結構與尺寸依賴于精確的實驗條件,如Ag+的濃度、溫度和反應時間等。這種方法制備的樹枝狀Ag不僅具有很好的實驗重復性,而且層級結構也有良好的表觀自相似性。樹枝狀Ag的這一特性,使得其具有重現性良好的SERS活性效應。
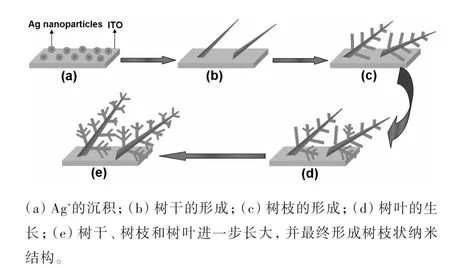
圖3 樹枝狀Ag的生長機理圖
2.3 樹枝狀銀的SERS效應
選擇R6G的水溶液作為探針分子研究了樹枝狀銀的SERS活性。R6G具有一定的熒光性,并能較好地吸附在貴金屬納米粒子上,產生較強的SERS效應且譜圖簡單,因而廣泛用于基底吸附分子的SERS活性研究。把樹枝狀銀微納米結構用N2吹干后作為基底,再把定量的R6G(濃度分別為10-7,10-8和10-10mol/L)水溶液滴在基底上,待水蒸發后測試其SERS性能。R6G分子的SERS光譜見圖4,可以明顯觀察到許多尖銳的R6G拉曼特征峰。其中在610和772 cm-1處的拉曼特征峰分別歸屬于環的面內變形振動和環的面外彎曲振動;1120 cm-1歸屬于C-H的面內彎曲振動;位于 1190,1360,1510,1572和1650 cm-1歸屬于處的 C-C 環伸縮振動[18]。從圖4可知,當R6G的濃度為10-10mol/L時,樹枝狀銀基體仍能檢測到R6G分子的SERS光譜,為了定量計算樹枝狀銀的SERS效應,基體的增強采用公式[19]:
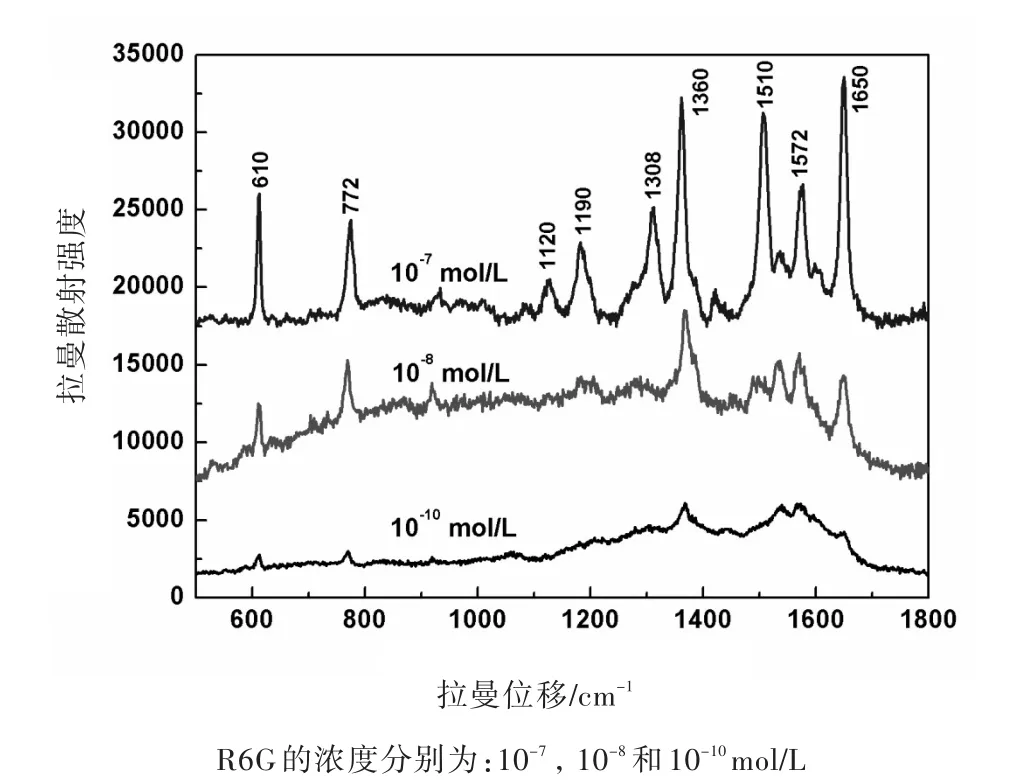
圖4 不同濃度的R6G吸附在樹枝狀銀表面的SERS光譜
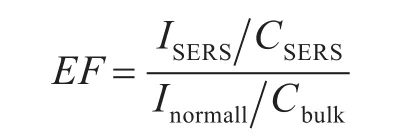
計算,其中Cbulk是本征R6G的濃度;CSERS是用于檢測SERS光譜的濃度;Inormall是本征拉曼散射頻率的特征振動峰的積分強度;ISERS是SERS拉曼頻散射率的特征振動峰的積分強度,以613 cm-1處的拉曼特征峰為依據,計算得到基底的增強因子為2.4× 107。
SERS產生的基本條件是金屬表面的粗糙化,金屬表面自由電子的集體振動增強導致表面局域等離子激元被激發引起電磁增強,使被測定物的拉曼散射產生極大的增強效應。樹枝狀銀之所具有良好地SERS效應,主要歸因于周期性變化的結構和粗糙的層級結構。具體表現在:一是具有樹干、樹枝和樹葉的樹枝狀銀相對于粗糙的金屬薄膜或光滑的納米線來說,有著更高的縱橫比[20]。理論上局部電磁場最大化的條件是納米粒表面具有高的彎曲率,從而引起高縱橫比納米結構SERS效應的最優化;其二是樹枝狀納米結構的樹枝和樹葉中占據著許多間隙帶(deep gaps or interstitials),彼此之間樅橫交錯形成較厚的銀膜結構。眾所周知,SERS效應是局部“活性熱點”(hot sopts)產生的局部電磁場作用所致,這些活性熱點能維持強烈的局部電磁場,對SERS效應具有重要的貢獻[21]。一般來講,金屬結構之間的間隙帶可以看做是局部的活性熱點,這些間隙帶周圍的光場強度遠遠大于其他的位置,受到激光輻射時,鄰近銀納米表面的電磁場相互耦合,在間隙空間中形成較強烈的局域電磁場,從而引起局部吸收分子拉曼信號的增強[22];其三,樹枝狀銀的樹葉可以看做是單晶結構,其尺寸在100 nm左右,這一納米尺寸能優化吸收分子的SERS效應[23]。因此,樹枝狀銀微納米結構在實驗中表現出很強的SERS活性,是一種良好的通用型SERS基底。
3 結論
筆者介紹了一種用檸檬酸為還原劑,采用兩電極電化學沉積法制備了樹枝狀銀微納米結構,方法簡單。制備的銀微納米結構是由樹干、樹枝和樹葉構筑的具有完美對稱性的樹枝狀層級結構。其生長機制是銀納米原電池在ITO的表面上能進行自組裝,檸檬酸的濃度和Ag+的濃度在晶體生長過程中起導向作用。由于樹枝狀Ag的高縱橫比、眾多的間隙結構和納米尺寸的單晶樹葉狀銀等結構因素,樹枝狀Ag表面電磁場的相互耦合作用,引起局域電磁場的增加,致使局部吸收分子拉曼信號的增強,使得樹枝狀銀微納米結構可用于超低濃度的單分子檢測,并表現出優異SERS活性效應。
[1]Fleischmann M,Hendra P J,McQuillan A J.Raman spectra of pyridine adsorbed at a silver electrode[J].Chem Phys Lett,1974,26:163-166.
[2]Moskovitz M.Surface-enhanced spectroscopy[J].Rev Mod Phys,1985,57:783-826.
[3]Anker J N,Hall W P,Lyandres O,et al.Biosensing with plasmonic nanosensors[J].Nat Mater,2008,7:442-453.
[4]Penn S,He L,Natan M.Nanoparticles for bioanalysis[J].Curr Opin Chem Biol,2003,7:609-615.
[5]Stiles P,Dieringer J,Shah N C,et al.Surface-Enhanced Raman spectroscopy[J].Ann Rev Anal Chem,2008,1:601-626.
[6]Gehan H,Fillaud L,Chehimi M M,et al.Hotspot-induced transformation of surface-enhanced Raman scattering fingerprints[J].ACS Nano,2010,4:3087-3094.
[7]Nie S,Emory S R.Probing single molecules and single nanoparticles by surface-enhanced Raman scattering[J].Science,1997,275:1102-1106.
[8]Xue G,Lu Y,Zhang J F.SERS studies of polymers on metal surfaces.4.cyclization and graphitization of polyacrylonitrile on rough silver surfaces[J].Macromolecules,1992,25:5855-5857.
[9]Li J F,Huang Y F,Ding Y,et al.Shell-isolated nanoparticle-enhanced Raman spectroscopy[J].Nature,2010,464:392-395.
[10]Camden J P,Dieringer J A,Wang Y M,et al.Probing the structure of single-molecule surface-enhanced Raman scattering hot spots[J].J Am Chem Soc,2008,130:12616-12617.
[11]Zhao L L,Jensen L,Schatz G C.Surface-enhanced raman scattering of pyrazine at the junction between two Ag20nanoclusters[J].Nano Lett,2006,6:1229-1234.
[12]McLellan J M,Li Z Y,Siekkinen A R,et al.The SERS activity of a supported Ag nanocube strongly depends on its orientation relative to laser polarization[J].Nano Lett,2007,7:1013-1017.
[13]Lee S J,Morrill A R,Moskovits M.Hot spots in silver nanowire bundles for surface-enhanced raman spectroscopy[J].J.Am Chem Soc,2006,128:2200-2201.
[14]Driskell J D,Shanmukh S,Liu Y,et al.The use of aligned silver nanorod arrays prepared by oblique angle deposition as surface enhanced Raman scattering substrates[J].J Phys Chem C,2008,112:895-901.
[15]Green M,Liu F M,Cohen L,et al.SERS platforms for high density DNA arrays[J].Faraday Discuss,2006,132:269-280.
[16]Wei G D,Nan C W,Deng Y,et al.Self-organized synthesis of silver chainlike and dendritic nanostructures via a solvothermal method[J].Chem Mater,2003,15:4436-4441.
[17]Peng K Q,Yan Y J,Gao S P,et al.Dendrite-assisted growth of silicon nanowires in electroless metal deposition[J].Adv Funct Mater,2003,13:127-132.
[18]Watanable H,Hayazawa N,Inouye Y,et al.DFT vibrational calculations of rhodamine 6G adsorbed on silver:analysis of tip-enhanced Raman spectroscopy[J].J Phys Chem B,2005,109:5012-5020.
[19]Rivas L,Sanchez-Cortes S,Garcia-Ramos J V,et al.Mixed silver/gold colloids:a study of their formation,morphology and surface-enhanced raman activity[J].Langmuir,2000,16:9722-9728.
[20]Wang D S,Kerker M.Enhanced Raman scattering by molecules adsorbed at the surface of colloidal spheroids[J].Phys Rev B,1981,24:1777-1790.
[21]Wang H H,Liu C Y,Wu S B,et al.Highly Raman-enhancing substrates based on silver nanoparticle arrays with tunable sub-10 nm gaps[J].Adv Mater,2006,18:491-495.
[22]Fang J X,Yi Y,Ding B J,et al.A route to increase the enhancement factor of surface enhanced Raman scattering(SERS)via a high density Ag flower-like pattern[J].Appl Phys Lett,2008,92:131115-131117.
[23]Krug J T,Wang G D,Emory S R,et al.Efficient Raman enhancement and intermittent light emission observed in single gold nanocrystals[J].J Am Chem Soc,1999,121:9208-9214.

