紫杉醇聯合替吉奧一線治療晚期胃癌25例生存分析
王 婷,馬 云
紫杉醇具有聚合和穩定細胞內微管的作用,可阻斷細胞于細胞周期的G2與M期,使癌細胞復制受阻斷而死亡。紫杉醇已在實體腫瘤中得到廣泛應用,也有臨床試驗證實單用或聯合順鉑或5-氟尿嘧啶(5-Fu)也有一定療效[1-2]。替吉奧是一種氟尿嘧啶衍生物口服制劑,包括替加氟、吉美嘧啶及奧替拉西。與5-Fu相比,替吉奧具有能維持較高的血藥濃度并提高抗癌活性、明顯減少藥毒性、給藥方便等優勢,單藥治療晚期胃癌的反應率可達20% ~50%[3-4]。日本多個臨床試驗證實,替吉奧聯合紫杉醇治療晚期胃癌的反應率可達40% ~60%[5-6]。因此,本研究中應用紫杉醇聯合替吉奧方案一線化療晚期胃癌,觀察其療效、毒性、耐受性等。
1 資料與方法
1.1 一般資料
入選條件:年齡18~75歲;經病理學確診的晚期胃癌(包括胃食管結合部腺癌),有可測量病灶(螺旋CT掃描不小于10 mm);ECOGPS評分為0~1分;預計生存期不少于3個月;主要器官功能正常,即血常規檢查標準需符合血紅蛋白(Hb)≥90 g/L(14 d內未輸血)、中性粒細胞 (ANC)≥1.5 ×109/L、血小板 (PLT)≥80×109/L,生化檢查需符合 BIL<1.25倍正常值上限(ULN)、丙氨酸氨基轉移酶和天冬氨酸氨基轉移酶(ALT和AST)<2.5×ULN,如有肝轉移,則ALT和AST<5×ULN,血清肌酐(Cr)≤1×ULN,內生肌酐清除率>50 mL/min(Cockcroft-Gault公式);既往未接受過姑息放化療;受試者自愿加入本研究,簽署知情同意書,依從性好,配合隨訪。患者曾接受過新輔助治療的紫杉醇或替吉奧治療間隔時間超過4周的仍可入選。合并有嚴重內科疾病、腦轉移、其他腫瘤以及對紫杉醇或替吉奧類似藥物過敏不得入選。
1.2 ECOG PS評分標準[7]
0分:活動能力完全正常,與起病前活動能力無任何差異;1分:能自由走動及從事輕體力活動,包括一般家務或辦公室工作,但不能從事較重的體力活動;2分:能自由走動及生活自理,但已喪失工作能力,白天不少于一半時間可以起床活動;3分:生活僅能部分自理,白天一半以上時間臥床或坐輪椅;4分:臥床不起,生活不能自理;5分:死亡。
1.3 方法
采用3周治療方案,紫杉醇(商品名福王,揚子江藥業),175 mg/m2,第1天靜脈注射3 h;替吉奧(商品名維康達,山東新時代藥業)依據體表面積(< 1.25 m2,40 mg;1.25 ~ 1.5 m2,50 mg;>1.5 m2,60 mg)連服第 1 至 14 天,1 天 2 次,早晚口服。連續給藥直至疾病進展,或毒性不可耐受,或患者拒絕治療退出研究。紫杉醇預處理方案按說明書給予。允許應用止吐藥物,如發生Ⅲ度或Ⅳ度粒細胞減少,允許應用粒細胞集落刺激因子(GCSF)。毒性評定參照NCI-CTC 3.0,如發生Ⅳ度血液學毒性,紫杉醇減量1/4,替吉奧降1個劑量等級。如發生神經毒性Ⅲ度,紫杉醇減量1/4。如發生其他非血液學毒性Ⅲ度紫杉醇減量1/4,替吉奧減量1個等級。允許減量2次,仍不能耐受則停止用藥。每次用藥前要求中性粒細胞>1.5×109/L,血小板>80×109/L,血紅蛋白>70 g/L。非血液學毒性恢復到Ⅰ級,神經毒性Ⅲ級以內,否則用藥推遲2周,仍不能恢復者退出研究。
1.4 療效評估及隨訪
入選之前進行篩選和評估,包括病史和體檢、心電圖、胸片、病灶增強CT、ECOG評分、血常規、肝功能、腎功能、電解質、腫瘤標志物(至少包括CEA、CA199)等。除胸片和增強CT外,每個周期前都行以上檢查。每2個周期進行1次病灶評估,療效評價參照RECIST 1.0[8]。所有入選病例均留下聯系電話及通信地址。治療結束后每2個月隨訪1次。
1.5 統計學處理
數據采用SPSS 13.0軟件包進行統計學處理。總生存時間(OS)定義為首次化療至死亡或失訪時間,疾病進展時間(PFS)定義為首次化療至疾病進展時間(影像證據支持進展或臨床癥狀進展)。計量資料以均數±標準差(X±s)表示,分類變量以計數和百分數表示。PFS和OS采用Kaplan-meier生存曲線評價。
2 結果
2.1 病例資料
本研究從2009年8月至2011年5月共納入28例晚期胃癌患者,其中有3例無法獲得評價資料,早期脫落,因此實際納入分析共 25例。年齡35~75歲,平均(60.2±10.51)歲,中位年齡62歲;其中男17例(68.00%),女8例(32.00%)。大部分病例具有良好的生活質量評分(ECOGPS評分,0或1分)。詳見表1。
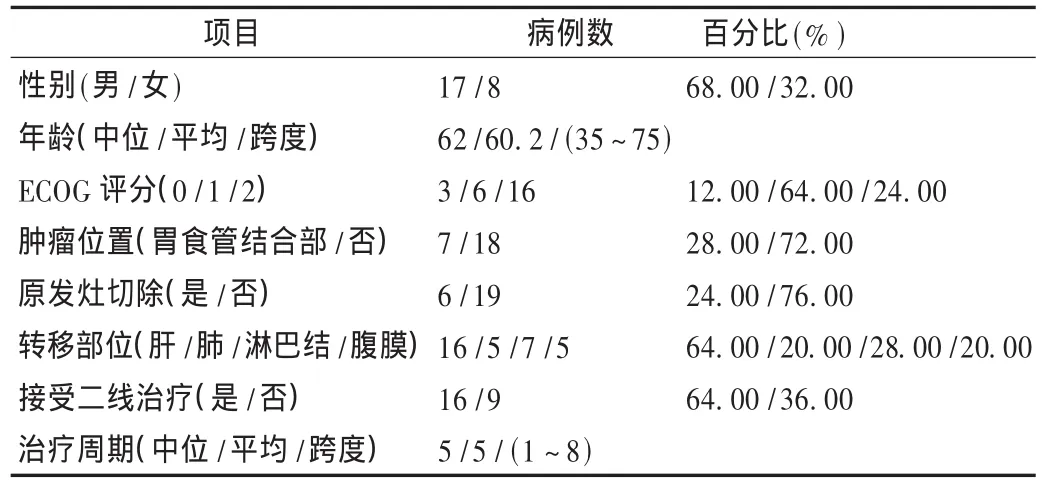
表1 病例資料(n=25)
2.2 療效和生存
25例患者平均接受5(1~8)個周期的方案,最佳療效評價見表2。患者隨訪時間為2~18個月,至隨訪結束,共8例死亡,3例失訪,達到事件終點。本組患者中位OS為15.5個月(95%CI,14.0~16.9 個月),1 年生存率為 76.00%,見圖 1。中位 PFS 為 8個月(95%CI,5.7 ~10.2 個月),見圖 2。
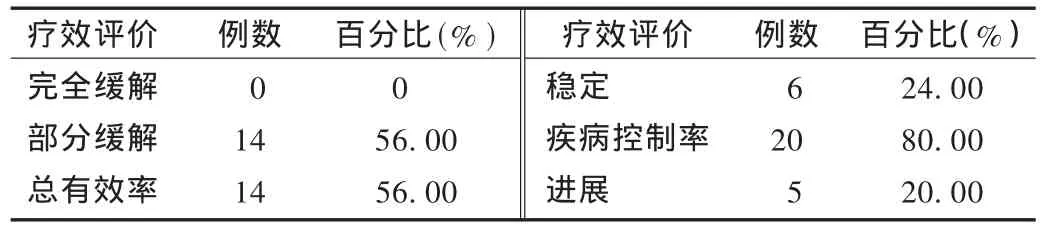
表2 最佳療效評價(n=25)
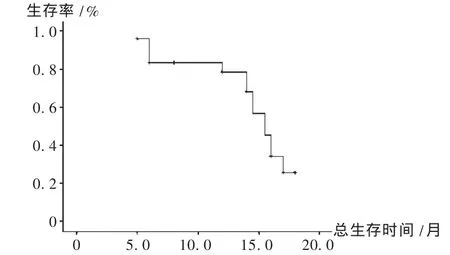
圖1 紫杉醇聯合替吉奧治療晚期胃癌總生存曲線(n=25)
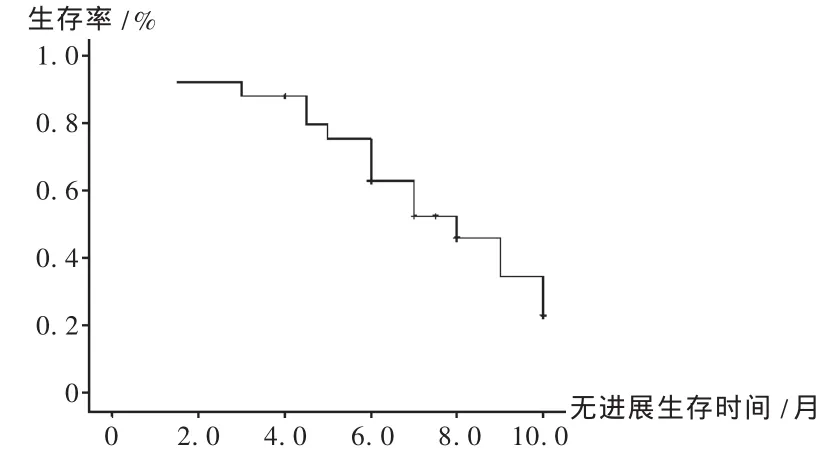
圖2 紫杉醇聯合替吉奧治療晚期胃癌無進展生存曲線(n=25)
2.3 毒性
毒性反應見表3。25例患者總共接受125個周期的紫杉醇聯合替吉奧一線化療,均可評價毒性。最常見的血液學毒性為貧血,粒細胞減少和白細胞減少也較為常見,未見有不低于Ⅲ度的血小板減少;脫發非常多見,25例患者都有不同程度的脫發。
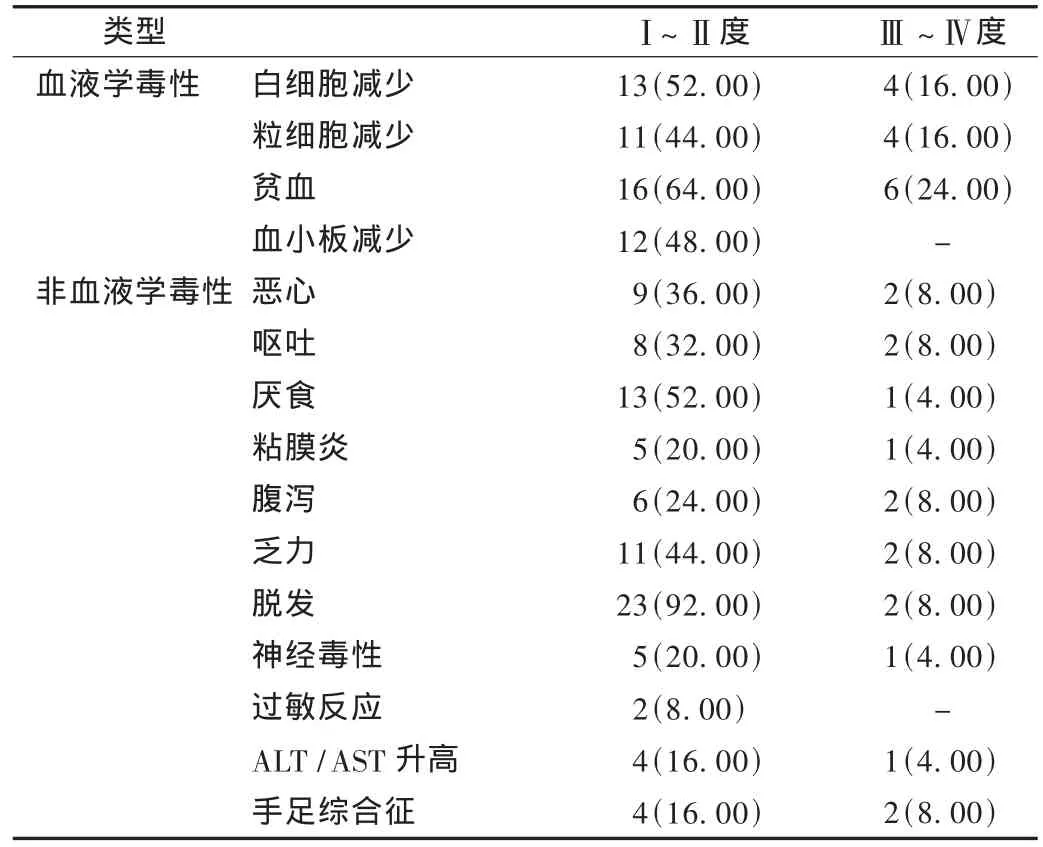
表3 患者的毒性反應分級[例(%),n=25]
3 討論
本研究中應用替吉奧聯合紫杉醇治療晚期胃癌一線治療,取得良好的療效,且毒性可控。既往有許多研究應用替吉奧聯合其他藥物如多西紫杉醇、順鉑,反應率可達40% ~70%,中位OS可達11~14個月[9-10]。Ⅲ期臨床試驗SPIRITS證實,替吉奧聯合順鉑治療晚期胃癌較單藥替吉奧總生存期長[11]。因此,在日本順鉑聯合替吉奧方案是胃癌治療的標準一線方案。該聯合方案雖然療效較好,但Ⅲ~Ⅳ度胃腸道毒性反應明顯升高。如在SPIRITS試驗中,30%患者有Ⅲ~Ⅳ度胃腸道毒性反應[8]。西方晚期胃癌人群中,FLAGS臨床試驗顯示,替吉奧聯合順鉑方案并不比5-Fu聯合順鉑方案優越,但毒性有明顯優勢[12]。其臨床試驗差異可能是由于兩組的替吉奧劑量不同,也有可能是由于東西方胃癌人群不同造成。
單藥紫杉醇治療胃癌的反應率約為20%~24.3%,其抗腫瘤機制與5-Fu不同且無交叉耐藥。Nukatsuka等[13]報道,在老鼠模型中發現替吉奧和紫杉醇具有協同機制。一項Ⅱ期臨床試驗顯示,紫杉醇聯合替吉奧治療胃癌反應率可達48.3%,中位生存期為13.9個月[14]。有報道這兩藥聯合方案治療胃癌伴惡性腹腔積液的患者也取得了良好療效[15-16],紫杉醇聯合替吉奧可能對該類患者有獨特之處。在本組病例中,有5例患者合并有惡性腹腔積液,1例PR,4例PD,效果欠佳,具體原因有待進一步探明。
在本組病例中,紫杉醇聯合替吉奧方案顯示出良好的療效,且胃腸道毒性反應輕,僅有不到10%的患者有Ⅲ/Ⅳ度惡心、嘔吐、腹瀉等胃腸道反應,且觀察到的血液學毒性不良反應也比其他聯合方案低,如順鉑/替吉奧、多西紫杉醇/替吉奧、多西紫杉醇/順鉑/5-Fu等。本組病例有超過一半的患者接受奧沙利鉑、伊立替康、希羅達等藥物的二線治療。這可能導致OS延長。
日本多個研究所采用的方案均為紫杉醇周療方案[14-16],本研究采用紫杉醇3周方案,周劑量強度基本相同,且總體療效和毒性和既往研究相比具有可比性。但本研究的方案給藥更方便。
總之,本研究結果提示,紫杉醇聯合替吉奧方案在晚期胃癌中療效佳,毒性相對較低。該組合可能會是未來晚期胃癌治療的標準方案,值得進一步行大樣本、多中心、隨機對照研究。
[1]Kollmannsberger C,Quietzsch D,Haag C,et al.A phaseⅡstudy of paclitaxel weekly,24 - hour continuous infusion 5 - fl uorouracil,folinic acid and cisplatin in patients with advanced gastric cancer[J].Br J Cancer,2000,83(4):458 - 462.
[2]Kim MK,Lee KH,Hyun MS,et al.A multi- center,phase Ⅱclinical trial of Padexol(paclitaxel)and cisplatin for patients suffering with advanced gastric cancer[J].Cancer Res Treat,2005,37(6):349 - 353.
[3]Chollet P,Schoffski P,Weigang-Kohler K,et al.PhaseⅡtrial with S-1 in chemotherapy - naive patients with gastric cancer.A trial performed by the EORTC Early Clinical Studies Group(ECSG)[J] .Eur J Cancer,2003,39(9):1 264 - 1 270.
[4]Jeung HC,Rha SY,Kim HK,et al.Multiinstitutional phase Ⅱ study of S-1 monotherapy in advanced gastric cancer with pharmacokinetic and pharmacogenomic evaluations[J].Oncologist,2007,12(5):543 - 554.
[5]Fujitani K,Narahara H,Takiuchi H,et al.Phase Ⅰand pharmacokinetic study of S-1 combined with weekly paclitaxel in patients with advanced gastric cancer[J].Oncology,2005,69(5):414 - 420.
[6]Fujiwara Y,Fujita J,Kan K,et al.A phase Ⅰstudy of combination chemotherapy using TS-1 and weekly paclitaxel for advanced gastric cancer[J].Gan To Kagaku Ryoho,2006,33(1):45 - 48.
[7]Oken MM,Creech RH,Tormey DC,et al.Toxicity And Response Criteria Of The Eastern Cooperative Oncology Group[J].Am J Clin Oncol,1982(5):649-655.
[8]Therasse P,Arbuck SG,Eisenhauer EA,et al.New guidelines to evaluate the response to treatment in solid tumors.European Organization for Research and Treatment of Cancer,National Cancer Institute of the United States,National Cancer Institute of Canada[J].J Natl Cancer Inst,2000,92(3):205-216.
[9]Wagner AD,Unverzagt S,Grothe W,et al.Chemotherapy for advanced gastric cancer[J].Cochrane Database Syst Rev,2010,17(3):CD004064.
[10]Power DG,Kelsen DP,Shah MA.Advanced gastric cancer-slow but steady progress[J].Cancer Treat Rev,2010,36(5):384 - 392.
[11]Koizumi W,Narahara H,Hara T,et al.S-1 plus cisplatin versus S-1 alone for fi rst-line treatment of advanced gastric cancer(SPIRITStrial):a phase Ⅲ trial[J].Lancet Oncol,2008,9(3):215 -221.
[12]Ajani JA,Rodriguez W,Bodoky G,et al.Multicenter phase Ⅲ comparison of cisplatin/S-1 with cisplatin/infusional fluorouracil in advanced gastric or gastroesophageal adenocarcinoma study:the FLAGStrial[J].JClin Oncol,2010,20,28(9):1 547 - 1 553.
[13]Nukatsuka M,Fujioka A,Nakagawa F,et al.Antimetastaticand anticancer activity of S-1,a new oral dihydropyrimidine-dehydrogenase-inhibiting fluoropyrimidine,alone and in combination with paclitaxel in an orthotopically implanted human breast cancer model[J].Int J Oncol,2004,25(6):1 531 -1 536.
[14]Narahara H,Fujitani K,Takiuchi H,et al.PhaseⅡstudy of a combination of S-1 and paclitaxel in patients with unresectable or metastatic gastric cancer[J].Oncology,2008,74(1 - 2):37 - 41.
[15]Hara A,Tsunemi S,Yamamoto M,et al.Efficacy of S - 1 combined with weekly Paclitaxel for gastric cancer with cancerous ascites[J].Gan To Kagaku Ryoho,2007,34(11):1 815 -1 818.
[16]Ishigami H,Kitayama J,Kaisaki S,et al.Phase Ⅱstudy of weekly intravenous and intraperitoneal paclitaxel combined with S-1 for advanced gastric cancer with peritoneal metastasis[J].Ann Oncol,2010,21(1):67-70.

