依托咪酯對腹外側視前區神經元GABA能傳遞的抑制作用
劉宇煒,黃 丹,陳曉青,許曉利,李長雷,艾永循
(江漢大學 醫學院,湖北 武漢 430056)
依托咪酯對腹外側視前區神經元GABA能傳遞的抑制作用
劉宇煒,黃 丹,陳曉青,許曉利,李長雷,艾永循
(江漢大學 醫學院,湖北 武漢 430056)
目的:研究依托咪酯對大鼠腹外側視前區神經元γ-氨基丁酸能傳遞的影響。方法:大鼠腹外側視前區切片,全細胞膜片鉗記錄神經元抑制性突觸后電流。結果:依托咪酯(0.1 μmol/L)可逆性地降低腹外側視前區神經元的誘發抑制性突觸后電流幅度,但未能顯著性改變其配對脈沖比率。依托咪酯(0.1 μmol/L)作用下,自發抑制性突觸后電流的頻率與幅度均顯著性下降,其動力學參數未受影響。結論:依托咪酯可作用于突觸前及突觸后γ-氨基丁酸受體而抑制對腹外側視前區神經元的γ-氨基丁酸能傳遞,這一作用可能使其處于興奮狀態,進而抑制結節乳頭體核的組胺能神經元,減少組胺釋放而發揮麻醉鎮靜作用。
依托咪酯;腹外側視前區;抑制性突觸后電流
睡眠和覺醒是人類的基本行為,其他如社會行為、飲食行為、性行為等與之密切相關。睡眠-覺醒周期乃機體生命之高級生理活動,是一個涉及多系統、多中樞的生理過程,具有復雜的神經調節機制。下丘腦腹外側視前區(ventrolat?eral preoptic area,VLPO)的神經元具有非常重要的促進睡眠作用[1]。腹外側視前區存在著兩類主要的神經元,它們對去甲腎上腺素(noradrena?line,NA)的反應截然相反。大多數(約68%)為去甲腎上腺素所抑制[NA(-)],而少部分為去甲腎上腺素所興奮[NA(+)][2]。NA(-)神經元為含有γ-氨基丁酸(γ-aminobutyric acid,GABA)的長投射到結節乳頭體核(tuberomamillary nucleus,TMN)的睡眠促進細胞,亦即文獻通常所指的腹外側視前區神經元;NA(+)神經元可釋放GABA而抑制NA(-)神經元的活動,屬該區局部神經元[2-3]。
依托咪酯(etomidate)是一種咪唑衍生類藥物,因其具有良好的血液動力學特性,被廣泛用于臨床快速誘導麻醉[4]。作為一種靜脈麻醉劑,依托咪酯的作用主要為增強GABA遞質傳遞,延長其突觸抑制作用時間[5],但其對腹外側視前區神經元的具體作用機制尚未明了。
在本實驗中,筆者采用全細胞膜片鉗技術,證明腹外側視前區GABA能神經元突觸前后均存在有功能性的GABAA受體,通過激活這些受體,依托咪酯可能通過抑制對這些神經元的GABA能傳遞而使處于興奮狀態,進而抑制結節乳頭體核的組胺能神經元而發揮麻醉鎮靜效應。
1 材料與方法
1.1 材料
Sprague-Dawley大鼠,鼠齡20~30天,雌雄不限,由江漢大學醫學院醫學實驗動物中心提供。
依托咪酯(etomidate),谷氨酸受體亞型拮抗劑(AP5和DNQX),γ-氨基丁酸A型受體阻斷劑(gabazine)和去甲腎上腺素(noradrenaline)購自Sigma公司,其余試劑為國產分析純。
孵育液(mmol/L):glycerol 250,KCl 1.6,NaH2PO41.2,MgCl21.2,CaCl22.4,NaHCO325,glucose 11,調pH值至7.3。
人工腦脊液(ACSF)(mmol/L):NaCl 125,KCl 1.6,NaH2PO41.2,MgCl21.2,CaCl22.4,NaHCO325,glucose 11,調pH值至7.3。
電極內液(mmol/L):CsF 135,KCl 5,MgCl22,Hepes 10,Mg ATP 2,GTP 0.2,調pH值至7.2。
1.2 方法
1.2.1 大鼠腹外側視前區腦片的制備 參照筆者以前的實驗方法[3],并在此基礎上稍加改進:無菌條件下迅速將大鼠斷頭取腦,置于混合氣(95%O2/5%CO2)飽和的冰冷(0~4℃)孵育液中約5 min。在0℃通混合氣條件下,采用振動切片機(VF-300,美國Precisionary公司)將腹外側視前區腦組織切成250 μm厚的冠狀切片,置于混合氣飽和的孵育液中,室溫(22~24℃)下孵育至少1 h以上。
1.2.2 電生理記錄 玻璃微電極由P-97電極拉制儀(美國Sutter公司)分兩步拉制,充灌電極內液后阻抗為4~6 MΩ。將腦片置于操作臺正中約0.4 mL凹槽內,用一鉑金環壓住。BX51正置顯微鏡(日本奧林巴斯公司)下選大鼠腹外側視前區神經元。全細胞膜片鉗記錄所用儀器為Axo?patch 700B膜片鉗放大器(美國Molecular公司),在電極與細胞膜之間形成高阻(1~5 GΩ)封接后,進一步將膜吸穿,調節電容和串聯電阻補償。數據以5 kHz過濾,使用Axonscope 1.1.1 acquisition軟件通過Axon DigiData-1440A記錄于電腦上。整個記錄過程中采用混合氣飽和的人工腦脊液持續灌流,灌流速度約2 mL/min。
1.2.3 統計學分析 采用Sigmaplot 11.0(Jandel Scientific)和SPSS 16.0進行處理、統計分析和制圖。實驗結果以均值±標準誤(mean±SEM)表示,統計結果采用配對t檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 依托咪酯對腹外側視前區神經元誘發抑制性突觸后電流的抑制作用
筆者以前的研究表明,NA(-)神經元形狀多為三角或多角形,短暫(30 s)給予去甲腎上腺素(100 μmol/L)后可引起超極化,并且神經元還具有低閾值放電(low-threshold spike,LTS)的特性[3],這和有關報道是一致的[2]。本次實驗選用的神經元均為NA(-)神經元。在AP5(50 μmol/L)和二硝基喹酮(6,7-Dinitro-1,4-dihydro-quinoxa?line-2,3-dione,DNQX,20 μmol/L)存在條件下,膜電位(VH)鉗制于0 mV時,通過刺激電極可激活誘發抑制性突觸后電流(eIPSCs),這些電流可被γ-氨基丁酸A型(GABAA)受體阻斷劑gabazine(10 μmol/L,未作圖示)完全阻斷,證明其為GABAA受體所介導。如圖1A所示,通過配對電刺激(刺激間距50 ms)誘發出成對的抑制性突觸后電流。依托咪酯(0.1 μmol/L)作用下第一個誘發抑制性突觸后電流幅度減小了(51.7±4.8)%(從(53±10)pA到(22±6)pA,n=8;P<0.01,圖1A和圖1B(a)),但未引起配對脈沖比率(paired-pulse ratio,PPR=IPSC2/IPSC1)發生顯著性改變(從(1.1±0.1)到(1.0±0.1),n=8;P>0.05,圖1A和圖1B(b)),發這一結果證明依托咪酯可減少突觸后GABAA釋放。
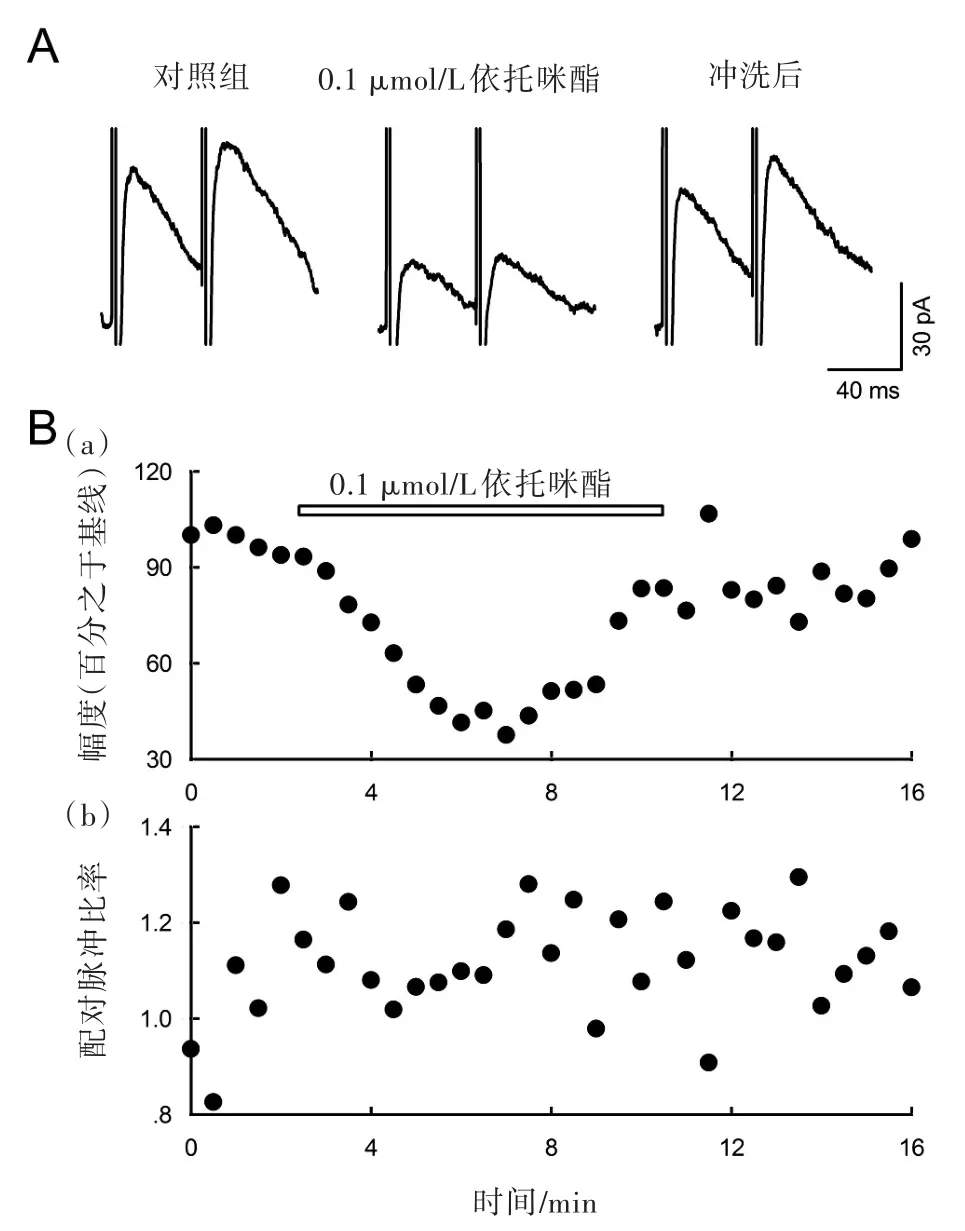
圖1 依托咪酯抑制腹外側視前區神經元誘發抑制性突觸后電流
2.2 依托咪酯對腹外側視前區神經元自發抑制性突觸后電流的抑制作用
進一步研究依托咪酯對腹外側視前區神經元自發抑制性突觸后電流(sIPSCs)的影響。在AP5(50 μmol/L)和DNQX(20 μmol/L)存在條件下,膜電位(VH)鉗制于0 mV時,自發抑制性突觸后電流可被gabazine(10 μmol/L,未作圖示)所完全阻斷,證明其為GABAA受體所介導。如圖2A所示,依托咪酯(0.1 μmol/L)作用下使自發抑制性突觸后電流頻率下降了(38.4±3.3)%(從(1.3± 0.5)Hz到(0.8±0.2)Hz,n=7;P<0.01),這一作用為可逆性的,在正常人工腦脊液沖洗之后,電流頻率恢復到對照組的(99.4±2.8)%(n=7;P>0.05)。第二次給予依托咪酯(0.1 μmol/L)后,自發抑制性突觸后電流頻率又下降了(39.9± 3.7)%,其下降幅度與第一次給藥間差異無統計學意義(n=7;P>0.05),并且其頻率在正常人工腦脊液沖洗后及時恢復。同時,在依托咪酯(0.1 μmol/L)作用下,自發抑制性突觸后電流(sIPSCs)幅度也降低了(10.3±0.8)%(從(17.8± 1.9)pA到(16.2±1.8)pA,n=7;P<0.05,圖2B),而其動力學參數并未改變(圖2B右)。
如圖2C所示,依托咪酯(0.1 μmol/L)的作用效果進一步為累積概率圖所顯示,其作用顯著延長了連續的自發抑制性突觸后電流之間的釋放間隔(K-S檢驗,P<0.01),同時明顯減小電流幅度(K-S檢驗,P<0.05)。

圖2 依托咪酯抑制腹外側視前區神經元自發抑制性突觸后電流
3 討論
依托咪酯是臨床上最常用的靜脈麻醉藥,由于它具有起效快、蘇醒迅速、對循環、呼吸系統影響較輕等優點,因此被廣泛用于全身麻醉的誘導和維持中。依托咪酯主要通過調節GABAA受體氯離子通道產生麻醉作用,它能夠增強GABAA受體的效能以及與配體結合的能力,間接抑制中樞興奮性遞質的傳遞[5-6]。
下丘腦腹外側視前區與睡眠調節密切相關。最近有報道指出腹外側視前核損毀前后給予依托咪酯,通過記錄腦電圖與心電圖,分析睡眠、覺醒時相變化及Fos基因在腹外側視前核的表達變化,認為依托咪酯可經腹外側視前核的γ-氨基丁酸能神經元通路產生促眠作用[7]。
本研究的全細胞膜片鉗表明,作用于腹外側視前區腦片時,依托咪酯(0.1 μmol/L)可逆性地降低腹外側視前區神經元誘發抑制性突觸后電流幅度,但未引起配對脈沖比率顯著性改變,這一結果表明依托咪酯可減少突觸后GABA釋放。接下來,在依托咪酯(0.1 μmol/L)作用下,sIPSCs的頻率與幅度均顯著性下降,其動力學參數未受影響,表明依托咪酯可作用突觸前及突觸后GABA受體而抑制對腹外側視前區神經元的GABA能傳遞。
腹外側視前區的GABA能神經元與結節乳頭體核的組胺能神經元之間的交互抑制在睡眠-覺醒轉換過程中起著最核心的調節作用。在睡眠過程中,腹外側視前區神經元快速放電,通過釋放GABA(以及galanin)抑制結節乳頭體核,引起自身去抑制,放電進一步增加;反過來,在覺醒狀態下,結節乳頭體核組胺能神經元放電增加,以釋放組胺(histamine)為主、同時還釋放少量GA?BA到腹外側視前區神經元,可產生抑制作用,進而去抑制結節乳頭體核神經元,使其放電活動更為增強[8]。
綜上所述,依托咪酯可作用于GABA受體而抑制對腹外側視前區神經元的GABA能傳遞,這一作用可能使其處于興奮狀態,進而抑制結節乳頭體核的組胺能神經元,減少組胺釋放而發揮麻醉作用。這很可能是依托咪酯產生麻醉鎮靜效果的重要作用機制之一。
[1] Nelson L E,Guo T Z,Lu J,et al.The sedative compo?nent of anesthesia is mediated by GABA(A)receptors in an endogenous sleep pathway[J].Nature neurosci?ence,2002,5(10):979-984.
[2] Gallopin T,Fort P,Eggermann E,et al.Identification of sleep-promoting neurons in vitro[J].Nature,2000,404(6781):992-995.
[3] Liu Y W,Li J,Ye J H.Histamine regulates activities of neurons in the ventrolateral preoptic nucleus[J].J Physiol,2010,588(Pt 21):4103-4116.
[4] Chan C M,Mitchell A L,Shorr A F.Etomidate is asso?ciated with mortality and adrenal insufficiency in sep?sis:A meta-analysis[J].Crit Care Med,2012,[Epub ahead].
[5] Garcia P S,Kolesky S E,Jenkins A.General Anesthet? ic Actions on GABAA Receptors[J].Curr Neurophar?macol,2010,8(1):2-9.
[6] Vanlersberghe C,Camu F.Etomidate and other non-barbiturates[J].Handb Exp Pharmacol,2008,(182):267-282.
[7] 張敏,范坤,邵玉峰,等.依托咪酯經腹外側視前核γ-氨基丁酸能神經元產生促眠作用[J].蘭州大學學報:醫學版,2011,37(1):1-5,10.
[8] Saper C B,Scammell T E,Lu J.Hypothalamic regula?tion of sleep and circadian rhythms[J].Nature,2005,437(7063):1257-1263.
Etomidate Inhibits GABAergic Transmission in Neurons in Ventrolateral Preoptic Area
LIU Yu-wei,HUANG Dan,CHEN Xiao-qing,XV Xiao-li,LI Chang-lei,AI Yong-xun
(School of Medicine,Jianghan University,Wuhan 430056,Hubei,China)
Objective:To study the effect of etomidate on GABAergic transmission in neurons of rat ventrolateral preoptic(VLPO)area.Methods:Rat ventrolateral preoptic area slices were pre?pared.Inhibitory postsynaptic current(IPSC)were investigated using whole-cell patch-clamp re?cording in VLPO neurons.Results:Etomidate(0.1 μmol/L)reversibly decreased the amplitude of evoked IPSC in VLPO neurons,without changing its paired-pulse ratio(PPR).Etomidate(0.1 μmol/L)decreased the frequency and amplitude of spontaneous IPSC,did not induce appreciable change in the kinetics of the spontaneous IPSC.Conclusion:Etomidate may act presynaptically and postsynaptically to suppress GABAergic transmission to VLPO neurons,this effect may excite these neurons,lead to the inhibition of histaminergic neurons in tuberomamillary nucleus,which will de?crease releasing of histamine and result in anesthesia and sedation.
etomidate;ventrolateral preoptic(VLPO)area;inhibitory postsynaptic current(IPSC)
R338.2-33
:A
:1673-0143(2013)01-0076-04
(責任編輯:范建鳳)
2012-10-08
湖北省自然科學基金重點項目(2008CDA053);武漢市科技計劃項目(201250499145-27)
劉宇煒(1973—),男,副教授,博士,研究方向:神經生物學。

