取向蠶絲蛋白支架與間充質干細胞的復合培養
袁翰,梁金,鄭欣,郭向可,李東亞,邱旭升,陳一心*
(1.南京中醫藥大學中西醫結合鼓樓臨床醫學院,江蘇南京 210008;2.南京大學醫學院附屬鼓樓醫院創傷骨科,江蘇南京 210008;3.南京大學化學化工學院,江蘇 南京 210093)
大段骨缺損常見于高能損傷導致的骨折、骨腫瘤的廣泛切除,骨髓炎的清創手術。隨著車禍的增加,大段骨缺損的修復在臨床上越來越常見,至今仍是一大難題。臨床上,對于大段骨缺損的治療,單純植骨往往不能解決問題,植入的骨組織常常被吸收,自體骨移植供骨量有限且存在取骨區感染風險,而同種異體骨移植存在傳染疾病的可能[1],這些缺點使得骨移植的應用受到限制。因此,研制新型的骨修復材料,通過引導骨組織再生來修復大段骨缺損是目前的研究熱點[2,3]。現階段,運用于臨床的骨組織修復材料存在力學性能不佳、骨誘導能力不足、生物相容性差等諸多缺陷[4,5]。
取向納米纖維材料能夠誘導細胞呈取向排布,并且增加細胞在其表面遷移的速率,甚至誘導間充質干細胞的分化[6]。蠶絲蛋白生物相容性較好,可作為制備納米纖維的原料。本研究通過制備合適尺度的取向納米蠶絲纖維,研究其對骨髓間充質干細胞(bone marrow stem cells,BMSCs)的排列、遷移、增殖及成骨分化的影響,為其將來作為大段骨缺損的修復材料應用于臨床提供實驗支持。
1 資料與方法
1.1 靜電紡絲法制備不同取向度蠶絲蛋白納米纖維支架以熱堿法脫去蠶絲絲膠,得到純蠶絲蛋白纖維。蠶絲蛋白纖維溶解于CaCl2/乙醇/H2O混合溶液(摩爾比1∶2∶8),混合溶液透析后蒸發干燥以取得蠶絲蛋白。空白對照組采用旋涂法施加蠶絲蛋白水溶液后常溫真空干燥。蠶絲蛋白取向納米纖維材料采用2 000 r/min轉速下的滾軸(直徑6 cm)接收裝置取得,無序納米纖維膜于500 r/min取得。將所得蠶絲蛋白納米纖維材料包覆于直徑14 mm的細胞爬片表面并以75%乙醇溶液處理。
1.2 取向蠶絲蛋白納米纖維對BMSCs增殖力的影響 人骨髓來自健康獻髓者,獻髓者事先已簽署知情同意書。將采集到的抗凝骨髓用密度梯度離心法分離骨髓中的單個核細胞。運用差速貼壁法純化細胞,4~5 d傳代一次。收集4~6代BMSCs調整濃度2×105/mL,分布接種于鋪有實驗組和對照組材料的24孔板中,每組復設4孔。分別于24 h、48 h、72 h、96 h、120 h 棄培養液,每孔加入噻唑藍(MTT)5 mg/mL,孵育4 d后棄上清加入二甲基亞砜200μL,振蕩溶解15 min,于酶標儀上測定570 nm處的光密度值,并設參考波長650 nm。細胞數量以吸光度單位來表示。
1.3 復合培養材料的形態學觀察 三組細胞以2×105/mL接種后,分布接種于鋪有實驗組和對照組材料的24孔板中,培養3 d后,將試樣切割為4 mm×4 mm后制樣,在掃描電子顯微鏡下觀察細胞在納米纖維支架材料上的生長密度和形態分布。另取三組細胞共培養后材料以4%多聚甲醛(pH 7.4)固定15 min。以Triton X-100通透5 min后。以1μg 4’,6-二脒基 -2- 苯基吲哚(4’,6-diamidino-2-phenylindole,DAPI)、5 μg/mL 鬼筆環肽常溫染色,抗熒光淬滅封片液封固。各組試樣于熒光顯微鏡下以496 nm和380 nm熒光激發成像,并使用Axio Vision軟件對各通道數據疊加處理。
1.4 不同取向度納米纖維膜力學性能測定 首先游標卡尺測量取向與非取向納米纖維膜的厚度,然后將其切成寬30 mm×長30 mm的試樣,在材料拉伸試驗機上測定強力與伸長。其中取向納米纖維材料測量兩次,分別沿取向方向(Y軸)和垂直取向方向(Z軸);無序納米纖維材料以方向隨機且通過試樣中心的軸線測量。從而得到強力-伸長曲線及有關力學指標,每種試樣測定5次,取其平均值。夾持部分的長度為5 mm每邊、拉伸速度5 mm/min,記錄被測支架斷裂前的受力動態變化,參數主要包括最大力(N)、最大力點的位移(mm)、拉抻強度(MPa)、最大力伸長率(%)、斷裂伸長率(%)等,并通過軟件計算拉伸強度和楊氏模量。
1.5 數據處理與統計分析 圖形化實驗數據通過NIH Image J軟件處理。實驗中其他數據和統計量化圖由SPSS計算并繪制。計量資料以(s)表示,三組各項指標的比較采用多組數據方差分析,P<0.05為差異有統計學意義。
2 結 果
2.1 取向納米蠶絲纖維的制備 制備提取得到純蠶絲蛋白溶液,使蠶絲蛋白紡絲液以約0.5 mL/h穩定連續的流出。調節接收距離及工作電壓,紡絲時間180 min。得到半透明膜狀取向納米蠶絲蛋白膜,電鏡下觀察取向納米纖維取向度好,非取向蠶絲蛋白納米纖維支架則呈無序分布。
2.2 取向納米蠶絲蛋白膜力學性能測定 通過材料拉伸試驗機測定取向、非取向納米蠶絲蛋白力學性能指標,統計結果見表1。取向蠶絲纖維軸向方向的最大力大于徑向方向,最大力伸長率小于徑向方向及非取向材料。楊氏模量大于徑向方向及非取向材料。
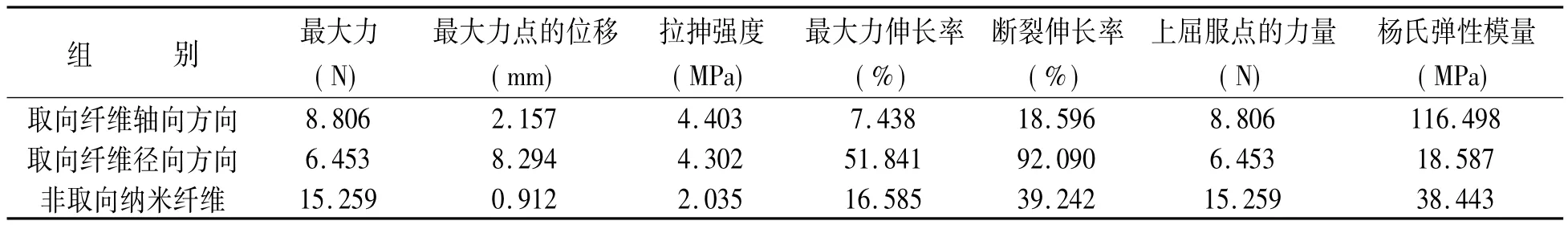
表1 納米蠶絲蛋白膜力學指標
2.3 BMSCs的體外分離、擴增 用比重1.073 g/mL的淋巴細胞分離液分離骨髓間充質干細胞,培養1 d后,未見明顯梭形貼壁細胞,大部分細胞為圓形未貼壁細胞。培養4 d后全量換液,除去未貼壁細胞,在顯微鏡下觀察,能看到散在存在的梭形貼壁細胞。1周后,數量稍微增多。至培養2周,已經能看到明顯聚集的梭形BMSCs。
2.4 取向納米蠶絲蛋白膜對BMSCs形態的影響 在取向納米蠶絲蛋白膜表面,細胞形態變長,呈梭形,細胞沿蠶絲方向有序排列,而亂序及平滑蠶絲蛋白膜材料表面,細胞在各個方向生長,隨機排列(見圖1)。掃描電鏡觀察,細胞黏附于納米蠶絲蛋白表面,沿蠶絲蛋白取向方向生長,其形態受到取向排列的蠶絲蛋白的影響,在2根蠶絲蛋白之間呈梭形。而在平滑蠶絲蛋白材料表面,細胞長軸在各個方向隨機排列。局部觀察到黏附于蠶絲表面的細胞偽足(見圖2)。FITC標記的鬼筆環肽與細胞內肌動蛋白結合后,顯示在各組實驗中細胞內肌動蛋白均沿細胞長軸方向。在平滑蠶絲蛋白材料及亂序納米蠶絲蛋白材料表面生長的BMSCs細胞均表現為梭形或多角形,細胞縱軸在各個方向隨機排列,而在取向納米蠶絲蛋白表面生長的BMSCs形態表現為充分伸長的梭形。細胞內部可見沿細胞長軸方向排列的肌動蛋白(見圖3)。
2.5 取向納米蠶絲蛋白對BMSCs增殖力的影響 MTT法測量細胞的增殖速率的結果示在1 d、2 d、3 d、4 d、5 d各檢測時間點,三組材料表面BMSCs細胞均快速增殖。在培養3 d后,取向及亂序納米蠶絲蛋白組細胞增殖力明顯高于普通蠶絲蛋白組(P<0.05)。從第4天開始,取向納米蠶絲蛋白組細胞增殖力明顯高于亂序納米蠶絲蛋白組(P<0.05,見表2)。
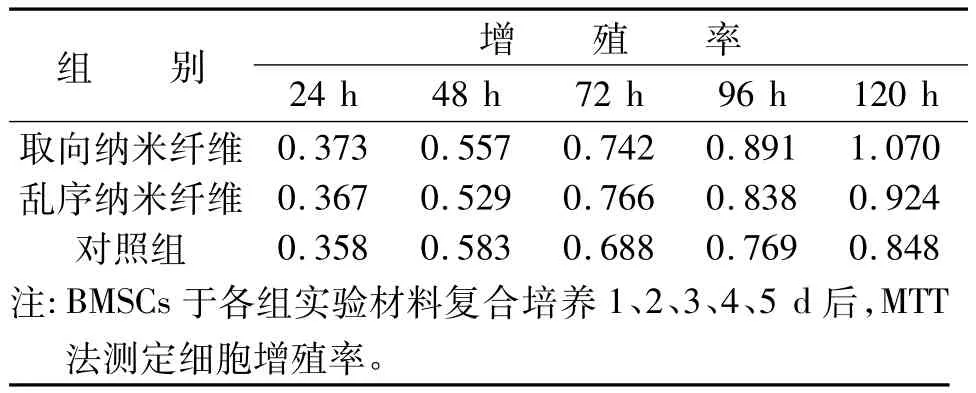
表2 MTT法測定BMSCs增殖力(吸光度OD)
3 討 論
3.1 取向納米蠶絲蛋白的制備 靜電紡絲技術是用于制備納米纖維的常用技術,通過改變合成條件,可以制造出不同直徑、密度以及排列的納米纖維。通過近十幾年的發展,眾多學者已將此項技術應用到對人造血管、創面覆蓋及引導組織修復方面的研究[7]。本實驗通過改進接收裝置滾輪轉速及電場強度,分別得到亂序及取向的蠶絲蛋白,直徑在500~1 000 nm之間。滾輪轉速為2 000 r/min時,電鏡顯示蠶絲蛋白取向度良好,隨著滾輪轉速的降低,蠶絲蛋白的取向度逐漸降低。當滾輪轉速降低至500 r/min時,蠶絲蛋白呈無序排列。厚度適中的半透明膜用于體外細胞實驗既有利于在光鏡及顯微鏡下觀察細胞形態,又具備一定的表面納米結構,適合用于體外細胞實驗的研究。通過控制紡絲時間,可以控制蠶絲蛋白的厚度,我們選取180 min的工作周期,最終得到厚度為50~100μm半透明的蠶絲蛋白膜。體外細胞共培養實驗證明,此種厚度的蠶絲蛋白納米纖維膜具有理想的實驗效果。
3.2 取向納米蠶絲蛋白的力學分析 用于骨科的植入材料需要具有一定的剛性及韌性。蠶絲蛋白雖然具有生物相容性好、體內可降解、易塑形等優點,但是其剛性及韌性較差,不能滿足骨科植入材料的需要[8]。有研究通過加入聚乳酸等制備成為復合材料,能夠增加其韌性,用于神經、血管等組織的修復[9,10]。但是加入的復合材料往往具有一定的生物毒性作用,體內不能降解,有的需要二次手術取出,增加了醫療費用的開支。本實驗通過增加蠶絲蛋白的取向度,并且控制其直徑為納米級別(500~1 000 nm),在不添加其余復合原料的情況下增加了蠶絲蛋白的軸向韌性,擴寬了蠶絲蛋白在醫學領域的應用范圍,使將來取向納米蠶絲的臨床應用成為可能。對于骨科領域,可增加取向納米蠶絲蛋白膜的厚度及密度,利于骨折斷端的輔助固定。
3.3 取向納米蠶絲蛋白對BMSCs形態的影響 人體骨骼組織中的膠原蛋白呈高度取向的束狀分布,是成骨細胞、間充質干細胞等生長所必需的細胞外基質。我們所制備的取向納米蠶絲纖維材料具有高度取向性,并且具有適當的纖維間隙,能夠提供細胞生長所需要的空間。它是一種模仿骨骼組織中細胞外基質成分的良好結構。電鏡及細胞骨架蛋白染色顯示骨髓間充質干細胞良好地附著于蠶絲蛋白表面,并且在取向蠶絲的誘導下變為梭形,長軸增加,向著蠶絲取向方向更好地遷移排列。肌動蛋白熒光染色更好地顯示了細胞形態及細胞有序排列,并且可以觀察到細胞內肌動蛋白呈相同方向束狀分布,這也初步解釋了細胞變長的可能機制。大量研究表明[6,11-19],生長于取向納米纖維材料表面的細胞不僅表現為黏著蛋白、張力蛋白、肌動蛋白等數量的變化,還檢測到細胞內某些信號通路甚至基因表達的改變。
Lu等[16]在高取向度的納米纖維表面,觀察到間充質干細胞可有序排列,并存在67個基因的表達差異,大部分與過氧化物酶體增殖物激活受體(peroxisome proliferator-activated receptor,PPAR)信號通路有關。因此我們推測,間充質干細胞通過整合素家族信號通路將細胞外的物理刺激轉變為能被細胞識別的生物信號并進一步影響細胞命運。我們從電鏡下觀察到BMSCs沿蠶絲取向方向伸出偽足黏附于蠶絲蛋白表面,這些現象都是細胞膜表面黏附蛋白與蠶絲蛋白相互作用的結果,與之前研究一致[6]。本實驗中肌動蛋白熒光染色后可以看到呈束狀排列并且有密度更高的肌動蛋白,顯示了細胞骨架的改變。
3.4 取向納米蠶絲蛋白促進BMSCs的增殖 目前對于成骨誘導材料的研究主要集中于兩方面,材料對成骨細胞增殖的促進作用,以及材料對骨髓間充質干細胞增殖及成骨分化的促進作用。隨著對材料表面物理形貌結構對細胞影響研究的深入,越來越多的學者開始研制具備一定納米形態的材料,促進成骨細胞增殖或者骨髓間充質干細胞的成骨分化。取向納米纖維材料是其中的一種,以往研究表明具備一定取向結構的納米纖維能夠促進間充質干細胞的增殖、分化[6,12,14,15]。我們首次選用生物相容性較好的蠶絲蛋白,通過靜電紡絲的方法制備取向納米蠶絲蛋白,研究其對BMSCs的影響,結果示具備一定取向的納米蠶絲蛋白能夠促進BMSCs的增殖活性,有利于骨折的愈合。
綜上所述,通過靜電紡絲法制備的蠶絲蛋白納米纖維支架可促進BMSC在其表面的增殖。提高納米纖維的取向程度后,還可進一步介導細胞的取向分布和成骨分化。材料具有獨特的力學特性,是一種極具潛力的骨修復生物材料。然而,取向納米纖維形貌如何影響BMSC的分化方向,以及取向蠶絲蛋白納米纖維支架于體內應用的效果,還需進一步研究。
(本文圖1~3見后插頁)
[1]Giannoudis PV,Dinopoulos H,E.Tsiridis.Bone substitutes:an update[J].Injury,2005,36(Suppl 3):S20-27.
[2]Masquelet AC,Begue T.The concept of induced membrane for reconstruction of long bone defects[J].Orthop Clin North Am,2010,41(1):27-37.
[3]Taylor BC,French BG,Fowler TT,et al.Induced membrane technique for reconstruction to manage bone loss[J].J Am Acad Orthop Surg,2012,20(3):142-150.
[4]Busuttil Naudi K,Ayoub A,McMahon J,et al.Mandibular reconstruction in the rabbit using beta-tricalcium phosphate(beta-TCP)scaffolding and recombinant bone morphogenetic protein 7(rhBMP-7)-histological,radiographic and mechanical evaluations[J].J Craniomaxillofac Surg,2012,40(8):461-469.
[5]Rezwan K,Chen QZ,Blaker JJ,et al.Biodegradable and bioactive porous polymer/inorganic composite scaffolds for bone tissue engineering[J].Biomaterials,2006,27(18):3413-3431.
[6]Teh TK,Toh SL,Goh JG.Aligned Fibrous Scaffolds for Enhanced Mechanoresponse and Tenogenesis of Mesenchymal Stem Cells[J].Tissue Eng Part A,2013,19(11-12):1360-1372.
[7]Bhardwaj N,Kundu SC.Electrospinning:A fascinating fiber fabrication technique[J].Biotechnology Advances,2010,28(3):325-347.
[8]Park SH,Gil ES,Kim HJ,et al.Relationships between degradability of silk scaffolds and osteogenesis[J].Biomaterials,2010,31(24):6162-6172.
[9]Diab T,Pritchard EM,Uhrig BA,et al.A silk hydrogel-based delivery system of bone morphogenetic protein for the treatment of large bone defects[J].J Mech Behav Biomed Mater,2012,11:123-131.
[10]Ak F,Oztoprak Z,Karakutuk I,et al.Macroporous silk fibroin cryogels[J].Biomacromolecules,2013,14(3):719-727.
[11]Yang F,Murugan R,Wang S,et al.Electrospinning of nano/micro scale poly(L-lactic acid)aligned fibers and their potential in neural tissue engineering[J].Biomaterials,2005,26(15):2603-2610.
[12]Baker BM,Nathan AS,Gee AO,et al.The influence of an aligned nanofibrous topography on human mesenchymal stem cell fibrochondrogenesis[J].Biomaterials,2010,31(24):6190-6200.
[13]Sengupta S,Park SH,Seok GE,et al.Quantifying Osteogenic Cell Degradation of Silk Biomaterials[J].Biomacromolecules,2010,11(12):3592-3599.
[14]Peng F,Yu X,Wei X.In vitro cell performance on hydroxyapatite particles/poly(L-lactic acid)nanofibrous scaffolds with an excellent particle along nanofiber orientation[J].Acta Biomater,2011,7(6):2585-2592.
[15]Capkin M,Cakmak S,Kurt FO,et al.Random/aligned electrospun PCL/PCL-collagen nanofibrous membranes:comparison of neural differentiation of rat AdMSCs and BMSCs[J].Biomed Mater,2012,7(4):045013.
[16]Lu LX,Wang XY,Mao X,et al.The effects of PHBV electrospun fibers with different diameters and orientations on growth behavior of bone-marrow-derived mesenchymal stem cells[J].Biomed Mater,2012,7(1):015002.
[17]Parrag IC,Zandstra PW,K.A.Woodhouse.Fiber alignment and coculture with fibroblasts improves the differentiated phenotype of murine embryonic stem cell-derived cardiomyocytes for cardiac tissue engineering[J].Biotechnol Bioeng,2012,109(3):813-822.
[18]Schneider T,Kohl B,Sauter T,et al.Influence of fiber orientation in electrospun polymer scaffolds on viability,adhesion and differentiation of articular chondrocytes[J].Clin Hemorheol Microcirc,2012,52(2-4):325-336.
[19]Wang Y,Gao R,Wang PP,et al.The differential effects of aligned electrospun PHBHHx fibers on adipogenic and osteogenic potential of MSCs through the regulation of PPARgamma signaling[J].Biomaterials,2012,33(2):485-493.

