“脂肪烴”的教學設計及反思
周新起
(浙江師范大學附中 浙江 金華 321004)
一、設計思路
新課改更關注的是學生在學習過程中的體驗,以及伴隨這一過程而產生的積極情感體驗和正確的價值觀,提倡學習方式多樣化,學生參與知識的形成過程,自主建構知識。本節課通過情景創設、圖表數據分析、動手做模型等方式激發學習主動性,更好地加深對脂肪烴結構與性質的理解,樹立“結構決定性質,性質反映結構”的學習思想,在設計上遵循新課改理念同時結合陶行知的教育思想,實現學生“在做中學”,更好地促進了學生對知識的理解。同時,本課在設計上突出“類別”,多處運用對比、重視學生的科學思維方法和能力的形成。
二、教材分析
本節課是蘇教版《有機化學基礎》中專題三第一單元。學生在《化學2》中初步認識了甲烷、乙烯的結構及相應的主要化學性質取代反應、加成反應、氧化反應,奠定了一定的知識基礎,本節課在此基礎上通過烷烴、烯烴、炔烴的結構和性質的比較、歸納,進一步學習取代反應、加成反應及聚合反應等有機反應,為后續各章節中其他烴及烴的衍生物的學習奠定基礎。
三、學情分析
學生在學習本節內容時已經學習了各類別有機物中的典型代表物質的性質和相應的化學反應,在學習本節課的知識時有一定認知基礎,有利于本節課學習的展開;在思維能力上,高二學生思維活躍,具備一定的空間想象能力、信息收集處理能力、提出問題、分析問題、解決問題和歸納的能力,只要在課堂上創設適宜的探究情境,激發學生的學習興趣,學生會樂于發揮自己的學習熱情,在課堂中會不知不覺完成知識遷移,將自己的認知從感性水平提高到理性水平;在情感上,高二學生自我意識高度發展,社會屬性增強,對價值有自覺追求,渴望得到同伴、教師的接納和尊重,期望自身價值的體現,為課堂開展探究活動提供可能性。
四、教學目標
1.知識與技能
(1)了解常見的脂肪烴的物理性質變化規律。
(2)能以典型代表物為例,列舉出烷烴、烯烴、炔烴和鹵代烴等有機化合物的主要化學性質。
(3)能區分取代反應和加成反應的含義和特點,能判斷有機化學反應的類型。
2.過程與方法
(1)通過圖表中的數據分析,養成分析問題、解決問題、知識整理和歸納能力。
(2)通過甲烷、乙烯、乙炔的結構、性質對比,形成學生的知識遷移能力、歸納能力。
(3)通過分子模型培養空間想象能力和邏輯思維能力,運用形象生動的實物、模型、計算機課件等手段理解概念、掌握概念。
3.情感、態度與價值觀
對有機物的認識從代表物質的性質上升到此類別的性質,由點及面,形成系統,學生樹立起“結構決定性質、性質反映結構”的學習理念。
五、教學重點、難點
1.重點:脂肪烴的結構和性質。
2.難點:有機物結構與性質的關系。
六、教學方法
本課堂采用探究的教學方法,通過圖表和數據的展示(直鏈烷烴的熔點和沸點、幾種烯烴的物理性質),設定一些問題,提出一些假設,再經過師生討論及驗證來得出結論。
七、教學過程
[引入]圖片展示:當把成熟的香蕉和盛開的鮮花放在一起的時候,鮮花凋謝了,請大家思考:成熟的香蕉釋放出了什么物質,促使鮮花加快凋謝?
[師生總結]乙烯,這是一種植物生長調節劑,加快了鮮花的調謝。
[過渡]展示圖片。其實烴與我們的生活聯系非常緊密,比如說,玫瑰之所以散發出芳香的氣味,是因為玫瑰能散發出一種苧烯的物質,其分子式為C10H16,同學們在飲食中經常會攝入大量的胡蘿卜素,它在人體內可以轉化成維生素A,能夠治療夜盲癥,提高人體免疫能力,這是目前最安全補充維生素A的產品,其分子式為C40H56,
(設計意圖:從生活中常見的植物花卉入手開始本節化學課的學習,感到化學來源于生活,激發學生學習的興趣,引出本節課的課題。)
[知識回顧]烴按照是否含有苯環如何分類?指導學生閱讀書本。
[總結]烴的分類。
[過渡]我們已經學習了甲烷、乙烯的物理性質,那么它們的物理性質有哪些遞變規律呢?
[投影]直鏈烷烴的熔點和沸點示意圖
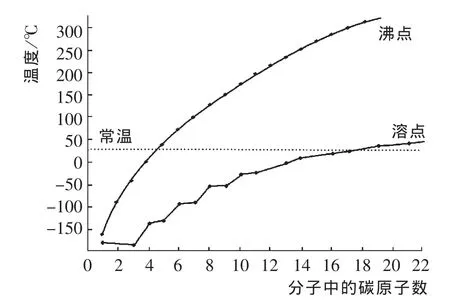
圖1 直鏈烷烴的熔點和沸點
觀察與討論:(1)直鏈烷烴的熔點具有哪些遞變規律?
(2)哪些烴常溫下為氣態?與分子中所含的碳數有何關系?
[討論總結]:
(1)隨著碳數的升高,烷烴的熔點逐漸升高。
(2)當分子中所含碳數小于等于4時,常溫下為氣態;當碳數介于5和16之間時常溫下為液態;當碳數大于16時,常溫下為固態。
[問題與探究]為什么烷烴的熔點隨碳數的增多而逐漸升高呢?
[學生討論、回答]隨著碳數的增多,相對分子質量逐漸增大,分子間作用力逐漸增大,所以熔點升高。
[追問]其他脂肪烴如烯烴、炔烴有沒有這樣類似的遞變規律?
[投影]烯烴、炔烴的物理性質遞變規律(表略)。
[師生總結]從以上圖表數據中我們可以知道脂肪烴的物理性質具有相似的遞變規律。
[過渡]我們知道結構決定性質。請同學們根據提供的分子模型搭建出乙烷、乙烯和乙炔的分子結構,并指出有哪些不同點?
[學生活動]用球棍模型連接乙烷、乙烯、乙炔的分子結構模型,直觀的認識到三者之間結構的主要差別。
[投影,引導學生填寫表格]
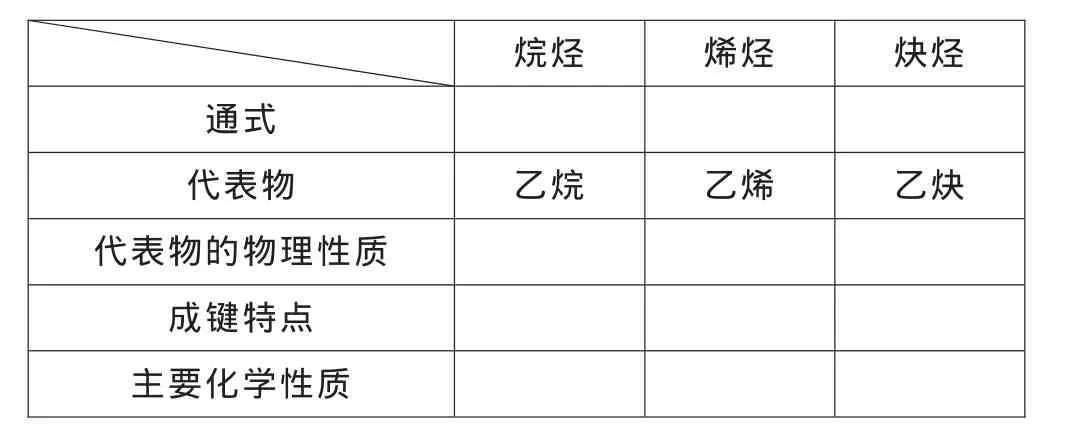
烷烴 烯烴 炔烴通式代表物 乙烷 乙烯 乙炔代表物的物理性質成鍵特點主要化學性質
(設計意圖:通過圖表中數據分析,掌握烴的物理性質遞變規律與碳原子數的密切關系,培養學生歸納能力,同時培養學生從烷烴到烯烴的知識遷移能力。通過學生利用球棍模型組裝分子結構,學生細心觀察其模型,培養空間想象能力,更充分地認識物質結構與物質性質之間的關系,為學習脂肪烴的性質奠定必備的基礎。以點帶面,顯示知識的內在規律:在化學2的基礎上,通過對比乙烷、乙烯結構、性質,演繹出烷烴、烯烴的結構與性質。教學時 “突出典型、挖掘本質、揭示規律、掌握類型”,運用從個別到一般的科學方法。縱橫對比、突出知識之間的聯系:學習中要不斷地對比,提示三者之間的異與同,以加深印象。這種對比成功之后,對滲透“結構決定性質,性質反映結構”這個有機化學的基本思想就水到渠成。)
[交流與討論1]氯乙烷可以通過乙烷和氯氣在光照條件下發生取代反應得到,也可以用乙烯和氯化氫在一定條件下發生加成反應得到,請問哪一種方法更好?
[學生回答]如果通過乙烷與氯氣發生取代反應,則所得的產物除了氯乙烷之外,還可能得到其他產物,而通過乙烯和HCl加成能得到較純凈的氯乙烷。
[交流與討論2]乙烯和溴單質有可能會發生哪些反應?如何證明乙烯與溴的四氯化碳溶液發生的是加成反應還是取代反應?
[學生分組交流、討論]學生經過思考后,提出:
(1)如果乙烯和溴的CCl4溶液發生取代反應則產物除了有機物外還有HBr生成:
Br2+CH2=CH2→CH2=CHBr+HBr
(2)如果乙烯和溴的CCl4溶液發生加成反應則反應只生成有機物:
Br2+CH2=CH2→CH2BrCH2Br
因此提出只要能檢驗出是否有HBr生成是關鍵,并設計出如下方案:

如果硝酸銀溶液產生淡黃色沉淀,則說明乙烯通入溴的四氯化碳溶液后產生了HBr,則為取代反應,若無明顯現象,說明兩者之間發生加成反應。
提出用溴水代替溴的四氯化碳溶液是否可行?教師根據溴水中含有HBr,如果利用上述方法進行驗證時會存在干擾,同時分析反應前后水溶液中的離子濃度大小,通過測定反應前后溶液的酸堿性變化,確定反應的類型。[如果發生取代反應則有HBr生成,會使溶液的酸性增強(pH變小);如果發生加成反應因為Br2的消耗會使溶液酸性減弱(pH變大)。]
[練習]請同學們書寫下列方程式:
乙烯與HCl的反應:
乙烯與H2O的反應:
乙炔與少量溴水反應:
乙炔與過量溴水反應:
(設計意圖:利用實驗方案的探究,通過對比、論證,加深對取代反應和加成反應的理解,完善、優化知識結構,培養分析問題、解決問題的綜合能力,強化科學探究意識,學生能從感性認識轉化為知識和技能,并內化到情感態度和價值觀中。)
[過渡]:如果是不對稱烯烴如 CH3—CH=CH2與HBr發生加成反應,那么可能會得到幾種產物?

[拓展視野]指導學生閱讀書本。馬氏規則:當不對稱的烯烴與鹵化氫發生加成反應時,通常“氫加到含氫較多的不飽和碳原子一側”。
[展示實物]展示聚乙烯、聚丙烯、聚苯乙烯、天然橡膠和丁苯橡膠新產品或圖片。提出問題:這些塑料制品是怎么得到的呢?
[播放動畫]CH2=CH2發生加聚反應生成聚乙烯。
(設計意圖:通過生活中常見的塑料制品,激發學生的好奇心和求知欲;通過動畫將乙烯的加聚反應從抽象化到具體化,增強教學的啟發性,將知識點化難為易,幫助學生理解其發生原理,提高課堂教學效率。)
[提問]乙烯能夠發生加聚反應主要與什么結構有關?
[學生]碳碳雙鍵在反應過程中不斷斷裂和連接。
[投影講解教師引入新概念]
加成聚合反應:這種一些具有不飽和鍵的有機化合物通過加成反應聚合生成高分子化合物的反應,簡稱加聚反應。該反應的原理可如下表示:
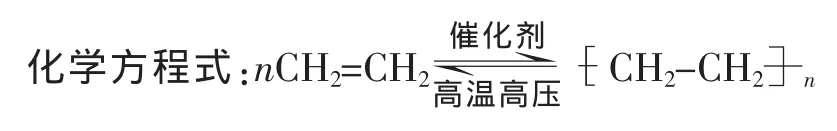
單體:合成聚合物的分子,如乙烯。
聚合物:相對分子質量較大高分子化合物,如聚乙烯。
聚合度:n
[練習]
1.聚丙烯的生成: ;
2.聚苯乙烯的生成: 。
(分別其指出單體、聚合物、鏈節和聚合度)
[師生活動]特別強調:能夠發生加聚反應是因為有機物分子中含有碳碳雙鍵的緣故。同時分析和解釋生成物的特點,及在書寫加聚反應時應注意反應的條件,反應物和生成物的書寫。
[課堂小結]脂肪烴物理性質和化學性質。
[課外思考]如果烴分子中含有兩個碳碳雙鍵,那么該烴能否發生加成反應,化學性質又有哪些變化呢?
八、課后反思
1.從教學設計角度反思教學效果
本堂課首先通過尋找生活中常見的脂肪烴作為情景引入,然后利用圖表等形式,通過學生交流與探究,學生歸納總結烷烴、烯烴、炔烴的物理性質變化規律,通過構建分子模型讓學生認識到烷烴、烯烴和炔烴的不同結構,并通過表格對比,培養學生“結構決定性質”的學習方法,通過證明乙烯與溴水是發生加成反應而不是取代反應,提高學生的實驗分析能力、探究能力和解決能力,通過丙烯和乙烯結構對比,引出丙烯的不對稱加成,通過生活中常見的聚合物的播放及形成原理,來探索加成反應原理及應用。學生雖然已經初步掌握了甲烷和乙烯基本結構和性質,但是本堂課不是簡單的知識重復,基本完成了教學目標,重視課堂新知識的自然生成,教師的教學在其中起到了穿針引線的指導作用。
2.從學生角度反思教學效果
本堂課是一堂理論課,且有些知識已經在《化學2》中已有了初步的認識,學生容易誤認為這是炒冷飯,所以本堂課通過生活中的化學情境、動手搭建模型、動畫等多種教學手段輔助教學,激發了學生的學習興趣,培養學生合作精神,提高學生課堂實踐能力。學生課堂上思維活躍,氣氛熱烈,積極思考課堂問題并能夠對問題大膽提出質疑,提出自己的見解,充分發揮了學生學習的主觀能動性和創造性,體現了學生在課堂中的主體性。如在驗證乙烯與溴單質發生取代反應時,有學生就提出疑問,溴水中本身就含有HBr,用溴的四氯化碳溶液代替更為合適,還有同學提出如果檢驗反應前后溶液的酸堿性變化可以的話,也可以通過測定反應前后溶液的導電性變化等,通過這些刺激了學生的求知欲。
[1] 張永紅.“酸和堿的反應”教學設計與反思[J].中學化學教學參考,2012,(4):30-32
[2] (美)加涅等著,王小明等譯.教學設計原理(第5版)[M].上海:華東師范大學出版社,2007
[3] 人民教育出版社化學室.全日制普通高中教材化學第二冊(必修加選修2)[M].北京:人民教育出版社,2000

