膠體金免疫層析試劑盒對甲型H1N1流感病毒(2009)抗原快速檢測的敏感性分析
田 棣,何 靜,劉 祎,張萬菊,徐 磊,陳功祥,周志統,胡蕓文
(1.上海市公共衛生臨床中心病原體檢測與生物安全部,上海 201508;2.浙江大學附屬第二醫院臨床檢驗中心,浙江 杭州 310009)
流感是由流感病毒引起的一種急性呼吸道傳染病,可引起地方性或世界性范圍的大流行[1]。2009年4月以來,一種新型的甲型H1N1流感在全球范圍內流行,引起廣泛的關注和重視。在大規模爆發的流感疫情中,首先需要快速查明病原體,才能對疫情控制以及患者治療提供幫助。目前甲型H1N1病毒(2009)的檢測方法主要是逆轉錄(RT)聚合酶鏈反應(PCR)和實時熒光PCR核酸檢測法[2],但此法對技術要求高,且用時較長。而常用的膠體金免疫層析法出結果較快,操作簡單,不需要特定的場所和儀器設備。基于此,本研究以實時熒光定量PCR(FQ-PCR)核酸檢測結果為參考,對膠體金免疫層析試劑盒在甲型H1N1流感病毒(2009)抗原快速檢測的敏感性和特異性進行了較為全面的分析。通過比較2種方法之間的相關性以及對不同病程、不同病毒核酸載量標本檢測的敏感性,為甲型 H1N1流感病毒(2009)的快速篩查提供依據。
材料和方法
一、材料
1.標本與來源 標本來自上海市公共衛生臨床中心2009年5至11月收治的疑似新甲型H1N1流感病例。采集標本均為鼻咽拭子,放置于帶有3 mL保存液的專用標本管中,分裝后-80℃低溫冰箱保存。
2.試劑與儀器 RNA提取試劑盒為德國QIAGEN公司產品(QIAamp viral RNA mini kit,Cat.No.52904);FQ-PCR試劑盒選用上海科華生物工程股份有限公司的甲型通用型和甲型H1N1流感病毒(2009)RNA檢測試劑盒(熒光PCR,批號為20090710);膠體金免疫層析試劑盒由杭州創新生物檢控技術有限公司提供,甲型流感病毒抗原檢測試劑盒批號為FA110101,甲型/乙型流感病毒抗原檢測試劑盒批號為FA110101;Mastercycler ep relplex PCR儀購自德國Eppendorf公司。
二、方法
1.FQ-PCR核酸檢測和拷貝數測定 按照試劑盒產品說明書進行測定,檢測通道分別為FAM(H1N1信號)及VIC(Flu A信號)。結果判斷:在陰陽性對照均成立的條件下,Ct<36為陽性;Ct≥40或無數值為陰性;36<Ct<40重測,復測結果Ct<36為陽性,否則為陰性。H1N1及Flu A信號均為陽性判為甲型H1N1流感病毒(2009)陽性。
2.膠體金免疫層析法甲型流感病毒檢測 按各自的說明書進行檢測,直接滴入解凍標本,等待15 min即可觀察結果。當試紙條判定部T、C處都確認有條帶時,結果判為陽性。
三、統計學方法
采用SPSS 17.0統計學軟件對結果進行統計分析,膠體金免疫層析法與FQ-PCR的檢測結果比較采用一致性檢驗;檢測結果與病程及核酸載量的相關性用Spearman相關分析和Logistic回歸分析;用幾何平均數計算核酸載量平均值;陰陽性標本的載量經對數轉換后采用t檢驗進行平均值比較,P<0.05表示差異有統計學意義。
結 果
一、膠體金免疫層析試劑盒檢測與FQ-PCR核酸檢測的比較
171例疑似甲型H1N1流感(2009)病例的鼻咽拭子標本,經FQ-PCR核酸檢測確認甲型H1N1流感病毒(2009)陽性151例、陰性20例。以甲型H1N1流感病毒(2009)PCR核酸檢測結果為標準,甲型流感病毒抗原檢測試劑盒的敏感性39.1%(59/151),特異性 90.0%(18/20);甲型/乙型流感病毒抗原檢測試劑盒的敏感性31.8%(48/151),特異性90.0%(18/20)。甲型流感病毒抗原檢測與PCR-熒光探針法核酸檢測結果的一致率Pa值為45.0%,在檢測結果無關聯的假定下期望一致率Pe值為39.1%,Kappa值為0.098;甲型/乙型流感病毒抗原檢測與PCR-熒光探針法核酸檢測結果的一致率Pa值為38.6%,在檢測結果無關聯的假定下期望一致率 Pe值為34.2%,Kappa 值為 0.068,見表1。
二、膠體金免疫層析試劑盒對不同病程標本的檢測結果比較
根據標本采集病例的發病天數將171例標本分成為1~、3~和5~d 3組,甲型流感病毒抗原試劑盒檢測的陽性率分別為66.7%、32.6%和27.3%;甲型/乙型流感病毒抗原檢測試劑盒的陽性率分別為62.5%、26.1%和20.0%,見表2。2種試劑盒的檢測陽性率與標本的病程均呈負相關(分別為Spearman相關系數-0.212,P <0.01和 Spearman相關系數為 -0.242,P <0.01),且為線性關系(分別為 χ2=8.59,P <0.01 和 χ2=11.18,P <0.01)。
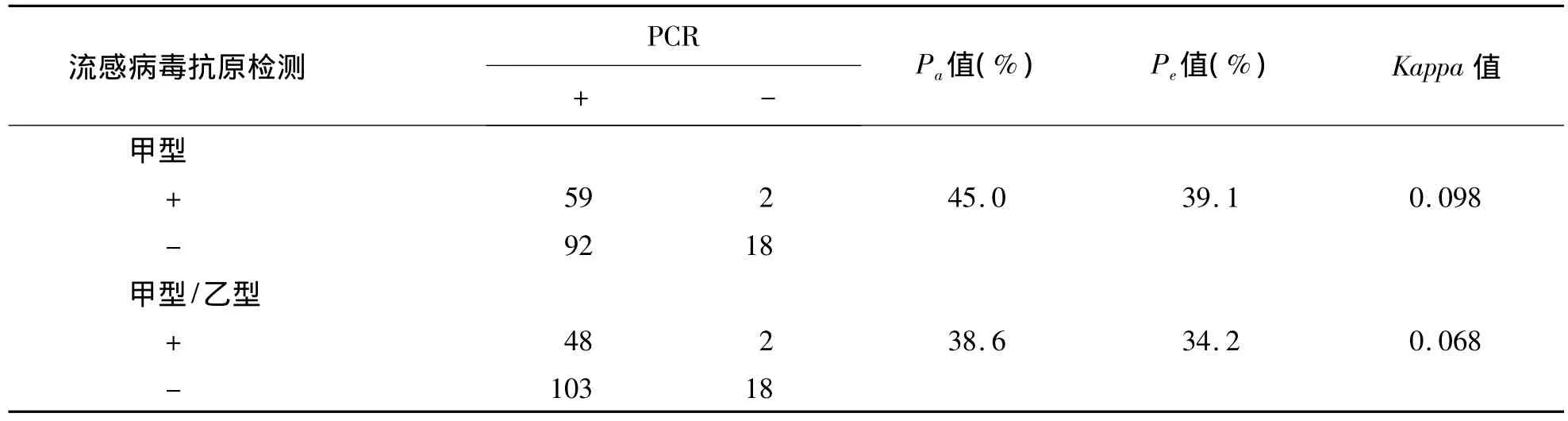
表1 膠體金免疫層析法和PCR的檢測結果比較

表2 不同病程標本的膠體金免疫層析法檢測結果
三、膠體金免疫層析試劑盒對不同病毒核酸載量標本檢測的敏感性比較
1.在151例甲型H1N1流感病毒(2009)PCR核酸檢測陽性標本中,膠體金免疫層析法甲型流感病毒抗原檢測試劑盒檢測陽性的標本核酸載量平均值為(2.41 ±1.55)×107拷貝/mL,檢測陰性的標本核酸載量平均值為(1.13±1.41)×106拷貝/mL,差異有統計學意義(t=5.48,P <0.0001);膠體金免疫層析法甲型/乙型流感病毒抗原檢測試劑盒檢測陽性的標本核酸載量平均值為(5.09±1.56)×107拷貝/mL,檢測陰性的標本核酸載量平均值為(1.11 ±1.38)×106拷貝/mL,差異有統計學意義(t=6.85,P <0.0001)。
2.根據病毒核酸載量將151例甲型H1N1流感病毒(2009)PCR核酸檢測陽性標本分成≥108、107~、106~、105~ 和 <105拷貝/mL 5 組。以甲型H1N1流感病毒(2009)核酸檢測結果為標準,膠體金免疫層析法甲型流感病毒抗原檢測試劑盒的敏感性分別為 73.3%、51.7%、36.7%、18.8%和16.7%;膠體金免疫層析法甲型/乙型流感病毒抗原檢測試劑盒的敏感性分別為73.3%、41.4%、26.7%、12.5%和 6.7%,見表 3。2種試劑盒的敏感性與標本的病毒核酸載量均呈正相關(Spearman相關系數分別為0.424,P<0.01和0.492,P <0.01),且為線性關系(分別為χ2=27.06,P <0.01 和 χ2=36.48,P <0.01)。
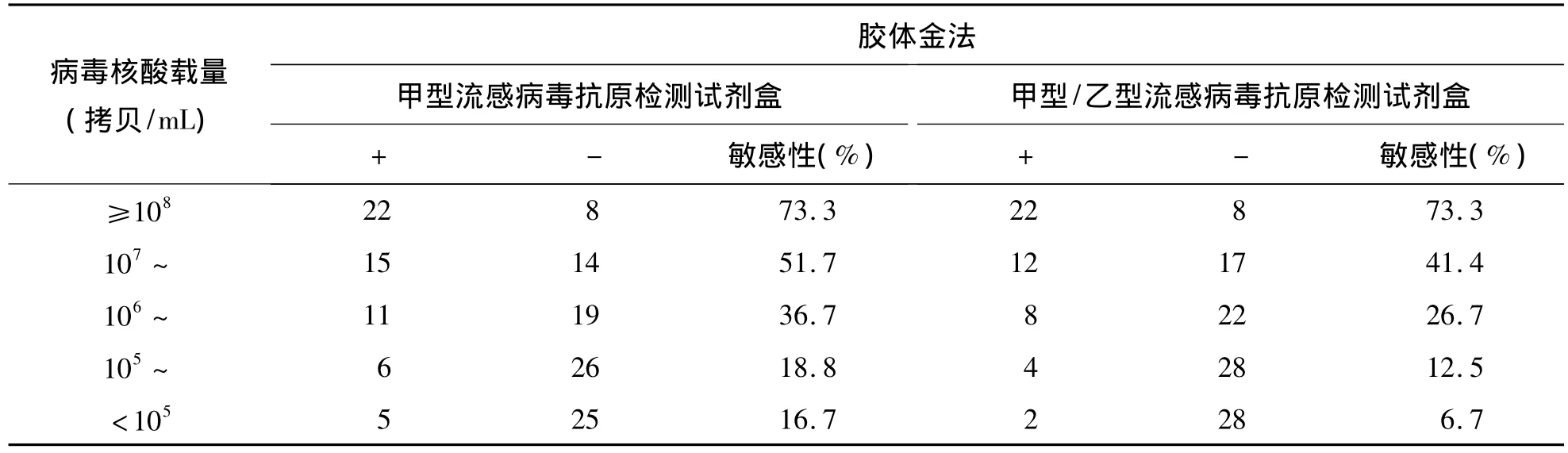
表3 不同病毒核酸載量的膠體金免疫層析法檢測結果
四、膠體金免疫層析法的理論敏感性分析
由于膠體金試劑盒要求將標本加入到0.5 mL的抽提液后立即檢測,而本研究采用了低溫凍存的咽拭子標本,其采集時加入了3 mL的專用標本采集液,相當于將標本的濃度稀釋了約6倍。為了評價上述情況對膠體金免疫層析試劑敏感性的影響,我們進一步對病毒載量與敏感性的關系進行Logistic回歸分析。假設試劑敏感性為M,病毒拷貝數的對數為L,甲型流感病毒抗原檢測試劑盒、甲型/乙型流感病毒抗原檢測試劑盒的敏感性為 MA、MA+B,則:

根據這個公式,我們可以推算出,2種試劑盒在發病后1~2 d取樣,標本的理論敏感性分別為77.3%和 74.6%。
討 論
流感病毒容易發生變異,其抗原性變異與流感的發生、流行密切相關[1],在流感爆發流行期早期快速診斷對于疫情防控至關重要,目前流感病毒常用的實驗室檢測方法包括病毒培養、免疫熒光、核酸檢測和血清學檢測法等。當甲型H1N1流感病毒(2009)開始在全球范圍內流行后,世界衛生組織 (WHO)以及美國疾病預防控制中心(CDC)推薦的實驗室檢測方法均為RTPCR或實時熒光PCR[3-4]。但這些方法需要特殊儀器設備,操作復雜且耗時較長,難以在醫院發熱門診和海關口岸開展現場篩查。膠體金免疫層析法作為一種快速抗原檢測技術,操作簡便,可在15 min左右得到結果,適合現場檢測。
在國內外文獻報道中,膠體金免疫層析法快速抗原檢測對新型甲型流感病毒的敏感性各不相同。Drexler等[5]發現膠體金免疫層析法快速檢測試劑對甲型H1N1流感病毒(2009)的敏感性只有11%,對2007至2008年及2008至2009年間的季節性流感病毒敏感性為37.5%和51.9%。而同種試劑在 Faix等[6]的研究中對甲型 H1N1流感病毒(2009)的敏感性為51%;在Uyeki等[7]的研究中對季節性流感病毒的敏感性只有27%。在國內關于膠體金免疫層析法檢測甲型H1N1流感病毒(2009)的文獻中,鄭海潮等[8]報道的敏感性為35.6%;尤鳳興等[9]報道的敏感性為 44.8%;穆煜等[10]報道的敏感性為 66.7%;程曉東等[11]報道的敏感性為 78.1%;而石漢振等[12]報道的敏感性則高達96.7%。本研究中使用膠體金免疫層析法甲型流感病毒抗原檢測試劑盒、甲型/乙型流感病毒抗原檢測試劑盒檢測甲型H1N1流感病毒(2009),以PCR核酸檢測結果為標準,2種試劑盒的敏感性分別為39.1%和31.8%,與PCR檢測一致性均較差(Kappa值<0.4)。一致性檢驗的結果與張素美等[13]、賈寧等[14]的報道基本相符,說明膠體免疫層析法檢測甲型H1N1流感病毒(2009)的敏感性存有一定的局限性。
我們分析導致各膠體金免疫層析試劑敏感性差異的原因,可能與各試劑生產廠家所采用的抗體和載體等原材料不同有關,且采用不同的參比標準得到的敏感性也會不同。比如在魏娟等[15]的報道中,同種膠體金免疫層析試劑與病毒培養相比的敏感性為63.6%,而與RT-PCR相比的敏感性則為73.8%。而本研究的結果提示,采樣時間以及體內病毒載量等因素也是影響其敏感性的關鍵因素。我們對不同病程標本的檢測陽性率進行了比較,發現甲型流感病毒抗原檢測試劑盒、甲型/乙型流感病毒抗原檢測試劑盒的陽性率在發病早期1~2 d時分別為66.7%和62.5%,發病后期5~d時分別為27.3%和20.0%;檢測陽性率隨病程延長而下降,兩者呈線性負相關(P<0.01)。在此基礎上,我們進一步對膠體金免疫層析法在不同病毒載量陽性標本中的檢測敏感性進行了比較,發現病毒載量≥108拷貝/mL時,2種試劑盒的敏感性均可達73.3%;而<105拷貝/mL時,2種試劑盒的敏感性分別只有16.7%和6.7%;檢測敏感性隨著病毒核酸載量的降低而下降,兩者間呈線性正相關(P<0.01)。另外,試劑盒說明書要求采集的鼻咽拭子標本應加入0.5 mL的抽提液后立即檢測,而本研究中的鼻咽拭子標本加入了3 mL的專用標本采集液,相當于稀釋了6倍左右,可能對敏感性有所影響。因此,我們對檢測敏感性進行了Logistic回歸分析,推測2種試劑盒在發病早期1~2 d取樣時的理論敏感性分別可達77.3%和74.6%,此理論值與國外Lee等[16]的報道基本相符。
本研究結果表明,盡管以膠體金免疫層析試劑盒檢測甲型H1N1流感病毒(2009)的敏感性仍有一定的局限性,但是其在發病早期及病毒載量較高時仍有較好的檢測效果。流感作為第1個實行全球性監測的傳染病,其危害引起人們的廣泛關注。當流感病毒發生抗原性變異導致新的病毒株產生時,則會出現局部及至全球性大流行[1]。鑒于膠體金免疫層析法流感病毒抗原檢測試劑還同時具備操作簡便、需時較短、結果判斷容易、不需要特殊儀器設備、處理大量標本更為快速方便等諸多優點,我們認為其可在流感病毒大范圍流行時,在醫院發熱門診以及機場、海關、學校等現場用于早期診斷,有效幫助快速篩查發病早期的患者和疑似患者。但是鑒于膠體金免疫層析法自身的局限性,其結果只能作為初步參考,最終的確認結果應以PCR結果為準。
[1]郭元吉,程小雯.流行性感冒病毒及其實驗技術[M].北京:中國三峽出版社,1997:1-4.
[2]中華人民共和國衛生部.甲型H1N1流感診療方案(2010年版)[S].衛辦醫政發[2010]79號,MOHC,2010.
[3]World Health Organization.WHO guidelines for pharmacological management of pandemic influenza A(H1N1)2009 and other influenza viruses[EB/OL].(2010-03-09)[2010-12-15].http://www.who.int/csr/resources/publications/swineflu/h1n1_guidelines_pharmaceutical_mngt.pdf.
[4]Centers for Disease Control and Prevention(CDC).Guidance for clinicians on the use of rapid influenza diagnostic tests for the 2010-2011 influenza season[EB/OL].(2010-12-22)[2011-03-15].http://www. cdc. gov/flu/pdf/professionals/diagnosis/clinician_guidance_ridt.pdf.
[5]Drexler JF,Helmer A,Kirberg H,et al.Poor clinical sensitivity of rapid antigen test for influenza A pandemic(H1N1)2009 virus[J].Emerg Infect Dis,2009,15(10):1662-1664.
[6]Faix DJ,Sherman SS,Waterman SH.Rapid-test sensitivity for novel swine-origin influenza A(H1N1)virus in humans[J].N Engl J Med,2009,361(7):728-729.
[7]Uyeki TM,Prasad R,Vukotich C,et al.Low sensitivity of rapid diagnostic test for influenza[J].Clin Infect Dis,2009,48(9):e89-e92.
[8]鄭海潮,馬超鋒,安建博,等.兩種國產甲型流感病毒抗原試劑檢測2009 H1N1流感病毒敏感性實驗研究[J].現代檢驗醫學雜志,2010,25(3):102-103.
[9]尤鳳興,居麗雯,張敬平,等.流感病毒快速檢測方法特異性和敏感性研究[J].檢驗醫學,2009,24(8):598-601.
[10]穆 煜,于俊峰,常 曉,等.快速甲型/乙型流感抗原篩查試驗與H1N1 PCR檢測結果的比較與評價[J].實驗與檢驗醫學,2010,28(2):105-106.
[11]程曉東,袁 權,蘇明權,等.新甲型H1N1流感和季節性流感臨床快速診斷的研究[J].現代檢驗醫學雜志,2010,25(3):61-64.
[12]石漢振,鄭智明,黃憲章,等.免疫層析法用于甲型H1N1流感病毒抗原篩查的初步評價[J].檢驗醫學,2011,26(6):402-404.
[13]張素美,李魯英,孟保平,等.兩種甲型H1N1流感病毒檢測方法的比較[J].中華實驗和臨床感染病雜志(電子版),2010,4(4):441-443.
[14]賈 寧,閆中強,劉 剛,等.免疫滲濾與膠體金快速檢測在篩查甲型流感中診斷效率分析[J].南方醫科大學學報,2010,30(10):2267-2269.
[15]魏 娟,陳杭薇,呂 楠,等.膠體金免疫層析法快速檢測甲型流感病毒的可行性[J].中華結核和呼吸雜志,2010,33(2):113.
[16]Lee CS,Lee JH,Kim CH.Time-dependent sensitivity of a rapid antigen test in patients with 2009 H1N1 influenza[J].J Clin Microbiol,2011,49(4):1702.

