CT引導下射頻消融聯合臭氧治療極外側型腰椎間盤突出癥
陳振中 陳小勇 姜成龍 吳海波
海南省三亞市中醫院,海南三亞 572000
隨著人們生活水平的進一步提高,腰椎間盤突出癥也在各類患者尤其是老年患者之中發病率呈逐年上升的趨勢,其發病后往往會造成腰腿痛以及其他肢體活動不便,往往會給患者的生活及工作造成較大的影響。近年來,腰椎間盤突出的微創治療得到迅速發展,其中臭氧融盤、射頻、激光消融以及腔鏡等技術已在很多醫院開展。因其創傷小、見效快而被更多患者接受。近年來,醫學界采取了不同的方法進行椎間盤突出癥的治療,取得了不錯的效果,如射頻消融以及臭氧治療等,都取得了較好的療效,尤其是臭氧治療對患者的損傷小,在我國及國外都有非常廣泛的應用。極外側椎間盤突出為腰椎間盤突出癥中的一種特殊類型[1],臨床上并不少見,其發生率占整個腰椎間盤突出癥的2.6%~11.7%[2],海南省三亞市中醫院(以下簡稱“我院”)應用CT引導下射頻消融聯合臭氧注射治療極外側型腰椎間盤突出,效果顯著,現報道如下:
1 資料與方法
1.1 一般資料
選擇2009年1~12月在我院接受治療的92例極外側型腰椎間盤突出癥患者作為研究對象,將其分為治療組和對照組。治療組53例,男33例,女20例;年齡20~59歲,平均43歲;病程2周~15年,平均8個月。對照組39例,男28例,女11例;年齡42~58歲;病程3周~2年,平均6個月。突出部位:L3/4椎間盤28例,L4/5椎間盤55例,L5/S1椎間盤39例,92例患者共計122個椎間盤。所有患者均接受了跟蹤隨訪,隨訪時間為3~28個月。
1.2 入選及排除標準
所有患者術前均經保守治療效果不滿意,所有患者均有典型的神經根刺激癥狀,伴有或不伴有腰部疼痛。排除骨性椎管狹窄、腰椎峽部裂、滑脫和不穩。
1.3 手術適應證
①腰痛伴下肢放射痛,病程≤3年,直腿抬高試驗<70°。②CT或MRI檢查發現相關的極外側型椎間盤突出,影像學顯示突出物不超過椎管容積的40%。反之以下則為禁忌證:①突出物嚴重鈣化、脫出、游離等;②合并心功能不全、腫瘤、出血傾向、精神障礙、安裝起博器等其他疾病;③伴Ⅱ度或Ⅱ度以上椎體滑脫,椎管狹窄和嚴重脊柱退行性變;④有射頻及臭氧治療禁忌等。
1.4 治療方法
患者俯臥于CT掃描床上,常規定位消毒局麻后,以專用穿刺針穿刺,經側后方安全三角區穿刺入路,進針點的選擇以脊柱中線為基準,在距該基準1 cm處小關節內緣部位以及距該基準4~6 cm處的小關節外緣部位選擇為進針點。在實施穿刺進針時,尤其是內源性進針,往往會有較強的突破感,并且在進針的同時推注水氣混合物,可使硬膜囊被推移,通過CT檢測如果針尖已達到突出物的中間部位,而回抽不回血及腦脊液,這樣表明穿刺成功,可以開始進行治療。
1.4.1 治療組 首先要通過檢測確定被治療的患者無神經根刺激征表現,治療過程中如果患者出現過度刺激癥狀如出現燒灼感,則表明刺激部位與神經根距離太近,則需要將射頻針退后少許再進行治療。根據CT定位及引導將射頻穿刺套針穿入椎間盤突出物的中后1/3處。確認正常后,給予70~90℃射頻治療2~3 min。另外,在原定位的基礎上進行附近區域的治療,定位區域為原定位點的0.5 cm左右。射頻熱凝術后。再注射濃度為50 μg/mL的臭氧20 mL,經CT掃描達到標準后于神經根旁注入40 μg/mL的臭氧5 mL,再次通過CT對盤內、盤外臭氧的分布進行掃描,滿意拔針。
1.4.2 對照組 依上法直接在突出物中注射濃度為50 μg/mL 的臭氧 20 mL。
術后兩組患者均常規靜滴甘露醇125 mL加地塞米松5 mg,連續使用3 d,24 h后戴腰圍下床,3個月內避免彎腰負重及重體力勞動。
1.5 療效評價
記錄患者下肢疼痛評分(采用視覺模擬評分法測量,VAS用于疼痛的評估在我國臨床使用較為廣泛,基本的方法是使用一條游動標尺,一面有10個刻度,兩端分別為“0”分端和“10”分端,“0”分表示無痛,“10”分代表難以忍受的最劇烈的疼痛,讓患者在直尺上標出能代表自己疼痛程度的相應位置,為其評出分數),療效判定根據改良的Macnab療效評定標準[3]進行評定。優:癥狀消失,工作和運動完全恢復;良:偶有腰部不適及下肢疼痛,工作無限制,一般情況下不需要特殊治療;差:癥狀無明顯改善,需用藥對癥處理。
1.6 統計學方法
應用SPSS 13.0統計軟件進行數據處理,計量資料采用均數±標準差(±s)表示,組間比較采用t檢驗,計數資料采用百分率表示,組間比較采用χ2檢驗。以P<0.05為差異有統計學意義。
2 結果
兩組患者均于術后3個月進行隨訪檢查。治療組與對照組治療后療效比較差異有統計學意義(P<0.05),治療組明顯優于對照組,見表1。治療組以及對照組治療前后下肢疼痛比較差異有統計學意義(P<0.05);治療組與對照組治療后比較差異有統計學意義(P<0.05),治療組優于對照組,見表2。
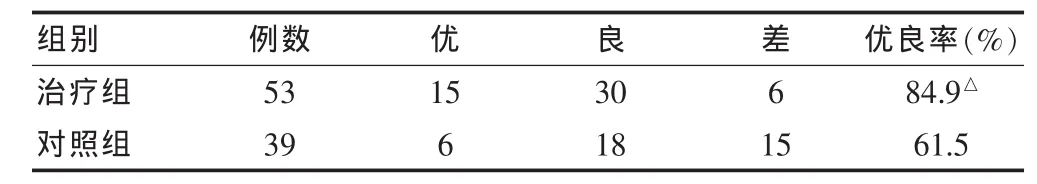
表1 兩組臨床療效比較(例)
表2 兩組治療前后下肢疼痛評分比較(分,±s)

表2 兩組治療前后下肢疼痛評分比較(分,±s)
注:與本組治療前比較,#P<0.05;與對照組治療后比較,△P<0.05
治療組對照組53 39 4.12±0.52 4.05±0.45 1.28±0.35#△1.64±0.65#組別 例數 治療前 治療后
3 討論
極外側型腰椎間盤突出是臨床上較為特殊的一型,以往對其認識不充分而容易漏診。臨床分為椎間孔型和孔外型。極外側型腰椎間盤突出癥由于突出椎間盤組織位于椎間孔或椎間孔以外,與常見后外側型椎間盤突出癥累及下一序數神經根不同,本型病變常累及同序數的神經根。臨床癥狀與其突出大小往往不成比例,臨床表現主要以下肢持續疼痛為主,不能平臥,站立或行走時加重,和(或)下位神經根。本病確診有賴于影像學,包括CT、MRI。近年來的文獻報道也多集中于手術治療方面,手術操作對組織結構的損傷和破壞較大,手術無論經椎板或峽部外緣均有一定難度到達患處,若過多切掉小關節會影響脊柱穩定性,易造成腰椎術后穩定性差,并發癥多。由于腰神經根管的結構復雜,所以我們選擇CT引導下有利于精準操作,避免盲穿所帶來其他并發癥。
多年來臨床研究表明,對于大部分極外側腰椎間盤突出癥患者多數在發現時以是晚期,往往具有嚴重的癥狀及病理特征,因此多數需要通過手術進行治療[4],隨著研究的不斷深入,對于該類手術的方式和方法有很多種類型,每種類型都有其優勢和劣勢,并且隨著手術方式的不斷發展,各個缺點也在不斷的被彌補[5-6]。最早報道該類手術入路的是20世紀80年代的Watkins,該種方法可以在最大限度條件下減少對患者的骨組織造成的損傷,并且可以直接在直視的條件下進行突出髓核的摘除。隨后Ohara等[7]提出Watkins的方法對于快速尋找脫出的椎間盤組織效果不好,從而經過臨床研究發現脊神經后支作為一個手術入路可以快速地找到脊神經根和神經節,并且安全性更高。Ohara等[7]以及Porchet等[8]均通過橫突間入路治療極外側腰椎間盤突出癥,均取得了較好的效果,具有較高的優良率。因為通過橫突間入路單純切除椎間盤突出髓核,對患者造成的損傷較小,與其他手術入路相比,有各種明顯的優越性,因此逐漸成為該類手術方法中的首選方法[9-10]。
據報道臭氧和射頻消融治療椎間盤突出癥有效率在68%~79%之間[11],射頻尚無確切報道。臭氧治療腰椎間盤突出的主要機制:①即刻氧化作用:氧化髓核內的蛋白多糖,使髓核發生變性、壞死而萎縮,在降低椎間盤壓力的同時也改變了局部的血液循環,增加氧供應而改善癥狀。②抗炎作用:通過拮抗免疫因子釋放起到抗炎作用。③鎮痛作用,臭氧的強氧化作用能迅速使上述炎性介質失活而達到止痛作用[12];而且還可通過破損的纖維環彌散和擴散到椎管內或椎旁發揮作用。臨床發現隨時間延長其療效逐漸下降,推測可能與椎間盤減壓不徹底有關。
射頻消融其主要作用機制是將熱凝與消融相結合以去除部分髓核,從而減小髓核體積,毀損竇椎神經和局部熱效應發揮作用[13],以達到減壓治療目的,但作用范圍較局限;對盤源性腰椎間盤突出療效顯著,對非包容性突出則需甄別應用[14-16]。
在本病的臨床治療過程中我們發現臭氧盤內溶盤治療極外側型腰椎間盤突出癥療效不佳,其主要原因是盤內治療對突出于椎間孔內或椎間孔外的椎間盤組織的作用有限,經CT、MR復查發現突出物對神經根的卡壓的根本問題未解決。表1表明其優良率不足65%,據此,本研究采用在CT引導下射頻消融聯合臭氧治療,把重點放在椎間孔內外突出物的消融。依據極外側型突出不同的層面表現,在CT引導下選擇突出較大的層面;圍繞突出物內外穿刺針可靈活變換角度,繞過椎間關節而擴大視野。直接靶點射頻消融可使髓核內的壓力減低,椎間盤突出部分有效回縮,達到對椎間盤周圍組織如神經根、動脈、馬尾神經等的減壓目的[17],同時高溫可滅活炎性因子、改善局部水腫。結合臭氧強氧化,抗炎和鎮痛作用,可使蛋白多糖變性,髓核組織萎縮,從而迅速降低椎間盤壓力[18],可達到優勢互補的作用 。
本治療組的3個月優良率仍保持在84%以上,說明射頻和臭氧聯合應用療效明顯高于單純臭氧應用[19]。兩者比較差異有統計學意義(P<0.05),兩者聯合彌補了單一技術的不足,使椎間盤內減壓更徹底,擴大了經皮穿刺微創技術治療腰椎間盤突出癥的適應證,使以前需要手術的患者可以通過微創技術解決。但本組中效果不佳的6例中最終有3例仍選擇了手術,術后癥狀緩解顯著,說明對于神經根卡壓嚴重,或療效差的患者,手術仍是一種徹底治療的手段。
CT引導下射頻聯合臭氧治療極外側型腰椎間盤突出癥能確保穿刺達到理想位置,射頻部位準確、臭氧能夠達到理想的彌散狀態。其操作較開放手術安全,創傷小,準確,不影響脊柱穩定性,經濟負擔少,療效也較單純臭氧注射顯著提高,是治療極外側型腰椎間盤突出的一種新興手段,值得臨床推廣,但仍需掌握一定適應證。
[1]胡有谷.腰椎間盤突出癥[M].北京:人民衛生出版社,2001:217-225.
[2]Maroon JC,Kopitnik TA,Schulhof LA,et al.Diagnosis andmicrosurgical approach to far.Itlteral disc herelation in the hmbarspine[J].J Neurosurg,1990,72:378-382.
[3]滕皋軍.經皮腰椎間盤摘除術[M].南京:江蘇科學出版社,2000:89.
[4]孫鳳翔,張文祥,季祝永,等.極外側型腰椎間盤突出癥發病機理及診治探討[J].中國矯形外科雜志,2003,11(7):494-496.
[5]Garg M,Kumar S.Interlaminar discectomy and selective foraminotomy in lumbar disc hemination [J].J Orthop Surg,2001,9(2):15-18.
[6]Ozveren MF,Bilge T,Barut S,et al.Combined approach for far lateral lumbar disc hemiation[J].Neurol Med Chir(Tokyo),2004,44(2):118-123.
[7]Ohara LJ,Marshall RW.Farlaterallumbar disc herniation[J].J Bone Joint Surg(Br),1997,79(11):943-947.
[8]Porchet,Fankhauser H,de Triboletn.Extreme lateral lumbar disc herniation:clinical presentation in 178 patients[J].Acta Neurochir Wien,1994,127(3):203-209.
[9]Tessitore E,de Triboletn.Far-lateral lumbar disc herniation:the microsurgical transmuscular approach[J].Neurosurgery,2004,54(4):939-942.
[10]謝曉勇,李平生,郭文榮,等.經椎板側方手術入路治療極外側腰椎間盤突出癥[J].中國骨與關節損傷雜志,2005,20(5):352-353.
[11]Velio B.Oxygen-Ozone therapy:a critical evaluation[M].Dordrecht:Kluwer Academic Publishers,2002:241-324.
[12]肖越勇.合理選擇聯合介入技術使椎間盤突出癥微創治療達到個體化或間盤化[J].中國疼痛醫學雜志,2005,11:320.
[13]謝珺田,秀英,李祥俊.射頻消融術[J].山東醫藥,2005,45:63-64.
[14]Yung CC,Sang-Heon L,Darwin C.Intradiscalpressure study ofdiscdecompressionwithnucleo-plastyinhumancadavers[M].NewYork:Nass Meeting of the Americans Ⅱ,2002.
[15]Stanley CJ,Ronald CF,Jamie MB.Sixmonth fol-low-up on lumbar disc nucleoplasty in 45 patients[M].NewYork:Nass Meeting of the AmericansⅡ,2002.
[16]Lewis S.Percutaneous disc decompression using nucleoplasty[M].NewYork:Nass Meeting of the Americans Ⅱ,2002.
[17]佘遠舉,劉軍,張浩,等.射頻消融髓核成形術改善腰椎間盤突出癥患者癥狀效果評估[J].中國臨床康復,2005,9(18):154-157.
[18]俞志堅,何曉峰,楊波,等.醫用臭氧治療腰椎間盤突出癥:術后癥狀“反跳”的分析及處理[J].臨床放射學雜志,2004,23(10):897-899.
[19]Nakano N,Nakano T,Nakano K.Long term results of anterior extra peritoneal lumbar discectomy[J].Acta Orthop Belg,1987,53:290-292.

