電鍍污泥中銅和鎳的回收
王春花,曾佳娜,林瑞玲
(惠州學院 化學工程系,廣東 惠州 516007)
電鍍污泥是電鍍廢水處理過程中產生的固體廢棄物,含有大量的有價金屬如銅、鎳、鉻、鋅等,是一種廉價的二次可再生資源。從電鍍污泥中回收重金屬一直是國內外的研究熱點,眾多研究者對其展開了廣泛而深入的研究,主要的資源化利用方法有浸出法(包括氨浸法和酸浸法)[1-2]、焙燒—浸出法[3]、熔煉法[4]、焚燒法[5]和生物浸取法[6]等。上述研究成果在實際工業應用過程中存在工藝路線長、設備投資大、運行不穩定、易造成二次污染等問題。因此,我國的電鍍污泥中重金屬的資源化回收利用技術還處于小作坊式的處理階段。
本工作采用一套完整的綜合回收利用電鍍污泥的工藝路線,實現了電鍍污泥中銅和鎳的全面回收。
1 實驗部分
1.1 材料、試劑和儀器
電鍍污泥:廣東省惠州市某電鍍廠,污泥顏色為藍綠色,含水質量分數為74.19%,干泥的主要成分見表1。
硫酸、硫化鈉、氨水、氟化鈉、碳酸鈉:分析純;鐵粉:200目,分析純。實驗用水為去離子水。

表1 干泥的主要成分 w,%
722型可見分光光度計:上海精科實業有限公司;DF-101型集熱式磁力攪拌器:鞏義市予華儀器有限責任公司; PHS- 3B型精密酸度計:上海啟威電子有限公司。
1.2 工藝流程
回收電鍍污泥中銅和鎳的工藝流程見圖1。電鍍污泥用稀硫酸酸浸,酸浸液經沉淀得粗品銅,濾液再經凈化除雜、沉淀工藝制取硫酸鎳。

圖1 回收電鍍污泥中銅和鎳的工藝流程
1.3 實驗方法
1.3.1 酸浸
采用文獻[7]報道的方法,取100目的干污泥,按液固比為3加水攪拌均勻,常溫下邊攪拌邊加入一定量濃度為0.1 mol/L的硫酸,以(120±5)r/min的攪拌轉速在磁力攪拌器上攪拌1.5 h,過濾,取酸浸液測定各重金屬離子含量,計算金屬的浸出率。
1.3.2 銅鎳分離
文獻[8]報道了采用氨水分步沉淀法、硫化鈉選擇沉淀法和鐵粉置換法沉淀分離出電鍍污泥酸浸液中的銅和鎳,其中氨水分步沉淀法要求嚴格控制體系的酸度,實際操作難以控制,而硫化鈉選擇沉淀法和鐵粉置換法都能取得較好的沉淀效果。本工作分別考察了硫化鈉選擇沉淀法和鐵粉置換法分離酸浸液中銅和鎳的分離效果。并選擇分離效果較好的方法進行后續實驗。
取20 mL酸浸液,加入鐵粉或硫化鈉,一定溫度下攪拌反應一段時間。過濾,沉淀為粗品銅。測定濾液中鎳含量。
1.3.3 凈化除雜
由文獻[9]的報道可知,三價鉻的氫氧化物完全沉淀時的pH(5.6)低于鎳的氫氧化物初始沉淀pH(7.4),因此,可采用水解沉淀方法從溶液中選擇性地沉淀三價鉻,到達凈化除雜目的。
用氨水調節濾液pH至5.5~6.0,使溶液中的鐵、鉻生成金屬氫氧化物沉淀;然后將溶液溫度加熱至95 ℃,加入一定量的氟化鈉,攪拌60 min,溶液中的鈣和鎂離子生成氟化物沉淀;為加速溶液中生成的沉淀物沉降,加入適量的絮凝劑聚丙烯酰胺,常溫靜止60 min,過濾,得凈化液,測定凈化液中鐵、鉻、鈣、鎂的含量。
1.3.4 沉淀制取硫酸鎳
在85~90 ℃、攪拌轉速為100 r/min條件下,向凈化液中加入碳酸鈉溶液,攪拌反應4 h,直至溶液中無綠色,反應終點pH控制在8.0左右,然后靜置、過濾、洗滌、沉淀,制得堿式碳酸鎳。再用濃度為1 mol/L的硫酸溶解堿式碳酸鎳,控制終點pH為4.5,經蒸發濃縮、結晶后的產品即為粗品硫酸鎳。
1.4 分析方法
采用分光光度法測定溶液中銅離子[10];采用丁二酮肟分光光度法測定溶液中鎳離子[10]。溶液中其他金屬離子采用原子吸收分光光度法分析[10];按國標方法測定粗品銅和粗品硫酸鎳[11-12]。
2 結果與討論
2.1 酸浸
采用濃度為0.1 mol/L的硫酸做銅鎳污泥的酸浸實驗,酸浸實驗的最終pH應控制在1.5左右。若pH過低,則會影響后面的凈化除雜工藝中氨水的消耗及凈化效果;若pH過高,則會降低銅和鎳的浸出率。酸浸實驗結果見表2。由表2可知:在該酸浸條件下,銅和鎳的浸出效果好,浸出率都在98.5%以上,而其他金屬離子的浸出率相對較低。

表2 酸浸實驗結果
2.2 銅鎳分離
2.2.1 鐵粉置換法
2.2.1.1 置換時間對銅沉淀率和鎳損失率的影響
鎳損失率為銅鎳分離中鎳離子的沉淀量占酸浸液中鎳離子總量的質量分數。當常溫、鐵粉加入量(以理論需求量的倍數計)為3 倍時,置換時間對銅沉淀率和鎳損失率的影響見圖2。由圖2可見:當置換時間為30 min時,銅沉淀率在80%以上,鎳損失率可在10%以內。實驗選擇最佳置換時間為30 min。

圖2 置換時間對銅沉淀率和鎳損失率的影響
2.2.1.2 置換溫度對銅沉淀率和鎳損失率的影響
當鐵粉加入量為3 倍、置換時間為30 min時,置換溫度對銅沉淀率和鎳損失率的影響見圖3。由圖3可知,隨著置換溫度的升高,銅沉淀率和鎳損失率都升高。因此,從回收銅的經濟性和能耗成本考慮,置換溫度選45 ℃以下為宜。

圖3 置換溫度對銅沉淀率和鎳損失率的影響
2.2.1.3 鐵粉加入量對銅沉淀率和鎳損失率的影響
當置換溫度為30 ℃、置換時間為30 min時,鐵粉加入量(以理論需求量的倍數計)對銅沉淀率和鎳損失率的影響見圖4。由圖4可知,鐵粉加入量為1.2倍時,銅沉淀率在85%以上,而鎳損失率在10%左右。因此,鐵粉最佳加入量為1.2倍。
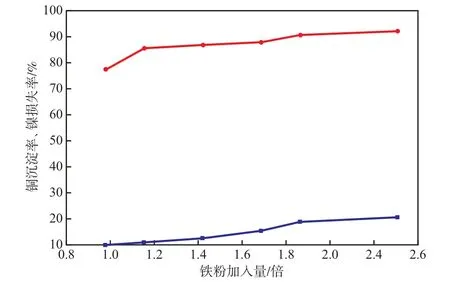
圖4 鐵粉加入量對銅沉淀率和鎳損失率的影響
2.2.2 硫化鈉選擇沉淀法
酸浸液中的銅、鎳和鋅離子都易與S2-反應生成沉淀,但各種金屬離子在溶液中的平衡濃度卻不相同。依據文獻[13]報道的溶度積進行計算,在pH為1.5時,銅、鋅、鎳的平衡濃度分別為6.774×10-17,2.668×10-3,3.44 mol/L。可見,銅和鋅的平衡濃度比鎳的要低得多。因此,可在溶液中加入適量S2-,使銅 、鋅與鎳分離,且銅的完全硫化沉淀pH也低于鎳開始沉淀的pH。可見,通過調節溶液pH及加入適量硫化鈉使銅離子和鋅離子選擇性沉淀,而鎳幾乎沒有損失,可實現銅和鎳的有效分離。所得沉淀用稀鹽酸洗滌,可將其中的硫化鋅與硫化銅溶解分離。
2.2.2.1 硫化鈉加入量對銅沉淀率和鎳損失率的影響
當常溫、硫化鈉沉淀時間為60 min時,硫化鈉加入量(以理論需求量的倍數計)對銅沉淀率和鎳損失率的影響見圖5。

圖5 硫化鈉加入量對銅沉淀率和鎳損失率的影響
由圖5可知,隨著硫化鈉加入量的增大, 銅沉淀率也不斷增大, 當硫化鈉加入量達到理論量的1.2倍時,銅沉淀率達到98%以上,且鎳的損失率都比較低。因此, 從成本考慮,選擇硫化鈉加入量為理論加入量的1.2倍。
2.2.2.2 硫化鈉沉淀時間對銅沉淀率和鎳損失率的影響
當常溫、硫化鈉加入量為1.2倍時,硫化鈉沉淀時間對銅沉淀率及鎳損失率的影響見圖6。由圖6可知,當硫化鈉沉淀時間達到30 min時, 銅沉淀率達到98% 以上,反應繼續進行, 銅沉淀率反而略有減小;此外,沉淀時間對鎳損失率基本沒有影響。因此,選擇最佳的硫化鈉沉淀時間為30 min。

圖6 硫化鈉沉淀時間對銅沉淀率和鎳損失率的影響
2.2.2.3 硫化鈉沉淀溫度對銅沉淀率和鎳損失率的影響
當硫化鈉加入量為理論需求量的1.2倍、硫化鈉沉淀時間為30 min時,硫化鈉沉淀溫度對銅沉淀率和鎳損失率的影響見圖7。

圖7 硫化鈉沉淀溫度對銅沉淀率和鎳損失率的影響
由圖7可知,硫化鈉沉淀溫度對銅沉淀率的影響較大。提高溫度有利于加快反應速率,溫度越高,銅沉淀率也越高;當溫度達到60 ℃時,銅沉淀率達98%以上,之后曲線變化不大,同時, 反應溫度對鎳的損失率影響較小,鎳損失率基本控制在5%左右;因此, 選擇硫化鈉沉淀溫度為60 ℃。
2.2.3 小結
綜上可知:采用鐵粉置換法分離酸浸液中的銅和鎳,銅沉淀率只能達到85%左右,若要進一步提高銅沉淀率,鎳的損失率也會進一步提高;而采用硫化鈉選擇沉淀法,銅的沉淀率可以達到98%以上,而鎳的損失率也能控制在5%左右。綜合考慮,本實驗采用硫化鈉沉淀法分離酸浸液中的銅和鎳,最優操作條件為:硫化鈉加入量1.2倍,硫化鈉沉淀溫度60 ℃,硫化鈉沉淀時間30 min。
在上述實驗條件下,取20 g干電鍍污泥,進行酸浸及硫化鈉銅鎳分離實驗,得到粗品銅2.91 g。經計算可知,銅的回收率在90%以上。
2.3 凈化除雜
凈化除雜實驗結果見表3。由表3可見:凈化除雜后,凈化液中鐵、鉻等雜質的質量濃度非常小,凈化效果較好。

表3 凈化除雜實驗結果 ρ,g/L
2.4 沉淀制取硫酸鎳
在凈化液中緩慢加入碳酸鈉溶液,生成堿式碳酸鎳沉淀,洗滌后再用硫酸重新溶解堿式碳酸鎳,溶液經蒸發濃縮后冷卻結晶得到粗品硫酸鎳。粗品硫酸鎳主要化學成分見表4。由表4可見:粗品硫酸鎳中,硫酸鎳含量在18%左右,鎳的回收率達80%以上,達到了工業一級標準[12]。

表4 硫酸鎳的主要化學成分 w,%
3 結論
a)采用硫酸酸浸—硫化沉銅—凈化除雜—沉淀制取硫酸鎳工藝從電鍍污泥中回收銅和鎳,銅的回收率可達90%以上,粗品硫酸鎳中硫酸鎳質量分數為18%,鎳的回收率達80%以上。
b)硫化鈉選擇沉淀法分離電鍍污泥酸浸液中銅和鎳的效果更好,可使銅的沉淀率達98%以上。最優操作條件為:硫化鈉加入量1.2倍,硫化鈉沉淀溫度60 ℃,硫化鈉沉淀時間30 min。
[1] 祝萬鵬,楊志華. 溶劑萃取法回收電鍍污泥中的有價金屬[J]. 給水排水,1995,21(12):16-18.
[2] Silva J E,Soares D,Paiva A P,et al. Leaching behaviour of a galvanic sludge in sulphuric acid andammoniacal media[J]. J Hazard Mater,2005,121:195-202.
[3] Rossini G,Bemardes A M. Galvanic sludge metals rere covery by pyrometallurgical and hydrometallurgical treat ment[J]. J Hazard Mater,2006,13l(1/2/3):210-216.
[4] 李紅藝,劉偉京,陳勇. 電鍍污泥中銅和鎳的回收和資源化技術[J]. 中國資源綜合利用,2005,23(12):7-10.
[5] Espinosa D C R,Tenório J A S. Thermal behavior of chromium electroplating sludge[J]. Waste Manage,2001,21(4):405-410.
[6] Diane Fournier,Réal Lemieux,Denis Couillard.Essential interactions betweenThiobacillus ferrooxidansand heterotrophic microorganisms during a wastewater sludge bioleaching process[J]. Environ Pollut,1998,101(2):303-309.
[7] 王春花,曾文榮,張喜斌. 電鍍污泥中重金屬最佳浸出條件的實驗研究[J]. 電鍍與環保,2011,31(2):36-39.
[8] 楊春,劉定富,龍霞. 電鍍污泥酸浸出液中銅和鎳分離的研究[J]. 無機鹽工業,2010,42(8):44-46.
[9] 郭學益,石文堂,李棟,等. 從電鍍污泥中回收鎳、銅和鉻的工藝研究[J]. 北京科技大學學報,2011,33(3):328-333.
[10] 原國家環境保護總局《水和廢水監測分析方法》編委會. 水和廢水監測分析方法[M]. 4版. 北京:中國環境科學出版社,2002:286-396.
[11] 大冶有色金屬集團控股有限公司,中國有色金屬工業標準計量質量研究所. GBT3884.13—2012 銅精礦化學分析方法[S]. 北京:中國標準出版社,2012.
[12] 中科銅都粉體新材料股份有限公司、中海油天津化工研究設計院、吉林吉恩鎳業股份有限公司.HG/T2824—1997 工業硫酸鎳[S]. 北京:化學工業出版社,1997.
[13] 楊宏孝. 無機化學[M]. 3版. 北京:高等教育出版社,2002:204-359.

