SPGR-T2*WI 序列對顱內出血的MRI 診斷價值
衣慧靈 劉蘭祥 齊曦明 劉永利
隨著MR 掃描技術的發展和序列應用,MRI 可以取代CT診斷早期腦出血已被多數學者證實[1],且MRI 可以提供比CT更全面的信息,但是在常規MR 序列中腦出血的信號變化復雜。本文將擾相梯度回波序列與常規MR 掃描序列各期信號相比較,探討不同序列對各期顱腦出血的診斷價值,明確顱內出血MRI 的最佳序列以及MR 診斷出血的優缺點,探討腦血管病MRI 一站式診斷的可行性。
1 資料與方法
1.1 一般資料腦出血患者18 例,其中男10 例,女8 例;年齡39 ~78 歲,中位年齡61 歲。腦出血病例共38 個病灶,位于大腦半球的31 個灶,位于腦干2 個灶,位于小腦7 個病灶。出血病例CT 和MR 檢查相隔不超過1 d。MR 檢查應用GE Signa EXCIIE 1.5T 超導型MR 機,8 通道頭線圈。常規行以下序列掃描:SPGR-T2* WI、T1WI、T2WI、T2-FLAIR、DWI;ESWAN 及CT,具體參數見表1。
1.2 設備及掃描方法
1.2.1 MR:GE Signa EXCIIE 1.5T 超導型MR 8 通道頭線圈。常規行以下序列掃描SPGR-T2* WI、T1WI、T2WI、T2-FLAIR、DWI,ESWAN。見表1。
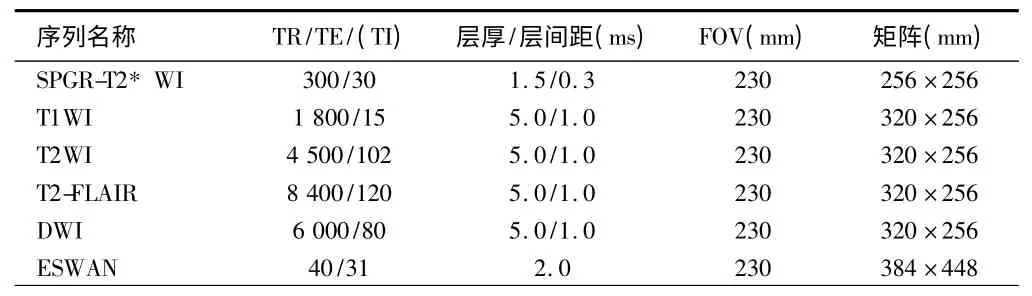
表1 具體序列掃描參數及方法
1.2.2 CT:GE64 排螺旋CT(Light speed VCT SYS#ct99)行常規掃描。
2 結果
出血在SPGR-T2*WI 序列及CT 的征象 38 例病例中有5 例患者同時有兩處及兩處以上出血灶,其中5 處位于腦干和小腦等位置且直徑小于1 cm。其中,急性Ⅰ期有3 例患者4 處病灶;急性Ⅱ期有2 例患者4 處病灶。急性期病灶SPGR-T2*WI 序列呈不均勻低信號影,小病灶(直徑小于10 mm 的微小出血灶)呈均勻低信號影,外周可見不規則片狀水腫帶。CT 示:除1 個小病灶(直徑小于10 mm 的微小出血灶)未在CT 掃描中發現,余急性期出血灶的CT 表現為圓形或不規則形、均勻高密度灶,CT 值均值約70 Hu。亞急性期有2 例患者3 處病灶,直徑小于25 mm,中心混雜低外周環形高信號影最外周低信號影,亞急性期13 例患者19 個病灶,直徑大于25 mm,腦內血腫在擾相梯度回波T2*WI 序列上有三層組成,中心為略低信號,范圍隨時間延長逐漸增大,邊緣在該序列顯示為細線狀或窄帶狀低信號。中央及邊緣低信號之間可見線條狀擾相梯度回波T2*WI 序列呈高信號,該信號寬度隨時間延長逐漸增寬(圖2)。CT 示:高密度影范圍較MR 所示范圍小,CT 值均值約為56 Hu 左右。慢性期2 個患者6 個病灶,SPGR-T2*WI 序列上中心混雜略高信號影外周明顯低信號影,CT 僅能發現1 個病灶,且該病灶血腫吸收中心囊腔形成,余小病灶吸收消失。見表2,圖1、2。
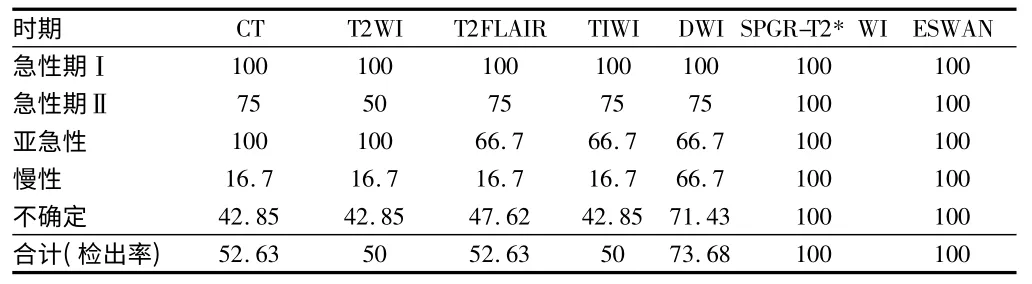
表2 CT 及核磁對出血及鈣化病變的檢出率
3 討論
腦出血約占腦卒中患者的20%,其與腦梗死的兩者具有相類似的中樞神經系統功能障礙的臨床表現,但是兩者的病因、病理變化及治療措施有著很大的區別,CT 對于早期腦梗死的診斷卻遠不及MRI,而腦卒中中腦梗死的發病率更是腦出血的既造成了患者經濟上的負擔,又延誤了最佳的治療時間。由于常規MR 序列中腦出血的信號變化復雜,腦出血如能得到及早診斷并能鑒別于腦梗死,明確其分期可為神經內、外科確定治療方案提供足夠信息,簡化患者就診程序、節省醫療開支,實現腦卒中的一站式檢查有著重要的意義[2]。
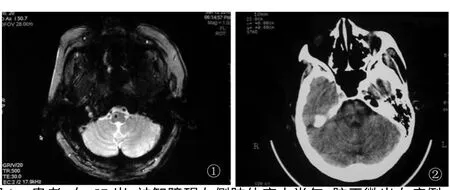
圖1 患者,女,57 歲,神智障礙左側肢體麻木半年,腦干微出血病例①SPGR-T2*WI(TE=30)可顯示腦干可見類圓形低信號影,直徑小于10 mm;②接近同層CT 未見確切異常
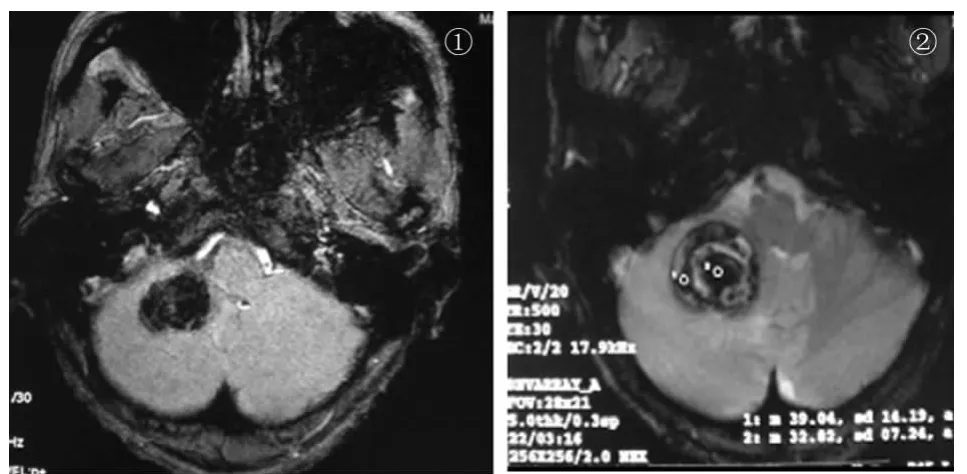
圖2 患者,男,51 歲,右側小腦半球出血,直徑大于25 mm 的較大亞急性期腦出血病灶分層圖例①為出血金標準ESWAN;②SPGR-T2*WI 圖像TE=30 ms
SPGR-T2*WI 較CT 出血發現率更高:擾相梯度回波T2*WI 序列對于血腫的總發現率為CT 的1.9 倍。38 例病例中有5 例患者同時有兩處及兩處以上出血灶,CT 能顯示1 ml 以上的血腫[3]。擾相梯度回波T2*WI 序列對血腫范圍顯示始終較CT 掃描更清晰,尤其是顯示小出血灶更敏感[4,5]。從表2 可見T2*序列在診斷急性腦內血腫中的敏感性和CT 相同,急性期達到100%。但對于亞急性后期及慢性期CT 對于出血的檢出率明顯的低于T2*WI。分析其原因CT 可以診斷濃度較高(>70%)的血腫,但是如果血液濃度≤50%。CT 就顯示能力明顯下降[6],且隨著吸收期出血灶的密度減低,CT 發現更加困難。CT 對于出血量小于1 ml 的病灶往往難以顯示,而SPGRT2*WI 序列可以顯示微小出血灶。
SPGR-T2*WI 較CT 對不同部位的出血檢出更好:大腦半球的同直徑范圍病灶數目未見明顯差異,而腦干、小腦等部位出血,其中5 處同直徑范圍的位于腦干和小腦等出血灶CT 上未能發現,分析可能與CT 偽影影響[7]及出血量少有關,SPGRT2*WI 序列比CT 檢查更有優勢,von Kummer 等[8]甚至認為MRI 將取代CT 成為診斷急性腦內血腫金標準。
SPGR-T2*WI 較CT 對不同時期出血的檢出更具優勢:急性期除急性期Ⅱ期一個病灶因直徑小于10 mm,CT 未見顯示余均顯示明確。亞急性期病灶,SPGR-T2*WI 序列中心混雜低外周環形高信號影最外周低信號影,但CT 示高密度影范圍較MR 所示范圍小,考慮由于顱內出血發生后,血液的MR 表現演變復雜,最早是由氧合血紅蛋白演變為去氧血紅蛋白,后者為順磁性分子,由于磁敏感效應(magnetic susceptibility effects)會造成信號缺失,特別是在SPGR-T2*WI 上更為明顯[9]。最早期的磁敏感性的改變可能是由于去氧血紅蛋白的順磁性效應。大部分學者認為去氧血紅蛋白的轉變是從出血后幾小時到幾天開始發生,去氧血紅蛋白造成的磁場不均勻引起病灶低信號外周范圍較CT 顯示的高密度灶范圍大的原因[10]。而對于直徑>25 mm 較大病灶的腦出血,在擾相梯度回波T2*WI 序列上形成的分層現象,分析其原因血腫內紅細胞內脫氧血紅蛋白向高鐵血紅蛋白轉化,高鐵血紅蛋白具有強順磁性,低信號位于血腫的核心;而位于血腫邊緣的紅細胞部分崩解,由此推測此期出現的,位于邊緣低信號及核心低信號之間的線狀高信號為細胞液內水成分,隨時間延長紅細胞崩解增多,血腫開始逐漸液化部分被吸收,邊緣低信號及核心低信號之間的高信號帶逐漸增寬,細胞外游離的高鐵血紅蛋白逐漸被巨噬細胞吞噬,逐漸轉化成含鐵血黃素沉積于邊緣,這也可以解釋后期出血邊緣低信號成因[10],也可作為較大亞急性期血腫一個較特征性改變。部分直徑<10 mm 的微出血因病灶吸收在慢性期CT 未見顯示,且部分病灶囊變,因而在CT 上僅顯示6 個病灶中的1個病灶。SPGR-T2*WI 序列與金標準ESWAN 序列均為梯度回波序列,慢性期出血吸收后后的含鐵血黃素因有較強的順磁性,因而即使吸收后少量存在,也能造成周圍小磁場明顯變化,因此形成的低信號影則顯示了微量的陳舊出血的存在。
此外,對于其他序列DWI 是較其他序列顯示出血較敏感的序列,38 個病灶其可以明確顯示的有28 例,并且有1 例患者腦出血并發急性腦梗死,DWI 提供了更為豐富的信息,但是DWI 的空間分辨率較差,在提供信息的基礎上,不同時期的出血DWI 信號復雜,在實際工作中必須結合常規及其他掃描序列尤其是擾相梯度回波序列才能作出可靠診斷。另外T2-FLAIR 對于蛛網膜下腔出血的發現也有較重要的意義,66.3%的蛛網膜下腔出血的患者在T1WI、T2WI、CT 無明顯變化,而在T2-FLAIR 序列上呈高信號,并對其位置也能明確判斷,這一點與以往其他學者的研究相符[11]。通過臨床38 個腦出血病灶分析可見MRI 各序列對診斷急性腦內血腫的敏感性和CT 檢查相當,而MR 各序列中以SPGR-T2*WI 序列的發現率與金標準ESWAN 最為接近,對于其他時期的小病灶特別是腦干小腦位置的微出血病灶GRET2*WI 序列較CT 更是有明顯的優勢。SPGR-T2*WI 序列可以在中、低場強機上使用,應用面廣,適用于所有的MR 機。另外掃描SPGR-T2*WI 序列較ESWAN掃描時間短,無需繁雜的后處理,也是其優勢,為實現腦卒中的快速一站式診斷奠定了基礎。
本研究的局限性在于,資料為小樣本,如果繼續擴大樣本量,減少誤差,搜集更多的中、低場強機的出血病灶CT 的結果比較將更有益于本課題的研究。梗死后出血及復雜血腫的SPGR-T2*WI 序列變化規律與CT 比較還有待于進一步的深入研究。
1 Linfante I,Llinas RH,Caplan LR,et al.MRI features of intracerebral hemorrhage within 2 hours from symptom onset.Stroke,1999,30:2263-2267.
2 陳星榮,沈天真主編.中樞神經系統計算機體層攝影(CT)和磁共振成像(MRI).第1 版.上海:上海醫科大學出版社,1992.345-346.
3 Chakeres DW,Bryan RN.Acute subarachnoid hemorrhage:in vitro comparison of magnetic resonance and computed tomography.AJNR Am J Neuroradiol,1986,7:223-228.
4 Viswanathan A,Chabriat H.Cerebral microhemorrhage.Stroke,2006,37:550-555.
5 Sorimachi T,Ito Y,Morita K,et al.Microbleeds on gradient-echo T2(*)-weighted MR images from patients with multiple simultaneous intracerebral haemorrhages.Acta Neurochir(Wien),2007,149:171-176,176-177.
6 Noguchi K,Ogawa T,Inugami A,et al.Acute subarachnoid hemorrhage:MR imaging with fluid-attenuated inversion recovery pulse sequences.Radiology,1995,196:773-777.
7 袁哲星,劉文,蔡宗堯,等.小腦出血的CT、MRI 診斷與臨床.中國醫學影像技術,2001,17:415-416.
8 von Kummer R.MRI:the new gold standard for detecting brain hemorrhage.Stroke,2002,33:1748-1749.
9 Perl JN,Tkach JA,Porras-Jimenez M,et al.Hemorrhage detected using MR imaging in the setting of acute stroke:an in vivo model.AJNR Am J Neuroradiol,1999,20:1863-1870.
10 王巖,崔冰.各期別腦內血腫在高場強磁共振EPI-FE-T2*WI 序列的演變規律.醫學影像學雜志,2005,8:614-631.
11 郎寧,韓鴻賓,裴新龍.急性顱內出血的MRI 診斷價值與序列優化.中國醫學影像技術,2004,7:989-992.

