巨大淋巴結增生癥的CT診斷
齊力
垂楊柳醫院 放射科,北京100022
巨大淋巴結增生癥(Castleman Disease,CD),是一種少見的淋巴組織異常增生性疾病。由于該病少見,對其影像學表現認識不足,術前易誤診為胸腺瘤、淋巴瘤、結節病、淋巴結轉移瘤或淋巴結結核等疾病。有鑒于此,筆者回顧性分析了有較完整資料,經手術及病理證實的CD 24例,并結合文獻討論該病的CT表現特點,旨在提高對本病的認識,減少誤診。
1 材料和方法
1.1 一般資料
收集2008年1月~2012年12月期間的CD病例共24例,其中男11例,女13例,年齡17~67歲,平均35歲。24例患者均接受了CT檢查。病理結果:局限型透明血管型CD 23例、彌漫型CD 1例。
局限型透明血管型CD的臨床表現:有支氣管炎癥狀者5例、聲音嘶啞者1例、干咳和痰中帶血者1例、腹部有逐漸增大的無痛性腫物者9例、無明顯不適者7例。1例彌漫型者呈現貧血、體重下降、發熱、肝脾增大、胸腔積液和表淺淋巴結腫大等全身性癥狀。實驗室檢查:血沉增快12例(25~58 mm/h)、血免疫蛋白異常者11例。其中免疫球蛋白IgG增高2例(18.0~21.4 g/L),免疫球蛋白IgA增高1例(4.37 g/L),血糖增高2例(31.4 mmol/L),肝腎功能異常2例。
1.2 檢查方法
采用美國GE公司16排螺旋CT。矩陣512×512,管電壓80~120 kV,管電流280~300 mA,常規采取層厚、層間距2.5 mm掃描。全部患者均行CT平掃和增強掃描,部分病例還同時做病灶區薄層掃描和三維重建。造影劑劑量選擇:1.5~2.0 mL/kg,或按體質指數(BMI=體重/身高2)比例給藥。采用靜脈團注非離子型對比劑(300 mgI/mL優維顯100 mL ,流率為2.5 mL/s)。掃描和延遲時間為:① 腹部:動脈期25~30 s,靜脈期65~70 s;② 胸部:動脈期18~23 s,實質期45~50 s。掃描結束后記錄以下內容:① 腫塊影像學表現:病變部位、形態大小和數量、密度、邊緣、強化程度、鈣化的分布和類型、有無出血和壞死囊變,以及周圍結構是否受壓或受浸潤等;② 手術所見和病理學特征。
2 結果
(1)11例胸部CD中有10例為局限型,位于前縱隔的3例、中縱隔的2例、后縱隔的3例、前中縱隔的1例、肺門處1例。病變表現為縱隔或肺門處圓形、類圓形或分葉狀較大的單發軟組織密度腫塊影,邊界多清楚銳利,直徑3~15 cm,平均5.5 cm。胸部CT平掃病變密度較均勻者9例;病變密度不均勻伴有中央區分支狀鈣化者1例。
CT平掃時CT值約32~62 HU,平均43 HU左右(圖1)。CT增強掃描時,有7例動脈期時病灶內部呈基本均勻的顯著強化,有3例呈非均勻性強化。CT值可高達102~206 HU,平均約138 HU左右(圖2)。延遲期仍持續強化(圖3),CT值約72~137 HU,平均96 HU左右。5例腫物周圍和/或外帶區可見增粗的滋養血管影。4例的病灶與周圍結構如血管、胸膜或氣管關系密切。1例有氣管受壓移位,但術中均較容易分離。這10例術前影像學診斷僅4例正確,其余分別誤診為胸腺瘤、結節病、淋巴瘤、淋巴結核和神經源性腫瘤等。
11例胸部CD中另有1例為彌漫型CD,位于中后縱隔。CT表現為中后縱隔內由多個大小不等的淋巴結融合而成的較大軟組織腫塊,大小約13 cm×12 cm×5 cm ,雙側少量胸腔積液、腹水。平掃CT值約78 HU,增強掃描動脈期不均勻性顯著增強,CT值約113 HU,延遲期增強仍較明顯。本例術前影像學誤診為淋巴瘤。

圖1 病例1左前上縱隔見5.0 cm×5.5 cm×7.2 cm大小的軟組織腫塊,邊緣銳利、密度均勻、腫塊周圍血管脂肪間隙存在,平掃CT值45.5 HU。
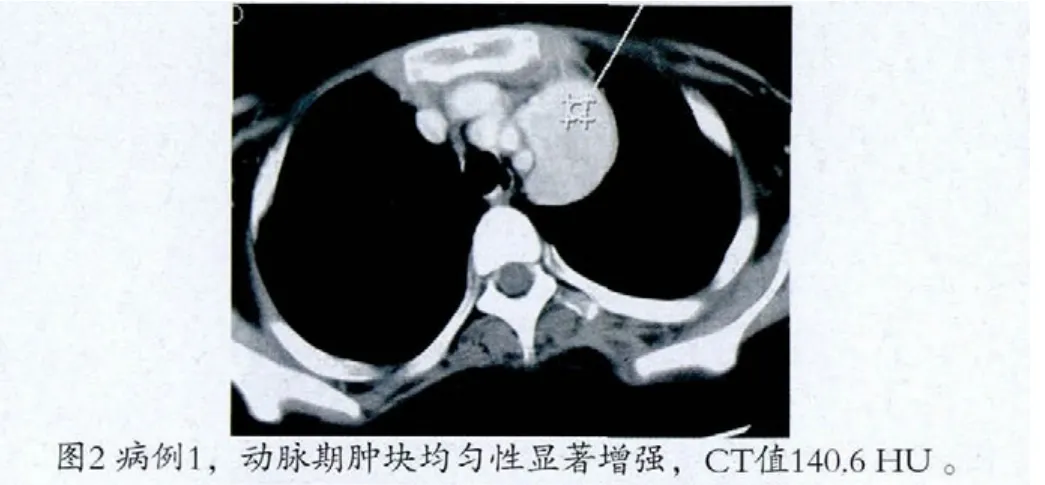

圖3 病例1,CT三維重建顯示延遲期腫塊持續增強,密度欠均勻,CT值102 HU。術前診斷:左前上縱隔占位病變;病理診斷:左前中上縱隔透明血管型CD。
(2)13例腹部CD在CT上多表現為類圓型的單發較大軟組織腫塊,直徑約5~15 cm,平均6.5 cm。邊緣清楚或有輕度分葉狀。病變位于腹膜后者8例、位于腸系膜根部者2例、位于盆腔者3例。
CT平掃8例顯示病變密度基本均勻,CT值38~58 HU,平均46 HU左右(圖4);5例密度不均伴有中央區分支狀或斑塊狀鈣化(圖4),占38%(5/13)。CT增強掃描動脈期顯示病變呈不同程度的基本均勻的明顯強化(圖5),CT值114 ~196 HU,平均136 HU左右,接近腹主動脈。延遲期病灶仍持續強化(圖6),CT值70~122 HU,平均92 HU左右。
局限型CD23例,占95.8%(23/24例),在CT像上均未見到壞死或出血等變化。

圖4 病例2 CT平掃:左降結腸后方有一直徑約6 cm的類圓形軟組織腫塊,邊緣不規則呈分葉狀,CT值48 HU,病灶中央可見分支狀鈣化,未見囊變壞死或出血等改變。

3 討論
CD是一種界于良、惡性之間的不典型淋巴結增生。組織學上分為透明血管型、漿細胞型及界于兩者間的混合型[1]。1985~1995年Weisenburger和Mccarthy等[2-3]將CD分為局限性和彌漫性2種類型,其中局限性所占比例較大[4]。前者呈良性特征,臨床常表現為無明顯癥狀的孤立軟組織腫塊,病理上96%為透明血管型,手術切除后預后良好。后者呈惡性表現,常累及多個器官且全身癥狀明顯,如發熱、盜汗、體重下降、肝脾大、胸腹水和血液系統異常等,病理學上均為漿細胞型。治療以放、化療和免疫抑制為主,預后不良。CD可以獨立存在,也可以伴發高球蛋白血癥、POEMS綜合征(一種與漿細胞病有關的多系統病變)等其他疾病。
巨大淋巴結增生癥的發生部位據統計胸部約60%~70%、頸部約占14%、腹部約占11%、余為其他部位[5-6]。發生在胸腔內時,多沿氣管支氣管淋巴鏈分布,好發部位依次為前縱隔、肺門、后縱隔,罕見于肺。
發生在腹腔和后腹膜者,腫瘤多沿腸系膜根部或后腹膜的淋巴鏈分布,呈生長緩慢的孤立結節或腫塊。
X線胸片可顯示CD腫塊的部位和大致形態,但對診斷缺乏特異性。常表現為邊緣清楚的球形或分葉狀腫塊,類似于胸腺瘤、淋巴瘤和神經源性腫瘤的表現。位于中縱隔和肺門者可致鄰近氣道受壓移位。腫塊可有斑狀、棉絮狀鈣化,本組有1例即有此種表現。本病常無臨床癥狀,多為偶然發現,本組11例胸部CD均為常規X射線胸部檢查時發現,且均誤診。
本組資料顯示,CT掃描能清晰顯示CD病變的部位、形態、數量、鈣化。增強CT掃描對CD的診斷和鑒別診斷具有實用價值。根據文獻[7-8]報道和本組資料的情況來看,CD的CT表現與其組織病理學特征密切相關,具有一定特點。
本組病例的特點是:均發生于縱隔、肺門區、腹膜后、腸系膜旁、盆腔等淋巴結豐富的特定部位。CT掃描均表現為腹膜后軟組織影[9],表現為圓形、類圓形或分葉狀孤立較大軟組織腫塊影、直徑約4~15 cm、呈中等密度、多數密度基本均勻、境界清楚銳利。
部分病例病灶中央區的斑塊狀、分支狀鈣化可看作是透明血管型CD病灶的一種特征性表現,24例CD患者中有4例于病灶中央區出現了分支狀、斑塊狀鈣化。鈣化的發生率約為16.7%(4/24例),明顯高于文獻報道的5%~10%的CD腫塊鈣化發生率[5]。
CT增強掃描對CD的診斷和鑒別診斷具有較高的實用價值,有一定的特征性,表現為動脈期顯著強化,腫塊強化峰值與胸腹主動脈強化程度相類似,CT值超過動脈CT值的2/3[10-12]。大多數腫塊表現為動脈期基本均勻的顯著強化和延遲期的持續強化。本組病例占95.8%(23/24例)的病例有如此表現,其CT值由平掃時的平均45 HU左右顯著增加到動脈期時的平均137 HU左右,延遲期時平均為94 HU左右。它表明腫塊的血供非常豐富,這與透明血管型CD具有較多的供養血管、病理性血管異常增生、毛細血管明顯擴張等因素有關。
本組彌漫型CD1例,增強掃描時動脈期呈現不均勻性明顯強化,CT值由平掃時的78 HU左右增高為113 HU左右,延遲期仍維持了較高水平的強化。
局限型CD的另一個特征是病灶內極少伴有出血和壞死灶。本組23例局限型CD,最小者直徑約3.0 cm,最大者直徑約為15 cm,CT掃描檢查均未見瘤灶內有出血和壞死灶,占100%(23/23例)。病灶較大而內部無出血或壞死,此點在其他類型的腫塊中比較少見,可能與其血供豐富和淋巴濾泡樣組織不易壞死的特性有關。
CD在CT上一般表現為富血管性病變,應與以下疾病相鑒別:① 縱隔內異位化學感受器瘤,與局限型CD較難區分,它同樣有豐富的擴張扭曲的血管。主要應從部位上鑒別,它常常沿著主動脈生長,而CD則按淋巴鏈分布;② 異位嗜鉻細胞瘤,無論發生在胸還是腹膜后,它常與大血管毗鄰。病灶易壞死囊變,雖然有強化,但密度或信號常不均勻,且臨床上有異常波動的惡性高血壓表現。實驗室檢查尿中兒茶酚胺及代謝產物VMA(3-甲氧—4-羥苦杏仁酸)升高。而CD一般無囊變壞死改變;③ 腸系膜淋巴結結核,形成的腫塊邊界多不清楚,增強掃描時腫塊一般為不規則邊緣強化,中心常可見壞死區,沒有延遲強化的特點,這些均與CD不同;④ 淋巴瘤,無論是動脈期還是延遲掃描其強化程度均較輕,明顯不同于CD。且淋巴瘤以多發居多,而CD以單發居多。
綜上所述,CT平掃加增強掃描有助于對CD的明確診斷和鑒別診斷,CD腫塊以動脈期顯著強化和延遲期的持續強化為特征性表現。胸、腹部局限型CD則以較大孤立性無壞死、無出血的腫物均勻性明顯強化、有時伴有病灶中央分支狀鈣化為特征。彌漫型CD的影像學表現復雜多樣,確診主要依靠病理和免疫組織化學檢查。
[1]王亮春,卜定方,陳喜雪,等.伴發Castle man病的副腫瘤性天皰瘡發病機制研究[J].中華皮膚科雜志,2004,11(1):38-40.
[2]Weisen burger DD,Nathwani BN,Winbeng CD,et al.Multicentric angiofollicular lymph node hyperplasia:a clinicopathologic study of 16 cases[J].Hum Pathol,1985,16(2):162-172.
[3]Mc Carthy MJ,Vukelja SJ,Banks PM,et al.Angiofollicular lymph node hyperplasia(Castleman's disease)[J].Cancer Treat Rev,1995,21(4):291-310.
[4]豐瑯,田野,呂文成,等.腹膜后Castleman病:附3例報告[J].現代泌尿外科雜志,2009,14(1):35-38.
[5]Mc Adams HP,Christenson MR,Fishba ck NF,et al.Castleman disease of the thorax:radiologic features with clinical and histopathologic correlation[J].Radiology,1998,209(10):221-228.
[6]Anagnostou D,Harrison Cv.Angiofollicular lymph node hype rplasia[J].Clin Pathol,1972,25(2):306-312.
[7]Kim TJ,Han JK,Kim YH,et al.Castle man disease of the abdomen imaging spectrum and clinicopathologic correlations[J].Computer Assist Tomography,2001,25(2):207-214.
[8]Libson E,Fields S,Strauss S,et al.Widespread Castleman,s disease:CT and US findings[J].Radiology,1988,166(3):753-755.
[9]霍紅軍,張杰,劉繼東,等.腹膜后巨大淋巴結增生癥的診療探討[J].中國醫師進修雜志,2010,33(26):66-68.
[10]彭澤華,蒲紅,白林,等.血管濾泡性淋巴結增生癥的影像擘表現與臨床病理特點[J].臨床放射學雜志,2009,28(2):242—246.
[11]鄒玉堅,鄭曉林,陳塑,等.局限型巨大淋巴結增生癥的影像學表現[J].中國CT和MRI雜志,2011,9(6):69-72.
[12]Libson E,Fields S,Strauss S,et al.Widespread castlemandisease:CT and US findings[J].Radiology,1988,166(3):753-755.

