肝細胞生長因子在TRAIL促進原代肝星狀細胞凋亡中的作用
張君紅 姜海行 覃山羽 孟云超 寧 琳 楊 文 沈妍華
(廣西醫科大學第一附屬醫院老年消化內科,廣西 南寧 530021)
研究表明肝纖維化的中心環節是活化的肝星狀細胞(HSCs)合成大量的細胞外基質〔1〕。前期研究表明骨髓間充質干細胞旁分泌肝細胞生長因子(HGF),能促進HSCs-T6的凋亡,可能與下調RhoA的表達有關〔2〕;而活化的HSCs系LX-2可以通過腫瘤壞死因子相關凋亡誘導配體(TRAIL)TRAIL-R2途徑凋亡〔3〕。本研究發現HSC-T6與原代HSCs的生物學特性有明顯區別,因原代HSCs更接近人體的生理狀態,選擇原代HSCs作為研究對象對臨床的應用更具有指導意義,而HGF及TRAIL在原代HSCs中的作用未見報道。本研究探討HGF在TRAIL促進原代HSCs凋亡中的作用。
1 材料與方法
1.1 材料 原代HSCs由廣西壯族自治區人民醫院張國博士惠贈。主要試劑及儀器:HGF、TRAIL蛋白(Peprotech公司);低糖DMEM培養基(Gibco公司);兔抗鼠DR5多克隆抗體(Abcam公司);優質胎牛血清(Hyclone公司);Annexin-V-FITC/PI雙染凋亡試劑盒(Biovision公司);熒光倒置相差顯微鏡(Zeiss公司)。
1.2 方法 原代HSCs復蘇、傳代與活化鑒定:從液氮灌中取出大鼠原代HSCs,37℃凍融后傳代使用,于L-DMEM培養液(15%胎牛血清)、37℃,5%CO2培養箱中培養,2~3 d后80%~90%的細胞鋪滿瓶底即可再次傳代,倒置相差顯微鏡下觀察活體細胞形態學改變,細胞增殖明顯可用于實驗。
1.3 分組 ①空白對照組:單純HSCs培養;② HGF組:單純培養HSCs,將100 ng/ml HGF作用于 HSCs;③ TRAIL組:將2 μg/ml TRAIL作用于HSCs;④ HGF+TRAIL組:將100 ng/ml HGF預先刺激HSCs 24 h,再加入2 μg/ml的 TRAIL。各實驗組細胞培養24、48 h后采用倒置相差顯微鏡下動態觀察活體細胞形態學改變。流式細胞儀Annexin-V-FITC/PI雙染法檢測HSCs凋亡以及Western印跡法檢測HSCs表面DR5蛋白的表達。
1.4 MTT法檢測各濃度HGF及TRAIL對HSCs增殖抑制率①將HSCs用0.25%胰酶消化貼壁細胞,細胞計數板計數,調整細胞濃度為1.5×105/ml,吹打,混勻;② 取96孔板,每孔加入100 μl(3 000個細胞),每時段設3個復孔,待細胞貼壁后分別加入50、100、150、200 ng/ml HGF 以及0.5、1、1.5、2 μg/ml的TRAIL蛋白,每種濃度設3個復孔。分別作用24 h及48 h,每孔加入10 μl MTT溶液,繼續在37℃,5%CO2培箱中培養4 h;③置96孔板于細胞培養箱內孵育4 h后,去除培養基,加150 μl DMSO充分溶解,在Biomark酶標儀,490 nm波長下檢測各孔OD值,并計算細胞抑制率。
1.5 流式細胞儀檢測各組HSCs的凋亡及Western印跡法檢測HSCs DR5蛋白的表達 HGF組及TRAIL組分別加入100 ng/ml HGF及2 μg/ml TRAIL 作用于 HSCs;HGF+TRAIL組中加入100 ng/ml HGF預處理24 h后再加入2 μg/ml的TRAIL,作用24、48 h后收集HSCs,使用PBS液懸混,采用 Annexin-V-FITC/PI凋亡試劑盒檢測凋亡及Western印跡法檢測HSCs的DR5蛋白表達,DR5濃度1∶200,其余嚴格按試劑說明書操作。
2 結果
2.1 HSCs的復蘇、傳代、形態學觀察 復蘇的HSCs第3天即可傳代,傳代的HSCs貼壁6 h后,開始伸展,胞體增大呈多邊形,表現為肌成纖維母細胞的特點,伸出許多細長偽足,呈星形外觀。見圖1。
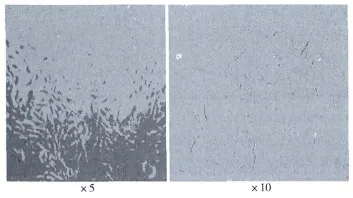
圖1 倒置相差熒光顯微鏡下復蘇的第四代HSCs形態
2.2 HGF及TRAIL對HSCs的增殖抑制率 HGF在50、100、150、200 ng/ml各濃度下增殖抑制率〔分別為(17.6±1.7)%、(19.1±2.5)%、(20.9±2.8)%、(18.7±2.1)%〕無明顯差異(P >0.05);TRAIL 在0.5、1、1.5 μg/ml各濃度下對 HSCs的增殖抑制率〔分別為(4.7±0.75)%、(4.4±1.3)%、(6.2±0.78)%〕無明顯差異(P>0.05);TRAIL在2 μg/ml作用下對HSCs有抑制作用,24 h及48 h增殖抑制率〔分別為(8.03±1.2)%、(24.6±0.8)%〕有顯著差異(P<0.01)。
2.3 各組中HSCs的凋亡情況及DR5蛋白的表達 HGF+TRAIL組凋亡率明顯高于空白對照組、HGF組(P<0.05)。TRAIL組DR5蛋白明顯高于空白對照組、HGF組及TRAIL組(P <0.01)。見表1,表2。
表1 各組各時間段凋亡率(s,%,n=3)

表1 各組各時間段凋亡率(s,%,n=3)
與空白對照組比較:1)P<0.01,2)P<0.05,下表同
時間 空白對照組 HGF組 TRAIL組 HGF+TRAIL組24 h 41.8±2.2 34.5±2.7 50.2±1.31) 58.2±2.21)48 h 44.0±1.7 49.5±1.12) 54.2±1.91) 67.0±1.41)
表2 各組各時間段DR5蛋白相對表達量(s,%,n=3)

表2 各組各時間段DR5蛋白相對表達量(s,%,n=3)
時間 空白對照組 HGF組 TRAIL組 HGF+TRAIL組24 h 0.25±0.1 0.26±0.13 0.39±0.121)0.48±0.111)48 h 0.25±0.2 0.28±0.11 0.65±0.171)0.97±0.121)
3 討論
HSCs是位于肝竇間隙的一種非實質細胞,正常情況下HSCs處于靜止狀態,當肝細胞受損時其被激活,合成大量的細胞外基質(ECM),膠原合成明顯增多,HSCs的激活與增殖在肝纖維化發生過程中起關鍵的作用〔1〕,因此促進HSCs凋亡,減少ECM分泌及膠原的合成,是緩解肝纖維化的關鍵〔4,5〕。
研究表明,參與HSCs凋亡的途徑主要有4條〔6〕,包括Fas-Fasl途徑、神經細胞生長因子(NGF)及NGFR途徑、外源性損傷途徑及TRAIL-TRAILR途徑。其中TRAIL-TRAILR途徑占重要地位。TRAIL是TNF家族成員之一,其中包括含有死亡結構域TRAIL-R1(DR4)和TRAIL-R2(DR5),與TRAIL結合時通過死亡結構域之間的相互識別作用與腫瘤壞死因子相關凋亡區域(FADD)結合與pro-caspase-8形成死亡誘導信號復合物,活化的caspase-8釋放到胞質中啟動caspase的級聯反應,導致細胞凋亡。HSC-T6是一種永生細胞系,與原代HSCs在形態學、生物學特征均有不同之處。本研究表明外源性HGF在50~200 ng/ml濃度范圍對HSCs的凋亡不起作用,與國外學者研究結果一致〔7〕。隨著TRAIL濃度的不斷增高,表現為細胞壞死。本結果說明HGF能增強TRAIL誘導的中晚期細胞凋亡,可能與主要調控中晚期凋亡的蛋白有關,HGF在對HSCs的抑制作用中不是直接的啟動因素,而需介導某些中介因素發揮其作用,TRAIL可能是其中因素之一。
HGF是一種促肝細胞生長的細胞因子,其通常以單鏈無活性前體合成及分泌〔8〕,在HGF前體激動劑HGFA的作用下被水解成有活性的HGF雙鏈,包括重鏈(α鏈)及無活性的輕鏈(β鏈),活化后的HGF與受體結合引起酪氨酸激酶活化,通過激活不同信號通路產生多種生物學功能如促細胞運動、上皮細胞生長、分化及血管形成等。研究發現,HGF對于不同的細胞類型發揮著細胞保護和促進細胞死亡的雙重作用〔9,10〕。HGF的表達可以活化Akt、上調Bcl-xl對Fas介導的肝細胞凋亡起保護作用〔11〕。Tulasne等〔12〕研究表明激活 HGF/c-met信號不同的下游信號分子可以抑制肝細胞的凋亡和促進HSCs凋亡的雙重作用。本研究中在使用Western印跡法檢測DR5蛋白的表達時發現HGF預先作用HSCs 24 h后可以上調HSCs表面DR5蛋白的表達,而DR5為TRAIL的特異性受體,其活性較DR4高103倍,在誘導HSCs凋亡的作用中占主要地位,即HGF上調DR5表達后增強了TRAIL誘導凋亡的作用,HGF可能是TRAIL及DR5的激動劑,可為TRAIL及激動劑治療肝纖維化提供新的思路,然而體內外的環境大相徑庭,加之動物實驗與臨床實驗之間的結果相差甚遠,本研究僅為臨床治療提供初步的思路。
1 Friedman SL.Mechanisms of hepatic fibrogenesis〔J〕.Gastroenterology,2008;134(6):1655-69.
2 陳國忠,姜海行,陸正峰,等.骨髓間充質干細胞共培養對肝星狀細胞增殖、凋亡和RohA表達的調控〔J〕.世界華人消化雜志,2010;18(16):1643-9.
3 Taimr P,Higuchi H,Kocova E,et al.Activated stellate cells express the TRAIL receptor-2/death receptor-5 and undergo TRAIL-mediated apoptosis〔J〕.Hepatology,2003;37(1):87-95.
4 Friedman SL.Hepatic stellate cells:protean,multifunctional,and enigmatic cells of the liver〔J〕.Physiol Rev,2008;88(1):125-72.
5 Gressner OA,Weiskirchen R,Gressner AM.Evolving concepts of liver fibrogenesis provide new diagnostic and therapeutic options〔J〕.Comparative Hepatol,2007;6(7):112-5.
6 Shen H,Fan J,Minuk G,et al.肝星狀細胞中細胞凋亡和存活的信號調控〔J〕.中南大學學報(醫學版),2007;32(5):726-34.
7 Li Y,Xing Fan,Rory C,et al.Hepatocyte growth factor enhances death receptor-induced apoptosis by up-regulating DR5〔J〕.BMC Cancer,2008;8:325-37.
8 Kataoka H,Miyata S,Uchinokura S,et al.Roles of hepatocyte growth factor(HGF)activator and HGF activator inhibitor in the pericellular activation of HGF/scatter factor〔J〕.Cancer Metastasis Rev,2003;22:223-36.
9 Lee KI-I,Choi EY,Kim MK,et al.Hepatocyte growth factor promotes cell survival by phosphorylation of BAD in gastric cancer cells〔J〕.Oncol Res,2008;17(1):23-32.
10 Wang X,Zhou Y,Kim HP,et al.Hepatocyte growth factor protects against hypoxia reoxygenation-induced apoptosis in endothelial cells〔J〕.J Biol Chem,2004;279:5237-43.
11 Suzuki H,Toyoda M,Horiguchi N,et al.Hepatocyte growth factor protects against Fas-mediated liver apoptosis in transgenic mice〔J〕.Liver Int,2009;29(10):1562-8.
12 Tulasne D,Foveau B.The shadow of death on the MET tyrosine kinase receptor〔J〕.Cell Death Differ,2008;15(3):427-34.

