急性肺損傷患者外周血Th17細胞水平及功能的研究
劉澤宇 夏書月 何巍
急性肺損傷(acute lung injury,ALI)是指心源性以外的各種肺內、外致病因素所導致的急性進行性缺氧性呼吸衰竭,病情兇險,死亡率高。失控的炎癥反應是發病機制的核心,避免炎癥反應失控是降低ALI病死率的關鍵。近年的研究發現了一種新型的T細胞亞群,可以產生IL-17,因此稱之為Th17細胞亞群[1]。維甲酸相關核孤兒受體γt(Retinoid-related orphan receptor gammat,RORγt)是調節Th17細胞分化的特異性轉錄因子,直接決定了Th17細胞的分化能力。Th17細胞通過分泌IL-17等細胞因子,在免疫調控網絡中發揮重要作用,參與炎性反應、自身免疫性疾病和移植排斥等。進一步的研究表明,Th17細胞和哮喘、COPD等多種肺部疾病具有相關性。但對于Th17細胞與ALI是否相關,目前還未見報導。本研究通過檢測ALI患者外周血中RORγt mRNA的表達量、Th17細胞的比例和血漿中IL-17的水平來了解Th17細胞的分化能力、數量多少和功能狀況,進而明確Th17細胞和ALI的關系,推測Th17細胞可能發揮的調控作用。
1 資料與方法
1.1 一般資料 選擇2009年10月至2011年12月期間,在沈陽醫學院奉天醫院呼吸內科住院的ALI患者10例。入選標準:符合中華醫學會重癥醫學分會制定的《急性肺損傷/急性呼吸窘迫綜合征診斷治療指南》所推薦的ALI診斷標準。其中男性6例,女性4例,平均年齡(68±11)歲,入組時患ALI的天數為(3±1)d,氧合指數(PaO2/FiO2)為(235±48)mm Hg。排除標準:留取血標本前已經應用了糖皮質激素。對照組為健康志愿者10人,同樣選取男性6例,女性4例,平均年齡(65±9)歲。本研究得到了沈陽醫學院奉天醫院倫理委員會批準,所有受試者均已簽署知情同意書。
1.2 研究方法
1.2.1 收集標本 清晨空腹抽取受試者外周血至少7 ml。其中5 ml用于提取RNA,1 ml用于流式細胞學檢測,1 ml用于酶聯免疫吸附試驗(ELISA)檢測。
1.2.2 RT-PCR檢測RORγt mRNA的表達量 Trizol(購自美國Invitrogen公司)法提取 RNA,配制 RNA/Primer混合物(RT-PCR試劑盒購自美國Invitrogen公司):總RNA5 μl+Oligo(dT)20 50 μM)1 μl+dNTP mix(10 mM)1 μl+ddH2O(DEPC 處理過)3 μl(補到 10 μl),再配制 cDNA Synthesis Mix:10 × RTbuffer2 μl+25 mM MgCl24 μl+0.1 m DTT 2 μl+RNaseOUT(40U/μl)1 μl+SuperScriptⅢ RT(200U/μl)1 μl。將10 μl cDNA Synthesis Mix 加入 RNA/Primer混合物中,反應后加入 RNase H降解殘留的 RNA。在 NCBI中查到RORγt的 cDNA 序 列,設 計 引 物 為:上 游 引 物5'GCAACAGCAGCAACAGGA3'、 下 游 引 物5'TCAGGGAGGCATAGGGTG3'、產物長度為428bp(引物由上海英駿生物技術有限公司合成)。將β肌動蛋白(β-actin)基因作為內參,上游引物為:5'GCTCGTCGTCGACAACGGCTC3'、下游引物為5'CAAACATGATCTGGGTCATCTTCTC3'、產物長度為353bp。將 PCR buffer、dNTPmix、上游引物、下游引物、Taq酶、cDNA模板、ddH2O加入一薄壁離心管中,進行PCR擴增(PCR儀為德國Promega公司產品)。反應條件為:94℃預變性5 min。94℃變性 30s,61.5℃退火 30s,72℃延伸 40s,30 個循環。最后72℃再延伸10 min。DM2000(購自北京天根生化科技有限公司)為DNA分子量標準,進行瓊脂糖凝膠電泳,用RORγt對β-actin的累積光密度(IOD)的比值作為RORγt的相對量,進行統計分析。
1.2.3 流式細胞術檢測Th17細胞的比例 將外周血按1∶1的比例與RPMI-1640培養基(購自美國Gibco公司)混勻,加入激活劑佛波酯(PMA),離子霉素(Ionomycin)和高爾基體阻斷劑Brefeldin-A(BFA)(均購自美國Sigma公司),培養4 h后與結合有FITC的抗人CD4單抗(購自美國BD公司)反應30 min。再經過溶血素(購自碧云天公司)裂解紅細胞,Fix&perm(購自美國Caltag公司)固定、破膜。最后與結合有PE的抗IL-17單抗(購自美國BD公司)反應,流式細胞儀檢測。
1.2.4 ELISA檢測IL-17濃度 取出包被有IL-17抗體的酶標板(購自美國R&D公司),分別加入血漿和不同濃度的標準品并孵育。此后依次經過與生物素化抗體、酶結合物、顯色劑、終止液的多步反應,最后測量OD450值,計算血漿中IL-17的濃度。
1.2.5 統計學方法 首先進行兩樣本的方差齊性檢驗,P>0.05為方差齊。再做兩個獨立樣本的t檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 外周血中RORγt mRNA的表達水平 RORγt mRNA在ALⅠ組的表達水平(0.56±0.08)高于對照組(0.19±0.05),差異顯著(P<0.01),見圖1。
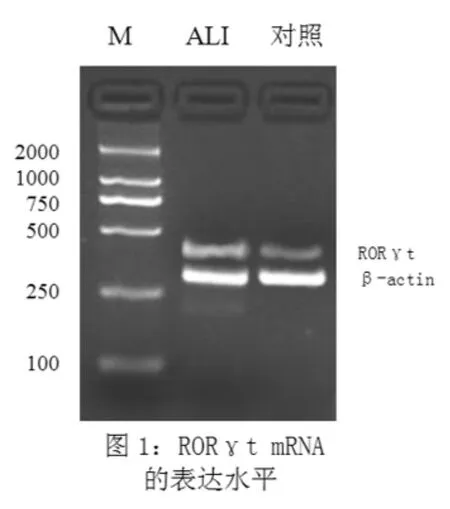
圖1 RORγt mRNA
2.2 外周血中Th17細胞的比例 Th17細胞在ALⅠ組的比例(32.60% ±5.51%)高于對照組(12.29% ±1.71%),有統計學差異(P<0.01),見圖2。
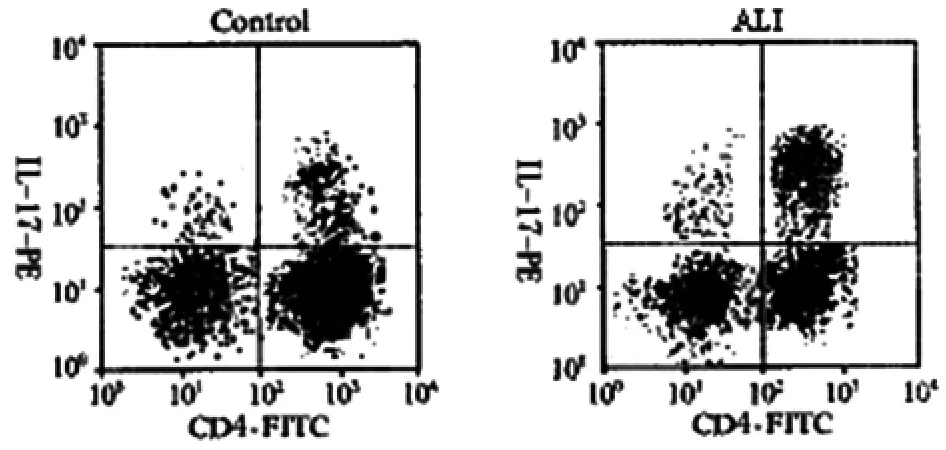
圖2 Th17細胞的比例
2.3 血漿中IL-17的濃度 IL-17在ALⅠ組的濃度(87.33±6.08)pg/ml明顯高于對照組(52.71±3.19)pg/ml,P <0.01,見圖3。
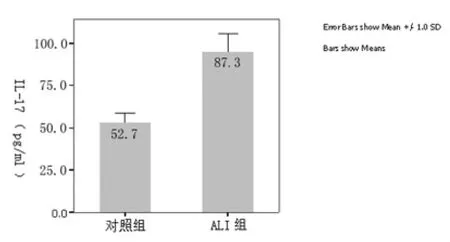
圖3 IL-17的濃度
3 討論
ALI屬于一種特殊類型的急性呼吸衰竭,具有病情兇險,死亡率高的特點。目前認為,失控的炎癥反應是發病機制的核心,避免炎癥反應失控是降低ALI病死率的關鍵,也是目前研究的熱點之一。
對于在免疫調控網絡中起重要作用的輔助性T細胞(Th),根據所分泌的細胞因子的不同,傳統上將其分為Th1和Th2兩個亞群。Th1細胞以分泌INF-γ和IL-2為主,Th2細胞以分泌IL-4、IL-5和IL-13為主。而近年的研究發現了一種新型的Th細胞亞群,以產生IL-17為主,但不能產生INF-γ和IL-4,因此稱之為Th17細胞亞群[1]。Th17細胞是由初始T細胞分化而來,在細胞和分子水平受到精細調節。TGF-β是啟動Th17細胞分化的始動因素[2],IL-6是協同促進Th17細胞分化的關鍵因子,而IL-23則對Th17細胞的存活和增殖發揮重要作用[3]。雖然Th17細胞可以分泌多種細胞因子,但主要還是通過分泌IL-17來發揮生物學作用,廣泛參與抗感染[4]、自身免疫[5]和移植排斥[6]等。
RORγt是調節 Th17細胞分化的特異性轉錄因子,在Th17細胞分化發育過程中起到極其重要的作用。體外實驗顯示,在TGF-β和IL-6的共同作用下,初始CD4+T細胞可以分化為Th17細胞,但需要RORγt的表達,即使沒有其他的外源性細胞因子,加強表達RORγt也足以誘導Th17細胞的分化[7]。當 RORγt缺乏時,Th17 細胞的數量也隨之顯著下降[8]。RORγt基因敲除的小鼠不易出現嚴重的自身免疫性疾病[9],炎癥組織中 Th17細胞也明顯減少[10]。這些研究結果均提示,RORγt可以通過促進Th17細胞的分化,間接起到上調炎癥反應的作用。本研究的結果表明,在ALI患者的外周血中,淋巴細胞表達RORγt的水平較對照組明顯升高,這會有力地促進初始CD4+T細胞向Th17細胞分化,進而上調炎癥反應,這與上面提到的研究結論是一致的。
雖然有多種細胞可以分泌IL-17,但IL-17的主要來源仍然是Th17細胞。作為一種細胞因子,參與包括哮喘和COPD在內的多種炎癥性疾病。利用動物模型,對Th17細胞/IL-17和多種肺部疾病之間關系所進行的研究,已經取得了一定進展。李鴻佳等[11]發現,哮喘小鼠外周血中Thl7細胞明顯增多,BALF中IL-17的水平顯著升高。在哮喘小鼠肺組織中,增多的Thl7細胞不但促進中性粒細胞在局部的浸潤,而且增強變應原誘導的氣道高反應性[12]。McKinley等[13]將 Th17細胞通過靜脈注入到T細胞缺失的哮喘小鼠體內,誘導出IL-17,氣道內中性粒細胞聚集和氣道高反應性。總之,哮喘小鼠體內IL-17可以通過募集并激活中性粒細胞等多種方式發揮促炎作用[14]。而在 COPD 方面,Alcorn等[15]對 IL-17RA 基因敲除的小鼠進行研究發現,香煙暴露導致肺氣腫的嚴重程度較野生型小鼠減低,說明IL-17對肺氣腫的形成有促進作用。Shen等[16]將抗IL-17抗體注入香煙暴露的小鼠腹腔內,去除小鼠體內的IL-17,肺組織勻漿中IL-17的濃度下降,支氣管肺泡灌洗液中中性粒細胞的水平降低,小氣道炎癥明顯緩解,從反面證明IL-17可以上調COPD的氣道炎癥反應。我們的研究表明,與對照組比較,ALI患者外周血中Th17細胞的比例增加,IL-17的濃度升高,差異有統計學意義。這提示Th17細胞可能通過分泌IL-17來上調炎癥反應,加重炎癥反應的失控。這與前面提到的哮喘和COPD動物模型中所見到的情況是相吻合的。
雖然Th17細胞與多種肺部疾病相關,但與ALI是否相關,目前還未見報導。我們對ALI患者外周血中Th17細胞和IL-17進行研究后發現:ALI患者外周血中Th17細胞的分化加強,數量增多,血漿中IL-17的水平增高。據此推測,Th17細胞參與了ALI的發病過程,可能通過分泌以IL-17為主的細胞因子,加重氣道炎癥反應。今后的研究方向包括進一步深化對Th17細胞生物學特點的認識,嘗試通過干預Th17細胞來控制炎癥反應,改善ALI的預后。
[1]Harrington LE,Hatton RD,Mangan PR,et al.Interleukin 17-producing CD4+effector T cells develop via a lineage distinct from the T helper type 1 and 2 lineages.Nat Immunol,2005,6(11):1123-1132.
[2]Mangan PR,Harrington LE,O'Quinn DB,et al.Transforming growth factor-beta induces development of the Th17 lineage.Nature,2006,441(7090):231-234.
[3]McGeachy MJ,Chen Y,Tato CM,et al.The interleukin 23 receptor is essential for the terminal differentiation of interleukin 17-producing effector T helper cells in vivo.Nat Immunol,2009 Mar;10(3):314-324.
[4]Bǎlǎnescu P,Lǎdaru A,Voiosu T,et al.Th17 and IL-17 immunity in chronic hepatitis C infection.Rom J Intern Med,2012,50(1):13-18.
[5]Chiricozzi A,Zhang S,Dattola A,et al.New insights into the pathogenesis of cutaneous autoimmune disorders.J Biol Regul Homeost Agents,2012,26(2):165-170.
[6]Nakagiri T,Inoue M,Minami M,et al.Immunology mini-review:the basics of T(H)17 and interleukin-6 in transplantation.Transplant Proc,2012,44(4):1035-1040.
[7]Cha HR,Chang SY,Chang JH,et al.Downregulation of Th17 cells in the small intestine by disruption of gut flora in the absence of retinoic acid.J Immunol,2010,184:6799-6806.
[8]Hirahara K,Ghoreschi K,Laurence A,et al.Signal transduction pathways and transcriptional regulation in Th17 cell differentiation.Cytokine Growth Factor Rev,2010,21(6):425-434.
[9]Kwan BC,Tam LS,Lai KB,et al.The gene expression of type 17 T-helper cell-related cytokines in the urinary sediment of patients with systemic lupus erythematosus.Rheumatology(Oxford),2009,48:1491-1497.
[10]Buonocore S,Ahern PP,Uhlig HH,et al.Innate lymphoid cells drive interleukin-23-dependent innate intestinal pathology.Nature,2010,464:1371-1375.
[11]李鴻佳,蓋慶玲,王立華,等.Thl7淋巴細胞在哮喘小鼠氣道炎癥中的初步研究。細胞與分子免疫學雜志,2011,27(1).
[12]Wilson RH,Whitehead GS,Nakano H,et al.Allergic sensitization through the airway primes Th17-dependent neutrophilia and airway hyperresponsiveness.Am J Respir Crit Care Med,2009,180(8):720-730.
[13]McKinley L,Alcorn JF,Peterson A,et al.TH17 cells mediate steroid-resistant airway inflammation and airway hyperresponsiveness in mice,J.Immunol,181,(2008):4089-4097.
[14]Iwakura Y,Ishigame H,Saijo S,et al.Functional specialization of interleukin-17 family members.Immunity,2011,34(2):149-162.
[15]Alcorn JF,Crowe CR,Kolls JK,et al.TH17 cells in asthma and COPD.Annu Rev Physiol,2010,72:495-516.
[16]Shen N,Wang J,Zhao M,et al.Anti-interleukin-17 antibodies attenuate airway inflammation in tobacco-smokeexposed mice.Inhal Toxicol,2011:23:212-218.

