急性腦梗死出血轉化危險因素研究
熊莉君,張臨洪
出血轉化(hemorrhagic transformation,HT)是腦梗死急性期常見的并發癥之一,嚴重者可以導致病情惡化甚至死亡。HT的發生可能與血管再通、血-腦脊液屏障破壞有關,通過不同的影像學檢查可以明確診斷。準確預測、篩查HT高危人群,及時完善影像檢查,對發現HT、指導下一步治療有著重要的現實意義。為此,本研究通過對135例腦梗死HT患者的臨床資料進行分析,探討急性腦梗死HT的危險因素。
1 資料與方法
1.1 一般資料 選取2011年6月—2013年6月在本院神經內科住院治療且資料完整的急性腦梗死患者818例,均符合全國第四屆腦血管病會議制定的診斷標準[1]。所有患者在起病2周內經CT或MRI等復查,檢出HT 135例(16.5%)(觀察組),余683例(83.5%)無HT者作為對照組。觀察組中,男93例,女42例;平均年齡(61.4±13.1)歲。對照組中,男479例,女204例;平均年齡(61.1±12.8)歲。兩組患者性別構成及年齡間有均衡性(見表1)。
1.2 方法 回顧性分析兩組患者的基礎疾病史和實驗室檢查結果。基礎疾病史包括:高血壓、糖尿病、冠心病、心房纖顫(房顫)病史,家族史,吸煙及飲酒史;實驗室檢查:腎功能、尿蛋白定性、空腹血糖、血脂〔總膽固醇、三酰甘油、低密度脂蛋白〕、肌酐、血紅蛋白、血小板計數、同型半胱氨酸、腦梗死面積。

2 結果
2.1 兩組患者觀察指標比較 兩組患者糖尿病、冠心病、房顫、飲酒、空腹高血糖、蛋白尿(+)、大面積腦梗死的發生率及空腹血糖水平比較,差異均有統計學意義(P<0.05);而兩組其他指標比較,差異無統計學意義(P>0.05,見表1、表2)。
2.2 Logistic回歸分析 以糖尿病、冠心病、房顫、飲酒、空腹高血糖、蛋白尿、大面積腦梗死為自變量,以HT為因變量進行Logistic回歸分析,變量賦值見表3。結果顯示,糖尿病、房顫、大面積腦梗死是急性腦梗死HT的獨立危險因素(P<0.05,見表4)。
3 討論
腦梗死HT是一種自然轉歸形式,臨床上較為常見,嚴重者可以導致死亡和病情惡化。HT影像學分型目前廣泛接受的是歐洲急性卒中合作研究(ECASS)分型[3]:HI-1型,沿梗死灶邊緣的小點狀出血;HI-2型,片狀無占位效應出血;PH-1型,血腫形成,有占位效應,但小于梗死面積30%;PH-2型,血腫超過梗死面積30%,有占位效應及遠隔區出血。但是對于癥狀性HT目前存在著不同的標準:NINDS標準、ECASSII標準、SITS-MOST標準[4]。
HT的發生率報道不一致,為3.36%~36.70%,溶栓組高達43.7%[5-6],但是各報道所統計的累積時間并不一致,為36 h~90 d。另外,不同的影像學技術也可能是導致HT發生率存在較大差距的原因之一。本組病例中HT檢出率為16.5%,尚在相應的范圍。
表3 急性腦梗死HT的危險因素Logistic回歸分析變量賦值
Table3 The assignment of Logistic regression analysis on risk factors for HT after acute cerebral infarction

變量賦值HTY是=0,否=1糖尿病X1是=0,否=1冠心病X2是=0,否=1房顫X3是=0,否=1飲酒X4是=0,否=1空腹高血糖X5是=0,否=1蛋白尿X6是=0,否=1大面積腦梗死X7是=0,否=1
注:HT=出血轉化
表4 急性腦梗死HT的危險因素Logistic回歸分析
Table4 Logistic regression analysis on risk factors for HT after acute cerebral infarction

變量β值Waldχ2值P值OR值95%CI糖尿病0 580 7 708 0 0051 787(1 186,2 691)房顫0 589 5 720 0 0171 802(1 112,9 919)大面積腦梗死1 86871 3410 0006 477(4 198,9 991)

表1 兩組急性腦梗死患者定性指標比較〔n(%)〕Table 1 Comparison of the qualitative indexes between two groups of patients with acute cerebral infarction
注:根據Adams等[2]分型法,大面積腦梗死是指梗死面積>3 cm2并累及腦解剖部位的2支大血管主干供應區
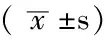
表2 兩組急性腦梗死患者定量指標比較Table 2 Comparison of the quantitative indexes between two groups of patients with acute cerebral infarction
注:*部分患者結果缺失:對照組66例,觀察組18例
3.1 糖尿病與HT 本研究結果顯示,急性腦梗死HT患者中糖尿病發生率高于急性腦梗死非HT患者,且回歸分析顯示糖尿病是急性腦梗死HT的一個獨立危險因素,急性腦梗死伴糖尿病者HT的風險是無糖尿病者的1.787倍。既往研究表明空腹高血糖是HT獨立危險因素[7],其機制可能是:高血糖加重細胞內無氧酵解,使乳酸等堆積,使基質金屬蛋白酶9(MMP-9)生成增加并破壞基底膜導致 HT的發生。但本研究單因素分析發現急性腦梗死HT患者空腹高血糖發生率及空腹血糖水平高于對照組,但回歸分析未顯示二者是急性腦梗死HT的危險因素。因此,我們認為糖尿病及空腹高血糖對HT存在不同的機制及預測價值。
3.2 房顫與HT 本研究結果顯示,急性腦梗死HT患者中房顫發生率高于急性腦梗死非HT患者,且回歸分析顯示房顫是急性腦梗死HT的危險因素,急性腦梗死伴房顫者HT的風險是無房顫者的1.802倍。135例HT患者中,房顫為32.6%,高于國內張雯君等[7]報道的21.4%,但低于國外Lodder等[8]基于病理確診的HT研究報道的61.2%。在TOAST病因分型中,心源性栓塞發生HT的概率最大[7]。房顫合并腦栓塞時,血管痙攣后栓子移向遠端,血管壁因缺血缺氧而受損,血流通過時易發生滲漏性出血或血管破裂出血。并且房顫患者新生側支循環代償能力不足,血管壁脆弱,受血流沖擊時增加HT發生率。
3.3 大面積腦梗死與HT 本研究結果顯示,急性腦梗死HT患者中大面積腦梗死發生率高于急性腦梗死非HT患者,且回歸分析顯示大面積腦梗死是急性腦梗死HT的一個危險因素,其HT的風險是非大面積腦梗死者的6.477倍,可以很好地預測HT的發生。王雪梅等[9]回顧性觀察875例腦梗死患者,發現大面積腦梗死HT發生率(38.31%)遠高于小梗死(3.85%)和腔隙性梗死(1.40%),表明梗死面積與HT的發生密切相關,即梗死面積越大,發生HT的概率越高。大面積腦梗死HT的可能機制為:腦水腫壓迫梗死區周圍組織毛細血管,造成血液淤滯,發生缺血壞死和內皮損害,加之側支循環開放(包括軟腦膜支),小血管重新灌注,但因長時間缺血缺氧內膜變性斷裂,引起梗死區及周邊出血。
3.4 HT的識別 目前HT的識別已經由過去簡單的CT平掃、MRI(T1、T2加權像)向更為敏感的影像識別發展。在多模CT方面:基于CT血管原始圖(CTA-SI)的Alberta 卒中早期CT評分系統(ASPECTS)可以極為有效地預測9 h內大腦中動脈梗死區癥狀性[10]。通透性成像是近年來用于評價血-腦脊液屏障的技術,顯示血-腦脊液屏障損傷的敏感度遠高于增強MRI,通透性增強可以很好地預測HT的發生,對溶栓和抗栓等治療具有很強的指導意義[11]。
3.5 HT對預后的影響 一般來說,HT發生時,局部少量滲血不會加重病情,但少數患者因血腫大出現頭痛、惡心、嘔吐及原有神經功能缺損癥狀加重或意識障礙甚至是臨床死亡等。在預后方面,只有當起病24 h內血腫體積超過梗死面積33%并伴有顯著水腫時(PH-2型)才會出現不良結局,其他類型在24 h及3個月內的死亡和殘障無差別[12],甚至有人認為HI-1型、HI-2型是血管早期再通的標志[13],并且減小了梗死體積、改善了3個月時的臨床預后。所以對于PH-2型患者,在HT發生后必須有針對性地調整治療方案。因此,腦梗死患者在急性期出現癥狀加重,尤其是大面積腦梗死患者,均應該復查顱腦CT等影像檢查,以重新評估抗栓藥物、脫水藥物的應用,必要時酌情手術干預,盡量減少殘障、避免死亡。
綜上所述:急性腦梗死患者梗死面積大,同時伴有糖尿病和房顫,2周內易出現HT。故應對此類患者給予重視,并進行CT復查或更先進的影像技術評估,以及時發現HT,并酌情調整藥物治療。
1 中華神經科學會,中華神經外科學會.各類腦血管疾病診斷要點[J].中華神經科雜志,1996,29(6):379-380.
2 Adams HP Jr,Bendixen BH,Kappelle LJ,et al.Classification of subtype of acute ischemic stroke.Definitions for use in a multicenter clinical trial.TOAST.Trial of Org 10172 in Acute Stroke Treatment[J].Stroke,1993,24(1):35-41.
3 Larrue V,von Kummer RR,Müller A,et al.Risk factors for severe hemorrhagic transformation in ischemic stroke patients treated with recombinant tissue plasminogen activator:a secondary analysis of the European-Australasian Acute Stroke Study(ECASS Ⅱ)[J].Stroke,2001,32(2):438-441.
4 Mazya M,Egido JA,Ford GA,et al.Predicting the risk of symptomatic intracerebral hemorrhage in ischemic stroke treated with intravenous alteplase:Safe Implementation of Treatments in Stroke (SITS) symptomatic intracerebral hemorrhage risk score[J].Stroke,2012,43(6):1524-1531.
5 高衛紅.出血性腦梗塞及其危險因素的臨床探討[J].國際醫藥衛生導報,2007,13(12):16-19.
6 Hacke W,Kaste M,Fieschi C,et al.Intravenous thrombolysis with recombinant tissue plasminogen activator for acute hemispheric stroke.The European Cooperative Acute Stroke Study(ECASS)[J].JAMA,1995,274(13):1017-1025.
7 張雯君,王偉平,李保華.腦梗死后出血轉化的危險因素分析[J].中國腦血管病雜志,2012,9(2):72-76.
8 Lodder J,Krijne-Kubat B,van der Lugt PJ.Timing of autopsy confirmed hemorrhagic infarction with reference to cardioembolic stroke[J].Stroke,1988,19(12):1482-1484.
9 王雪梅,杜會山,杜明艷.出血性腦梗死相關因素分析[J].腦與神經疾病雜志,2008,16(11):108-110.
10 Lin K,Zink WE,Tsiouris AJ,et al.Risk assessment of hemorrhagic transformation of acute middle cerebral artery stroke using multimodal CT[J].J Neuroimaging,2012,22(2):160-166.
11 Lee M,Saver JL,Alger JR,et al.Blood-brain barrier permeability derangements in posterior circulation ischemic stroke:frequency and relation to hemorrhagic transformation[J].J Neurol Sci,2012,313(1/2):142-146.
12 Berger C,Fiorelli M,Steiner T,et al.Hemorrhagic transformation of ischemic brain tissue:asymptomatic or symptomatic?[J].Stroke,2001,32(6):1330-1335.
13 Molina CA,Alvarez-Sabín J,Montaner J,et al.Thrombolysis-related hemorrhagic infarction:a marker of early reperfusion,reduced infarct size,and improved outcome in patients with proximal middle cerebral artery occlusion[J].Stroke,2002,33(6):1551-1556.

