蛋清蛋白質凝膠化機理的研究進展
陳彰毅,趙 燕,*,涂勇剛,李建科,羅序英,王俊杰,鄧文輝
(1.南昌大學食品科學與技術國家重點實驗室,江西南昌330047;2.南昌大學生物質轉化教育部工程研究中心,江西南昌330047;3.江西農業大學食品科學與工程學院,江西南昌330045)
蛋清蛋白質凝膠化機理的研究進展
陳彰毅1,2,趙 燕1,2,*,涂勇剛3,李建科1,2,羅序英1,2,王俊杰1,2,鄧文輝1,2
(1.南昌大學食品科學與技術國家重點實驗室,江西南昌330047;2.南昌大學生物質轉化教育部工程研究中心,江西南昌330047;3.江西農業大學食品科學與工程學院,江西南昌330045)
蛋清蛋白質以其優異的凝膠性能廣泛應用于食品加工中,而加工中不同的誘導方式和條件使其形成凝膠的類型及性能均有較大差異,凝膠化機理也有所不同。本文主要從凝膠形成誘導方式及其條件出發,著重介紹熱誘導和強堿誘導下蛋清蛋白質凝膠化機理的研究進展,以期為進一步豐富和完善蛋清蛋白質凝膠化機理理論體系的研究提供參考。
蛋清蛋白質,熱誘導,強堿誘導,凝膠化機理
凝膠是指在分散介質中的膠體粒子或高分子溶質形成整體構造而失去了流動性,或膠體雖含有大量液體介質但處于固化的狀態,是食品中一種較為常見的形態[1]。作為食品主要成分的蛋白質,其最重要的功能特性之一就是凝膠化作用。禽蛋蛋清固形物中90%以上為蛋白質,其中富含卵白蛋白、卵轉鐵蛋白、卵粘蛋白、卵類粘蛋白、溶菌酶等多種蛋白質,豐富的蛋白質組成為其凝膠的形成奠定了物質基礎[2]。因蛋清蛋白質優異的凝膠性能對相關食品的質構、形態、持水力、稠度和粘結性等方面皆會產生影響,所以極受國內外研究者的重視[3-5]。目前大部分研究偏重于對蛋清蛋白質的改性以提高其凝膠性能的方面;而涉及其凝膠化機理,尤其是對眾多誘導方式以及不同誘導條件下形成的多種凝膠結構的形成機理,尚未有深入和系統的研究。本文將對幾種主要誘導方式下蛋清蛋白質凝膠形成機理的研究進行綜述,并著重闡述常見的熱誘導和強堿誘導蛋清蛋白質形成機理的研究進展,以期為進一步豐富和完善蛋清蛋白質凝膠化機理理論體系的研究提供參考;對更好地應用蛋清蛋白質的凝膠性能,指導相關食品的加工具有重要意義。
1 蛋清蛋白質凝膠的形成類型和誘導方式
通常根據凝膠外形分類,蛋白質能形成凝結塊(不透明)凝膠和透明凝膠兩種類型[6],這可能主要取決于預凝膠狀態的蛋白質分子聚集速率和變性速率之間的關系;如果前者大于后者時,可形成隨機的不透明或透明度低的凝結塊凝膠,反之則形成非常有序的透明度高的凝膠網絡結構[7]。
目前,按凝膠誘導方式,蛋白質凝膠主要可分為熱誘導凝膠、冷凍凝膠、高壓誘導凝膠、酸堿誘導凝膠、金屬離子誘導凝膠及酶誘導凝膠等[8-12],且不同的誘導方式會使蛋白質形成不同類型和功能性質各異的凝膠結構。另外,蛋白質凝膠的形成還與其本身的結構、性質以及分子間(蛋白質-蛋白質和蛋白質-溶液體系)相互作用密切相關。蛋白質濃度、pH、溫度、離子強度和離子類型等外部條件及氫鍵、疏水作用、二硫鍵、靜電作用、蛋白質分子量和氨基酸組成等內在因素[13]在凝膠形成過程中會影響分子間吸引力、排斥力和相互交聯等作用,并決定蛋白質凝膠化的具體機制。
蛋清蛋白質在不同凝膠條件下亦能形成凝結塊凝膠和透明凝膠兩種不同類型的凝膠結構,例如水煮蛋的蛋白是蛋清蛋白質在加熱條件下形成的乳白色不透明凝結塊凝膠;而中國傳統蛋制品皮蛋的蛋白卻是堿處理蛋清蛋白質形成的半透明或透明狀凝膠。前者是熱誘導方式,主要受溫度影響;后者是強堿誘導,堿濃度(或pH)則是主要影響因素。另外,壓力、金屬離子和酶以及它們與熱誘導共同作用的方式對蛋清蛋白質的凝膠化也有相關報道,且對其凝膠性能都具有很大的影響[5,14]。由此可見,不同的誘導方式加與之結合的外部條件及具體的內在因素,是蛋清蛋白質形成凝膠類型和性能差異的關鍵,也是區別其凝膠化機理的關鍵。而且,多種方式下復雜的凝膠化過程并不能一概而論,應當結合外部條件和內在因素具體分析。
2 熱誘導蛋清蛋白質凝膠化機理
2.1 內在分子機理
熱誘導的蛋清蛋白質凝膠最常見、應用最為廣泛,對其凝膠化作用機理的研究也相對較為豐富。許多學者將熱誘導蛋清蛋白質凝膠(凝結)化機理闡述為以下過程:天然單體蛋白質→變性單體→可溶性聚集→凝膠或凝結[15]。這是根據蛋白質變性理論,即變性時蛋白質分子間氫鍵斷裂,功能基團暴露,熵效應促使疏水相互作用加強等基礎上推斷而來。早先由Johnson等[16]研究報道,混合的蛋清蛋白質加熱時蛋白質分子的聚集發生在明顯的兩個不同溫度區間:在61.5~62.5℃范圍內,卵轉鐵蛋白或其他蛋白開始變性和部分聚集;在71.0~73.0℃之間時,蛋白質分子聚集加速,形成凝結塊凝膠的主體。后來,Pezennec等[17]對蛋清熱凝結研究中闡明,凝膠的形成過程是蛋清中蛋白質先由天然狀態轉變為變性狀態,通過β-折疊作用形成高相對分子質量的可溶性聚集物,然后在二硫鍵的作用下,預凝膠聚集物逐漸變稠,形成凝膠(gelation)或凝結(coagulation),最終形成凝膠還是凝結則取決于蛋白質展開和聚集的相對速度。并且,Vassilios等[18]發現熱誘導蛋清蛋白凝膠前后SDS-PAGE條帶明顯變化,證明蛋白質分子發生了相互交聯,出現了高分子量交聯蛋白質分子。這些研究基本能印證熱誘導體系下對蛋清蛋白質凝膠形成機制主體構架的推斷,即先變性而后聚集。
在此推斷的基礎上,Mine[15]將熱誘導蛋清蛋白質凝膠化過程更細致地劃分為三個主要步驟:首先,加熱使蛋白質變性并促使疏水效應加強,產生球狀構象的蛋白質分子聚集體并導致蛋清液呈渾濁狀;其次,因蛋清蛋白質中巰基與二硫鍵之間的交換反應,大量預凝膠狀聚集體不斷形成;最后,冷卻階段溫度下降,單聚體和少量二聚體迅速聚集形成凝膠,并有大量氫鍵在聚集體之間重新生成,使凝膠彈性上升,網絡結構趨于平衡。另外,在此結論前后,相繼有研究報道熱誘導卵白蛋白變性過程中存在“熔融球蛋白”(molten globule)的過渡態[19-20],稱這種中間態的存在可能會加速蛋白質分子的聚集作用,與其熱誘導凝膠化機制密切相關[15,21],又進一步豐富和完善了這一凝膠化機理理論。
就目前而言,一般認為熱誘導蛋清蛋白質凝膠化過程如圖1所示[15]。在受熱狀態下蛋清中蛋白質三級和四級結構遭到破壞,適度變性或完全變性;蛋白質分子從適度展開到完全展開并伴隨融球態過渡,必須數量的功能基團暴露,蛋白質分子間或蛋白質與溶液分子相互作用加強;此時,疏水相互作用可能使卵白蛋白、卵轉鐵蛋白和溶菌酶的二級結構中α-螺旋結構減少,β-折疊結構增多,且β-折疊結構對于穩定蛋白質變性后聚集至關重要[22]。功能基團之間較強的疏水作用以及靜電相互作用使得蛋白質分子發生疏水性聚集,形成凝膠網絡結構;但此時分子間二硫鍵形式的交聯對形成凝膠并不必要,只是后續對穩定凝膠網絡有重要作用;且冷卻階段聚集體之間氫鍵重新生成使得凝膠基質更加穩定[15]。
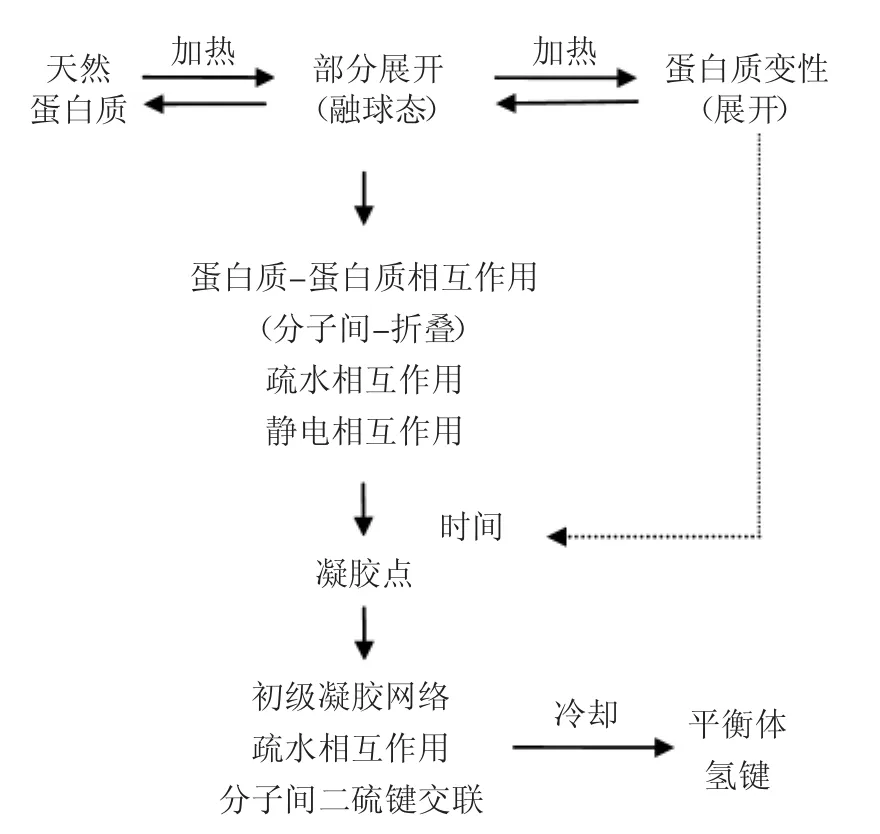
圖1 熱誘導蛋清蛋白質凝膠化過程示意圖Fig.1 Schematic representation of heat-induced gelation of egg white proteins
2.2 外部條件對熱誘導凝膠形成的影響
在影響凝膠類型方面,有學者通過控制誘導蛋清蛋白質凝膠化的外部條件,如pH、離子強度和加熱方式(兩步加熱),采用熱誘導方式得到了透明類型的凝膠[23-24]。這可能因為受熱時溫度的變化,影響了蛋白質變性和聚集的相對速率;同時,pH和離子強度通過影響分子內疏水性基團和分子間靜電作用,改變蛋白質分子溶解性和聚集速率,可溶性復合物締合速度緩慢等,最終導致變性和聚集的相對速率發生變化并保持一定的平衡狀態,形成了網絡結構相對有序和透明類型的凝膠。
在影響凝膠性能方面,Handa等[25]通過研究不同pH對熱誘導蛋清蛋白質凝膠的質構、持水力和微觀結構的影響,發現堿性條件下,溶液pH越高,其形成的凝膠質構更好,網絡結構更有序。此外,Croguennec等[26]研究發現不同的金屬離子與pH對蛋清蛋白質凝膠性能有顯著影響;pH為7時,Fe3+、Ca2+和Mg2+能影響凝膠的粘彈性和微觀結構,且Fe3+最為顯著;而高濃度的NaCl能降低凝膠的持水力。也有報道添加糖類和鹽能導致蛋白質溶液變性溫度的提高和延緩蛋白質分子聚集[18],特別是添加結冷膠、黃原膠和阿拉伯膠會對蛋清蛋白凝膠強度產生較大的影響[27]。這些研究說明,外部條件的介入勢必引起內在因素的改變,進而使蛋清蛋白質凝膠機制的具體化。
總的來說,熱誘導蛋清蛋白質凝膠化機理,不論是形成凝結塊還是透明凝膠,都可以概括為變性和聚集兩大步驟:變性是蛋白質分子在一定程度上的展開和構象的變化;而聚集過程的分子間鍵合或非鍵合力決定形成凝膠的最終類型,后一階段機制往往非常復雜,且不同條件參與下的凝膠化機制均要具體分析。蛋白質分子聚集組裝的行為受到各種因素的影響,導致形成不同結構和功能差異的凝膠。利用現代發展的新興技術,如激光共聚焦顯微鏡、傅立葉轉換紅外顯微鏡、拉曼共聚焦顯微鏡以及原子力顯微鏡等[28],集中研究蛋白質分子聚集階段的動力學和形成凝膠的微觀結構,將能更好地補充和完善熱誘導下的蛋清蛋白質凝膠化形成理論體系。
3 強堿誘導蛋清蛋白質凝膠化機理
蛋清在一定的pH條件下會發生凝固,一些學者研究了蛋清在酸、堿作用下的凝膠化現象,發現蛋清在pH2.3以下或pH12.0以上都會形成凝膠,在pH2.3~12.0之間則不發生凝膠化[29]。強酸誘導的蛋清蛋白凝膠在食品加工中很少運用,而強堿誘導的蛋清蛋白凝膠卻有典型代表——皮蛋蛋白。皮蛋(松花蛋、變蛋)是中國獨創的傳統蛋制品,正是由強堿誘導加工而成,是討論該方式誘導蛋清蛋白質凝膠化機理的理想對象。本課題組實驗發現,皮蛋在腌制過程中蛋白凝膠pH的變化呈現先迅速升高,后逐漸下降,再緩慢回升的趨勢,在第8d達到最大值,約為11.39[30]。說明皮蛋蛋白透明或半透明、富有彈性的凝膠其形成與強堿動態誘導密切相關。
為獲得皮蛋良好凝膠性能,堿濃度的動態變化至關重要,而不論是傳統腌制方法還是目前工業生產所用清料法,均未擺脫通過添加重金屬化合物對堿的滲入進行調控。目前一般認為重金屬化合物在加工初期可與強堿反應離子化,從而滲入蛋內,其中以[Pb(OH)3]-的滲透力最強;在加工后期Cu2+、Fe3+、Zn2+、Pb4+等可與蛋內蛋白質分解產生的S2-結合,生成難溶性復合物而堵塞蛋殼孔,發揮調控堿滲入蛋內速度的作用[31]。但上述重金屬化合物對皮蛋凝膠品質有較大的影響,具體總結如表1[32-35]。
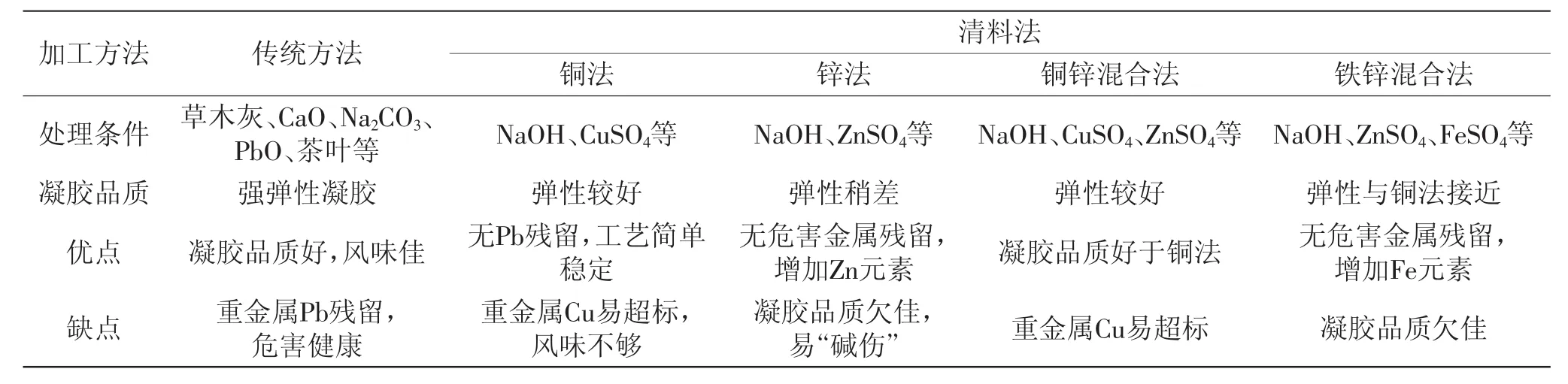
表1 加工方法與重金屬化合物種類對皮蛋蛋白凝膠品質影響Table.1 Effect of different processing methods and heavy metal compounds on the quality of preserved egg protein gel
目前一般認為皮蛋加工過程中,因強堿誘導,皮蛋蛋白凝膠的形成經過了化清、凝固、轉色、成熟四個階段。在化清階段,蛋清蛋白質在堿作用下完全變性,束縛水變成了自由水,粘稠蛋白變成稀的透明水樣溶液,但蛋白質分子的一、二級結構尚未受到破壞。在凝固階段,蛋白質分子在堿的作用下,二級結構開始受到破壞,氫鍵斷開,親水基團增加,大量自由水變為結合水,并與蛋白質分子連接呈透明凝膠體。在轉色階段,蛋白質分子一級結構發生破壞,使單個分子的分子質量下降,蛋白凝膠的彈性開始下降,同時發生美拉德反應。在成熟階段,蛋白全部轉變為褐色的半透明凝膠體,具有一定的彈性[29]。但上述對皮蛋蛋白凝膠的形成機理尚屬理論推測,需要直接、充足、系統的實驗數據予以支撐。本課題組對皮蛋腌制過程中未凝固之前的蛋清流變特性變化進行了監測,發現其黏度先增大,再逐漸減少[36]。表明蛋清蛋白在強堿的誘導下并未直接進入化清階段,說明在動態強堿誘導下其凝膠的形成過程與機理可能更為復雜。
本課題組還將強堿誘導的皮蛋蛋白凝膠與蛋清熱誘導凝膠的性能進行了對比,結果發現皮蛋蛋白凝膠的強度只有蛋清熱誘導凝膠的50%左右,但是其彈性與凝結性卻是蛋清熱誘導凝膠的1.5倍。我們進一步對其微觀結構進行了觀察,發現堿誘導下的蛋清蛋白形成了疏松且孔洞分布較為規則的纖絲狀結構,與熱誘導下形成的層疊致密顆粒狀凝膠結構差異明顯,說明堿加工方式使皮蛋蛋白凝膠具有較為特殊的性能與組裝方式。
由于皮蛋工藝與品質的獨特,近年來國內外學者也開始對我國這一獨創蛋制品顯示出濃厚的興趣。Ji等[37]通過研究在真空條件下皮蛋腌制前期(化清期)的化學和結構變化:發現隨腌制時間增加,蛋清蛋白質中總巰基數和表面疏水力逐漸增加,而二硫鍵數逐漸減少;運用傅立葉紅外光譜和圓二色譜技術分析皮蛋蛋白中二級結構的變化,結果表明,α-螺旋和β-轉角結構的下降伴隨著β-折疊和無規卷曲結構的增加;SDS-PAGE電泳對比發現真空下腌制期間前4d內與新鮮鴨蛋蛋白質種類無顯著變化,但在第5d有部分蛋白質條帶消失,非真空條件下第6d直至后期成熟階段只有清晰的卵白蛋白條帶。這說明強堿誘導蛋清蛋白質凝膠化前期,存在內在因素的復雜變化;包括對疏水作用、二硫鍵、氫鍵和蛋白質分子量等因素均有明顯影響。Eiser等[38]從材料學的角度出發,運用掃描電鏡、圓二色譜、熒光光譜等現代分析技術試圖闡明皮蛋蛋白在加工過程中的物相轉變,推斷出皮蛋蛋白凝膠是一種非特定聚合途徑形成的高度無形但結構穩定的精細鏈狀蛋白質聚合物,并認為這種聚合物是膠體粒子通過長程靜電斥力作用和短距吸引力而聚集。但上述研究尚不夠深入系統,在聚集過程中哪種蛋白質參與凝膠的主導作用,其組裝聚集過程與交聯方式又如何等諸多問題仍未解決。
綜上所述,目前對強堿誘導蛋清蛋白質凝膠化機理的研究相對薄弱,還僅限于皮蛋蛋白凝膠領域,且未形成完整的體系。后續研究可在此基礎上,進一步探明強堿誘導蛋清蛋白質凝膠化過程中蛋白質分子間的相互作用,以及蛋白質凝膠網絡結構的主導作用力和參與凝膠組裝的關鍵蛋白質或多肽組分。進而從分子水平闡明強堿誘導蛋清蛋白質凝膠結構與功能的關系,更好地理解蛋白質分子組裝聚集機理,完善其凝膠化機制體系,也可為皮蛋工藝改進與品質控制提供理論基礎。
4 其他條件誘導蛋清蛋白質凝膠化機理
在適當的條件下,壓力、金屬離子參與和酶作用這三種誘導方式,也能促使蛋白質凝膠化,誘導網絡結構的形成[39]。研究這三種方式誘導蛋清蛋白質凝膠化機理的文獻相對較少,但對于豐富其凝膠理論的多元化和系統化具有一定的意義。
4.1 高壓
蛋清蛋白質在400MPa靜壓力處理時會發生部分凝集,在600MPa以上加壓30min會形成較硬的凝膠;特別在500~1000MPa靜壓力范圍下,此類凝膠和熱誘導方式下相比,在光澤、黏性和彈性方面更好,也更具有天然的味道[15]。Messens等[40]進一步對卵白蛋白在靜壓力400MPa的構象進行研究,推測其凝聚的穩定性可能是其分子中所含四個二硫鍵和非共價鍵共同維持的結果。Van等[41]在利用DTNB法對比研究熱誘導(50~85℃)和壓力誘導(10~60℃,100~700MPa)蛋清蛋白質中總巰基變化時發現,兩者均能使巰基基團暴露并通過巰基氧化反應和SS-SH交換反應而使總含量發生明顯下降;但壓力條件下巰基基團更容易暴露,下降更為明顯,且使蛋白質分子發生可溶性聚集程度更大。這可能是壓力誘導凝膠與熱誘導凝膠性能差異的主要原因。動力學研究也得出相同的結果,并發現壓力誘導時溫度越高,凝膠性能越與熱誘導方式相似[14,42]。
4.2 金屬離子
金屬離子能減弱蛋白質分子間靜電斥力,且隨離子強度增加,靜電斥力減小,促進蛋白質分子聚集;Ca2+或其他二價金屬離子能在相鄰多肽的特殊氨基酸殘基之間形成交聯,形成鹽橋,強化蛋白質凝膠結構[43]。劉西海[44]在研究各種金屬離子對咸蛋腌制期間蛋清蛋白質結構的影響時發現:添加金屬離子,增加了蛋清蛋白質的β-折疊,分子展開而促進交聯;長時間金屬離子的處理可導致蛋白質分子通過疏水作用部分簇集,使其表面疏水性下降;蛋清蛋白加熱后α-螺旋減少、β-折疊比例增加,同時增加蛋白質表面疏水性;金屬離子通過影響蛋清蛋白結構,促進蛋白質在加熱過程中隨機聚集,形成凝膠網絡交聯度降低,結構粗糙、空洞多、網絡不均勻;二價金屬離子對蛋清蛋白質構象和蛋清凝膠微觀結構的影響較一價離子更強。這說明金屬離子在凝膠前期對蛋白質分子結構的影響非常大,并對蛋清凝膠質構特性起主導作用;但具體到某種金屬離子對蛋清蛋白質凝膠化的誘導機制尚不明確。
4.3 酶
酶通過誘導蛋白質或肽鏈之間進行交聯而使蛋白質形成凝膠。目前在食品凝膠中應用最廣泛的酶是轉谷酰胺酶(TGase),它可以催化相同或不同蛋白質分子間的交聯與聚合,形成新的共價鍵[39]。徐幸蓮等[45]研究發現TGase酶添加濃度在10~40U/g蛋白質時,熱處理后會使蛋清蛋白質凝膠化極限濃度降低和凝膠硬度提高。酶誘導蛋白質凝膠化作用主要在蛋白質聚集階段,而且對蛋白質的熱、強堿或高壓的前處理可能還具有必要性。后續研究可重點放在其他食品凝膠酶的開發及誘導機制的探索上。
5 展望
蛋清中所含蛋白質種類復雜多樣,性質各異,在其凝膠化過程中可能發揮各自不同功能,也可能相互協同,并不能籠統而談。加之諸多誘導方式與各種具體條件相結合,使得蛋清蛋白質凝膠化機理更為復雜。
熱誘導體系下蛋清蛋白質凝膠化機理的研究已較為豐富和成熟,但其他誘導體系相對薄弱。特別是對強堿誘導方式,可從結構與功能角度出發,在其凝膠特性、微觀結構、蛋白質聚集作用力及其分子結構與構象變化等方面著重研究,從而在分子水平上深入探明其凝膠化機制,這對豐富和充實食品蛋白質凝膠化機理理論體系意義深遠。
[1]李云飛,殷涌光,金萬鎬.食品物性學[M].北京:中國輕工業出版社,2005.
[2]MINE Y.Recent advances in egg protein functionality in the food system[J].World’s Poultry Science Journal,2002,58:31-39.
[3]YANG S C,BALDWIN R E.Functional properties of eggs in foods[M].New York:Food Products Press,Binghamton,1995,405-463.
[4]MATSUDOMI N,NAKANO K,SOMA A,et al.Improvementof gel properties of dried egg white by modification with galactomannan through the maillard reaction[J].Journalof Agricultural and Food Chemistry,2002,50(14):4113-4118.
[5]CAMPBELL L,RAIKOS V,EUSTON S R.Modification of functional properties of egg-white proteins[J].Food/Nahrung,2003,47(6):369-376.
[6]王璋,許時嬰,湯堅.食品化學[M].北京:中國輕工業出版社,2010:171-173.
[7]遲玉杰.蛋清蛋白質的糖基化產物結構與凝膠強度關系的探究[J].食品科學,2009,30(21):485-488.
[8]SUN X D,ARNTFIELD S D.Gelation properties of saltextracted peaprotein induced by heattreatment[J].Food Research International,2010,43(2):509-515.
[9]MADADLOU A,EMAM-DJOMEH Z,MOUSAVI M E,et al. Acid-induced gelation behavior of sonicated casein solutions[J]. Ultrasonics Sonochemistry,2010,17(1):153-158.
[10]GOH K,BHAT R,KARIM A.Probing the sol-gel transition of egg white proteins by pulsed-nmr method[J].European Food Research and Technology,2009,228(3):367-371.
[11]NAVARRA G,GIACOMAZZA D,LEONE M,et al.Thermal aggregation and ion-induced cold-gelation of bovine serum albumin[J].European Biophysics Journal,2009,38(4):437-446.
[12]LI F,KONG X,ZHANG C,et al.Gelation behaviour and rheological properties of acid-induced soy protein-stabilized emulsion gels[J].Food Hydrocolloids,2012,29(2):347-355.
[13]PHILLIPS L G,WHITEHEAD D M,KINSELLA J E. Structure-function properties of food proteins[M].San Diego(USA):Academic Press,1994:179-204
[14]VAN DER PLANCKEN I,VAN LOEY A,HENDRICKX M E.Combined effect of high pressure and temperature on selected properties of egg white proteins[J].Innovative Food Science& Emerging Technologies,2005,6(1):11-20.
[15]MINE Y.Recent advances in the understanding of egg white protein functionality[J].Trends in Food Science&Technology,1995,6(7):225-232.
[16]JOHNSON T M,ZABIK M E.Gelation properties of albumen proteins,singly and in combination[J].Poultry Science,1981,60(9):2071-2083.
[17]PEZENNEC S,GAUTHIER F,ALONSO C,et al.The protein net electric charge determines the surface rheological properties of ovalbumin adsorbed at the air-water interface[J]. Food Hydrocolloids,2000,14(5):463-472.
[18]RAIKOS V,CAMPBELL L,EUSTON S R.Rheology and texture of hen’s egg protein heat-set gels as affected by pH and the addition of sugar and/or salt[J].Food Hydrocolloids,2007,21(2):237-244.
[19]HIROSE M.Molten globule state of food proteins[J].Trends in Food Science&Technology,1993,4(2):48-51.
[20]HAGOLLE N,RELKIN P,DALGLEISH D,et al.Transition temperatures of heat-induced structural changes in ovalbumin solutions at acid and neutral pH[J].Food Hydrocolloids,1997,11(3):311-317.
[21]MINE Y.Effect of pH during the dry heating on the gelling properties of egg white proteins[J].Food Research International,1996,29(2):155-161.
[22]GOSAL W S,ROSS-MURPHY S B.Globular protein gelation[J].Current Opinion in Colloid&Interface Science,2000,5(3):188-194.
[23]KITABATAKE N,SHIMIZU A,DOI E.Preparation of heatinduced transparent gels from egg white by the control of pH and ionic strength of the medium[J].Journal of Food Science,1988,53(4):1091-1095.
[24]KITABATAKE N,SHIMIZU A,DOI E.Preparation of transparent egg white gel with salt by two-step heating method [J].Journal of Food Science,1988,53(3):735-738.
[25]HANDA A,TAKAHASHI K,KURODA N,et al.Heatinduced egg white gels as affected by pH[J].Journal of Food Science,2008,63(3):403-407.
[26]CROGUENNEC T,NAU F,BRULE G.Influence of pH and salts on egg white gelation[J].Journal of Food Science,2002,67(2):608-614.
[27]涂勇剛,趙燕,王丹,等.糖類對蛋清蛋白凝膠強度的影響[J].食品工業科技,2013,34(4):72-75.
[28]胡坤,方少瑛,王秀霞,等.蛋白質凝膠機理的研究進展[J].食品工業科技,2006,27(6):202-205.
[29]馬美湖.蛋與蛋制品加工學[M].北京:中國農業出版社,2007:41,88-89.
[30]楊有仙,趙燕,涂勇剛,等.皮蛋腌制過程中堿度,pH及質構特性變化規律的研究[J].食品工業科技,2012,33(16):111-114.
[31]歐陽玲花,馮健雄,閔華,等.皮蛋加工研究現狀與展望[J].食品工業科技,2009,30(4),349-354.
[32]Wang J,Fung D Y.Alkaline-fermented foods:a review with emphasis on pidan fermentation[J].Critical Reviews in Microbiology,1996,22(2),101-138.
[33]閻華,朱端衛.銅,鋅,鐵在皮蛋加工中作用差異研究[J].食品科學,2006,27(12),164-167.
[34]GANASEN P,BENJAKUL S.Chemical composition,physical properties and microstructure of pidan white as affected by different divalent and monovalent cations[J].Journal of Food Biochemistry,2011,35(5),1528-1537.
[35]趙燕,徐明生,涂勇剛.皮蛋加工相關機理研究進展[J].食品科學2010,31(17),472-475.
[36]涂勇剛,趙燕,徐明生,等.皮蛋加工過程中流變與凝膠特性的變化規律[J].食品科學,2012,33(19):21-24.
[37]JI L,LIU H,CAO C,et al.Chemical and structural changes in preserved white egg during pickled by vacuum technology[J]. Food Science and Technology International,2013,19(2):123-131.
[38]EISER E,MILES C S,GEERTS N,et al.Molecular cooking:Physical transformations in chinese‘century’eggs[J].Soft Matter,2009,5(14):2725-2730.
[39]ANGSUPANICH K,EDDE M,LEDWARD D.Effects of high pressure on the myofibrillar proteins of cod and turkey muscle[J].Journal of Agricultural and Food Chemistry,1999,47(1):92-99.
[40]MESSENS W,VAN CAMP J,HUYGHEBAERT A.The use of high pressure to modify the functionality of food proteins[J]. Trends in Food Science&Technology,1997,8(4):107-112.
[41]VAN DER PLANCKEN I,VAN LOEY A,HENDRICKX M E.Changes in sulfhydryl content of egg white proteins due to heat and pressure treatment[J].Journal of Agricultural and Food Chemistry,2005,53(14):5726-5733.
[42]VAN DER PLANCKEN I,VAN LOEY A,HENDRICKX M E.Kinetic study on the combined effect of high pressure and temperature on the physico-chemical properties of egg white proteins[J].Journal of Food Engineering,2007,78(1):206-216. [43]TOTOSAUS A,MONTEJANO J G,SALAZAR J A,et al.A review of physical and chemical protein-gel induction[J]. International Journal of Food Science&Technology,2002,37(6):589-601.
[44]劉西海.金屬離子對蛋清蛋白質結構的影響研究[J].中國家禽,2012,34(1):27-31.
[45]徐幸蓮,程巧芬,周光宏.轉谷氨酰胺酶對蛋白質凝膠性能的影響[J].食品科學,2003,24(10):38-43.
Research progress in the gelation mechanism of egg white proteins
CHEN Zhang-yi1,2,ZHAO Yan1,2,*,TU Yong-gang3,LI Jian-ke1,2,LUO Xu-ying1,2,WANG Jun-jie1,2,DENG Wen-hui1,2
(1.State Key Laboratory of Food Science and Technology,Nanchang University,Nanchang 330047,China;2.Engineering Research Center of Biomass Conversion,Ministry of Education,Nanchang University,Nanchang 330047,China;3.College of Food Science and Engineering,Jiangxi Agricultural University,Nanchang 330045,China)
Egg-white proteins are extensively utilized as food ingredients due to their excellent gelling properties,while the type and performance of egg-white protein gels are greatly different,as well as the gelation mechanism,due to the greatly different induction ways and conditions.This paper mainly discussed gel formation induced by various treatments and the combination of different treatments,the research progress of thermal-induced and alkali-induced egg-white protein gelation mechanism was emphatically introduced.This review was to provide a reference to further enrich and perfect the theory system on gelation mechanism of egg-white proteins.
egg-white proteins;thermal-induced;alkali-induced;gelation mechanism
TS253.1
A
1002-0306(2014)04-0369-06
2013-07-05 *通訊聯系人
陳彰毅(1988-),男,碩士研究生,研究方向:食品科學。
國家自然科學基金(31101293,31101321,31360398);食品科學與技術國家重點實驗開放基金課題(SKLF-KF-201008)。

