L-谷氨酸包覆四氧化三鐵水基磁流體的制備
黃秋霞(廣東省高州農業學校)
一、前言
隨著科技和人類生產、生活需求的快速發展,越來越多種新型材料被人們研制和應用到各個領域。磁流體作為一種新型智能材料,是一種既有固體強磁性又有液體流動性的新型功能材料,尤其是具有良好生物相容性的水基磁流體在生物醫藥領域有著廣泛的應用。
1.L-谷氨酸概述
谷氨酸(2—氨基戊二酸)有左旋體、右旋體和外消旋體。左旋體,即L-谷氨酸。L-谷氨酸(L-Glutamicacid),化學名稱為L-2-氨基戊二酸或L-α-氨基戊二酸,分子式:C5H9NO4,結構式:HOOC-CH2-CH2-CH(NH2)-COOH,分子量:147.13 g/moL,是一種鱗片狀或粉末狀晶體,呈微酸性,無毒。微溶于冷水,易溶于熱水,幾乎不溶于乙醚、丙酮及冷醋酸中,也不溶于乙醇和甲醇。
L-谷氨酸是一種重要的化合物,是動植物氮平衡中非常重要的一種氨基酸,主要用發酵法生產,玉米、小麥、甘薯、大米、甘蔗糖蜜、甜菜糖蜜等是發酵生產L-谷氨酸的淀粉質主要原料。來源豐富且生產工藝成熟,目前我國谷氨酸總發酵能力已接近160萬噸,約占全球L-谷氨酸產能的75% 。同時,大量存在于谷類蛋白質中,動物腦中含量也較多。L-谷氨酸在生物體內的蛋白質代謝過程中占重要地位,參與動物、植物和微生物中的許多重要化學反應。醫學上L-谷氨酸主要用于治療肝性昏迷,還用于改善兒童智力發育。
2.本文研究的目的、內容和意義
(1)研究的目的 在前人大量的水基磁流體實驗基礎上,基于上述L-谷氨酸眾多的化學和生物特性,以L-谷氨酸為包覆劑、以水為載液、以Fe3O4為磁性粒子研究制備具有良好生物相容性、超順磁性、高穩定性、強磁響應性的四氧化三鐵水基磁流體制備的最佳工藝。
(2)研究的內容 本文主要研究以水為載液、以Fe3O4為磁性粒子、以L-谷氨酸為表面活性劑制備水基磁流體的工藝。關于水基磁流體的制備,前人已有大量的實驗和大量文獻顯示,同時本實驗室已有合適的制備四氧化三鐵水基磁流體制備的工藝,并在此基礎上利用各種物理化學方法,同時借鑒前人的經驗,將會從包覆階段的以下幾個方面進行深層次的研究:L-谷氨酸的用量、反應的pH值、包覆時間的把握、包覆溫度的控制、反應時間和攪拌速度。
(3)研究的意義 L-谷氨酸化學吸附在納米四氧化三鐵粒子表面,制備得到強生物親合性的水基磁流體。可作為生物醫用的磁流體,達到磁性粒子、表面活性劑、基液都具有良好的生物相容性,以及在人體血液的pH值弱酸性范圍內具有較好的穩定性的要求[1],在實際應用過程中,一次治療或一次給藥的時間間隔一般為數小時到數十小時,而L-谷氨酸磁流體即使在敞口的狀態下,20天后,其磁性衰減都在5%以內,具有很強的磁穩定性,所以這種氨基酸磁流體具有很好的實用價值。這種磁流體在磁性藥物載體、磁共振造影劑、磁高熱治療腫瘤、視網膜磁流體夾 (用于視網膜分離的修復手術)和血流的磁測量等領域有良好的應用前景[2]。通過研究水基磁流體的包覆機理,可以更好地制備性能優良的磁流體,將可以更好地指導制備無毒可生物降解的磁流體實驗。在實際應用上提高實用價值。
二、實驗及結果分析
1.實驗儀器及藥品
(1)實驗儀器
JJ型電動攪拌器、HH-2A恒溫水浴鍋 、KQ-250DB型數控超聲波清洗器 、古埃磁天平Avatar 360 FT-IR、PHS-3C精密PH計、FA 1004型電子天平
(2)實驗藥品
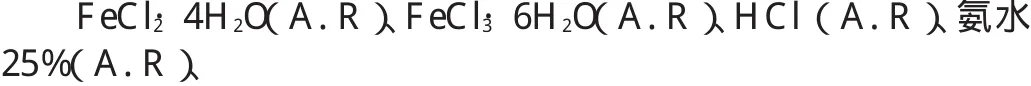
L-谷氨酸(化學純)
2.實驗的基本原理
本實驗采用化學共沉淀法,其反應原理如下:
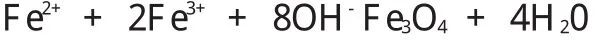
由上述反應可知Fe2+、Fe3+、OH-的理論物質的量之比為1:2:8,但實際上在反應過程中有且肯定會有一部分Fe2+會被氧化為Fe3+。因為反應是在有氧環境中進行的,而且在加熱攪拌過程中,也會造成一部分Fe2+被氧化為Fe3+。。只有當Fe3+與Fe2+的比例恰當時,才能制出飽和磁化強度最大的Fe3O4粒子。很明顯Fe3+/Fe2+應該小于2(物質的量之比),本文沒有對此作深入的研究,因為已有大量資料研究顯示,該值為1.7-1.75是比較合理的,若反應溫度較高,則Fe3+/Fe2+值較小,在查閱了大量資料后,最終選擇Fe3+/Fe2+為1.75進行實驗。
3.工藝流程設計
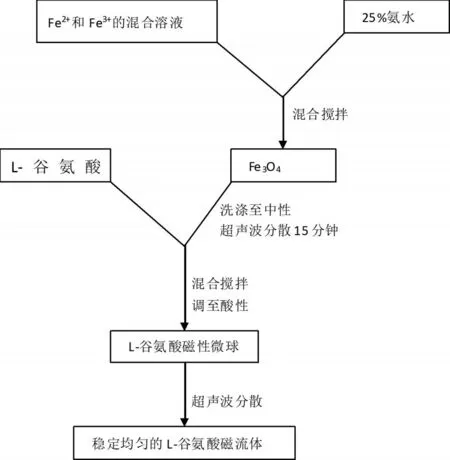
圖1 L-谷氨酸磁流體的制備工藝流程圖
4.實驗過程
磁性粒子的制備 (1)用二次蒸餾水清洗實驗用的所有玻璃儀器,保證沒有雜質混入,然后量取約150mL的二次蒸餾水于250mL燒杯中用電爐加熱煮沸,驅除溶解在水中的氧氣,冷卻到室溫。
(2)然后用電子天平準確稱量FeC13·6H2O 2.7036g置于沖洗好的燒杯中,加入100mL煮沸后已冷卻到室溫的二次蒸餾水,滴入3~4滴稀HCl,再加入準確稱量的FeC12·4H2O 1.1376g攪拌溶解后待用。
(3)用量筒量取8mL或稍多一點的25%的氨水置于三頸燒瓶中,打開電動攪拌器,開始時轉速調低一點(約800r/m in,驅趕氧氣),然后迅速將剛才配制好的混合溶液倒入其中,可以看到馬上有亮黑色的沉淀生成。
(4)加完混合液后,將三頸燒瓶塞好,盡量減少空氣的進入,并將轉速盡量調高(3000r/m in),以保證生成的粒子能夠快速得到分散,使其粒徑更小。35℃條件下,反應約60m in,即得活性粒子Fe3O4。
水基磁流體的制備
(1)準確稱取0.0202g的L-谷氨酸于小燒杯中,加入10mL二次蒸餾水,用玻璃棒攪拌使L-谷氨酸完全溶解在水中,待用。
(2)將制得的Fe3O4活性粒子倒入250mL的燒杯中,加入100mL二次蒸餾水洗滌,將燒杯置于磁鐵上幫助吸降。同時將水溫升到500C。
(3)待粒子沉降后,連著磁鐵一起傾瀉倒出上層水液。重復水洗3至4次洗去液相中的過多的NH3·H2O。洗滌過程盡量要快。
(4)然后加入30mL二次蒸餾水,馬上進行超聲波分散。分散過程中并用玻璃棒不停攪拌,將上述制備好的L-谷氨酸溶液倒入,并用二次蒸餾水調節溶液的體積約為50mL,一邊攪拌一邊用稀鹽酸調pH值為1~2,超聲波分散約15分鐘。
(5)然后加入到三頸燒瓶中,打開攪拌器,將轉速盡量調高(3000r/m in),50℃進行包覆60 m in,即得由L-谷氨酸包覆的水基磁流體。
包覆完成后將產物倒入燒杯中,超聲波分散30m in,即得穩定均勻的水基磁流體。最后,把黑亮色的產品倒進試劑瓶保存。
5.不同實驗條件對結果的影響及分析 在查閱了大量資料后[3],本實驗中經過實驗實踐,最終選取反應液的起始濃度為0.15mol/L,采用氨水作為沉淀劑,在35℃下制得的Fe3O4粒子磁性和穩定性是最好的,并取得較好的效果。在查閱大量文獻之后,結合本實驗的情況本人主要在L-谷氨酸用量的確定、包覆溫度和時間的確定、攪拌速度的確定和pH值的影響這些方面進行討論,具體如下:
(1)pH值 溶液在反應過程中必需處于堿性條件下才能生成磁性粒子Fe3O4。參考前人的經驗以及本人實驗證明,反應過程中溶液pH≤8,磁性粒子Fe3O4生成少,產物磁性極弱;pH≥11,溶液體系反應速度過快,生成的磁性粒子粒徑大,導致穩定性下降;pH=9~11,磁性粒子的分散性很好,磁性強。因此,在制備磁性粒子Fe3O4時,應控制體系的pH=9~11。
L-谷氨酸分子中含有兩個酸性的羧基和一個堿性的氨基,是一個既有酸性基因,又有堿性基因的兩性電解質,與酸或堿作用都可以生成鹽。由于羧基離解力大于氨基,所以L-谷氨酸是一種酸性氨基酸。L-谷氨酸溶解于水后,呈離子狀態存在,其解離方式取決于溶液的pH值,在酸性介質中,α—羧基的解離受到抑制,L-谷氨酸主要以陽離子(GA+)狀態存在,帶正電荷,形成雙電層;由雙電層穩定理論可知,膠體表面電荷越多,膠體之間的排斥力就越大,膠體就越穩定,顆粒沉降的速度就越慢。在pH=1~6的溶液中,膠體表面電荷隨著pH的升高而降低,則磁流體的穩定性隨著pH的升高而降低[1]。而且L-谷氨酸在不同的pH值溶液中有不同的溶解度,L-谷氨酸在pH=1.0附近或堿性情況下,溶解度很高。
對于水基磁液,pH值對磁液穩定性的影響是顯著的。pH值過高(>12)會造成離子強度太高,不利于表面活性劑的包覆,而且容易導致粒子在包裹過程中被氧化而變為紅棕色[4]。 pH值調整為何值最理想,與使用的表面活性劑有關。實驗表明:使用L-谷氨酸作包覆劑,在最佳pH值=1~2的條件下,可以獲得穩定性好的磁流體。如表1:
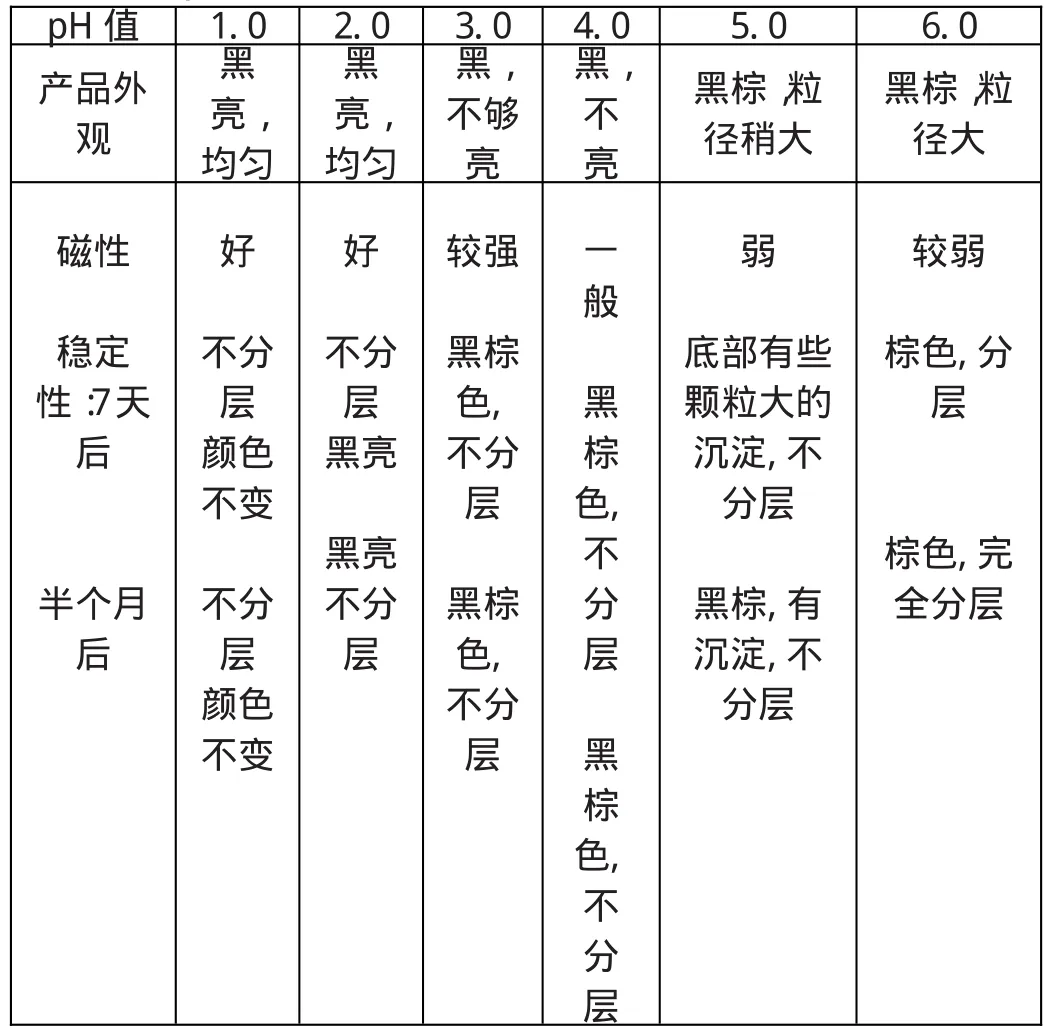
表1 pH值對產物的影響
(2)包覆劑的用量 一種好的磁流體,磁性粒子在基液中應具有所要求的濃度并是穩定的膠態體系,在制備磁流體時使用的包覆劑(分散劑)是影響的重要因素。磁性Fe3O4微粒必須借助包覆劑才能均勻地分散在水相中。
包覆劑的分散作用可以克服范德華力所造成的顆粒凝聚、削弱靜磁吸引力、改變磁性顆粒表面的性質、使顆粒和基液渾成一體、同時還可以防止磁性顆粒的氧化[5]。 加入L-谷氨酸后,L-谷氨酸以氫鍵或配位鍵的形式纏繞在Fe3O4表面,形成一層保護膜,阻止了納米粒子的團聚,同時,由于空間位阻效應和有機基團之間的相互斥力,克服了納米Fe3O4粒子的自身重力和相互之間的磁力吸引,使之能穩定分散于基液中,提高磁流體的分散性和穩定性[6]。因此,包覆劑對磁性微球在載液中的懸浮穩定性起著至關重要的作用,其用量的把握是一個關鍵。
當包覆劑的劑量較少,不足以完全覆蓋所有磁性粒子,或磁微粒包覆劑包覆層較薄時,包覆劑間產生的斥力不足以克服磁引力和范德華力的作用而發生磁顆粒團聚,會使磁顆粒變大。若包覆劑用量過多,在磁性微粒表面形成多層包覆,同時表面活性劑的長鏈互相交織在一起,從而又使顆粒粘結在一起而變大,并降低了磁性顆粒的穩定性和導致磁性能下降[7]。如表2所示,為了獲得高穩定性和強磁性能的磁流體,工藝條件不變、基液一定的情況下,僅改變L-谷氨酸的用量,包覆劑的最佳用量控制為0.0200g/50mL。
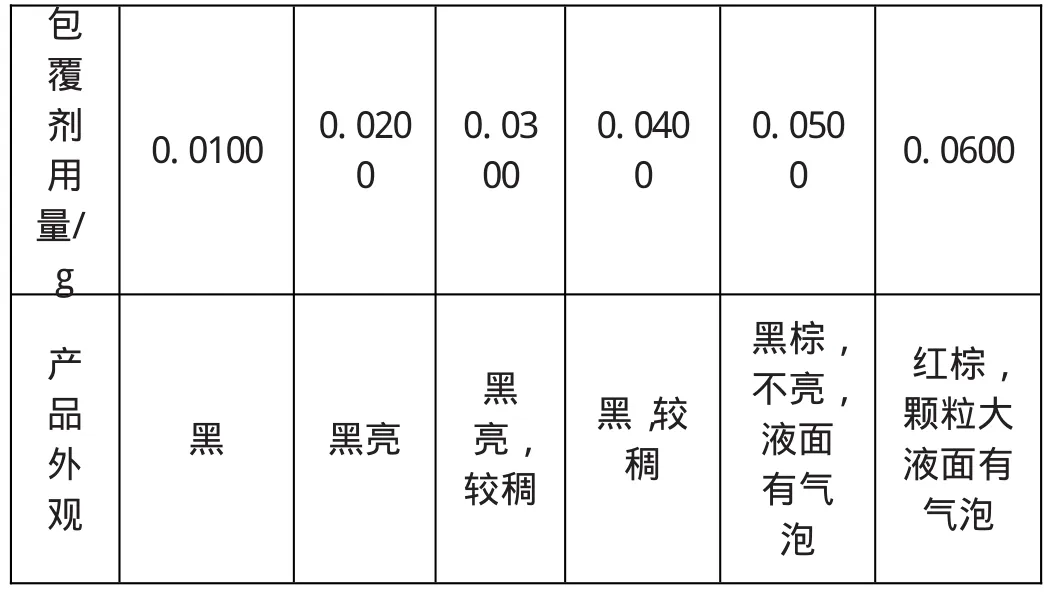
表2 L-谷氨酸用量對產物的影響
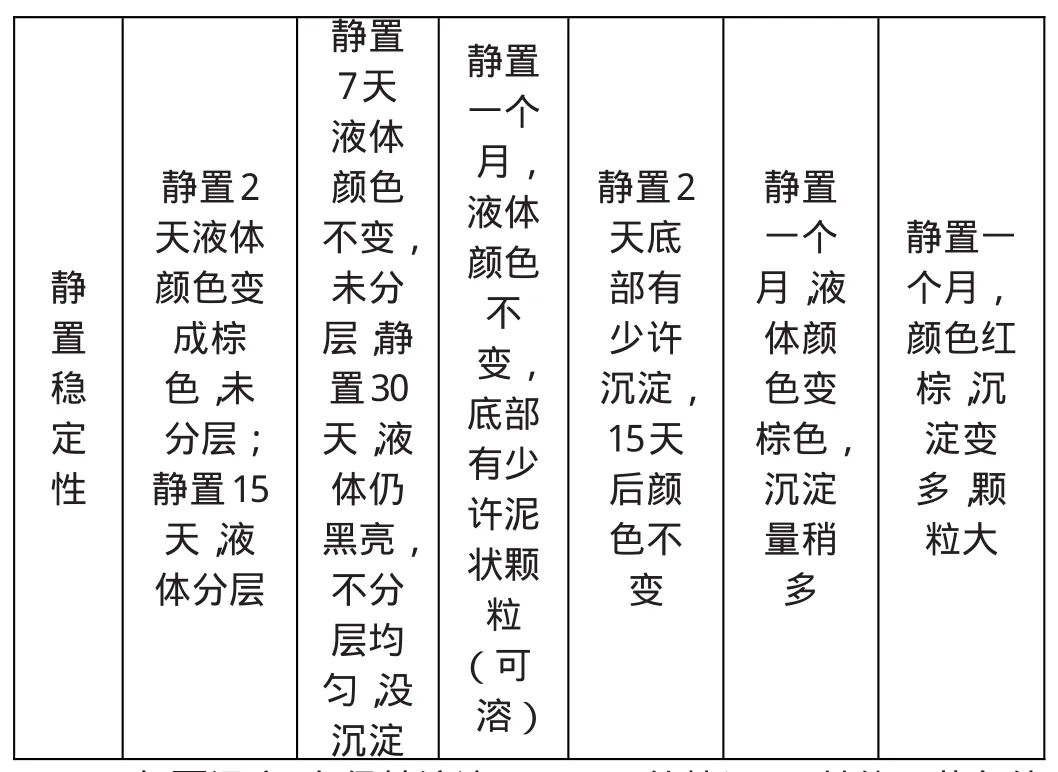
靜置穩定性靜置2天液體顏色變成棕色,未分層;靜置15天,液體分層靜置7天液體顏色不變,未分層;靜置30天,液體仍黑亮,不分層均勻,沒沉淀靜置一個月,液體顏色不變,底部有少許泥狀顆粒(可溶)靜置2天底部有少許沉淀,15天后顏色不變靜置一個月,液體顏色變棕色,沉淀量稍多靜置一個月,顏色紅棕,沉淀變多,顆粒大
(3)包覆溫度 在保持溶液pH=1-2的情況下,其他工藝條件不變的情況下,對于制備用L-谷氨酸作包覆劑的水基磁流體,本人經過多次實驗表明:L-谷氨酸包覆磁性粒子的最佳溫度是50℃,在此溫度下,其包覆量達到最大值,包覆得最完全,而且磁性粒子粒徑小,磁性高,穩定性好;如表3所示:
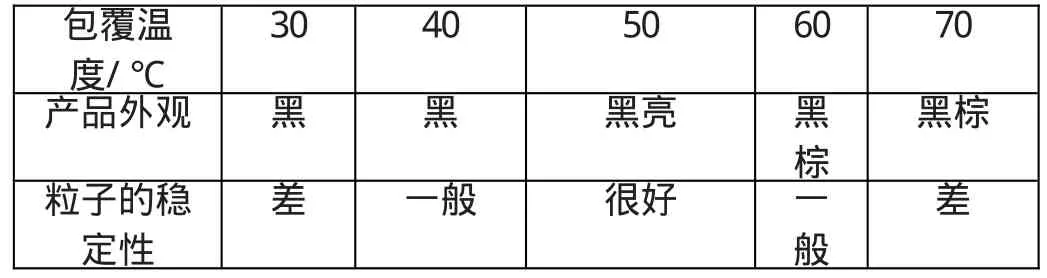
表3 包裹溫度對產物的影響
(4)包覆時間 根據文獻[8],一個表面活性劑分子通過溶劑化層和離子吸附層的擴散、滲透、取代、吸附進而牢固結合的過程,需要一定的時間才能形成牢固的表面活性劑包覆層。本實驗在密封的條件下,從不同時間和攪拌速度進行探討:
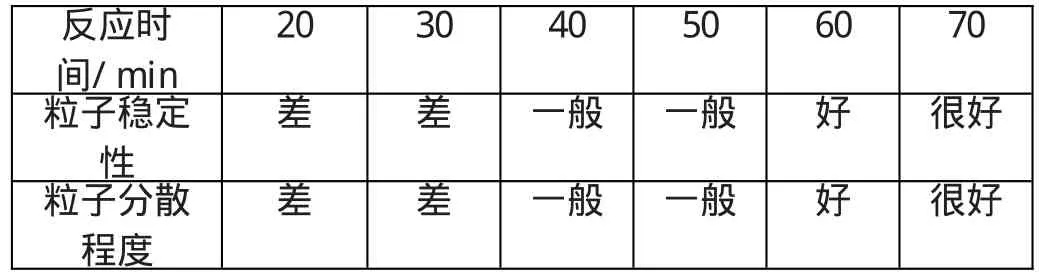
表4 反應時間的影響
表4結果表明,當包覆時間足夠長,攪拌足夠充分,所制得的粒子越難沉降,經過表面處理后,粒子的穩定性越高。這是因為包覆時間保證了攪拌時間足夠長,使螯合反應得以完全,反應過程形成的粒子團聚得到充分的打散,粒子變得越小,分散性越好。如果反應時間太短,就如表4所示,反應不完全,粒子的穩定性很差,分散性也不好。雖然包覆時間足夠長會更好,根據實驗室實際情況和為了節約時間和資源,包覆進行60m in已經足夠生成穩定性好分散程度好的磁流體。
(5)攪拌速度 在包覆劑包裹過程中,攪拌速度對磁性顆粒有著重要影響。本實驗中所用的攪拌器從起動到最大速,轉速從0到3000 r/m in,共分六等分,每格是500r/m in。本實驗在密封的條件下,探討了攪拌速度對產物的影響,(固定其它因素),具體見表5。
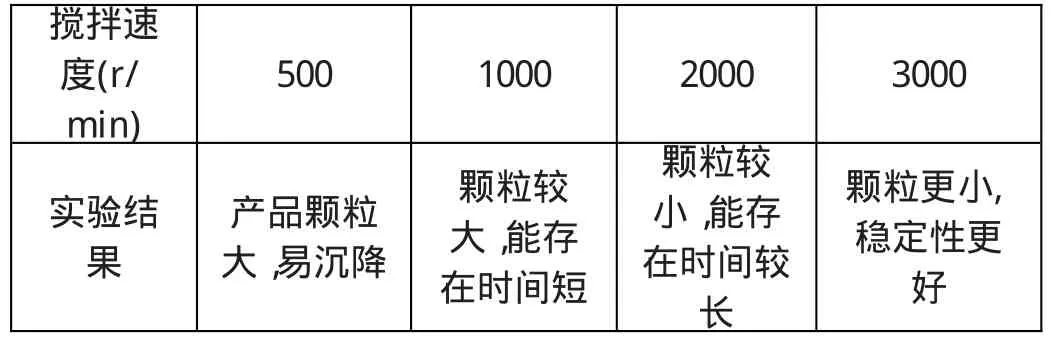
表5 攪拌速度對產物的影響
如果不攪拌,磁性顆粒會凝結成團狀,導致包裹無法繼續進行;攪拌速度過慢,制得的磁性顆粒粒徑大,包裹不均勻,不能使生成的顆粒得到及時的分散,最終會生成沉淀聚沉下來。由試驗表明:本人選擇在最大攪拌速度(3000r/m in)下進行反應和包覆,所制的磁流體效果最好。
(6)超聲波分散對產物的影響 利用超聲波溶解技術對產品分散,是加速試樣溶解的一種物理方法。一般適宜在室溫溶解樣品,根據需要調節功率和頻率,使之產生振蕩,可使試樣粉碎變小。
超聲波分散的原理是其所產生的瞬態高溫效應、空化效應在很小的范圍內形成高達數千大氣壓的壓力從而可以在固體或液體內部產生巨大的粉碎作用[5]。機械攪拌分散不能替代超聲波分散,機械攪拌是長程力的分散,適用于均勻混合和打開較大的團聚體。而超聲波是把小的團聚體打開,是一種短程力的分散,適用于打開較小的團聚體(納米級)。磁性微球的粒徑處于納米級別,具有巨大的表面自由能,吸附能力強,團聚趨勢大。雖然在反應過程中有強力攪拌防止其團聚長大,但是這個作用并不完全。另一方面,粒子在洗滌過程中采用磁鐵來幫助吸降,更加容易造成粒子的團聚。在開始時團聚屬于軟團聚,需要馬上將其分散,以防止進一步變成硬團聚。所以在洗滌、包覆完成后應馬上進行超聲波分散,分散過程中并用玻璃棒攪拌,可以達到更好的分散效果。表6可以說明超聲波分散的作用。

表6 超聲波分散對產物的影響
小結 以上各條件若控制得好,可以得到高質量的用L-谷氨酸包覆的水基磁流體。下面是本人總結前人的經驗和通過多次實驗得出的結果,總結出制備用L-谷氨酸包覆四氧化三鐵水基磁流體的最佳制備工藝條件,具體如下:
1.反應物Fe3+/Fe2+(物質的量)之比在1.70~1.75之間;
2.以25%NH3·H2O作為沉淀劑,沉淀劑應過量20~30%,這樣制出的粒子磁性較好;
3.在35℃條件下制備磁性粒子,溶液pH=9~11;
4.以L-谷氨酸作為包覆劑,L-谷氨酸的最佳用量是每50mL反應液0.0200g;
5.用L-谷氨酸包覆時的最佳溫度為50℃,包覆時間為60m in;
6.用L-谷氨酸包覆時的最佳pH=1.0~2.0;
7.反應階段和包覆階段攪拌速度都應該盡量調高(3000r/m in);
8.在洗滌和包覆粒子之后應馬上進行超聲波分散。
[1]熊隆榮,文玉華,易成,等.聚乙二醇-4000包覆Fe3O4磁流體的制備及穩定性研究[J].材料導報,2007,21(8):195-197.
[2]高道江,賴欣,王建華.磁性流體制備技術的現狀與展望[J].磁性材料及器件,1997,29(2):20-23.
[3]張銀燕,王遵義,等.納米磁性液體的制備和影響因素研究[J].湖南文理學院學報(自然科學版).2004,16(2):23-26.
[4]苑星海,林穗云.二次包裹Fe3O4磁性流體的制備與表征[J].廣州化工,2007,35(3):41-43.
[5]陳曉青,張俊山等.雙層表面活性劑分散制備水基磁流體[J].無機化學學報,2005,16(5):549-552.
[6]楊瑞成,鄖棟,穆元春.納米Fe3O4磁流體的制備及表征[J].蘭州理工大學學報,2008,34(1):22-25.
[7]趙靜,劉勇健.磁流體制備中表面活性劑的選擇及其包裹條件的影響[J].應用化工,2008,37(2):198-217.
[8]張金升,尹衍,張銀燕,馬來鵬,等.均勻超細Fe3O4磁流體的研究[J].應用進展,2003,22(5):494-498.
[9]張金升.磁性流體中納米Fe3O4包覆結構的研究[J].中國學報,2003,33(7):611-613.

