蘘荷紅色素分離純化及噴霧干燥工藝優化
卜曉英,卜小慶,楊 勇
(1.吉首大學 林產化工工程湖南省重點實驗室,湖南 張家界 427000;2.張家界市敦誼小學,湖南 張家界 427000;3.張家界市民族中學,湖南 張家界 427000)
蘘荷紅色素分離純化及噴霧干燥工藝優化
卜曉英1,卜小慶2,楊 勇3
(1.吉首大學 林產化工工程湖南省重點實驗室,湖南 張家界 427000;2.張家界市敦誼小學,湖南 張家界 427000;3.張家界市民族中學,湖南 張家界 427000)
研究分離純化及噴霧干燥化蘘荷紅色素的工藝條件。比較10 種大孔吸附樹脂對紅色素的靜態、動態吸附與解吸效果,紅色素純化液經真空濃縮后用噴霧干燥法制備紅色素的粉末。結果表明:LSA-21大孔吸附樹脂分離純化蘘荷紅色素效果好,其工藝條件為上柱液pH 5.0、上樣液質量濃度3.85 mg/mL、吸附流速 2 BV/h,以酸性蒸餾水為解吸劑,解吸流速3 BV/h;噴霧干燥工藝條件為加入待噴液質量 分數2%的可溶性淀粉,調整可溶性固形物質量分數 達到 12%~14%、進料速率3.0~4.0 kg/h、進口風溫度 174~177 ℃、出口風溫度 65~71 ℃、排風速率 0.34~0.38 m3/min、霧化壓強100 kPa。紅色素粉末經薄層層析色譜與高效液相色譜檢測均由3 種單體構成。
噴霧干燥;大孔吸附樹脂;紅色素;薄層層析色譜;高效液相色譜
蘘荷(Zingiber mioga Rosc.),俗稱野姜,為姜科姜屬多年生食藥同源蔬菜[1],而食用天然色素大多為花青素類、黃酮類、類胡蘿卜素類化合物,對人體健康沒有不良影響,安全性高,而且許多還具有營養、保健及藥效作用[2-4]。而合成色素對人體有一定的危害性,有的甚至有致癌作用,因此,不少合成色素在各國允許使用的程度被大大限制,尤其是在食品、醫藥和化妝品行業中,越來越多的國家開始禁止使用合成色素[5-7]。到目前為止,我國允許使用的食用合成色素有:日落黃、檸檬黃、莧菜紅、胭脂紅、赤蘚紅、誘惑紅、新紅、亮藍、靛藍和它們各自的色淀以及酸性紅、β-胡蘿卜素、氧化鐵黒(紅)、葉綠素銅鈉和二氧化鈦等,并對其使用范圍和最大使用量作了嚴格的限制[8-10]。利用食用植物提取天然色素符合消費者對天然健康食品趨勢的要求,受到消費市場青睞,因此用食物提取天然色素來取代合成色素已成必然趨勢[11-13]。
在前期微波燙漂輔助提取蘘荷中紅色素[14]的基礎上,研究蘘荷紅色素提取液經旋轉真空濃縮后LSA-21大孔吸附樹脂分離純化紅色素的效果[15-17],以及分離純化后紅色素溶液噴霧干燥法制備紅色素粉末的優化條件。尚未見對蘘荷紅色素大孔吸附樹脂分離純化和噴霧干燥制備紅色素粉末的報道,因此本實驗以武陵山區蘘荷紅色素為研究對象,利用LSA-21大孔吸附樹脂對紅色素進行分離純化并研究用小型GB-22噴霧干燥器制備紅色素粉末的工藝條件,為武陵山區蘘荷紅色素開發利用提供節能、環保性工業化生產工藝提供理論依據。
1 材料與方法
1.1 材料與試劑
蘘荷采集于湖南省張家界山區沙提蘘荷種植基地,洗去泥沙,取苞片,瀝干水分,置于-4 ℃冰箱中保存備用;大孔吸附樹脂 LX-5、D101、AB-8、LSA-10、LSA-21、LSA-40、XDA-1、LX-17、LSA-7、XDA-7 安徽三星樹脂科技有限公司;硅膠G 青島海洋化工有限公司;羧甲基纖維素鈉(carboxymethylcellulose sodium,CMCNa) 上海德津實業有限公司。
丙酮、甲醇、無水乙醇、95%乙醇、乙酸乙酯、石油醚、乙酸、甲酸、36% HCl溶液、2% NaOH溶液、NaCl均為分析純;酸性乙醇用無水乙醇與質量分數36% HCl溶液配制,且現用現配,酸性蒸餾水用36% HCl溶液調pH值至4.5~5.5;CMC-Na(質量分數1%)溶液現用現配。
1.2 儀器與設備
AEG-220電子分析天平、RE540-AW旋轉蒸發儀、LC-20AT型高效液相色譜儀 日本島津公司;D8023CTL-K4微波爐 格蘭仕集團;UV3900紫外-可見分光光度計 日本日立公司;LGJ-1真空冷凍干燥儀 西安中諾爾儀器有限公司;HH-6恒溫水浴鍋 富華儀器公司;MHA恒溫電熱套 北京科永興儀器有限公司;SHE-D(Ⅲ)循環水式真空泵 予華儀器有限責任公司;FD-230紅外水分儀 日本KETT公司;MDF-292AT超低溫冰箱 日本三洋公司;DF42恒溫干燥箱、DN-63烘箱、GB-22小型噴霧干燥器 日本雅馬拓公司;HM-20S便攜pH計 日本TOA公司。
1.3 方法
1.3.1 蘘荷紅色素的提取
取蘘荷新鮮材料100 kg按文獻[14]所選提取條件,分20 批次經微波燙漂處理后,用體積分數60%的酸性乙醇按料液比1∶60(g/mL)、溫度 55 ℃ 、時間40 min進行紅色素提取。每份提取液用旋轉蒸發儀在50 ℃、40 r/min的真空條件下濃縮,得20 份500 mL濃縮液待用。
1.3.2 大孔吸附樹脂的選擇
1.3.2.1 大孔吸附樹脂預處理
稱取10 種大孔吸附樹脂各10.00 g,先以蒸餾水浸泡12 h,再用質量分數40% 的NaCl 溶液浸泡12 h,然后用質量分數2% NaOH溶液攪拌浸泡5 h,水洗至中性,再用質量分數5% HCl溶液攪拌浸泡5 h,水洗至中性,最后用體積分數70%乙醇浸泡12 h,水洗至無絮狀物,去離子水浸泡備用。
1.3.2.2 大孔吸附樹脂靜態吸附
將10 種濕樹脂自然風干,紅外水分儀測各自水分含量,按比例稱相當干質量3.00 g大孔吸附樹脂于100 mL錐形瓶中,分別加入20 mL已濃縮的蘘荷紅色素溶解液,攪勻后靜置,室溫條件下靜態交換6 h過濾,測定吸附前、后紅色素溶液535 nm波長處的吸光度,以紅色素濃縮原液質量分數為1計算出各樹脂對紅色素的吸附量與吸附率。
1.3.2.3 大孔吸附樹脂靜態解吸
將1.3.2.2節吸附了蘘荷紅色素的大孔吸附樹脂分別置于20 mL體積分數為70%的酸性乙醇中,室溫條件下靜置解吸6 h,濾液用紫外分光光度計測其535 nm波長處的吸光度,計算出各樹脂對紅色素的解吸率。
1.3.3 解吸劑的選擇
稱取處理好的LSA-21樹脂3.00 g(相當干質量)共6 份,分別加入20 mL紅色素濃縮液,6 h后過濾,用50 mL醇體積分數60%的乙醇、酸性乙醇、甲醇、丙酮、蒸餾水和酸性蒸餾水各解吸一組已吸附的樹脂,測各解吸液535 nm波長處的吸光度。
1.3.4 不同質量濃度色素液對LSA-21樹脂吸附的影響
稱取5 份處理好的LSA-21樹脂3.00 g(相當干質量),分別加入20 mL上述解吸液經旋轉真空濃縮、冷凍干燥成粉末的紅色素所配成質量濃度為7.85、3.85、2.56、1.18、0.876 mg/mL的紅色素溶液,置50 ℃恒溫水浴鍋中,每隔1 h取樣檢測溶液中紅色素質量濃度,按下式計算LSA-21樹脂吸附紅色素的量。
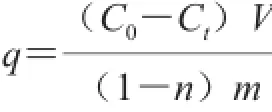
式中:q為樹脂吸附量/(mg/g);C0為溶液初始質量濃度/(mg/mL);Ct為t時刻時質量濃度/(mg/mL);V為溶液體積/mL;m為樹脂質量/g;n為樹脂含水量/%。
1.3.5 上柱液pH值對LSA-21樹脂吸附的影響
稱取6 份已處理好的LSA-21樹脂各3.00 g(相當干質量),加入質量濃度為3.85 mg/mL的溶液,pH值分別為3、4、5、6、7、8的紅色素粉末液20 mL,于50 ℃恒溫水浴鍋中靜置6 h,測濾液535 nm波長處的吸光度并計算樹脂吸附量。
1.3.6 LSA-21樹脂的動態吸附與解吸實驗
取20.0 g LSA-21樹脂(3 份)按濕法裝柱,分別用2、3、4 BV/h的流速對紅色素溶液進樣,按每管5 mL收集流出液,稀釋至10 mL測流出液535 nm波長處的吸光度,至流出液質量濃度與進樣質量濃度一致來檢測LSA-21樹脂動態吸附量;然后用酸性蒸餾水分別以2、3、4 BV/h的流速對其進行解吸,按每管5 mL收集解吸液,稀釋至10 mL,測定各管解吸液535 nm波長處的吸光度,以紅色素的吸光度代替其含量進行比較分析。
1.3.7 蘘荷紅色素解吸液噴霧干燥條件的優化[18-20]
為探索噴霧干燥最佳工藝參數,在霧化壓強確定為100 kPa的情況下,本研究選用A進口風溫度、B出口風溫度、C進料速率、D排風速率、E可溶性淀粉添加量、F待噴霧溶液質量分數 6 個影響因素,按文獻[20]設計正交試驗方案進行噴霧干燥條件優化,每個處理重復3 次,每次500 mL。因素水平安排見表1,試驗設計及結果見表2。

表1 噴霧干燥正交試驗因素水平Table 1 Factors and levels used in orthogonal array design for spray drying

表2 紅色素溶液噴霧干燥正交試驗設計Table 2 Orthogonal array design scheme for spray drying
按選擇的噴霧干燥條件對10.0 kg蘘荷樣品提取液經真空濃縮與大孔吸附樹脂吸附分離純化后的溶液進行噴霧干燥,在控制室內相對濕度低于65%時,將色素粉末過200 目篩后密封于干燥器中保存待測。
1.3.8 薄層層析色譜(thin layer chromatography,TLC)分析
1.3.8.1 硅膠薄板的制備
將1 份硅膠G和3 份CMC-Na溶液在研缽中研磨混勻,去除表面氣泡,然后將其均勻涂布(厚度為0.25 mm)于玻璃平板上,置水平臺上室溫晾干,110 ℃活化30 min,置密封干燥劑中保存備用。
1.3.8.2 蘘荷紅色素的層析檢測
稱取蘘荷紅色素粉末3.85 g,用酸性乙醇溶解并定溶于1 000 mL容量瓶中,得3.85 mg/mL紅色素溶液,用該溶液點樣50 μL于硅膠G薄層板上,在展層劑正丁醇-乙酸-水(4∶1∶2,V/V)中展開。
1.3.9 高效液相色譜(high performance liquid chromatography,HPLC)分析
色譜條件:SpheriSorb ODS C18(250 mm×4.6 mm,5 μm)色譜柱,柱溫為室溫,流速為1.00 mL/min,進樣量20 μL,質量濃度3.85 mg/mL,流動相為甲醇-水-甲酸(39.5∶60∶0.5,V/V),檢測器為紫外吸收檢測器。
2 結果與分析
2.1 大孔吸附樹脂的選擇

表3 樹脂的選型Table 3 Adsorption and desorption performance of ten kinds of macroporous reessiinn
由表3可知,LSA-21、LSA-40兩種中極性樹脂及XDA-1、LX-17、LSA-7三種極性樹脂對蘘荷紅色素的吸附能力較強;LSA-21型中極性樹脂及LX-5型非極性樹脂對蘘荷紅色素的解吸能力較強;從吸附與解吸效果來看,LSA-21的吸附率與解吸率均較大,綜合考慮,選擇LSA-21為蘘荷紅色素的大孔吸附樹脂。
2.2 解吸劑的選擇
用體積分數60%的乙醇、酸性乙醇、甲醇、丙酮、蒸餾水和酸性蒸餾水解吸已吸附蘘荷紅色素的LSA-21樹脂,解吸液的535 nm波長處吸光度見表4,乙醇及酸性乙醇的解吸效果較好,但考慮到工業生產的成本以及噴霧干燥時乙醇易爆炸的特性,同時酸性蒸餾水與乙醇的解吸效果相差不大,因此本研究選擇酸性蒸餾水作為解吸劑。

表4 不同洗脫液中紅色素的測定結果Table 4 Effect of different solvents on the desorption efficiency of red pigment
2.3 不同色素質量濃度對LSA-21樹脂吸附紅色素的影響
LSA-21樹脂對質量濃度分別為7.85、3.85、2.56、1.18、0.876 mg/mL紅色素的吸附效果見圖1,顯示LSA-21樹脂對紅色素吸附起始階段呈線性加速,隨后逐漸趨于平緩,最后達到吸附平衡。吸附速率與溶液質量濃度密切相關,溶液質量濃度為7.85 mg/mL時樹脂吸附平衡所需時間約1 h到質量濃度0.876 mg/mL平衡所需時間約6 h不等,因此初始質量濃度選擇為3.85 mg/mL。
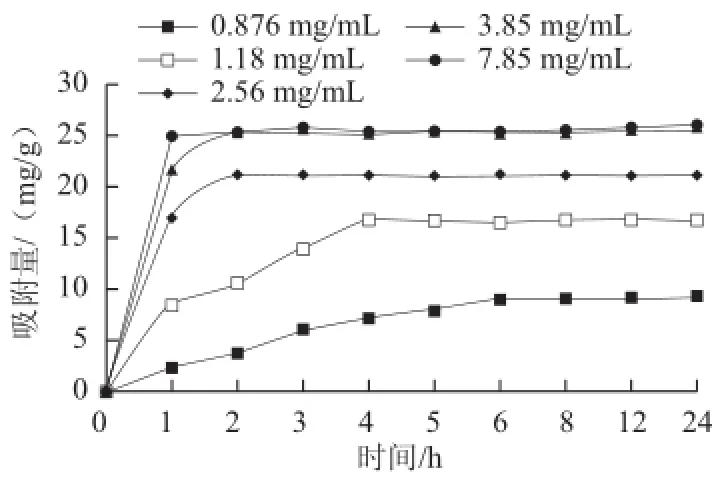
圖1 不同質量濃度紅色素溶液的吸附量動態變化圖Fig.1 Dynamic adsorption curves of red pigment with different concentrations
2.4 上柱液pH值對樹脂吸附的影響

圖2 上柱液不同pH值對吸附量的影響Fig.2 Effect of sample pH on adsorption quantity
由圖2可見,當上柱液pH值為4~5時紅色 素的吸附效果最好,上柱液的pH 5.0時達到高點,而隨著上柱液pH值的繼續升高,吸附率明顯下降,但樹脂上仍有一定的吸附量,因此選擇上柱液pH值為5.0。
2.5 吸附流速對樹脂動態吸附效果的影響

圖3 不同流速條件下色素在樹脂上的動態吸附曲線Fig.3 Effect of sample loading flow rate on adsorption efficiency
當用質量濃度為3.85 mg/mL的紅色素溶液分別以 2、3、4 BV/h流速進樣時,各進樣液前20 管流出液中紅色素質量濃度基本一致(圖3),而收集時間差異明顯。收集21~40 管流出液時,紅色素質量濃度在流出液中增大。至流出液質量濃度與進樣質量濃度一致時各進樣流速平均需收集120、103、92 管,耗時平均分別為3.2、3.0、2.5 h,綜合考慮選擇進樣流速為2 BV/h。
2.6 解吸流速對解吸效果的影響

圖4 解吸流速對樹脂上紅色素解吸的影響Fig.4 Effect of desorbent flow rate on desorption efficiency
分別采用不同流速對已吸附色素的樹脂進行解吸,結果如圖4所示。解吸流速為2、3、4 BV/h時,開始洗脫時洗脫效果相差較大,即當洗脫液流速為4 BV/h時,開始階段解吸效果明顯較弱,而2 BV/h流速的解吸效果較好(圖4),雖然解吸流速越慢效果越好,但太慢又會使工作周期延長,綜合考慮,選擇解吸液流速為3 BV/h。
2.7 噴霧干燥優化結果
蘘荷紅色素溶液噴霧干燥正交試驗結果以噴霧干燥制品的含水量、溶解時間、紅色素在水溶液中的溶解性和粉末的吸濕性為檢驗指標,各指標按文獻[21]的方法測定,對各因素進行綜合考察,選出蘘荷紅色素溶液噴霧干燥的優化試驗條件,3 次平行結果見表5。

表5 紅色素溶液噴霧干燥正交試驗結果Table 5 Results of the orthogonal array design for spray drying
運用文獻[20]對正交試驗分析,對表5的試驗結果結合實驗儀器性能進行綜合評選,得出蘘荷紅色素溶液噴霧干燥的優化實驗條件如下:加入待噴液質量分數2%的可溶性淀粉,用以調整其可溶性固形物質量分數達到12%~14%;進料速率3.0~4.0 kg/h;進口風溫度174~177 ℃;出口風溫度65~71 ℃;排風速率0.34~0.38 m3/min;霧化壓強100 kPa。
2.8 薄層層析及高效液相色譜分析
蘘荷紅色素在展層劑中分離結果見圖5,經LSA-21樹脂分離純化后的蘘荷紅色素經薄層層析出現3 個分離點,檢測與計算三點的比移值(Rf)分別為0.285、0.335、0.449,據此可知該紅色素由3 個組分構成。

圖5 薄層層析圖譜Fig.5 TLC profile
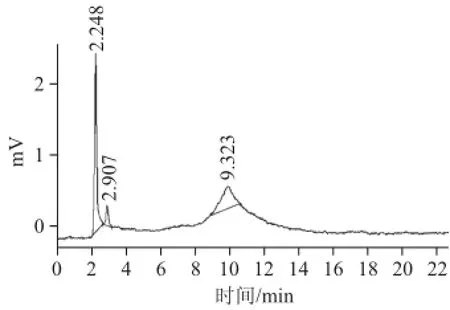
圖6 高效液相色譜圖譜Fig.6 HPLC chromatogram
按上述HPLC色譜條件進行紫外檢測器的檢測其結果見圖6,經LSA-21純化后的蘘荷紅色素的HPLC檢測時出現3 個波峰,可見該紅色素溶液由3 個組分構成。由薄層層析與高效液相色譜檢測結果可知LSA-21樹脂對蘘荷紅色素的分離純化較好。
3 結 論
本研究通過對10 種大孔吸附樹脂對蘘荷紅色素的靜態吸附與解吸、動態吸附與解吸實驗,研究各大孔吸附樹脂對紅色素的分離純化效果。結果LSA-21樹脂對蘘荷紅色素分離純化效果最佳,分離純化時上柱液pH 5.0、上樣液質量濃度3.85 mg/mL、吸附流速2 BV/h,以酸性蒸餾水為解吸劑,解吸液流速3 BV/h。
將可溶性淀粉按質量分數2%加入到紅色素濃縮液中,充分攪勻,去除雜質沉淀,使可溶性固形物含量達到12%~14%。通過正交試驗研究了噴霧干燥的最佳工藝條件:進料速率3.0~4.0 kg/h、進口風溫度174~177 ℃、出口風溫度65~71 ℃、排風速率0.34~0.38 m3/min、霧化壓強100 kPa;按以上條件對10.0 kg蘘荷樣品提取液經真空濃縮與大孔吸附樹脂吸附分離純化后的溶液進行噴霧干燥,噴霧干燥所得紅色素粉末經檢測各項指標都達到或超過了文獻[15]中的各項指標,通過薄層層析與HPLC法檢驗了LSA-21分離純化后噴霧干燥成粉末的蘘荷紅色素,顯示該紅色素均由3個組分構成。因此LSA-21樹脂完全適合蘘荷紅色素的分離純化,經檢測噴霧干燥所得紅色素粉末含水量約4.25%、在水中溶解時間約148s、溶解性0.719、色價13.17、吸濕性0.069 3,其微生物的含量遠低于國家標準(細菌總數(個/g)<100、大腸桿菌(個/g)<20、致病菌未檢出),說明此噴霧干燥法完全適宜于工業化生產。
[1] 吳德鄰. 中國植物志[M]. 北京: 科學出版社, 1981: 140.
[2] 魏麗, 童軍茂. 大孔樹脂純化向日葵籽殼紅色素的研究[J]. 食品工業科技, 2010, 31(6): 263-266.
[3] 劉偉, 黃立新, 張彩虹. 天然梔子黃色素的低溫真空干燥研究[J].林產化學與工業, 2011, 31(1): 57-62.
[4] ARAPITSAS P, SJOBERG P J, TURNER C. Characterisation ofanthocyanins in red cabbage using resolution liquid chromaigraphy coupled with photodiode array detection and electrospray ionization-linear ion trap mass spectromery[J]. Food Chemistry, 2008, 109(1): 219-226.
[5] MEKKAWY H A, ALI M O, El-ZAWAHRY A M. OP3A18—Toxic effect of synthetic and natural food dyes on renal and hepatic functions in rats[J]. Toxicology Letters, 1998, 95(S1): 155.
[6] PAZMI?O-DURáN E A, GIUSTI M M, WROLSTAD E, et al. Anthocyanins from Oxalis triangularis as potential food colorants[J]. Food Chemistry, 2001, 75(2): 211-216.
[7] 楊青珍, 王鋒, 孫元琳. 甜櫻桃果實紅色素的提取和穩定性研究[J].食品科學, 2010, 31(4): 120-122.
[8] 劉成梅, 游海. 天然產物有效成分分離與應用[M]. 北京: 化學工業出版社, 2003: 442.
[9] 胡金奎, 戴軍, 張九勛, 等. 樹脂法分離純化桑葚花色苷[J]. 食品與發酵工業, 2012, 38(8): 190-196.
[10] 丁成翔, 代漢慧, 陳冬東. 六種著色劑毒性研究進展[J]. 檢驗檢疫學刊, 2009, 19(2): 70-73.
[11] 錢疆, 楊方, 陳弛, 等. 超高效液相色譜飛行時間質譜測定食品中36 種合成色素[J]. 食品科學, 2013, 34(6): 215-218.
[12] 董愛文, 唐純翼, 向中, 等. HPD-600樹脂吸附和分離爬山虎色素及色素的理化性質研究[J]. 食品科學, 2004, 25(4): 74-80.
[13] 許立松, 馬銀海. 大孔樹脂吸附法提取玫瑰茄紅色素[J]. 食品科學, 2009, 30(12): 120-122.
[14] 卜曉英, 唐克華, 陳曉華, 等. 微波燙漂蘘荷苞片后紅色素提取工藝條件的研究[J]. 食品工業科技, 2012, 33(21): 227-230.
[15] 趙慧芳, 李維林, 王小敏, 等. 黑莓果實色素純化及干燥工藝研究[J].食品科學, 2009, 30(12): 35-39.
[16] 劉晶晶, 劉進前, 王雪鋒, 等. 樹脂法純化鴨血糯色素的研究[J]. 食品科學, 2011, 32(12): 156-159.
[17] 劉廣文. 噴霧干燥[M]. 北京: 化學工業出版社, 2005: 58-69.
[18] SEDA E, YURDAGEL U M I. Croencapsulation of anthocyan in pigments of black carrot (Daucus carota L.) by spray drier[J]. Journal of Food Engineering, 2007, 80: 805-812.
[19] RODRíGUEZ-HERNáNDEZ G R, GONZáLEZ-GARCíA R, GRAJALES-LAGUNES A, et al. Spray drying of cactus pear juice (Opuntia streptacantha): effect on the physicochemical properties of powder and reconstituted product[J]. Drying Technology, 2005, 23(4): 955-973.
[20] 方開泰. 均勻設計[J]. 戰術導彈技術, 1994, 3(1): 55-56.
[21] 董愛文, 卜曉英, 李悅豐. 噴霧干燥法制備爬山虎色素粉末工藝條件研究[J]. 食品科學, 2010, 31(2): 6-9.
Separation and Purification by Macroporous Resin, and Spray Drying of Red Pigment from Zingiber mioga Rosc.
BU Xiao-ying1, BU Xiao-qing2, YANG Yong3
(1. Forest Products Chemical Engineering Key Laboratory of Hunan Province, Jishou University, Zhangjiajie 427000, China; 2. Zhangjiajie Dun Yi Primary School, Zhangjiajie 427000, China; 3. Zhangjiajie Min Zu Middle School, Zhangjiajie 427000, China)
Objective: To investigate the separa tion and purification of red pigment from the bracts of Zingiber mioga Rosc. and the preparation of red pigment powder by spray drying. Methods: Comparison of ten kinds of macroporous resin was carried out for the static and dynamic adsorption and desorption of red pigment. The purified red pigment was vacuumconcentrated before spray drying. Results: LSA-21 macroporous resin was found to be the best sorbent for the purification of red pigment. The best results were obtained when the sample (3.85 mg/mL, pH 5.0) was loaded at a flow rate of 2 BV/h and the adsorbed red pigment was eluted with acidified distilled water at a flow rate of 3 BV/h. The purified pigment solution was added with 2% soluble starch a nd adjusted to a soluble solid content of 12%-14% prior to spray drying at a feeding rate of 3.0-4.0 kg/h, an air inlet temperature of 174-177 ℃, an air outlet temperature of 65-71 ℃, an exhaust velocity of 0.34–0.38 m3/min, and an atomization pressure of 100 kPa. The resulting powder consisted of three monomers as detected by high performance liquid chromatography (HPLC) and thin layer chromatograph (TLC). Conclusion: LSA-21 macroporous adsorption resin is applicable for separation and purification of red pigment from Zingiber mioga Rosc. and the optimized spray drying conditions are suitable for industrial production of red pigment powder from Zingiber mioga Rosc.
spray drying; macroporous resin; red pigment; TLC; HPLC
TS202.3
A
1002-6630(2014)22-0104-05
10.7506/spkx1002-6630-201422019
2014-03-24
張家界市科技局科技計劃項目(2013YB26;2014ZK02);湖南省重點實驗室——“林產化工重點實驗室”開放基金資助課題(JDZ201404);湖南省科技廳科技計劃項目(2013NK3078);生態旅游湖南省重點實驗室開放基金資助課題(JDSTLY1403)
卜曉英(1971—),女,高級實驗師,碩士,研究方向為藥用植物及功能食品。E-mail:xyingbu@163.com

