新疆額爾齊斯河周叢藻類群落結構特征研究
李 君周 瓊謝從新王 軍韋麗麗
(1. 華中農業大學水產學院, 農業部淡水生物繁育重點實驗室, 武漢 430070; 2. 淡水水產健康養殖湖北省協同創新中心,武漢 430070)
LI Jun1,2, ZHOU Qiong1,2, XIE Cong-Xin1,2, WANG Jun1,2and WEI Li-Li1,2
(1. Key Laboratory of Freshwater Animal Breeding, College of Fishery, Ministry of Agriculture, Huazhong Agricultural University, Wuhan 430070, China; 2. Freshwater Aquaculture Collaborative Innovation Center of Hubei Province, Wuhan 430070, China)
新疆額爾齊斯河周叢藻類群落結構特征研究
李 君1,2周 瓊1,2謝從新1,2王 軍1,2韋麗麗1,2
(1. 華中農業大學水產學院, 農業部淡水生物繁育重點實驗室, 武漢 430070; 2. 淡水水產健康養殖湖北省協同創新中心,武漢 430070)
周叢藻類是新疆跨境河流土著及特有魚類重要的基礎餌料資源, 然而在該地區有關周叢藻類的研究目前尚屬空白。有鑒于此, 2012年7、8、10月對新疆跨境河流——額爾齊斯河全流域的周叢藻類群落結構進行了系統的調查分析。結果表明, 周叢藻類隸屬7門70屬178種, 由硅藻門、綠藻門、藍藻門、裸藻門、黃藻門、金藻門和甲藻門組成, 其中硅藻門有 92種并占據絕對優勢(51.7%), 綠藻門 49種(30.3%), 藍藻門20種(11.8%), 裸藻門5種(2.8%), 黃藻門3種(1.7%), 金藻門2種(0.1%), 甲藻門僅1種(0.6%), 周叢藻類在不同月份的種類數存在顯著差異(P<0.01)。優勢種主要為硅藻門的嗜鹽舟形藻(Navicula halophila)、鈍脆桿藻(Fragilaria capucina Desm)、極小橋彎藻(Cymbella perpusilla Cl)以及藍藻門的皮狀席藻(Phormidium corium Gom)等。研究期間, 額爾齊斯河周叢藻類的密度和生物量的均值分別為1105.5×106ind./m2和2692.0 mg/m2, 不同月份間密度和生物量的分布差異不顯著, 但在空間分布上整體趨勢為中下游地區高于上游地區。水溫和營養鹽成為影響其分布的主要環境因子。Simpson多樣性指數、Shannon-Wiener多樣性指數、Pielou均勻度指數和Margalef豐富度指數的平均值分別是0.38、3.04、0.66和2.55。運用多樣性指數和藻類豐度對額爾齊斯河水質評價為輕度污染。
周叢藻類; 種群結構; 豐度; 多樣性指數; 水質評價; 額爾齊斯河
額爾齊斯河, 是我國唯一流入北冰洋的河流,源出中國阿爾泰山西南坡, 自東南向西北奔流出國,經俄羅斯的鄂畢河注入北冰洋。全長2969 km, 在中國境內546 km, 流域面積5.7萬km2, 年徑流量多達119億 m3, 水量僅次于伊犁河居新疆第二位, 號稱新疆第二大河[1]。額爾齊斯河上游主要靠融雪、融冰和降水補給, 下游主要來源于融雪、降水和土壤中的水[2]。額爾齊斯河不僅水資源豐富, 也是新疆水生生態環境保持較為原始的區域。上游坡降較大,水溫較低, 水流湍急, 是高山冷水性水生生物良好的棲息場所, 該流域棲息有哲羅鮭(Hucho taimen Pallas, 俗稱大紅魚)、細鱗鮭(Brachymystax lenok Pallas, 俗稱小紅魚)、北極茴魚(Thymallus arcticus arcticus Pallas)等珍稀、瀕危魚類[3]。
周叢藻類即著生藻類, 是指浸沒在水中各種基質表面的有機體集合[4], 它不僅是湖泊重要的初級生產力, 而且為魚類、底棲動物等提供豐富的食物來源[5], 同時由于其方便采集、對外來干擾敏感性強及固著生長等特性, 著生藻類已經廣泛應用于河流生態系統的環境評價[6]。額爾齊斯河流域常年棲息著多種珍稀特有的名貴魚類, 隨著人類經濟活動的加劇, 如: 水利工程建設、農業灌溉和工業引排水等,對土著與特有魚類及其餌料資源產生嚴重的影響。周叢藻類作為土著和特有魚類的重要餌料資源, 其生態功能非常關鍵。對額爾齊斯河流域的周叢藻類種類組成、優勢種屬、時空分布及群落多樣性指數進行了調查分析, 并首次報道新疆地區跨境河流周叢藻類群落結構特征。比較全面了解和掌握該水域水生生物物種資源狀況, 從而更加有效地利用水生生物監測水質并保護新疆跨境河流土著、特有魚類種質資源。
1 材料與方法
1.1 采樣位置與采樣時間
額爾齊斯河流域具有較長的冰封期(11月初至翌年 4月中旬)[2], 根據額爾齊斯河的氣候條件, 本研究選擇7月、8月和10月作為采樣時間。根據額爾齊斯河的生態特點, 上游為山區, 中游為半山區, 下游為荒漠平原區[7], 在額爾齊斯河的干流、主要支流及重要附屬水體設置了10個采樣點(表1), 從下游到上游的順序依次為: 185團(北灣)、別列則克、哈巴河大橋、托洪臺水庫、布爾津河口、充乎爾大橋、小635、克蘭河上游、富蘊縣、可可托海。各采樣點的設置主要依據河道情勢、交通條件、采樣條件等因素。
1.2 樣品的采集和處理
用 MAGELLAN 全球定位系統( eXplorist-200)記錄采樣點的經緯度和海拔高度(表1)。在采樣點河流上下游 100 m 范圍內, 依據河流生境的不同(流速、水深和透明度), 對周叢藻類進行定性和定量樣品的采集。周叢藻類定性樣品是采用天然基質采樣法, 采集附有藻類的石頭用硬毛刷將附著其上的藻類刷入裝有蒸餾水的磁盤中, 定量至 1000 mL, 回到實驗室濃縮至50 mL樣品瓶中, 采用甲醛溶液固定[8]。定量樣品是選擇附有藻類的形狀規整、易于測量表面積的石塊, 用毛刷刮取藻類并用蒸餾水沖刷至不銹鋼托盤中后裝入 1 L塑料瓶中, 用魯哥氏液 15 mL固定, 帶回室內沉淀 24h后至樣品瓶中,定容至50 mL。水質指標采用alalis MP3500便攜式pH/電導率/溶氧儀現場測定。
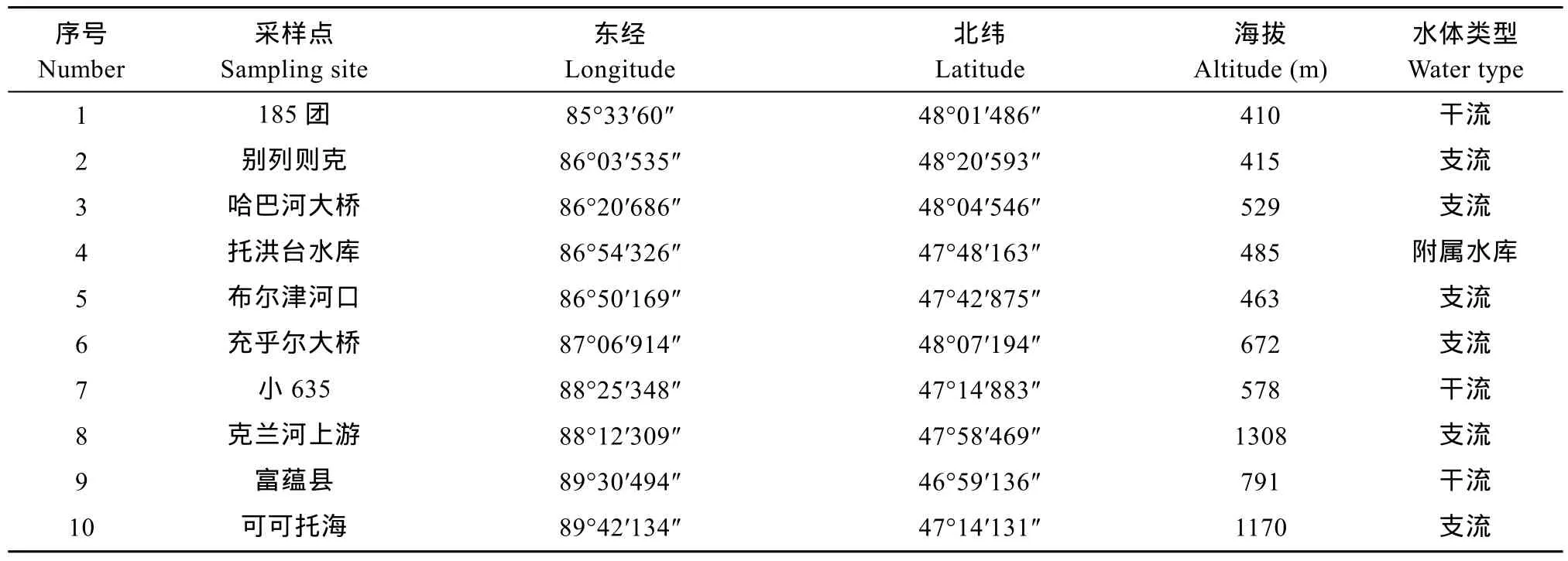
表1 額爾齊斯河采樣點分布Tab.1 Sampling sites in the Irtysh River
1.3 周叢藻種類的鑒定與計數
將處理好的樣品在×40倍光學顯微鏡下觀察, 用面積為20 mm×20 mm, 容量為0.1 mL計數板對周叢藻類進行計數, 每片計數不得少于300個, 每瓶樣品計數2次, 2次計數結果之差應在15%之內, 否則增加計數次數, 有效統計數值取平均后即為該片的周叢藻類數量。每一樣品的周叢藻類密度由單位面積上的細胞個體數表示(ind./m2)。藻類的鑒定主要參照《中國淡水藻類》[9]。最后計算出人工基質上每種著生藻類的相對豐度(用百分含量表示) 和每個采樣點的藻密度。生物量的測算采用體積換算法[10]。根據周叢藻類的體形, 按最近似的幾何形測量其體積,形狀特殊的種類分解為幾個部分測量, 然后結果相加。由于藻類的密度接近1, 故可以直接由藻類的體積換算成生物量。生物量為各種藻類的數量乘以各自的平均體積, 單位為mg/m2。
1.4 數據處理與統計分析
多樣性的分析

式中 Ni為i種的個體數, N為所有種類總個體數, S為物種數。H′ 值0—1為重污, 1—3為中污 (其中1—2為α-中污, 2—3為β-中污), > 3為輕污或無污[14]。
優勢種的確定 全年調查周叢藻類的優勢種根據每個種的優勢度值(Y)來確定:
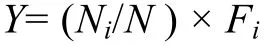
式中, Ni為i種的個體數, N為所有種類總個體數, Fi為第i種出現的頻率。Y值大于0.02的種類為全年調查的優勢種[15]。
統計分析 多樣性指數、優勢度的計算均在Excel 2003中完成, 周叢藻類的種類數量、密度、生物量及多樣性指數在不同采樣季節和采樣點之間的差異通過單因子方差分析(One-way ANOVA)進行處理, 密度和與環境因子(水溫、水深、透明度、流速、pH、鹽度)的相關性分析用偏相關分析(Pearson-Correlation)處理。差異水平設置為P=0.05和P=0.01。統計分析軟件為SPSS 19.0, 圖表的繪制均在Origin 8.0中進行。
2 結果
2.1 種類組成與優勢種
光程倍增光纖陀螺的偏振誤差,可分為振幅型和強度型.本文主要考慮偏振環行器的插入帶來的偏振誤差.由于偏振合束器由晶體、轉置器和尾纖組成,所以可將晶體與轉置器以及轉置器與尾纖之間的耦合點視為一個耦合點,在圖1中用點A、B、C、D、E、F來表示;a、b、c、d、e、f分別為對應轉置器的耦合尾纖中的串擾點.設經Y波導后輸入偏振環行器的順(CW)、逆(CCW)時針光束與分別沿平行偏振軸與垂直偏振軸方向傳輸,考慮到實驗所用的Y波導消光比ε達50 dB以上,所以本文僅考慮波列.光路中耦合點的功率串擾系數統一表示為ρ,偏振環行器損耗幅值系數與線圈損耗功率系數分別為α、γ.
當前研究的采樣點涵蓋了額爾齊斯河干流、支流及其附屬水體(表1)。在10個樣點所采得的周叢藻,共檢查到硅藻門(Bacillariophyta)、藍藻門(Cyanophyta)、綠藻門(Chlorophyta)、黃藻門(Cryptophyta)、裸藻門(Euglenophyta) 、甲藻門(Pyrrophyta)和金藻門(Chrysophyta)等7個門類, 共計70屬178種。其中硅藻、綠藻和藍藻的數量占到了93.8%, 以硅藻的種類數最多, 為92種占51.7%; 其次是綠藻有49種占30.3%; 藍藻的種類數位居第3, 20種占11.8%; 黃藻3種占1.7%, 裸藻5種占2.8%; 金藻2種占1.1%, 甲藻僅1種占0.6%。
從周叢藻種類的時間分布來看, 8月份最多為95種, 其次為10月份和7月份, 分別為65種和50種, 三個季節間的種類數差異極其顯著(P= 0.006)。從周叢藻在各水域的分布來看, 7月以富蘊、克蘭河、布爾津、小635最多, 分別為26種、18種、17種、17種; 8月份以185團、充乎爾和克蘭河最多, 分別為35種、35種、30種; 10月份185團、富蘊、別列則克最多, 分別為29種、26種和22種, 相比于8月份有所下降。
調查期間, 7月份的優勢種為硅藻門的嗜鹽舟形藻、橢圓舟形藻、短小舟形藻、極小舟形藻、弧形峨眉藻、雙頭菱形藻以及藍藻門的兩棲顫藻。8月份的優勢種為硅藻門的嗜鹽舟形藻、近緣橋彎藻、胡斯特橋彎藻、扁圓卵形藻、鈍脆桿藻和藍藻門的皮狀席藻。10月份優勢種為硅藻門的弧形峨眉藻、鈍脆桿藻、嗜鹽舟形藻、極小橋彎藻和藍藻門的阿式顫藻, 3個月份均出現的優勢種為嗜鹽舟形藻。7月份的優勢種中硅藻占 85.7%, 硅藻中的橢圓舟形藻出現頻率為86%, 8月份和10月份優勢種中藍藻門的比例雖有所增加, 但硅藻仍占絕對優勢。
2.2 周叢藻類的密度與生物量
2012年 7、8、10月份新疆額爾齊斯河流域周叢藻密度各門平均總計 1105.5 ind./mm2, 其中硅藻門最多(858.5×106ind./m2)占 77.7%; 綠藻門次之(123.3×106ind./m2)占11.2%; 藍藻門114.5×106ind./m2,占10.4%; 黃藻門5.4×106ind./m2, 占0.5%; 裸藻門3.2×106ind./m2占 0.3%, 金藻門和甲藻門均為 0.3× 106ind./m2, 各占0.03% 。
由于各支流水域環境不同, 因而周叢藻的密度在各水域分布也不同。由圖 1可知哈巴河最多(3204.9×106ind./m2), 其次是充乎爾、托洪臺水庫、小 635, 分別為 1934.2×106、1532.1×106和 1274.9× 106ind./m2, 富蘊最低為 106.6×106ind./m2。各支流7、8和10月的密度分布差異不顯著(P>0.05), 總的趨勢是7月密度最大, 10月最小。7月以托洪臺水庫、小635、別列則克、哈巴河為高, 分別為2790.3×106、2535.8×106、2012.7×106和1181.0×106ind./m2, 富蘊最低為 159.0×106ind./m2; 8月份哈巴河最高為8106.8×106ind./m2, 小635最低位14.1×106ind./m2; 10月份布爾津最高為3083.3×106ind./m2, 富蘊最低為102.0×106ind./m2。
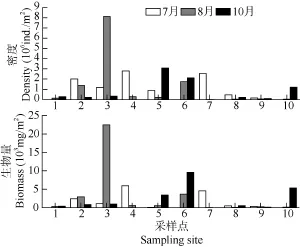
圖1 額爾齊斯河周叢藻密度和生物量分布Fig. 1 The distribution of periphyton density and biomass in Irtysh River
調查期間, 額爾齊斯河周叢藻生物量各門平均總計 2692.0 mg/m2。其中硅藻門最多(2383.2 mg/m2)占 88.5%, 綠藻門次之(228.9 mg/m2)占 8.5%, 藍藻門(64.4 mg/m2)占2.4%, 裸藻門(6.3 mg/m2)占0.2%,黃藻門(5.4 mg/m2)占0.2%, 金藻門和甲藻門分別為3.1 mg/m2、0.7 mg/m2, 共占0.1%。
從圖 3可知, 7月份托洪臺水庫的生物量最高(5909.9 mg/m2), 布爾津河最低(45.4 mg/m2); 8月哈巴河最高(22475 mg/m2), 小635最低(26.2 mg/m2); 10月份可可托海最高(5332.1 mg/m2), 富蘊最低(134.2 mg/m2),三個月份間的生物量差異不顯著(P>0.05)。
2.3 多樣性指數
額爾齊斯河周叢藻 7、8、10月份 Shannon-Wiener多樣性指數(H′)、Simpson多樣性指數(D)、Pielou均勻度指數(J)和 Margalef豐富度指數(d)的數值見圖2。其中Shannon-Wiener多樣性指數(H′)、Simpson多樣性指數(D)和 Pielou均勻度指數(J)的變化范圍分別為 0.42—4.34、0.06—0.96 和0.10—0.97, 多樣性指數、豐富度和均勻度在3個月份間均存在顯著性差異, P值均小于0.05。
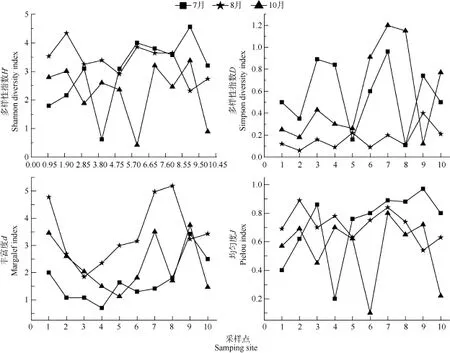
圖2 額爾齊斯河周叢藻多樣性指數(D, H′)、豐富度(d)和均勻度(J)Fig. 2 Diversity indices (D, H′), abundance (d) and evenness (J) of Periphyton in Irtysh River
3 討論
3.1 不同月份的周叢藻類群落結構比較
2012年7、8、10月在新疆額爾齊斯河流域的10個樣點中共采集到了周叢藻類7門178屬, 其中硅藻的種類數最多。硅藻在優勢種中也占據絕對的優勢, 7月份的優勢種中硅藻占85.7%, 硅藻中的橢圓舟形藻出現頻率為86.0%, 8月份和10月份優勢種中藍藻門的比例雖有所增加, 但硅藻仍占絕對優勢,這是由于額爾齊斯河屬于高緯度、高寒溫地區, 水體水溫存在典型的季節變化, 因此周叢藻出現了以硅藻為優勢的類群。
周叢藻類的平均密度為 1105.5×106ind./m2, 各個支流在 7、8和 10月的密度分布差異不顯著(P>0.05), 總的趨勢是7月密度最大, 10月最小, 這是由于 7月份剛進入夏至, 晝長夜短, 新疆白天長達 20h[2], 而光照可以影響周叢藻生物量和周叢群落的初級生產力[16], 同時 7月份的溫度升高, 有利于周叢藻類的生長繁殖, 因此 7月份的周叢藻密度最大。
大量研究已證明, 周叢藻類群落特征, 如生物量[17]和種類組成[18]等能對水質變化作出響應, 從而可作為評價河流受污染程度和受人類活動干擾程度的重要生物監測指標。周叢藻的生物量在7、8、10月由于環境及水文條件的不同而發生波動。7月份托洪臺水庫的生物量最高(5909.9 mg/m2), 遠遠高于其他支流的生物量, 這主要是由于托洪臺水庫受人類活動產生的污染輸入的影響, 導致水庫水體N、P含量高, 藍綠藻大量繁殖所致。8月份由于是豐水期, 水位上漲, 水體渾濁不利于周叢藻類的繁殖[7], 因此8月份的周叢藻生物量低于7月份。值得注意的是, 在所有采樣點中哈巴河大橋在8月份的密度和生物量均最高, 而且遠高于7月份和10月份, 這是由于哈巴河大橋地處下游的高海拔地區, 未被 8月份上漲的洪水淹沒因此有大量的營養物質滯留, 同時隨著水溫的升高和光照時間增長, 促進了大量的富營養型指示物種(魚腥藻和微囊藻)的生長, 藻類的大量繁殖推高周叢藻類的豐富度(密度和生物量)。
3.2 周叢藻類群落結構的空間變化
額爾齊斯河流域的周叢藻類種類數的分布雖隨季節變化而有顯著性差異(P<0.01), 但在空間分布上, 不同采樣點間的差異并不顯著(P>0.05), 而硅藻始終作為藻類群落的主要種類, 上游區域藻類的優勢度和群落多樣性均較高。整個水體除硅藻、綠藻和藍藻的比例基本保持一致外, 金藻和裸藻的群落數量僅在河流中上游地區表現出增長趨勢。
已有研究報導表明, 水溫、溶解氧、營養鹽及其他水文因子是影響河流中周叢藻類群落長期季節變化的主要因子[19,20]。調查期間額爾齊斯河周叢藻類密度和生物量的空間分布差異均不顯著, 但其總的分布趨勢是中下游地區高于上游地區, 這與采樣點處水溫的變化趨勢相一致(表2)。由額爾齊斯河各采樣點的理化因子與豐度的相關性分析得出, 以P=0.05為標準時, 豐度與水溫、鹽度均成顯著性相關(P<0.05, 表 3)。同時密度也與營養鹽成正相關,這表明, 水溫和營養鹽是影響額爾齊斯河周叢藻類空間分布的主要因素。
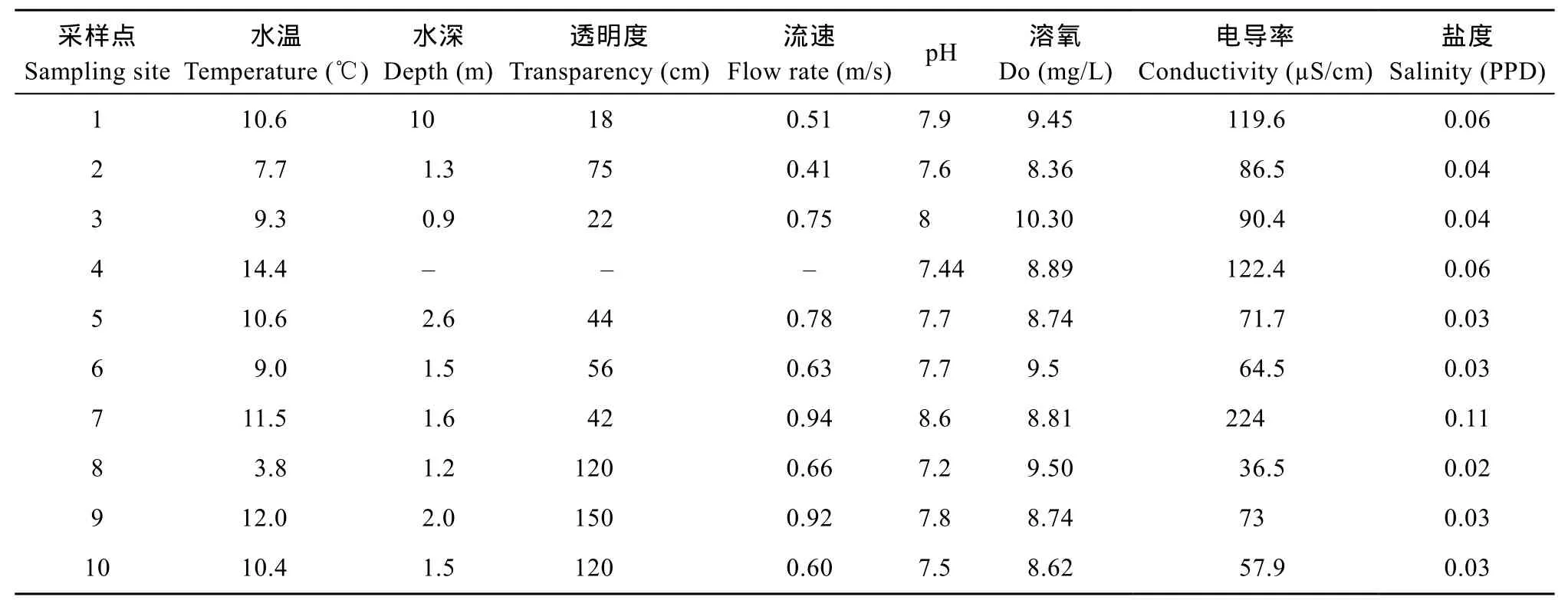
表2 額爾齊斯河各采樣點的理化因子Tab. 2 The environment metrics of different sampling sites in Irtysh River

表3 周叢藻類密度與環境因子的相關性Tab. 3 The correlation between periphyton density and environment factors
3.3 周叢藻類的群落結構與水質的關系
物種多樣性是衡量群落規模和重要性的基礎,也是反映水體營養狀況信息的重要參數[21,22]。因而,周叢藻類的多樣性指數也就成為判斷湖泊水庫等水體營養狀況最常用的檢測指標。藻類多樣性指數值越小, 說明水質污染程度越嚴重[23]。在水質較好的上游, 周叢藻類群落結構較復雜, 多樣性指數高;而在人為活動較頻繁的別列克則銅礦橋和托洪臺水庫, 周叢藻類群落表現出種類組成相對單一, 藻類多樣化性出現下降的趨勢。
多樣性指數(D、H′)表現出相似的變化趨勢(圖2): 相比于7和10月, 8月的多樣性指數值最低。一般而言, 種類越多或各個種類的個體數量分布越均勻,物種群落的Shannon-Wiener多樣性指數(H′)的值越大[16,24], 而8月份的種類數最多, 由于均勻度反映的是群落內各物種分布的均勻程度[17], 那么夏季較低的均勻度可能是引起多樣性指數低的主要原因之一。同時Shannon-Wiener多樣性指數(H′)越大表明水質越好, 這與額爾齊斯河的8月份豐水期, 水質渾濁的自然條件相一致[2]。
額爾齊斯河周叢藻 Margalef豐富度指數(d)的變化范圍為0.7—5.19。就總體而言, 各流域在8和10月的物種豐富度變化趨勢基本相似, 僅在個別采樣點略有差異。同一采樣點8月的物種豐富度高于7和10月。8月溫度適宜, 陽光照射充足, 適宜周叢藻的生長, 這可能是周叢藻豐富度在8月份增多的主要原因。
對調查期間額爾齊斯河各樣點周叢藻的多樣性進行分析, 結果顯示除了人為活動頻繁的可可托海和托洪臺水庫外, H′的平均值為3.04, 故判斷額爾齊斯河整體上屬于輕污染類型河流。比較各采樣點處的H′值發現, 雖然各H′值之間略有差異, 但差值并不顯著。由此說明, 除了個別受人為影響的流域之外, 額爾齊斯河各樣點的水質營養狀況整體水平相當。
[1] Xinjiang Geographic Society. Xinjiang Geography Manual [M]. Urumqi: Xinjiang People Press. 1983, 90—98 [新疆地理學會. 新疆地理手冊. 烏魯木齊: 新疆人民出社. 1983, 90—98]
[2] Li D Z. Watershed hydrological characteristics of Irtysh River [J]. Hydrologic, 1999, (3): 54—56 [李定枝. 額爾齊斯河流域水文特性. 水文, 1999, (3): 54—56]
[3] Ren M L. Fishes and fish fauna composition in Ergis River, China [J]. Arid Zone Research, 2002, 19(2): 62—66 [任慕蓮.我國額爾齊斯河的魚類及魚類區系組成. 干旱區研究, 2002, 19(2): 62—66]
[4] Liu J K. Advanced Hydrobiology [M]. Beijing: Science Press. 1999, 260—261 [劉建康. 高級水生生物學. 北京:科學出版社. 1999, 260—261]
[5] Yin X W, Zhang Y, Qu X D, et al. Community structure and biological integrity of periphyton in Hunhe River water system of Liaoning Province, Northeast China [J]. Chinese Journal of Applied Ecology, 2011, 22(10): 2732—2740 [殷旭旺, 張遠, 渠曉東, 等. 渾河水系著生藻類的群落結構與生物完整性. 應用生態學報, 2011, 22(10): 2732—2740]
[6] Hong S, Chen J S. Structure characteristics of aquatic community from the main rivers in China [J]. Acta Hydrobiologica Sinica, 2002, 26(3): 295—305 [洪松, 陳靜生. 中國河流水生生物群落結構特征探討. 水生生物學報, 2002, 26(3): 295—305]
[7] Jiang Z F, Zhang L R, Zhao W, et al. Community structure of phytoplankton in the branches of Xinjiang Ertix River [J]. Chinese Journal Fisheries, 2009, 22(4): 36—41 [姜作發, 張麗榮, 趙文, 等. 新疆額爾齊斯河支流浮游植物種群結構特征. 水產學雜志, 2009, 22(4): 36—41]
[8] National Environmental Protection Agency《 Aquatic Monitoring Handbook》 Editorial Committee. Aquatic Monitoring Handbook [M]. Nanjing: Northeastern University Press. 1993, 19—23 [國家環保局《水生生物監測手冊》編委會. 水生生物監測手冊. 南京: 東南大學出版社. 1993, 19—23]
[9] Hu H J, Wei Y X. The Freshwater Algae of China. Systematics, Taxonomy and Ecology [M]. Beijing: Science Press. 2006, 27—915 [胡鴻鈞, 魏印心. 中國淡水藻類一系統、分類及生態. 北京: 科學出版社. 2006, 27—915]
[10] Zhang Z S, Huang X F. Study Methods of Freshewater Plankton [M]. Beijing: Science Press. 1991, 340–344 [章宗涉, 黃祥飛. 淡水浮游生物研究方法. 北京: 科學出版社. 1991, 340—344]
[11] Shannon C E, Weaver W.The Mathematical Theory of Communication [M]. Berkeley: University of California Press. 1949, 1—144
[12] Margal EF R. Information theory in ecology [J]. International Journal of General Systems, 1958, 3: 36—71
[13] Pielou E C. Ecological Diversity [M]. New York: Wiley. 1975, 1—165
[14] Guan Y Q, Guo Y X, Li B, et al. Phytoplankton community character and water quality assessment of Juma River [J]. Journal of Hebei University (Natural Science Edition), 2007, 27(4): 401—406 [管越強, 郭云學, 李博, 等. 拒馬河浮游植物群落特征及水質評價. 河北大學學報(自然科學版), 2007, 27(4): 401—406]
[15] Wang Y L, Yuan J, Shen X Q. Ecological character of phytoplankton in spring in the Yangtze River estuary andadjacent waters [J]. Journal of Fishery Sciences of China, 2005,12(3): 300—306 [王云龍, 袁驥, 沈新強. 長江口及鄰近水域春季浮游植物的生態特征. 中國水產科學, 2005, 12(3): 300—306]
[16] Guo P Y, Shen H T, Liu A C, et al. The species composition, community structure and diversity of zooplankton in Changjiang estuary [J]. Acta Ecologica Sinica, 2003, 23(5): 892—900 [郭沛涌, 沈煥庭, 劉阿成, 等. 長江河口浮游動物的種類組成、群落結構及多樣性. 生態學報, 2003, 23(5): 892—900]
[17] Biggs B J F. Biomonitoring of organic Pollution using Periphyton, South Branch, Canterbury; New Zealand [J]. Journal of Marine and Freshwater Research, 1989, 23: 263—274
[18] Lowe R L. Periphyton Patterns in Lakes. In: Stevenson R J, Bothwell M L, Lowe R L (Eds.), Algal Ecology: Freshwater Benthic Ecosystems [M]. New York: Academic Press. 1996, 57—76
[19] Reilly J F, Horne A J, Miller C D. Nitrate removal from a drinking water supply with large free-surface constructed wetlands prior to groundwater [J]. Ecological Engineering, 2000, 14: 33—47
[20] Dai G Y, Li J, Li L, et al. The spatio-temporal pattern of phytoplankton in the north basin of lake Dianchi and related environmental factors [J]. Acta Hydrobiologica Sinica, 2012, 36(5): 946—956 [代龔圓, 李杰, 李林, 等. 滇池北部湖區浮游植物時空格局及相關環境因子. 水生生物學報, 2012, 36(5): 946—956]
[21] Zhang H F, Chen Y N, Chen Y P, et al. Species quantity change and ecosystem dynamics in the lower reaches of Tarim River [J]. Chinese Journal of Ecology, 2004, 23(4): 21—24 [張宏峰, 陳亞寧, 陳亞鵬, 等. 塔里木河下游植物群落的物種數量變化與生態系統動態研究.生態學雜志, 2004, 23(4): 21—24]
[22] Sun Z Q, Shi X L, Xu L L, et al. The protozoan community structure and its response to the change of water quality in a typical wetland landscape in summer [J]. Acta Hydrobiologica Sinica, 2013, 37(2): 290—299 [孫志強, 施心路, 徐琳琳, 等. 景觀濕地夏季原生動物群落結構與水質關系. 水生生物學報, 2013, 37(2): 290—299]
[23] Wang X H, Ji B C, Li M D, et al. Phytoplankton and bio-assessment of water quality in upper waters of Yinluan Project [J]. Research of Environmental Sciences, 2004, 17(4): 18—24 [王新華, 紀炳純, 李明德, 等. 引灤工程上游浮游植物及其水質評價. 環境科學研究, 2004, 17(4): 18—24]
[24] Li K Z, Yin J Q, Huang L M, et al. Dynamic variations of community structure and quantity of zooplankton in Zhujiang River estuary [J]. Journal of Tropical Oceanography, 2005, 24(5): 60—68 [李開枝, 尹健強,黃良民, 等. 珠江口浮游動物的群落動態及數量變化.熱帶海洋學報, 2005, 24(5): 60—68]
STUDIES ON THE COMMUNITY STRUCTURE OF PERIPHYTON IN THE IRTYSH RIVER OF XINJIANG UYGUR AUTONOMOUS REGION
Periphyton acts as the primary basal food resource of indigenous and unique fishes in the cross-border rivers of Xinjiang Uygur Autonomous Region. Research of the periphyton in this region is still limited. To investigate the community structure of periphyton, samples were collected in July, August and October 2012 from Irtysh River located in Xinjiang Uygur Autonomous Region. Our study indicated that the periphyton assemblage was composed of 178 species in total, belonging to seven taxonomic groups. Bacillariophyta showed the highest number of taxa (92), followed by Chlorophyta (49), Cyanophyta (20), Euglenophyta (5), Cryptophyta (3), Chrysophyta (2) and Pyrrophyta (1). Species number of periphyton showed significantly differences in different seasons (P<0.01). Bacillariophyta was predominant in species composition, especially N. halophila, Fragilaria capucina, C. perpusilla and Phormidium corium Gom. The average cell density and biomass of periphyton were 1105.5 ind./m2and 2692.0 mg/m2, respectively. Although seasonal and spatial distribution of density and biomass were not significant difference, the overall trend of spatial distribution showed that the density and biomass in lower-middle region were higher than those in upper region. Average values of diversity indices (D, H′), evenness (J) and abundance (Dm) of periphyton were 0.38, 3.04, 0.66 and 2.55, respectively. The water quality of Irtysh River has mild contamination based on the diversity index and phytoplankton abundance.
Periphyton; Community structure; Abundance; Diversity indices; Water quality evaluation; Irtysh River
LI Jun1,2, ZHOU Qiong1,2, XIE Cong-Xin1,2, WANG Jun1,2and WEI Li-Li1,2
(1. Key Laboratory of Freshwater Animal Breeding, College of Fishery, Ministry of Agriculture, Huazhong Agricultural University, Wuhan 430070, China; 2. Freshwater Aquaculture Collaborative Innovation Center of Hubei Province, Wuhan 430070, China)
S932.7
A
1000-3207(2014)06-1033-07
10.7541/2014.152
2013-10-11;
2014-02-12
國家科技基礎性工作專項“新疆跨境河流水生生態和魚類資源調查(2012FY112700)”; 中央高校基本科研業務費專項資金(2010QC024)資助
李君(1989—), 女, 湖北黃岡人; 碩士; 主要從事重金屬污染及藻類生態學研究。E-mail: kele8happy@webmail.hzau.edu.cn
周瓊(1978—), 男, 湖北浠水人; 博士、副教授; 主要從事漁業資源與淡水生態學研究。E-mail: hainan@mail.hzau.edu.cn

