抗生素和紫外照射聯合處理制備無菌微囊藻株
李 靜 李建宏 李文斌
(南京師范大學生命科學學院, 南京 210023)
抗生素和紫外照射聯合處理制備無菌微囊藻株
李 靜 李建宏 李文斌
(南京師范大學生命科學學院, 南京 210023)
目前我國大多數地表水體均已達到富營養化的程度,滇池、太湖等水體暴發的藍藻水華已造成了巨大的經濟損失和環境災難[1], 其中以銅綠微囊藻(Microcystis aeruginosa)在數量和發生頻率上占絕對優勢[2]。由于常用微囊藻藻種附生細菌的存在, 不能準確地應用于藻類生理生化以及藻菌間相互作用, 特別是不能探索微囊藻與某一特定細菌的相互關系。另外, 由于細菌與藍藻有較近的遺傳距離, 很多從分子水平開展的研究工作, 也需要避免細菌的干擾, 因此, 獲得無菌的純培養物是許多研究的基本保證。目前對微囊藻水華的產生與水體中的各種理化因素的相互關系已有了一些研究[3], 但迄今對微囊藻水華產生的生物學機理所知有限。為在實驗室控制條件下揭示微囊藻自身形成水華的機理, 亟需無菌的藻種作為研究材料。
藻種的無菌化通常可采用固體培養基平板畫線、殺菌劑(抗生素、雙氧水等)、離心洗滌、紫外線處理等方法[4—8]。對于一些生長繁殖迅速且對化學藥物耐受性較強的藻類,傳統的分離方法較易獲得無菌藻株, 但對于微囊藻而言卻十分困難。在實驗室培養過程中, 一方面微囊藻群體豐富的細胞壁多糖很容易裹挾細菌, 這些細菌難以通過畫線清除; 另一方面, 微囊藻對大多數化學藥物十分敏感,殺菌的藥物同樣也對藻細胞也產生強烈毒害作用, 因此難以直接用于清除細菌。
為獲得無菌的藻株用以深入開展微囊藻的細胞生物學研究, 本研究對一株群體微囊藻(M. aeruginosa XW01)進行了無菌化處理, 分別通過附生菌抗生素敏感性篩選, 找出了有效抑殺細菌的抗生素種類、濃度和作用時間, 并結合紫外殺菌, 最終獲得了無菌的培養物。為基因測序等進一步的分子生物學研究及生理生化研究提供了有用材料。
1 材料與方法
1.1 藻種及培養條件
群體狀態銅綠微囊藻M. aeruginosa XW01(以下簡稱XW01), 為本實驗室分離培養。微藻培養液為BG11[9], 所用培養基均高壓滅菌處理。
培養溫度為(26±2)℃, 光照條件為30—40 μmol/(m2·s), 40 W日光燈連續光照, 培養期間每天振蕩數次。
1.2 藻液中藻細胞與細菌數量的測定
藻濃度用A650測定, 細胞數量采用血球計數板計數。
培養物中細菌的濃度采用混勻平板菌落計數法計數。培養基采用LB固體培養[10], 每樣3個平行, 37℃培養48h后計數。
1.3 抗生素處理法
抗生素對XW01生長的影響 選取氨芐青霉素(Amp)、卡那霉素(Km)、硫酸慶大霉素(Gm)、四環素(TE)、新霉素(N) 5種抗生素(購于上海生工生物工程有限公司)配制成10 mg/mL的母液, 使用時按需要量加入培養物。按照預實驗設置各種抗生素的使用濃度分別為0、0.01、0.1、0.5、1、5 mg/L。每個濃度設置3個平行組, 以未加抗生素的為對照組。取對數生長期的藻液3 mL接種于含有不同濃度抗生素的50 mL BG11液體培養基中(100 mL錐形瓶)培養。
XW01藻液中細菌的分離鑒定 經鏡檢, 群體微囊藻外膠鞘上黏附大量細菌。取藻液100 μL 涂布于LB固體培養基上, 37℃培養3d, 挑取不同形態的單菌落劃線純化。通過16S rDNA基因于NCBI上比對鑒定分離的菌株[11]。
分離細菌對抗生素的敏感性實驗 將分離的細菌用LB液體培養基搖菌培養, 24h后, 取50 μL菌液在LB平板上進行涂布。將分別含有5 μg/片的各含Amp、Km、Gm、TE和N濾紙片(直徑5.5 mm, 購自上海生工生物工程有限公司)平貼于該平板表面在溫室中培養3d, 檢測抑菌圈直徑。選擇抑菌圈直徑≥20 mm的抗生素為較敏感種類, 選為除菌藥物。
抗生素除菌時間的選擇 經預實驗可知, 微囊藻處于對數生長期時, 其附生菌對抗生素更敏感。基于藥物敏感實驗的結果, 分別采用5 mg/L N、5 mg/L N+5 mg/L Gm、5 mg/L N+5 mg/L Km+5 mg/L Gm對處于對數生長期微囊藻進行無菌化處理。設置處理時間組為4、10、24、48h, 于不同處理時各取1 mL進行細菌數量檢測。以初始藻液中菌數量為對照。
抗生素作用后藻的處理 將組合抗生素處理XW01后的藻液用無抗生素的BG11離心洗涕兩次, 以去除抗生素的影響。取100 μL置于BG11 固體培養基上培養;同時另取藻液3 mL于50 mL BG11液體培養基中(100 mL錐形瓶)培養。待藻成活后檢測是否無菌。
1.4 實驗室培養藻紫外(UV)照射處理
UV光源為30 W UV燈管, 距離燈管40 cm處UV強度為1.25 μW/cm2, 通過調整照射時間控制輻射劑量。各實驗組總UV照射劑量列于表1。
取 15 mL處于生長對數期的藻液, 將其倒入直徑9 cm高1.8 cm的培養皿中, 使其的初始濃度一致。置于距光源40 cm處進行照射處理, 在預實驗的前提下, 設計20—50min的輻射時間。在處理過程中加入電磁攪拌子進行攪拌。分別于不同照射時間, 取樣分析殘留細菌數量,同時培養藻樣。以未經UV照射為對照。

表1 不同照射時間下的總UV輻射劑量Tab. 1 UV irradiation amount of different exposure times
1.5 抗生素結合UV照射處理
藻培養物中加入組合抗生素(5 mg/L N+5 mg/L Gm)處理, 同時分別進行5、10、20min UV照射處理。對照組加入等量的抗生素。然后置于UV燈下照射, 分別在照射5、10 和20min后取樣分析細菌, 并培養藻細胞。整個操作過程中抗生素的處理時間為1h。
1.6 數據統計
實驗設置1個對照組, 3個實驗平行組, 取平均值作為實驗結果(Mean±SD)。用Origin 8.0進行差異顯著性分析, T-test檢驗對照組與實驗組之間的差異。
2 結果
2.1 微囊藻培養過程中細菌含量的變化
在微囊藻的液體培養物中, 細菌的數量隨著藻的生長而同步增加(圖 1)。在藻生長對數期, 細菌的增殖也處于旺盛階段。由于處于快速生長階段的細菌通常對毒害條件更敏感, 因此, 采用對數生長期的藻培養物(第 6天到第10天)進行作為除菌材料應更有利。
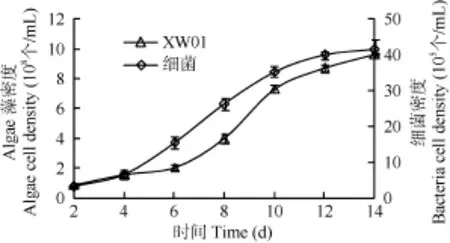
圖1 液體培養微囊藻XW01的生長曲線和培養物中細菌含量Fig. 1 The growth curve of M. aeruginosa XW01 and bacteria number in culture liquid
2.2 抗生素處理的效果
通過稀釋涂布平板法培養, 從微囊藻中分離出 4株優勢菌株。對其進行16S rDNA 測序比對鑒定。4株菌分別為 B1: 單胞菌(Pseudomonas sp.)、B2: 鞘氨醇單胞菌(Sphingomonas sp.)、B3: 鞘脂單胞菌(Sphingomonas sp.)、B4: 門多薩假單胞菌(Pseudomonas mendocina), 對這4株菌進行抗生素抑菌實驗結果如表2。
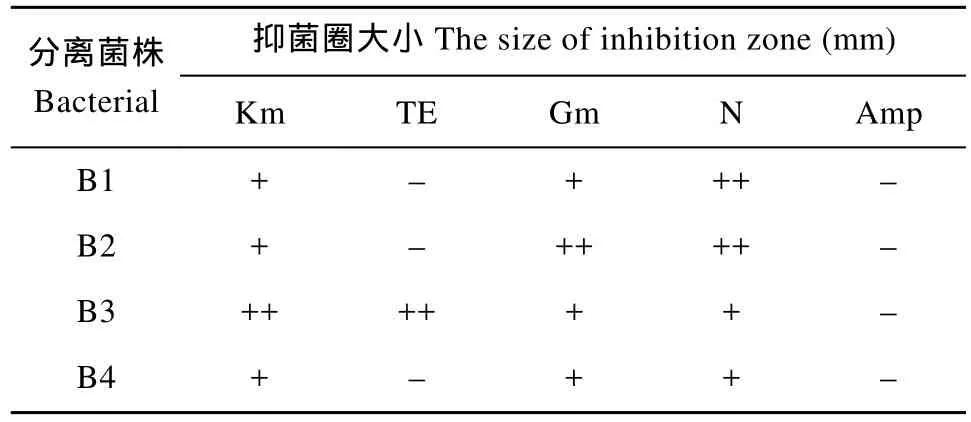
表2 分離細菌的抗生素抑菌實驗結果Tab.2 Antibiotic sensitivity of bacterial isolation
從表2的結果可見, 只有Km、Gm和N對4株菌均有抑制作用, Amp對4株菌均無作用, TE僅對B3有一定的作用。3種有明顯抑菌效果的抗生素對不同的菌株抑制效果也各不相同。可見如果采用單種抗生素除菌, 很難有效除去所有細菌。因此選擇了N、Km、Gm進行組合純化微囊藻XW01。
經過預實驗, 抗生素濃度為 5 mg/L較為合適, 更高的濃度容易殺死藻細胞。比較了 3個不同的抗生素組合: 5 mg/L N、5 mg/L N+5 mg/L Gm、5 mg/L N+5 mg/L Km+ 5 mg/L Gm, 處理后微囊藻細胞密度后細菌數量如圖2所示。
由圖2結果可見: 處理24h后, 5 mg/L N的藻液中菌落數為 15個/mL, 說明單一的 N 未能完全殺滅細菌; 5 mg/L N+5 mg/L Gm組合抗生素除菌率為100%; 但在5 mg/L N+5 mg/L Gm的基礎上, 再加入5 mg/L Gm抑菌效果反而降低, 不能將藻液中的細菌完全排除。其原因可能是抗生素之間存在相互拮抗, 這與林偉利用抗生素純化微藻結果一致[12]。延長抗生素作用時間可提高殺菌效果, 但同樣也對藻細胞的活力產生傷害, 第3天藻細胞數量開始減少。經抗生素處理超過24h時, 雖然顯微鏡下藻細胞形態未見明顯變化, 但大部分藻細胞已不能再生長繁殖, 藻細胞逐漸死亡。經5 mg/L N+5 mg/L Gm組合處理后, 經過一個月左右的培養, 藻細胞培養存活情況見表3。
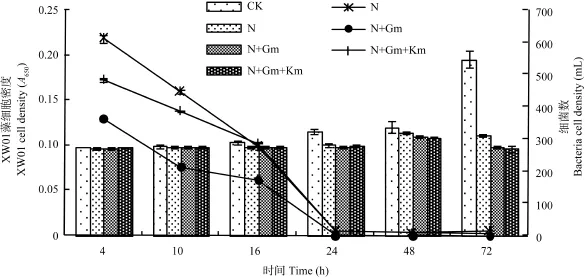
圖2 不同處理時間不同組合抗生素對細菌的影響Fig. 2 The effect of different treating time and different antibiotic combinations on the amount of bacteria
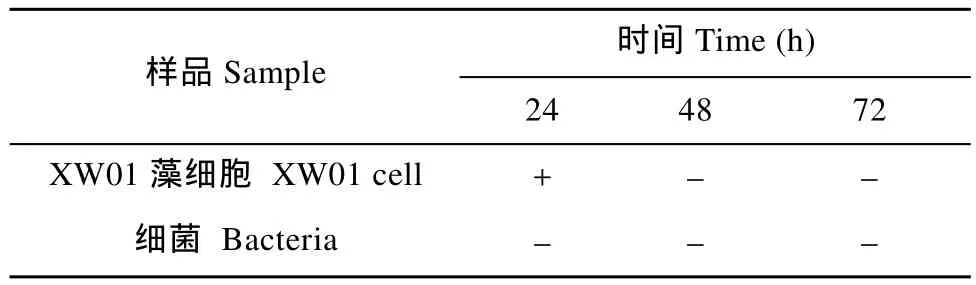
表3 組合抗生素處理XW01藻細胞和細菌的生長情況Tab. 3 The survive of XW01 cell and bacteria after treatment of mixed antibiotics
經5 mg/L N+5 mg/L Gm處理24h后的藻液初步測定已無菌化。取出上層漂浮的 XW01藻細胞經過兩次洗滌后, 分別接入BG11固體和液體培養基中培養。經抗生素傷害后的藻細胞長勢均很緩慢, 固體培養基上一個月左右才出現單藻落, 液體培養基中 25d左右明顯可見藻生長。處理48h、72h的藻液在兩種培養基上均未見生長。實驗過程中抗生素處理 24h后再培養的無菌藻大部分不再存活, 僅通過大量重復才獲得無菌藻株。
2.3 UV輻射除菌結果
對藻液進行不同時間UV照射處理后的菌落個數見圖3, 微囊藻培養物中細菌數量與UV照射處理時間成反比。
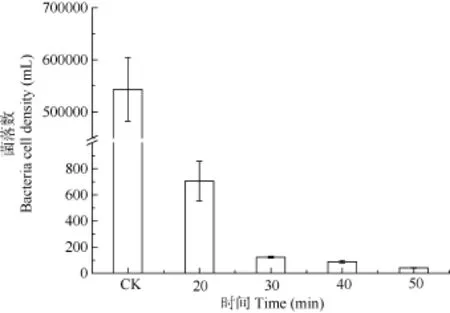
圖3 不同UV照射時間藻液中細菌數量Fig. 3 The amount of bacteria under different treating times with UV radiation
在照射30min時, 除菌率已達到了99.97% (P<0.01)。但繼續增加處理時間(40和50min), 除菌率則基本不再下降(差異不顯著P>0.05)。UV處理30 min時, 細菌個數約122個/mL, 處理 50min時, 細菌數約 40個/mL, 但大于30 min的UV照射后藻細胞也基本全部被殺死, 難以再培養。因此, UV照射的時間不能超過30min。
2.4 抗生素結合UV照射的除菌效果
為有效獲得無菌藻株, 將 UV照射和抗生素處理相結合同時處理對微囊藻進行了除菌純化。將含有 5 mg/L N+5 mg/L Gm的藻液經不同UV照射時間處理的除菌結果見圖 4: 未經 UV處理的 XW01藻液中細菌數為 844個/mL, 添加組合抗生素的藻液在UV照射5min時, 細菌數量就迅速減少到了8個/mL, 處理10min時, 藻液中細菌已完全除去。
再培養的 XW01藻細胞和細菌的生長情況見表 4:經過10min聯合處理的藻液, 細菌已全部殺滅, 藻細胞依然有部分存活; 但處理 20 min的藻, 卻無法再培養出藻細胞。
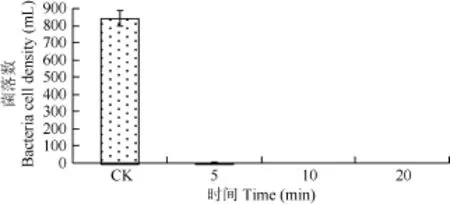
圖4 抗生素結合UV照射除菌效果Fig. 4 The sterilization effect of mixed antibiotics combined with UV radiation
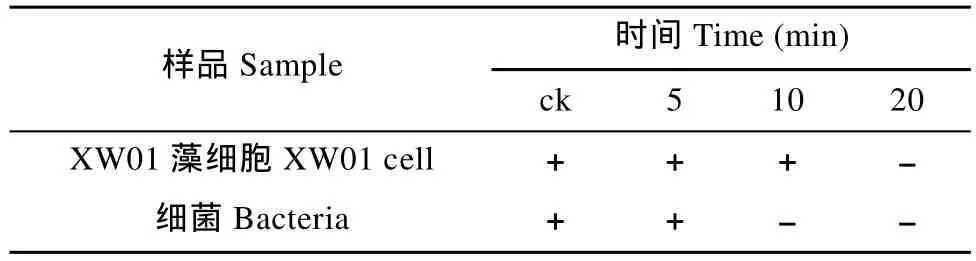
表4 抗生素-UV聯合處理后再培養的XW01藻細胞和細菌的生長結果Tab. 4 The survive of XW01 cell and bacteria after treatment of mixed antibiotics combined with UV radiation
3 討論
對于可產生氣囊漂浮于水面的藍藻, 獲得無菌藻株的經典方法是通過離心洗滌去除細菌, 或(和)通過平板稀釋劃線獲得無菌藻株, 這兩種方法運用于單細胞藻是有效的, 但對于微囊藻這樣很多細胞形成的群體則難以奏效。其原因可能是群體中豐富多糖裹挾的細菌, 通過簡單的洗滌和稀釋難以使菌藻分離。Sensen, et al.利用流式細胞儀分離出了無菌的單細胞藍藻[13]。Makoto, et al.運用1.4%的UV低溫凝膠處理一個月, 分離出了7株無菌的藍藻[14]。Ichiro, et al.設置了20—30 μmol/(m2·s)的燈光利用藻細胞的上浮性獲得無菌藻株[15]。這些方法都是利用了微藻與細菌的某些不同特征得到無菌藻株, 但這些方法單一的處理對群體的微囊藻而言并不能分離出無菌藻株。
不同的抗生素可通過不同的途徑抑制細菌的繁殖,可作為藻培養物除菌的有效工具[16]。本文通過比較附生的細菌對抗生素敏感性不同, 選擇5 mg/L N和5 mg/L的Gm混合加入到處于生長期的XW01藻液中可分離純化出無菌藻株。實驗發現, 組合抗生素處理藻液 24h, 除菌效果即可達到最佳狀態, 處理時間越短對藻細胞活性影響越小, 這與Droop, et al.研究得一致[17]。但是本研究也發現, 僅僅采用抗生素處理的方法, 很難在清除細菌和保留微囊藻活性間找到平衡點, 這與Sakami, et al.對具毒岡比甲藻(Gambierdiscus toxicus)兩個分離株生長結果相似[18]。可能是因為藍藻(藍細菌)與其他細菌具有類似的細胞結構和生理代謝過程, 超過藻類閾值的抗生細素濃度會對藻細胞造成傷害, 破壞藻細胞, 抑制藻細胞組成成分的形成[19]。本研究經過一年時間多次重復嘗試后才獲得無菌藻株。
在自然環境下, 藍藻常常暴露在高強度的 UV輻射下, 并且擁有一套完整的自我保護機制[20]。藍藻細胞在陽光的誘導下合成了抗氧化相關的超氧化物歧化酶(SOD)和過氧化氫酶(CAT)、促進胞外多糖的產生并形成較大的群體[21]、并形成偽枝藻素(Scy)、類菌胞素氨基酸(MAAs)等UV屏障物質來抵抗UV的傷害[22,23], 因此, 藍藻具有較強的抗UV能力。但絕大多數細菌的抗UV保護機制遠弱于藍藻, 在UV下更易受到傷害。這為消除藍藻附生細菌提供了一條可用的途徑。Gerloff, et al.就采用UV殺菌獲得了無菌聚球藻[24], 本研究運用組合抗生素聯合 UV照射方法純化群體微囊藻, 加入5 mg/L N和5 mg/L Gm結合UV處理10min時即可無菌化XW01藻株, 藻培養存活的機率大大高于抗生素長時間處理。N和Gm都為氨基糖苷類抗生素, 主要與細菌核糖體30S亞單位結合, 抑制細菌蛋白質的合成。在加入組合抗生素后, 殺滅細菌效率大大提高, 這可能與細菌產生的一種R因子使細菌對UV輻射抗性減弱有關[25]。本研究最終獲得無菌藻株結果表明, 選擇合適的抗生素結合一定的UV照射是獲得無菌微囊藻的有效方法。
[1] Bittencourt-Oliveira M C. Detection of potential microcystinproducing cyanobacteria in Brazilian reservoirs with a mcy B molecular maker [J]. Harmful Algae, 2003, 2: 51—60
[2] Reynolds C S. The Ecology of Fresh Water Phytoplankton [M]. Cambridge Studies in Ecology. London: Cambridge University Press. 1984
[3] Wang X, Lu X G, Zhang X L. Isolation of axenic strain of Microcystis Aeruginosa in Songhua Lake and its growth feature [J]. China Environment Science, 2004, 24(5): 579—583 [王霞, 呂憲國, 張學林. 松花湖銅綠微囊藻無菌株的分離及生長特征. 中國環境科學, 2004, 24(5): 579—583]
[4] Jiang L L, Wen X B, Geng Y H, et al. A newly selected lipid-rich microalgae strain and its molecular identification [J]. Acta Hydrobiologica Sinica, 2013, 37(4): 606—612 [江麗麗, 溫小斌, 耿亞洪, 等. 一株產油微藻的篩選及分子鑒定. 水生生物學報, 2013, 37(4): 606—612]
[5] Wang B F, Zhang L X, Ye J, et al. The research development of aseptic purification technique of Microalgaes [J]. Microbiology, 2007, 34(2): 363—366 [汪本凡, 趙良俠, 葉霽, 等. 微藻無菌化技術的研究進展. 微生物學通報, 2007, 34(2): 363—366]
[6] Zhao P, Wang X Q, Zhu C F, et al. Study of three commonly antibiotics in the axenic culture of Marine-Microalgae [J]. Journal of Tianjin Normal University (Natural Science Edition), 2007, 27(2): 27—30 [趙培, 王雪青, 朱潮峰, 等. 3種常用抗生素應用于海洋微藻無菌化培養的研究. 天津師范大學學報(自然科學版), 2007, 27(2): 27—30]
[7] Gan X H, Tang X Y, Liu G J, et al. Purificaton of Spirulina sp. [J]. Microbiology, 2005, 32(2): 1—4 [甘旭華, 唐欣昀,劉廣金, 等. 螺旋藻的純化. 微生物學通報, 2005, 32(2): 1—4]
[8] Zobell J, Long C E. Studies on the isolation of bacterial-free culture of marine phytoplankton [J]. Journal of Marine Research, 1938, 1: 328—333
[9] Waterbury J B. The cyanobacteria-isolation, purification and identification [J]. Prokaryotes, 2006, 4 :1053—1073
[10] Fang X R, Li G W, Shen P. Microbiology Experiments [M]. Beijing: Higher Education Press. 1997 [范秀榮, 李廣伍, 沈萍. 微生物學試驗. 北京: 高等教育出版社. 1997]
[11] Su B, Kang J P, Huang J, et al. Identification of one strain of bacillus using 16S ribosomal DNA sequence [J]. Food and Fermentation Technology, 2010, 46(5): 1—3 [蘇波, 康建平,黃靜, 等. 16S rDNA 序列分析鑒定一株芽孢桿菌. 食品與發酵科技, 2010, 46(5): 1—3]
[12] Lin W. Axenization of several marine Microalgal cultures [J]. Marine Sciences, 2000, 24(10): 4—6 [林偉. 幾種海洋微藻的無菌化培養. 海洋科學, 2000, 24(10): 4—6]
[13] Sensen C W, Heiman K, Melkonian M. The production of clonal and axenic cultures of microalgae using fluorescenceactivated cell sorting [J]. European Journal of Phycology, 1993, 28: 93—97
[14] Makoto M N, Watanabe M, Masayuki K, et al. Purification of freshwater picoplanktonic cyanobacteria by pour-plating in ultra-low-gelling-temperature agarose [J]. Phycological Research, 1998, 46(Suppl.): 71—75
[15] Imax I, Yamaguchi M. A simple technique for establishing axenic cultures of phytoflagellates [J]. Bulletin of Japanese Society of Microbial Ecology, 1994, 9: 15—17
[16] Wang H B, Cheng M, Yang Y Y, et al. The responses of algae Pavlova viridis and Karenia mikimotoi to three conventional antibiotics stress [J]. Fisheries Science, 2012, 31(6): 329—332 [王洪斌, 成明, 楊艷艷, 等. 綠色巴夫藻和米氏凱倫藻對 3種常見抗生素脅迫的響應研究. 水產科學, 2012, 31(6): 329—332]
[17] Droop M R. Marine Station, A procedure for routine purification of algalcultures with antibiotics [J]. British Phycological Bulletin, 1967, 3(2): 295—297
[18] Sinha R P, Klisch M, Gr?niger A, et al. Responses of aquatic algae and cyanobacteria to solar UV-B [J]. Plant Ecology, 2001, 154: 221—236
[19] Jiang L, Chen S Y, Yin D Q. Effects of Tetracycline on photosynthesis and antioxidant enzymes of Microcystis aeruginosa [J]. Journal of Ecology and Rural Environment, 2010, 26(6): 564—567 [姜蕾, 陳書怡, 尹大強. 四環素對銅綠微囊藻光合作用和抗氧化酶活性的影響. 生態與農村環境學報, 2010, 26(6): 564—567]
[20] Sinha R P, Klisch M, Gr?niger A, et al. Mycosporine-like amino acids in the marine red alga Gracilaria cornea-effects of UV and heat [J]. Environmental and Experimental Botany, 2000, 43: 33—43
[21] Wang Y, Li S S, Li J H, et al. Physiological response of Microcystis to solar UV radiation [J]. Acta Ecologica Sinica, 2011, 31(21): 6532—6539 [汪燕, 李珊珊, 李建宏, 等. 銅綠微囊藻對紫外輻射的生理代謝響應. 生態學報, 2011, 31(21): 6532—6539]
[22] Zudaire L, Roy S. Photoprotection and long-term acclimation to UV radiation in the marine diatom Thalassiosira weissflogii [J]. J Photochem Photobiol B, 2001, 62: 26—34
[23] Meckes M C. Effect of UV light disinfection on antibiotic-resistant coliforms in wastewater effluents [J]. Applied and Environmental Microbiology, 1982, 43(2): 371—377
[24] Gerloff G C, Fitzgerald G P, Skoog F. The isolation, purification, and culture of blue-green algae [J]. American Journal of Botany, 1950, 37: 216—218
[25] Marsh E B, Smith D H. R factors improving survival of Escherichia coli K-12 after ultraviolet irradiation [J]. Bacteriol, 1969, 100: 128—139
PREPARATION OF AN AXENIC MICROCYSTIS STRAIN WITH ANTIBIOTICS AND UV IRRADIATION
LI Jing, LI Jian-Hong and LI Wen-Bin
(College of Life Sciences, Nanjing Normal University, Nanjing 210023, China)
微囊藻; 無菌株; 抗生素; 紫外照射
Microcystis; Axenic strains; Antibiotic; Ultraviolet radiation
Q-33
A
1000-3207(2014)03-0592-05
10.7541/2014.84
2013-12-03;
2014-03-01
國家自然科學基金(31370217); 江蘇省優勢學科建設工程項目; 國家基礎科學人才培養基金(J1103507)資助
李靜(1988—), 女, 湖北黃岡人; 碩士研究生; 主要專業方向為藻類學。E-mail: lj5633258@163.com
李建宏(1963—), 教授; 主要研究方向為藻類學。E-mail: lijianhong@njnu.edu.cn

