微藻培養基平衡pH的研究
張 丹朱曉艷溫小斌耿亞紅李夜光
(1. 中國科學院武漢植物園, 中國科學院植物種質創新與特色農業重點實驗室, 武漢 430074; 2. 中國科學院大學, 北京 100049)
微藻培養基平衡pH的研究
張 丹1,2朱曉艷1,2溫小斌1,2耿亞紅1李夜光1
(1. 中國科學院武漢植物園, 中國科學院植物種質創新與特色農業重點實驗室, 武漢 430074; 2. 中國科學院大學, 北京 100049)
“平衡pH”是“培養基中二氧化碳分壓與空氣中二氧化碳分壓平衡時的pH”, 是微藻培養基的一個重要特征參數。選用常用的三種微藻培養基: BG11培養基、BBM培養基和Zarrouk培養基, 使用鼓泡通入空氣的方法, 研究碳源、氮源、磷源濃度和鹽度對培養基平衡pH的影響。結果如下: 在NaHCO3濃度0—16.8 g/L范圍內, 三種培養基的平衡pH都隨碳源濃度的增加而升高; NaNO3濃度在0—2.5 g/L范圍內, 對培養基平衡pH沒有影響; 0.1 g/L KH2PO4使BG11培養基的平衡pH稍有升高, 與之相反, BBM培養基的平衡pH稍有下降, 進一步提高磷(P)濃度(最高 0.4 g/L), BG11培養基和 BBM培養基的平衡 pH不再變化; P濃度變化對Zarrouk培養基的平衡pH沒有影響; 三種培養基的平衡pH都隨鹽度的升高而降低。碳源濃度是影響培養基平衡 pH的最主要因素, 平衡 pH與碳源濃度的關系可以用回歸方程 y=0.3504ln(x)+8.9647(R2=0.9708)表示,氮源濃度對平衡pH沒有顯著影響, 磷源濃度和鹽度對培養基平衡pH有影響, 但影響不大。控制藻液pH不低于平衡pH, 可以提高微藻培養中CO2的利用效率, 有利于實現微藻CO2生物固定的環境效益。
微藻; 平衡pH; 培養基; 碳濃度
世界上商業化生產的微藻(Micro algae)主要有螺旋藻(Spirulina)、小球藻(Chlorella)、紅球藻(Haematococcus)和杜氏藻(Dunaliella)等[1—4], 已經被開發為保健品和珍貴水產品的飼料添加劑。某些微藻細胞中可以積累大量油脂, 其中的三酰甘油酯(TAG)經過轉酯化生成脂肪酸甲酯, 就是生物柴油,可以替代化石燃料[5,6], 利用微藻生產生物柴油具有多種優勢[7,8]。微藻有望成為繼糧食作物生物乙醇、纖維素生物乙醇和陸生作物生物柴油之后第三代生物質能源的原材料[9]。
目前, 規模化培養微藻都是采用液體培養, 如何高效地向藻液中補充 CO2, 一直是研究者們關注的一個問題[10]。研究者們注意到, 在一定的條件下, 藻液中的CO2會向空氣中釋放, 造成碳源的浪費[11,12]。李夜光等[13,14]研究發現藻液的 pH決定螺旋藻培養液向空氣中釋放 CO2, 還是從空氣中吸收 CO2, 當藻液的 pH高于“培養液的 CO2濃度與空氣中 CO2濃度相平衡時的 pH”, 藻液從空氣中吸收 CO2, 反之, 藻液向空氣中釋放 CO2。我們在培養微藻的過程中發現“培養液的 CO2濃度與空氣中 CO2濃度相平衡時的 pH”是微藻培養基的一個重要特征參數,將其稱為“空氣平衡 pH”, 簡稱“平衡 pH”, 并給“平衡pH”一個規范的定義: “培養基中二氧化碳分壓與空氣中二氧化碳分壓平衡時的 pH”。與螺旋藻培養基一樣, 當各種微藻培養基 pH低于其“平衡 pH”,藻液向空氣中釋放 CO2, 隨著 CO2的釋放, 培養基pH升高, 直到達到平衡pH, 培養基不再向空氣中釋放CO2; 當培養基的pH高于平衡pH, 培養基從空氣中吸收CO2, 隨著CO2的吸收, 培養基pH下降, 直到達到平衡 pH, 培養基不再從空氣中吸收 CO2, 此時, CO2的吸收和釋放達到動態平衡。利用煙道氣中的 CO2為碳源培養產油微藻是目前微藻生物柴油研發的一個重要指導思想。對于大規模培養, 如何高效地利用CO2, 盡量減少培養過程中CO2向空氣的釋放,是必須解決的關鍵技術問題。目前, 未見對微藻培養基平衡pH深入研究的報道。
本文選擇有代表性的三種培養基, BG11培養基、BBM培養和Zarrouk培養基, 研究培養基的主
1 材料與方法
改良的BG11培養基[15]; BBM培養基; 改良的Zarrouk培養基(除NaHCO3濃度根據實驗設計變化外, 培養基其他成分及濃度與Zarrouk培養基相同)。
1.2 碳源、氮源、磷源及鹽度濃度設置
碳源、氮源、磷源及鹽度實驗使用的藥品及其濃度見表1。
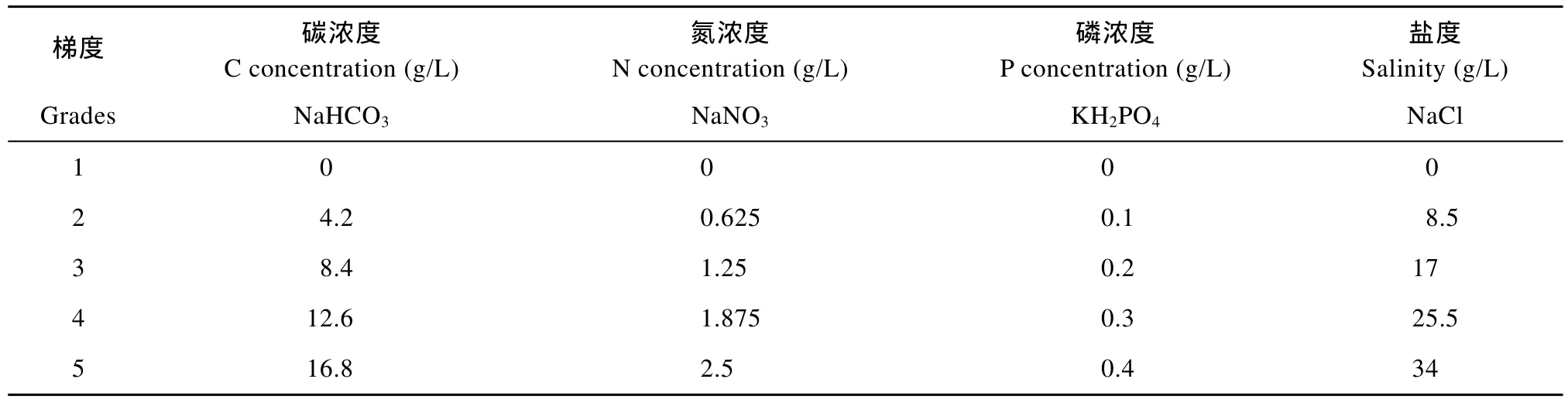
表1 培養基 C、N、P濃度及鹽度Tab. 1 Salinity and the concentration of C, N and P of the medium
根據表1中的濃度配制BG11、BBM、Zarrouk培養基。BG11培養基的磷源為K2HPO4·3H2O, BBM培養基的磷源為K2HPO4·3H2O和KH2PO4, Zarrouk培養基的磷源為KH2PO4。
1.3 實驗裝置及實驗條件
1.4 培養基pH的測定
采用 MODEL 868 pH 計(Thermo Electron Corporation)測定培養基的pH。
1.5 培養基平衡pH的測定
取200 mL培養基于通氣培養裝置的玻璃培養管中(每種處理設3個平行樣), 在液面處做標記。向培養基中通入空氣, 每隔一段時間測定培養基的 pH,測pH之前向玻璃培養管中加入蒸餾水使液面回到初始位置, 補充蒸發的水分。待培養基的pH沒有顯著變化時停止通氣, 此時的pH即為培養基的平衡pH。
2 結果
2.1 碳源濃度對培養基平衡pH的影響
向不同碳源濃度的培養基鼓泡通入空氣, BG11、BBM和Zarrouk培養基的pH表現出相同的變化趨勢, 這種變化又分為兩種模式: (1)沒加碳源的培養基pH基本沒有變化, 維持初始的pH; (2)補加碳源的培養基的 pH在通氣后的 5h內快速升高, 5—10h, pH上升明顯減緩, 10h后, pH雖然隨著通氣時間的延長而升高, 但是變化已經非常緩慢, 30h后, pH達到穩定(圖1)。
培養基的pH保持穩定, 說明培養基向空氣中釋放 CO2的速率與從空氣中吸收 CO2的速率相同, 表示培養基中CO2的分壓等于空氣中CO2的分壓[14,16],根據平衡pH的定義, 對應的pH就是培養基的平衡pH。不同碳源濃度培養基的平衡pH見表2。
2.2 氮源濃度對培養基平衡pH的影響
不同氮源濃度的 BG11和BBM培養基的初始pH分別在7.8和6.7上下, 通氣后, BG11和BBM培養基的 pH稍有下降, 很快分別穩定在 7.3和 6.6上下(圖未顯示);不同氮源濃度的Zarrouk培養基的初始pH在7.8上下, 在通氣后, 30h后達到穩定(圖未顯示)。不同氮源濃度的BG11、BBM和Zarrouk培養基的平衡pH如表3所示。
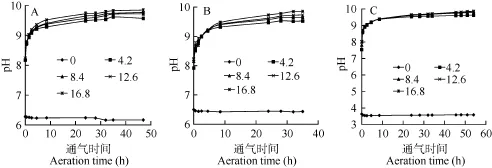
圖1 不同碳源濃度的培養基pH隨通氣時間的變化Fig. 1 pH value-time course of medium with different concentration of carbon during bubbling aeration
2.3 磷源濃度對培養基平衡pH的影響
不同磷源濃度的BG11和BBM培養基的初始pH分別為6.9—7.8和6.18—8.57, 在通氣后, BG11和BBM培養基的pH稍有下降, 逐步達到穩定; 不同磷源濃度的 Zarrouk培養基的初始 pH 在7.71—8.19范圍內, 在通氣后, pH逐步上升, 30h后達到穩定(圖未顯示)。不同磷源濃度的BG11、BBM和Zarrouk培養基的平衡pH如表4所示。
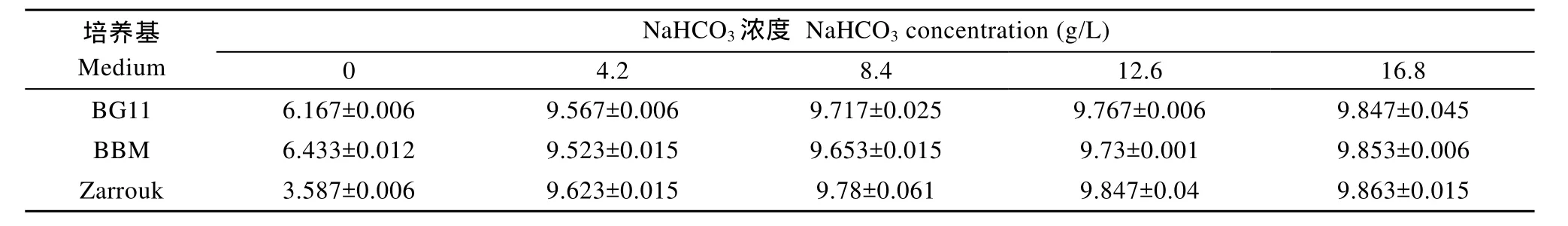
表2 不同碳源濃度培養基的平衡pH(平均值±標準差) Tab. 2 Equilibrium pH values (means±SD) of medium with different concentration of NaHCO3
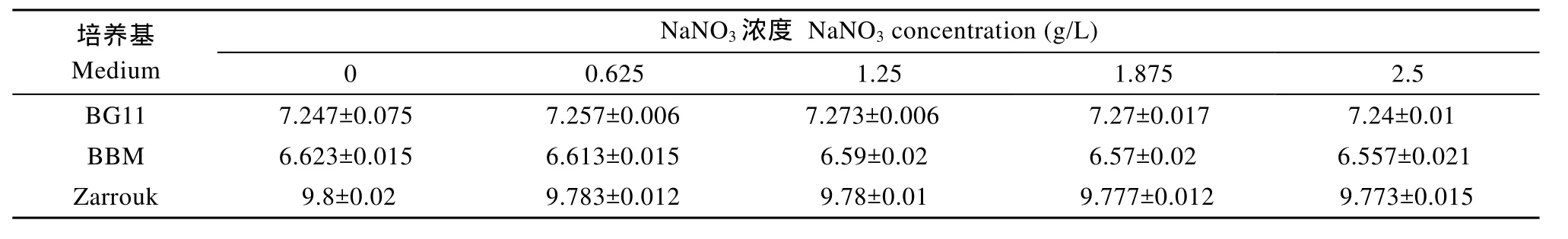
表3 不同氮源濃度培養基的平衡pH(平均值±標準差)Tab. 3 Equilibrium pH values (means±SD) of medium with different concentration of NaNO3
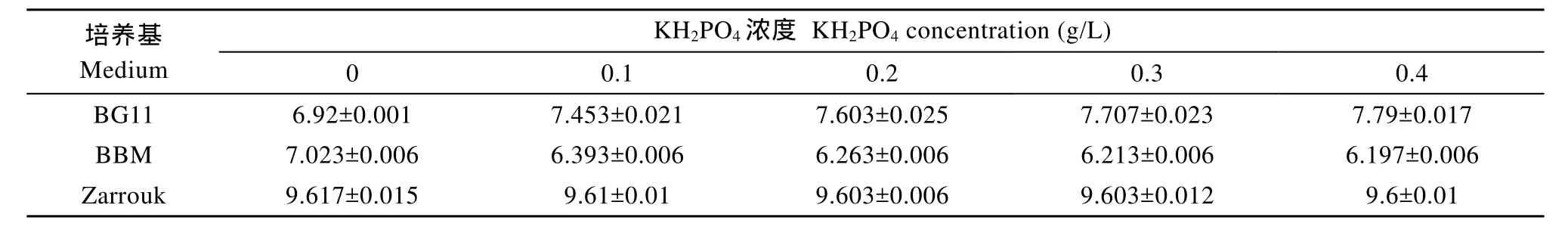
表4 不同磷源濃度培養基的平衡pH(平均值±標準差)Tab. 4 Equilibrium pH values (means±SD) of medium with different P concentration
2.4 鹽度對培養基平衡pH的影響
不同鹽度的BG11和BBM培養基的初始pH分別為7.3—7.5和5.9—6.3, 通氣后, BG11和BBM培養基的pH稍有下降, 10h后達到穩定; 不同鹽度的Zarrouk培養基的初始 pH7.6—7.8, 在通氣后, pH逐步上升, 35h后達到穩定(圖未顯示)。不同鹽度的BG11、BBM和 Zarrouk培養基的平衡 pH如表 5所示。
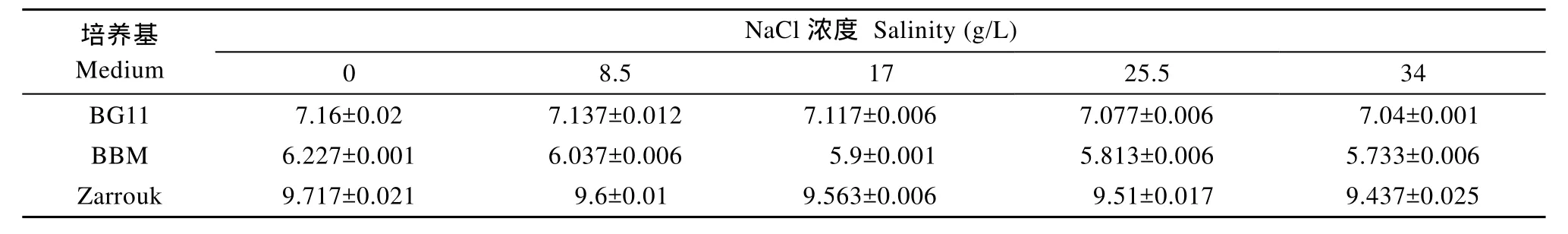
表5 不同鹽度培養基的平衡pH(平均值±標準差)Tab. 5 Equilibrium pH values (means±SD) of medium with different salinities
3 討論
3.1 碳源濃度對平衡pH的影響
培養基“平衡pH”的定義是: 培養基中二氧化碳分壓與空氣中二氧化碳分壓相等時的 pH。空氣中CO2相對穩定, 培養基中二氧化碳分壓主要取決于碳源的濃度, 可見, 碳源濃度是影響微藻培養基平衡pH的主要因素。
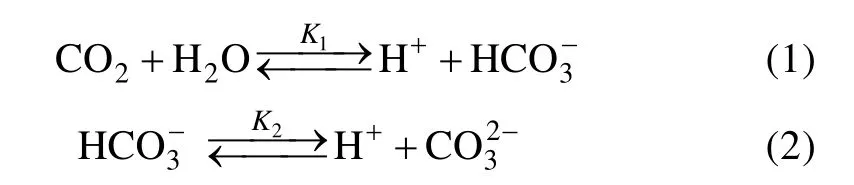
表 2數據顯示, 當培養基其他成分不變, 隨著碳源濃度的增加, 平衡pH先快速升高, 碳源濃度對培養基的平衡 pH的影響達到極顯著水平(P<0.01);然后升高幅度趨于緩慢, 當碳源濃度達到4.2 g/L時,平衡 pH幾乎不再隨著碳源濃度的增加而升高, 碳源濃度的影響不顯著(P>0.05)。出現這種情況很可能與 CO2的活度有關, 當碳源濃度較高時, 隨著碳源的進一步增加, 雖然 CO2的濃度增加, 但是其活度并未顯著增加, CO2分壓相應也沒有顯著增加, 平衡pH基本不變。
除了不加碳源使Zarrouk培養基的平衡pH明顯低于BG11和BBM培養基, 其他碳源濃度下, 三種培養基的平衡pH很接近。以BG11培養基為例, 將平衡pH對碳源濃度做圖(圖2), 培養基平衡pH與碳源濃度的關系可以用回歸方程 y=0.3504ln(x)+8.9647 (R2=0.9708)表示。
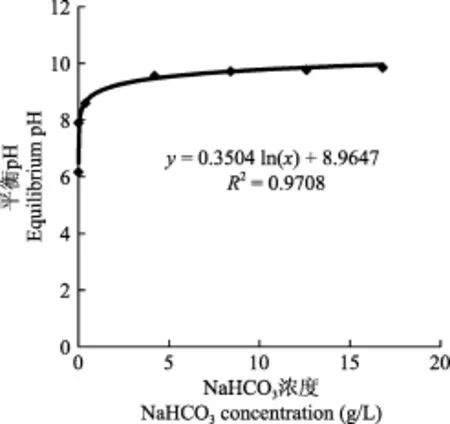
圖2 平衡pH隨碳源濃度的變化Fig. 2 Equilibrium pH values changing with NaHCO3concentrations
3.2 氮源濃度對平衡pH的影響
BBM培養基不含碳源, BG11培養基含有低濃度碳源(0.02 g/L Na2CO3), Zarrouk培養基含有高濃度碳源(6 g/L NaHCO3), 三種培養基的平衡pH都不隨氮源濃度的改變而變化(P>0.05)(表 3), 表明無論培養基 CO2分壓高或低, 都不受氮源(NaNO3)濃度變化的影響。氮源濃度對平衡pH沒有影響, 我們認為有兩方面原因: (1)NaNO3是中性化合物, 不能與三種碳源形式發生任何的化學反應從而影響化學反應方程式(1)和(2)的平衡移動; (2)在實驗設定的濃度范圍內, NaNO3濃度的變化沒有對CO2的活度產生顯著的影響。
3.3 磷源濃度對平衡pH的影響
磷源(K2HPO4·3H2O、KH2PO4)濃度對 BG11和BBM培養基的平衡pH有一定作用, 但是影響不大。0.1 g/L磷源小幅度提高了BG11培養基的平衡pH,但是卻小幅度降低了BBM培養基的平衡pH, 磷源濃度的進一步升高, 兩種培養基的平衡 pH基本不再變化(表4)。為什么磷源提高BG11的平衡pH, 卻降低了BBM的平衡pH?可能與兩種培養基的化學成分不同有關: BG11培養基含有少量Na2CO3(0.02 g/L), BBM 培養基不含碳源; BG11培養基的磷源是K2HPO4·3H2O, BBM培養基的磷源是K2HPO4·3H2O+ KH2PO4。
磷源濃度對Zarrouk培養基的平衡pH沒有顯著影響(P>0.05), 是因為 Zarrouk培養基中的 NaHCO3濃度高(6 g/L), NaHCO3是決定培養基平衡pH的因素, 磷源對平衡pH的影響不能表現出來。
3.4 鹽度對平衡pH的影響
鹽度降低了三種培養基的平衡 pH(表 5)。鹽度是影響CO2溶解度的重要因素, 鹽度越高CO2溶解度越低[16]。CO2溶解度降低, 其分壓降低, 平衡 pH隨之降低。
實驗設置的最高鹽度是 34, 達到海水的鹽度。NaCl濃度由0升高到34 g/L, 三種培養基的平衡pH沒有大幅度變化。可以推測, 如果用海水配制BG11、BBM和Zarrouk三種培養基, 其平衡pH稍有降低, 但是變化不會太大。也就是說, 本文研究的培養基主要成分對平衡 pH影響的結果, 也基本適用于海水培養基。
3.5 藻細胞對平衡pH的影響
在光照條件下, 藻細胞進行光合作用, 吸收利用培養基中的碳源, 使培養基pH不斷升高[15]。所以,直接測定藻細胞對平衡 pH的影響是非常困難的。從理論上分析, 藻細胞進行光合作用吸收利用培養基中的碳源, 使培養基碳源濃度降低, 平衡pH隨之降低; 藻細胞還同時吸收利用培養基中的氮源和磷源, 氮源濃度改變不影響培養基平衡 pH; 但是, 磷源濃度改變會對BG11培養基和BBM培養基的平衡pH產生一定的影響(表4)。所以, 藻細胞對平衡pH的影響主要是通過改變碳源、磷源等營養成分的濃度間接發揮作用。
3.6 平衡pH概念的擴展及其在微藻培養中應用
平衡pH是“空氣平衡pH”的簡稱, 特指培養基的CO2分壓與空氣中CO2的分壓平衡時的pH。以CO2為碳源培養微藻, 通常是將 CO2與空氣以一定比例混合[1%—5% (v/v)]后通入藻液中。利用煙道氣中的CO2為碳源培養微藻, CO2的比例在5%—15% (v/v)的范圍內。顯然, “空氣平衡pH”的概念太狹窄,需要進行擴展。在平衡pH的前面標明CO2的濃度(v/v), 例如“1% CO2平衡pH”, “5% CO2平衡pH”和“15% CO2平衡pH”, 分別表示培養基的CO2分壓與1%、5%、15%的混合氣體中CO2分壓平衡時的pH。概念擴展后, “平衡pH”適用于任何比例的CO2混合氣體, 適用范圍更寬。
掌握了培養基的平衡 pH, 制定 pH調控策略,在規模培養過程中控制藻液pH不低于平衡pH, 藻液中的 CO2就不會向氣相中(CO2混合氣體)釋放,不僅可以提高微藻培養的經濟效益, 而且有利于實現微藻CO2生物固定的環境效益。
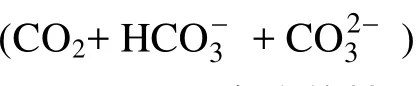
[1] Richmond A. Spirulina [A]. In: Borowitzka M A, Borowitzka I J (Eds.), Micro-algal Biotechnology [C]. Cambridge: Cambridge University Press. 1988, 85—121
[2] Iwamoto H. Industrial production of microalgal cell-mass and secondary products—species of high potential: Chlorella [A]. In: Amos, Richmond (Eds.), Handbook of Microalgal Culture: Biotechnology and Applied Phycology [C]. Oxford: Blackwell Science Ltd. 2004, 255—263
[3] Zhang B Y, Geng Y H, Li Z K, et al. Production of astaxanthin from Haematococcus in open pond by two-stage growth one-step process [J]. Aquaculture, 2009, 295(3): 275—281
[4] Zhu Y H, Jiang J G. Continuous cultivation of Dunaliella salina in photobioreactor for the production of β-carotene [J]. European Food Research and Technology, 2008, 227(3): 953—959
[5] Chisti Y. Biodiesel from microalgae [J]. Biotechnology Advances, 2007, 25(3): 294—306
[6] Hu Q, Sommerfeld M, Jarvis E, et al. Microalgal triacylgly-cerols as feedstocks for biofuel production: perspective and advances [J]. Plant Journal, 2008, 54(4): 621—639
[7] Hao Z D, Liu P H, Yang X, et al. Screen and identification of tropical freshwater microalgae for lipid production [J]. Acta Hydrobiologica Sinica, 2013, 37(3): 547—552 [郝宗娣,劉平懷, 楊勛, 等. 熱帶淡水產油微藻的分離篩選與鑒定.水生生物學報, 2013, 37(3): 547—552]
[8] Xu J, Xu X D, Fang X T, et al. Screening and lipid analyses of high oleaginous Chlorella species [J]. Acta Hydrobiologica Sinica, 2012, 36(3): 426—432 [徐進, 徐旭東, 方仙桃, 等. 高產油小球藻的篩選及其油脂分析. 水生生物學報, 2012, 36(3): 426—432]
[9] Li J, Zhang X C, Hu H J, et al. Prospects and research strategies for the microalgal industry [J]. Chinese Science Bulletin, 2012, 57(1): 23—31 [李健, 張學成, 胡鴻鈞, 等.微藻生物技術產業前景和研發策略分析. 科學通報, 2012, 57(1): 23—31]
[10] M?rkl H, Mather M E. Mixing and aeration of shallow open pond [A]. In: Becker W, Tubingen (Eds.), Advance in Limnology, Vol. 20, Production and use of microalgae [C]. Germany , E: Schweizerbart’Sche Verlags Buchhandlung . 1985, 20: 85—93
[11] Livansky K. Losses of CO2in outdoor mass algal cultures: determination of the mass transfer coefficient KL by means of measured pH course in NaHCO3solution [J]. Archiv für Hydrobiologie. Supplementband. Untersuchungen des Elbe-Aestuars, 1990, 85: 87—97
[12] Vasquez V, Heussler P. Carbon dioxide balance in open air mass culture of algae [A]. In: Becker W, Tubingen (Eds.), Advance in Limnology, Vol. 20, Production and use of microalgae [C]. Germany, E: Schweizerbart’Sche Verlags Buchhandlung. 1985, 20: 95—113
[13] Li Y G, Hu H J, Gong X M. Studies on the mechanism of pH value change and carbon conversion ratio of Spirulina media [J]. Chinese Journal of Biotechnology, 1996, 12(sl): 242—248 [李夜光, 胡鴻鈞, 龔小敏. 螺旋藻培養液pH變化的機理和碳源利用率的研究. 生物工程學報, 1996, 12(增刊): 242—248]
[14] Li Y G, Hu H J. Studies on the characteristics of absorption of CO2by Spirulina medium [J]. Journal of Wuhan Botanical Research, 1996, 14(3): 253—260 [李夜光, 胡鴻鈞. 螺旋藻培養液吸收CO2特性的研究. 武漢植物學研究, 1996, 14(3): 253—260]
[15] Zhang G Y, Wen X B, Liang F, et al. The effects of physical and chemical factors on the growth and lipid production of Chlorella [J]. Acta Ecologica Sinica, 2011, 31(8): 2076—2085
[張桂艷, 溫小斌, 梁芳, 等. 重要理化因子對小球藻生長和油脂產量的影響. 生態學報, 2011, 31(8): 2076—2085]
[16] Gu F Y. Solubility of Carbon dioxide in aqueous sodium chloride solution under high pressure [J]. Journal of Chemical Engineering of Chinese Universities, 1998, 12(2): 118—123 [顧飛燕. 加壓下二氧化碳在氯化鈉水溶液中的溶解度. 高校化學工程學報, 1998, 12(2): 118—123]
STUDIES ON EQUILIBRIUM PH VALUES OF MICRO ALGAL MEDIUM
ZHANG Dan1,2, ZHU Xiao-Yan1,2, WEN Xiao-Bin1,2, GENG Ya-Hong1and LI Ye-Guang1
(1. Key Laboratory of Plant Germplasm Enhancement and Speciality Agriculture, Wuhan Botanical Garden, Chinese Academy of Sciences, Wuhan 430074, China; 2. University of Chinese Academy of Sciences, Beijing 100049, China)
Equilibrium pH value, one of the important chemical parameter of medium, is the pH value when CO2partial pressure in the micro alga medium equals to CO2partial pressure in the air. The three mostly used medium (BG11 medium, BBM medium and Zarrouk medium) were used to study the effects of carbon, nitrogen and phosphorus concentration and salinity on the equilibrium pH value by air bubbling aeration of the medium. Our results demonstrated that the increased NaHCO3concentration in the range of 0—16.8 g/L enhanced the equilibrium pH values of all three medium. In the concentration range of 0—2.5 g/L, NaNO3had no significant effect on equilibrium pH value of these three medium. 0.1 g/L KH2PO4raised the equilibrium pH value of BG11 medium, but decreased it in BBM medium. The further increased P concentration (maximum 0.4 g/L) did not regulate the equilibrium pH value of both BG11 and BBM medium. The P concentration in the range of 0—0.4 g/L did not affect the equilibrium pH value of Zarrouk medium. The salinity in the range of 0—34 decreased the Equilibrium pH value of all three medium. Carbon concentration is the most important factor to influence the equilibrium pH value of micro algae medium, and the relationship between equilibrium pH value and carbon concentration can be described with the regression equation: y=0.3504ln(x)+8.9647 (R2=0.9708). N concentration had no significant effect on equilibrium pH value. P concentration and salinity had limited impact on equilibrium pH value. The efficiency of CO2utilization will be improved at higher pH value compared with the equilibrium pH value. These results support the environmental benefit of biofixation of CO2by micro algae.
Microalgae; Equilibrium pH value; Medium; Carbon concentration
Q93-335
A
1000-3207(2014)03-0401-06
10.7541/2014.57
2013-03-28;
2013-10-14
中國石化集團微藻生物柴油成套技術開發項目(No. 210080); 國家“863”項目(No. 2013AA065805); 國家自然科學基金項目(No. CNSF31272680)資助
張丹(1987—), 女, 山東濟寧人; 碩士研究生; 主要從事藻類學研究。E-mail: lantian0224@126.com
李夜光, E-mail: yeguang@wbgcas.cn

