建鯉ODC1基因型與增重的相關性分析
李紅霞 李建林 唐永凱 俞菊華
(中國水產科學研究院淡水漁業研究中心, 農業部淡水漁業和種質資源利用重點實驗室, 無錫 214081)
建鯉ODC1基因型與增重的相關性分析
李紅霞 李建林 唐永凱 俞菊華
(中國水產科學研究院淡水漁業研究中心, 農業部淡水漁業和種質資源利用重點實驗室, 無錫 214081)
構建了建鯉(Cyprinus carpio var. jian) 鳥氨酸脫羧酶 (Ornithine decarboxylase, ODC) jlODC1a基因上6個和jlODC1b基因上4個SNP位點的PCR-RFLP方法, 檢測了這10個位點在12個家系約900尾建鯉選育群體中的基因型, 各位點的基因型頻率存在差異, 最小等位基因頻率 (MAF)為0.14—0.48。各位點不同基因型與增重相關分析結果, 其中 7個 SNPs與建鯉增重顯性相關的位點, ODC1s基因上與雌魚增重相關的SNP位點(7個)較雄魚(4個)多。標記富集結果表明富集與建鯉增重相關的優勢基因型的SNP個數越多的個體增重速度越快SNP個數越多的個體增重速度越快, 富集 4個的平均增重顯著快于富集0—3的個體增重,且比0標記的快約14%, 這反映出生長為數量性狀。進一步對所檢測位點進行雙倍型分析, 結果顯示具有四個優勢基因型且全部雜合優勢基因型的4567 (XXXXXXACCTCTCT)組的增重最快, 比0優勢基因型的增重快達 26.6%, 可以考慮用于今后的快增長建鯉的選育計劃中。此外, 雙倍型分析結果還表明, 不同位點之間可能存在或頡抗或協同的互作, 如1和4之間存在拮抗關系, 因此在今后的選育計劃中, 在考慮標記富集的情況下還應考慮標記之間的關系。宜在選擇互為協同作用優勢基因型的前提下, 富集盡可能多的SNP標記。
建鯉; 鳥氨酸脫羧酶; 基因型; SNP-增重相關分析
鳥氨酸脫羧酶(Ornithine decarboxylase, ODC)為多胺合成的限速酶, 催化鳥氨酸脫羧生成腐胺, 腐胺再相繼生成精脒和精胺, 腐胺、精脒和精胺統稱多胺, 多胺是細胞增殖、分化的關鍵物質, 因此, ODC及多胺對細胞的生長、機體的生長具有重要的調節作用。研究表明, 鳥氨酸脫羧酶的活性在生長旺盛的組織內明顯高于生長緩慢的細胞和組織, 可以作為細胞增殖的指標[1,2]。在養殖業中, ODC就被作為與生長密切相關的候選基因, 肌肉鳥氨酸脫羧酶活性被認為是與蛋白合成相關的生化指標。雞(Gallus domestiaus)的鳥氨酸脫羧酶基因位于生長QTL區內, 該基因啟動子上的多態性與生長和軀體框架特征顯著相關[3]。在水生動物的研究中, 生長快的大西洋鮭(Salmo salar)幼魚背軸肌肉鳥氨酸脫羧酶活性明顯高于生長慢的個體[4], 能作為特定生長率的指標[5]。本實驗通過測定6個個體基因序列, 在建鯉的2個ODC1基因上構建了10個SNPs位點的PCR-RFLP檢測方法, 分析了10個位點在12個家系建鯉群體中的分布, 以及不同基因型與雌、雄及各自魚種階段、成魚階段增重的相關性, 篩選與生長性狀相關的分子標記, 為分子輔助育種奠定基礎。
1 材料與方法
1.1 材料
實驗魚為中國水產科學研究院淡水漁業研究中心宜興養殖基地繁育的建鯉選育群體, 12家系, 繁殖后分家系于網箱養殖, 約1個月, 每家系PIT標記約90尾, 測初重等數據后混合于同一池塘養殖。養至當年底掃描標記并測定體重等數據, 減去初重計為魚種階段增重, 第二年繼續養殖至11月份, 測定體重等數據, 減去第二次測定的體重計為成魚階段增重。養殖過程中存在標記丟失、魚死亡等意外事件, 最終實驗魚約942尾。
1.2 實驗方法
DNA抽提 實驗魚尾靜脈采血, 蛋白酶K消化過夜, 傳統酚-氯仿法提取基因組DNA[6], DNA完整性使用瓊脂糖凝膠電泳檢驗, 濃度使用紫外分光光度計測定, A260/280一般為1.8左右。TE將DNA樣品稀釋成50—100 ng/μL備用。
多態位點篩選和檢測 根據本實驗室分離到的CcODC1s基因設計引物[7], 測定6尾建鯉ODC1s序列, 使用 Clustal W[8]軟件比對, 以同一位點不同堿基出現比例大于 1/3認定為 SNPs 位點。再通過分析SNP位點附近序列特征兼顧考慮a和b特異性擴增, 設計 SNP特異擴增引物, 結果 jlODC1a與jlODC1b上分別查找到 6個和 4個可以使用PCR-RFLP方法檢測的SNPs。各位點所使用的PCR引物、限制性內切酶以及不同基因型酶切片段信息見表1。在10個位點中, 有6個位于外顯子上, 其中有2個為非同義突變, 均位于jlODC1a上, 分別為E6_A212G改變氨基酸M(A)→V(G), E9_G19A改變氨基酸S(G) →N(A)。PCR擴增體系為12.5 μL, 其中含模板DNA 1.0 μL, 引物0.25 μL (10 μmol/L)。反應結束取6 μL PCR產物至10 μL酶切體系, 其中含內切酶 0.2 μL, 在不同酶推薦的溫度下反應3h, 然后用1.5%—3%瓊脂糖凝膠電泳檢測, 確定基因型。
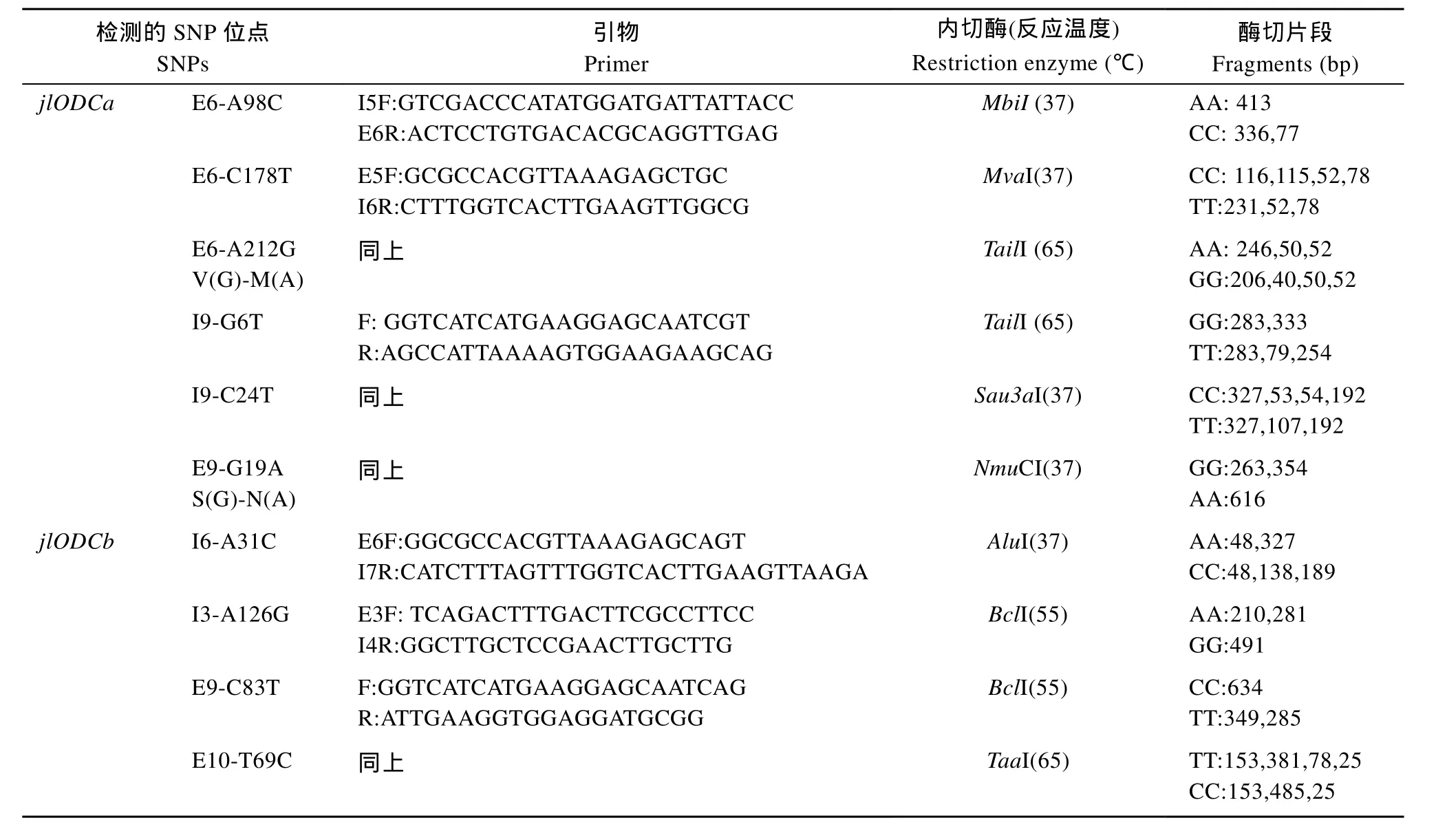
表 1 10個SNP位點的檢測引物, 限制性內切酶及酶切片段Tab. 1 Primers, restriction enzymes and restriction fragments of the 10 SNP loci
SNP位點的雙倍型分析 增重優勢基因型a-E6-A212G(AA)記為1, a-E9-G19A(AA)記為2, b-I3-A126G (AA)記為3, a-E6-A98C (AC)記為4, a-E6-C178T(CT)記為5, b-E9-C83T(CT)記為6, b-E10-T96C(CT)記為7, 同時考慮7個位點, 所檢測的建鯉可分為不含優勢基因型的0組; 有1個優勢基因型的4、6、7組; 有2個優勢基因型的14、17、26、56、57、67組; 有3個優勢基因型的146、147、167、256、456、 567組; 有4個優勢基因型的1467、1567、2567、4567組以及5個優勢基因型的14567組共21組個體組。其余各種優勢基因型或組合的樣本低于15尾的, 不列入統計范圍。通過21種雙倍型與增重的關聯分析,篩選出可用于建鯉選育計劃的基因型。
統計分析 利用SPSS軟件包的GLM模型進行SNP位點不同基因型、不同雙倍型與實驗魚不同階段增重的關聯分析。
2 結果
2.1 SNP位點的不同基因型檢測及與增重的相關性
本文所檢測的10個位點中有7個位點與增重呈顯著相關, 其中, a基因外顯子 6上有三個位點, A98C(AC型)、C178T(CT型)及A212G(AA型); 外顯子9上一個位點, G19A (AA型); b基因外顯子9上一個位點, C83T (CT型); 外顯子10上一個位點, T96C (CT型); 內含子 3上一個位點 A126G (AA型)。7個位點的基因型分布存在差異, 最小等位基因頻率 (MAF)為0.14—0.48(表2)。
表 2 10個SNPs位點在所檢測家系中的基因型分布以及與增重的相關性Tab. 2 Genotype distribution in experiment families of 10 SNPs and correlation with weight gain (±SE)

表 2 10個SNPs位點在所檢測家系中的基因型分布以及與增重的相關性Tab. 2 Genotype distribution in experiment families of 10 SNPs and correlation with weight gain (±SE)
注: 不同大寫字母表示同一位點不同基因型間差異極顯著(P<0.01); 不同小寫字母表示差異顯著(P<0.05)Note: Different capital and lowercase letters indicate significant difference of different genotypes of one same SNP site at P<0.01 and P<0.05 level, respectively
雄魚增重Male weight gain (g)位點SNPs基因型Genotype 魚種Juvenile雌魚增重Female weight gain (g)成魚Adult樣本數Sample魚種Juvenile成魚Adult樣本數Sample最小等位基因頻率MAF a-E6-A212G (1) AA 100.78±1.97 636.98±8.05 181 115.46±2.53A814.40±14.70A166 AG 103.67±4.71 657.15±9.00 216 107.27±2.45AB782.36±11.04AB200 G(0.39) a-E9-G19A (2) b-I3-A126G (3) a-E6-A98C (4) GG 96.17±2.87 652.59±14.48 83 98.76±2.72B744.19±16.07B70 AA 105.86±2.72 686.90±13.94A107 114.68±3.53a817.38±16.45a101 A(0.29) AG 98.51±2.09 648.50±10.06B159 109.09±2.75ab795.43±15.01ab151 GG 101.90±4.87 633.31±8.02B209 106.25±2.42b771.08±12.08b177 AA 107.16±4.29 745.19±22.41A49 124.47±5.75A860.44±30.70A50 A(0.32) AG 103.92±5.22 645.94±8.31B196 109.66±2.63B788.67±12.70B185 GG 98.68±1.80 633.15±8.02B231 105.65±1.96B774.80±10.59B203 AA 101.19±5.98 700.88±134.68A21 110.72±7.72AB780.36±38.07AB11 AC 105.16±2.06 671.36±10.18A174 119.82±2.78A838.02±15.33A165 A(0.22) CC 99.32±3.70 633.06±7.02B285 102.84±1.88B759.85±8.98B260 a-E6-C178T (5) b-E9-C83T b-E10-T96C (7) a-I9-C24T a-I9-G6T b-I6-A31C CC 98.08±1.71 643.56±8.56 215 104.75±1.82b782.46±11.76 182 CT 107.67±5.27 663.32±9.76 196 112.38±2.63a803.35±12.38 196 T(0.28) TT 95.95±3.30 632.64±12.88 71 111.61±5.41b764.24±24.98 61 CC 91.89±3.06B593.27±13.52B75 107.57±3.37B754.96±19.24b75 CT 117.85±3.68A676.61±7.53A287 122.25±2.23A808.72±10.52a249 C(0.47) TT 107.30±2.58A622.74±11.09B114 116.71±3.35AB774.58±17.58ab86 CC 98.99±5.01 639.40±8.62 204 99.98±1.67B769.56±11.04B193 CT 104.38±1.80 658.36±8.43 247 118.63±2.70A817.10±12.87A209 T(0.30) TT 93.71±5.08 636.89±27.02 19 99.03±4.55B715.38±24.13B22 CC 113.62±7.65 597.27±27.00 18 119.42±11.75 716.08±52.89 12 CT 96.55±8.41 576.71±22.08 16 90.54±5.39 671.76±27.95 15 C(0.14) TT 100.20±3.01 626.55±12.36 105 112.11±3.86 749.30±17.14 112 GG 101.14±2.33 668.81±12.70 125 108.26±2.88 779.18±16.31 119 GT 97.23±1.87 642.42±8.57 200 107.10±2.56 784.78±12.00 187 G(0.48) TT 107.79±6.83 643.10±9.94 149 114.35±2.99 810.101±15.53 124 A A 102.03±3.21 623.60±12.56 98 113.99±4.01 756.21±19.10 95 AC 105.20±4.46 612.98±15.30 53 115.28±5.67 732.01±18.79 58 C(0.23) CC 102.83±8.66 614.56±36.92 10 121.06±26.19 868.36±137.94 8
各位點的基因型分布及與增重相關性結果(表 2), b-E9-C83T 的CT型雄魚魚種增重極顯著高于CC型 (P<0.01); a-E6-A98C (AC)、a-E9-G19A (AA)、b-I3-A126G (AA)與 b-E9-C83T (CT)的雄魚成魚增重與其他類型相比均達到極顯著水平(P<0.01), 此次獲得的 7個陽性位點均與雌魚魚種增重顯著相關, 其中極顯著相關的有 5個分別為a-E6-A98C(AC)、a-E6-A212G (AA)、b-I3-A126G (AA)、b-E9-C83T (CT)、b-E10-T96C (CT) (P<0.01); 其余 2個與雌魚魚種增重顯著相關(P< 0.05)。與雌魚魚種增重極顯著相關的5個位點中除了 b-E9-C83T (CT,顯著水平)外, 其余4個也均與雌魚成魚的增重極顯著相關, 另外還有a-E9-G19A (AA)位點與雌魚成魚增重顯著相關(P<0.05)。圖1為7個陽性位點的基因分型圖。
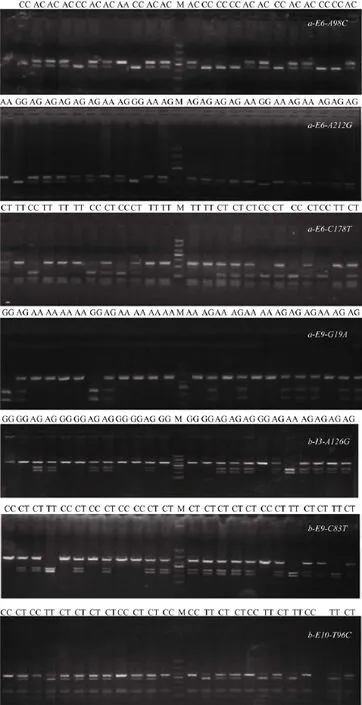
圖1 7個陽性SNP 位點不同基因型的電泳結果Fig. 1 Electrophoresis patterns of different genotypes in seven SNP loci M. DNA marker (DL1000)
2.2 標記富集與雙倍型分析
本次所獲得的7個與增重相關標記, 4個位于jlODCa上分別為即a-E6-A98C (AC)、a-E6-A212G (AA)、a-E6-C178T(CT)、a-E9-G19A(AA); 3個位于 jlODCb上分別為 b-I3-A126G1a(AA)、b-E9-C83T (CT)、b-E10-T96C(CT)。在7個位點中, 富集個數最多的為6個(表3)。分析結果, 隨著標記富集個數的增加, 建鯉增重隨之增加。富集3個標記的個體增重比無標記的個體增重快13.6% (P<0.05), 4個標記個體增重極顯著高于 3個標記個體增重(P<0.01)。而富集5個標記的個體增重比富集4個標記的個體增重有增高, 但差異不顯著; 富集 6個標記的個體僅有12尾, 雖然平均增重極顯著高于富集4個標記的個體增重,但不能列入統計范圍。在所檢測的建鯉群體中有 4個標記的魚有 178尾, 約占19.1%。
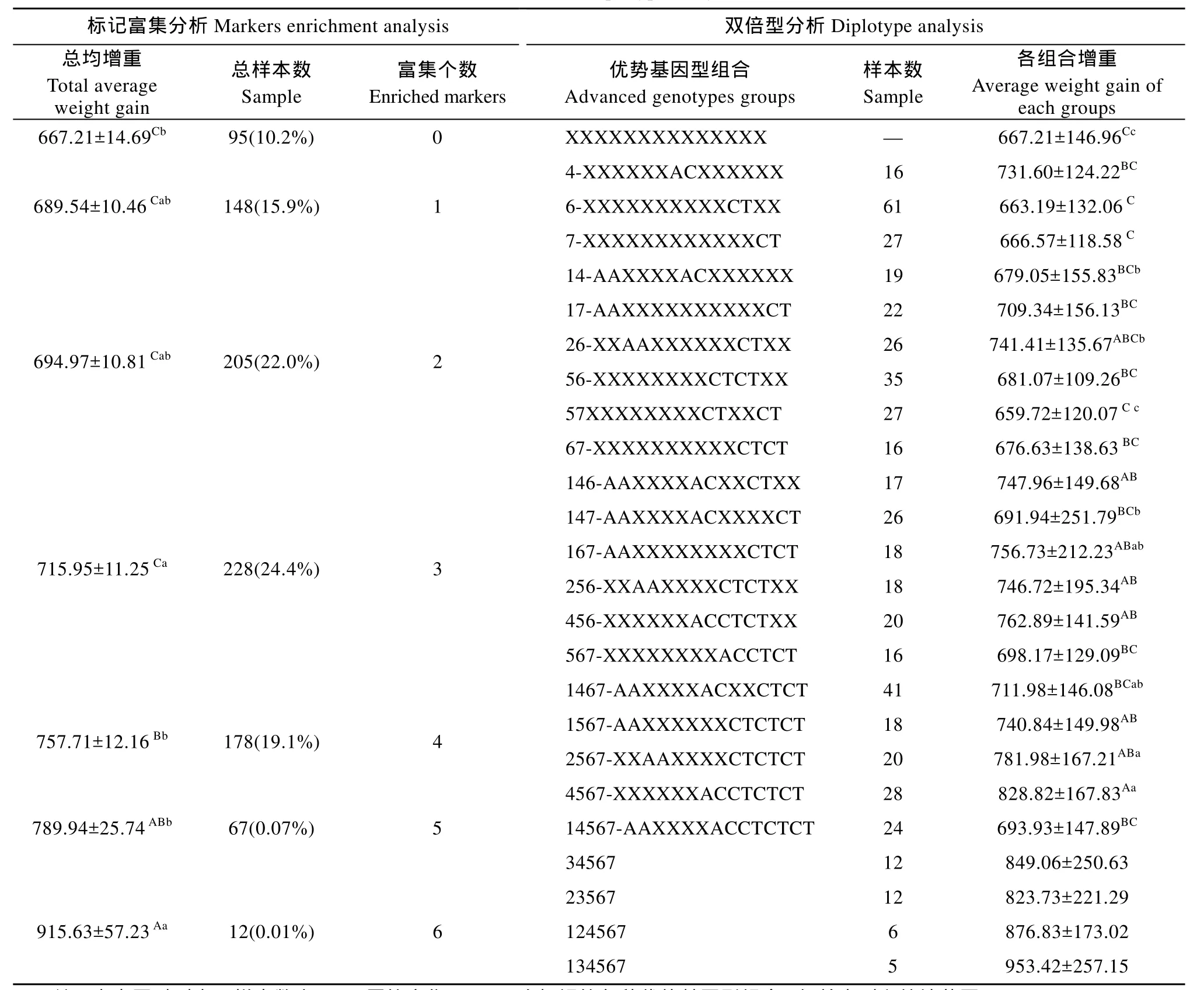
表3 標記富集及雙倍型分析Tab. 3 Markers enrichment and diplotype analysis of screened SNPs
21組雙倍型與增重關聯分析顯示, 0組與1個優勢基因型各組均沒有顯著差異, 其中 4組增重最快達731.6 g, 較0組增重約11.7%。在有2個優勢基因型的 6組中, 只有 26組增重(741.41 g)顯著快于57組(659.72 g) (P<0.05); 其余差異不顯著。3個優勢基因型的各組差異不顯著; 四個優勢基因型各組中, 4567組增重為所有檢測組中最高(823.82 g)極顯著高于1467組(711.98 g) (P<0.01)且各組增重均大于700 g。有5個優勢基因型有三組, 34567、23567和14567, 前兩組樣本數均為12尾, 樣本大于15的僅有14567一組, 但增重僅為693.93 g, 為三組中增重最慢的。而同時有 6個優勢基因型的僅有兩組124567和134567, 二者雖然增重都比較快, 但由于二者樣本數均少于10尾, 不能列入統計范圍。
3 討論
單核苷酸多態性 (Single nucleotide polymorphism, SNP), 主要指在基因組水平上單個核苷酸的變異所引起的DNA序列多態性, 在基因組中分布廣泛。在畜禽類養殖業中, SNP位點可能與機體的各種生長或經濟性狀相關, 可用于現有品種改良與新品種的選育。Orexin基因5′調控區篩選到了與牛(Bos tarurs)增重相關的SNP位點[9], PNRCI基因的3′非翻譯區篩選到了與菜鴨(Tsaiya ducks)繁殖性能相關的SNP位點[10]。水產養殖業中至今也有較多報道, 如斑節對蝦(Penaeus monodon)[11]、羅非魚(Oreochromis niloticus)[12]、大口黑鱸(Largemouth bass)[13]的生長相關位點。本實驗室在關于SNP位點篩選方面也做了大量的研究, 如尼羅羅非魚的 IGF-2基因[14], 吉富羅非魚(Genetically improved farmed tilapia, GIFT)的GH[15]、GHR[16]、IGF-1[17]基因, 尤其是在建鯉的與生長相關的基因上, 如 MSTN[18]、GHR[19]、GHSR[20]、IGFBP1[21]、IGFBP3[22]、IGF-Ia[23]、FABP2[24]、FABP3[25], 篩選了多個可以應用于選育的生長相關的SNP位點。
在分離了2個建鯉jlODC1s基因并確定該基因的表達與建鯉生長相關后[7], 通過查找兩基因上的SNP位點, 本實驗在jlODC1a與 jlODC1b兩個基因上分別構建了6和4個SNP位點的PCR-RFLP檢測方法, 從實驗圖譜可以看出, 檢測結果清晰、可靠。將 SNP位點的不同基因型與增重進行相關性分析,結果共獲得了 7個與建鯉增重顯性相關的位點, 其中4個位于jlODC1a基因上, 3個位于jlODC1b基因上, 與雄魚魚種階段增重極顯著相關的SNP位點1個 (P<0.01); 與成魚階段增重極顯著相關的位點有4個 (P<0.01)。與雌魚魚種階段增重相關的位點有7個, 分別呈顯著(P<0.05)和極顯著差異(P<0.01); 與雌魚成魚階段增重相關的有 6個。可見在 ODC1s基因上與雌魚增重相關的SNP位點較雄魚多, 俞菊華等在ODC1s基因的表達研究中報道, 肌肉組織中ODC1s基因雌魚的表達量明顯高于雄魚, 且無論雌魚雄魚, a基因的表達在腦、肝臟、肌肉、性腺等組織中一般都要高于 b基因的表達, 尤其是肝臟中達到顯著差異水平(P<0.05)[7], 這可能也是造成本次與建鯉增重顯性相關SNP位點的篩選中a基因(4個)略多于b基因(3個)的一個原因。另外, 同一位點基因型在雌、雄魚的表現不完全一致, 如a-E6-A212G、a-E6-C178T、a-I9-C24T及b-E10-T96C四個位點均與雌魚增重顯性相關, 但與雄魚增重并未表現出相關性; 同一位點在魚不同生長階段的表現也不完全一致, a-E6-A98C、a-E9-G19A及b-I3-A126G位點與雄魚成魚增重極顯著相關, 但與雄魚魚種階段增重則相關性不顯著; 這些差異可能與該基因在不同性別和不同階段的表達差異有關, 如阮瑞霞等在進行篩選吉富羅非魚GHR上增重相關SNP時就出現類似雌雄差異的情況是與基因表達水平相一致的[16]。
標記富集結果反映了生長為數量性狀, 總的來說富集標記越多的個體增重速度越快, 富集 4個標記以上的增重比0標記的快約14%。雙倍型分析結果顯示同時具有4個優勢基因型的1467、1567、2567與4567等4組增重均大于700 g, 其中4567組增重(828.82±167.83) 明顯快于其他三組, 其中極顯著快于1467組(711.98±146.08) (P<0.01)。就此次研究的建鯉 ODC1s的 SNP位點, 要選擇培養的是富集 4個標記, 且基因型分別為 4567 (XXXXXXACCT CTCT)基因型的個體, 其增重較 0優勢基因型的個體快 26.6%, 比群體平均增重快約 13%, 可以考慮用于今后快速增長建鯉的育種計劃中。本次所得 7個陽性位點中共 3個純合型, a-E6-A212G(AA)、a-E9-G19A(AA)與 b-I3-A126G(AA), 說明純合型對增重優勢起到了一定的作用, 而在雙倍型分析中 4個優勢基因型的4組中, 全部為雜合型的4567組增重明顯快于各包含一個純合、三個雜合型的其他三組, 其中極顯著快于1467組。就此次研究而言雜合型位點對于個體增重的貢獻更多。
各位點雙倍型分析結果還顯示, 單獨具有4(AC)的個體增重明顯快于具有兩個優勢基因型的14、56、67、17、57、67組、三個優勢基因型的147、567, 以及4個優勢基因型的1467組的個體。由此, 4 (AC)為建鯉ODC1s基因上與增重相關的主效 SNP位點, 且各位點之間存在著或頡抗或協同的作用。比較 4與 14組合, 平均增重由 731.60 g降至679.05 g, 尤其4567與14567組相比, 增重由828.82 g驟降至693.93 g, 由此1與4表現為頡抗;與之相反, 比較7與17組合, 6與26組合, 二者分別由666.57與663.19增至709.34與741.41 g, 由此推測1與7、2與6表現為協同作用。本次標記富集分析與雙倍型分析的結果有些不太相符, 一方面可能由于多位點一起分析后, 各小群的樣本數不夠大, 各位點之間是否還存在我們尚未清楚的相互關系, 而這些相互關系可能就導致標記富集數與增重之間不完全是一致的結果?本次研究最終僅得到了富集 4個標記的一種最優基因型組合, 將來是否可以篩選到富集五個甚至六個的最優基因型組合?接下來我們將擴大樣本數對這個問題進一步驗證, 且此次五、六個標記的各基因型組合也展現出增重明顯上升的趨勢, 因此繼續這個思路的篩選工作具備充分的可行性, 另一方面也提示我們在今后的選育過程中, 在選育富集多SNP標記個體的同時也要注重各優勢基因型的組合, 揚長避短, 在選擇互為協同作用優勢基因型的前提下, 富集盡可能多的SNP標記。
[1] Tsuji T, Todd R, Meyer C, et al. Reduction of ornithine decarboxylase antizyme (ODCAz) level in the 7,12-dimethylbenz (a) anthraceneinduced hamster buccal pouch carcinogenesis model [J]. Oncogene, 1998, 16: 3379—3385
[2] Favre C, Camovale C E, Monti J A, et al. Inhibition by interferon alpha-2b of rat liver regeneration: effect on ornithine decarboxylase and total protein synthesis [J]. Biochemical Pharmacology, 2001, 61(12): 1587—1593
[3] Uemoto Y, Sato S, Ohtake T, et al. Ornithine decarboxylase gene is a positional candidate gene affecting growth and carcass traits in F2intercross chickens [J]. Poultry Science, 2011, 90(1): 35—41
[4] Benfey T J, Saunders R, Knox D E, et al. Muscle ornithine decarboxylase activity as an indication of recent growth in pre-smolt Atlantic salmon, Salmo salar [J]. Aquaculture, 1994, 121(1—3): 125—135
[5] Arndt SKA, Benfey T J, Cunjak R A. A comparison of RNA concentrations and ornithine decarboxylase activity in Atlantic salmon (Salmo salar) muscle tissue, with respect to specific growth rates and diet variations [J]. Fish Physiology and Biochemistry, 1994, 13(6): 463—471
[6] Sambrook J, Fritsch E F, Maniatis T (Eds.), Huang P T, trans. Molecular Cloning-A Laboratory Manual [M]. Beijing: Science Press. 2002, 463—465
[7] Yu J H, Li H X, Tang Y K, et al. Characterization and expression analysis of ornithine decarboxylase 1 genes of Cyprinus carpio l [J]. Acta Hydrobiologica Sinica, 2013, 37(3): 566—571 [俞菊華, 李紅霞, 唐永凱, 等. 鯉魚鳥氨酸脫羧酶基因的序列特征和表達. 水生生物學報, 2013, 37(3): 566—571]
[8] Thompson J D, Higgins D G, Gibson T J. CLUSTAL W: improving the sensitivity of progressive multiple sequence alignment through sequence weighting, position-specific gap penalties and weight matrix choice [J]. Nucleic Acids Research, 1994, 22: 4673—4680
[9] Zhang A, Zhang L, Zhang L, et al. Single Nucleotide polymorphism (SNP) analysis of orexin gene 5′regulatory region in Chinese indigenous cattle populations [J]. Agricultural Sciences in China, 2011, 10(8): 1273—1279
[10] Chang M T, Cheng Y S, Huang M C. A novel SNP of the PNRC1 gene and its association with reproductive traits in Tsaiya ducks [J]. Theriogenology, 2012, 78(1): 140—146
[11] Prasertlux S, Khamnamtong B, Chumtong P, et al. Expression levels of RuvBL2 during ovarian development and association between its single nucleotide polymorphism (SNP) and growth of the giant tiger shrimp Penaeus monodon [J]. Aquaculture, 2010, 308(1): S83—S90
[12] Liu F P, Bai J J, Ye X, et al. Cloning of MC4R gene and study on the association between SNPs of MC4R and growth trait in tilapia (Oreochromis niloticus) [J]. Journal of Fishery Sciences of China, 2009, 16(6): 816—823 [劉福平, 白俊杰,葉星, 等. 羅非魚 MC4R基因克隆及與生長相關的 SNP位點. 中國水產科學, 2009, 16(6): 816—823]
[13] Yu L Y, Bai J J, Fan J J, et al. SNPs detection in largemouth bass myostatin gene and its association with growth traits [J]. Journal of Fisheries of China, 2010, 34(6): 665—671 [于凌云, 白俊杰, 樊佳佳, 等. 大口黑鱸肌肉生長抑制素基因單核苷酸多態性位點的篩選及其與生長性狀關聯分析.水產學報, 2010, 34(6): 665—671]
[14] Yu J H, Chen X F, Li J L, et al. Isolation of IGF2 and association of IGF2 polymorphism with growth trait in genetically improved farmed tilapias, Oreochromis niloticus L [J]. Aquaculture Research, 2010, 41(11): e743—e750
[15] Tang Y K, Yu J H, Xu P, et al. Cloning of growth hormone (GH) gene of genetically improved farmed tilapia (GIFT) and association of the single nucleotide polymorphisms (SNPs) of GH gene with the weight gain [J]. Journal of Hunan Agricultural University (Natural Sciences), 2012, 38(4): 422—425 [唐永凱, 俞菊華, 徐跑, 等. 吉富羅非魚生長激素(GH)的分離及其SNPs與增重的相關性. 湖南農業大學學報, 2012, 38(4): 422—425]
[16] Ruan R X, Yu J H, Li H X, et al. Isolation of two growth hormone receptor genes and SNPs associated with body weight in GIFT strain tilapia Orechromis niloticus [J]. Chinese Journal of Zoology, 2011, 46(3): 37—46 [阮瑞霞,俞菊華, 李紅霞, 等. 吉富羅非魚兩種生長激素受體基因的分離及與增重相關的 SNPs位點. 動物學雜志, 2011, 46(3): 37—46]
[17] Ruan R X, Yu J H, Li H X, et al. Effects of IGF-1 genotype on weight gain and body form in GIFT strain Orechromis niloticus [J]. Journal of Fishery Sciences of China, 2011, 18(3): 682—688 [阮瑞霞, 俞菊華, 李紅霞, 等. 吉富羅非魚IGF-1基因的基因型對生長和體型的影響. 中國水產科學, 2011, 18(3): 682—688]
[18] Yu J H, Li H X, Tang Y K, et al. Myostatin (MSTN) genes in Cyprinus carpio var. jian: isolation, expression, correlation between polymorphisms and body form, ADG [J]. Journal of Agricultural Biotechnology, 2010, 18(6): 1062—1072 [俞菊華, 李紅霞, 唐永凱, 等. 建鯉生長抑制素基因 MSTN的分離、表達及多態性與體型、平均日增重相關性研究. 農業生物技術學報, 2010, 18(6): 1062—1072]
[19] Tao W J, Ma L J, Yu J H, et al. SNP loci associated with weight gain on growth hormone receptor genes in Cyprinus carpio var. jian [J]. Acta Hydrobiologica Sinica, 2011, 35(4): 622—629 [陶文靜, 馬龍俊, 俞菊華, 等. 建鯉GHR基因多態性及與增重相關的SNP位點的篩選. 水生生物學報, 2011, 35(4): 622—629]
[20] Yu J H, Li H X, Li J L, et al. Characterization of growth hormone secretagogue receptor 1(GHS-R1) genes andweight gain associated SNP loci in Cyprinus carpio var. jian [J]. Journal of Fishery Sciences of China, 2012, 19(3): 390—398 [俞菊華, 李紅霞, 李建林, 等. 建鯉生長激素促泌素受體1基因的特性及其與增重相關SNP位點的篩選.中國水產科學, 2012, 19(3): 390—398]
[21] Wei K P, Yu J H, Li H X, et al. Isolation of IGFBP1 and SNP loci related to body weight gain in Cyprinus carpio var. jian [J]. Acta Agriculturae Boreali-Sinica, 2012, 27(3): 75—80 [魏可鵬, 俞菊華, 李紅霞, 等. 建鯉IGFBP1基因的克隆及與增重相關的SNP位點分析. 華北農學報, 2012, 27(3): 75—80]
[22] Wei K P, Yu J H, Li H X, et al. Isolation of IGFBP3 gene and SNPs associated with body weight gain in Cyprinus carpio var. jian [J]. Chinese Journal of Zoology, 2012, 47(1): 94—102 [魏可鵬, 俞菊華, 李紅霞, 等. 建鯉IGFBP3基因多態性對生長的影響. 動物學雜志, 2012, 47(1): 94—102]
[23] Li H X, Liu N N, Pu T N, et al. Isolation, SNPs identification and the correlation analysis with weight gain of IGF-Ia in Cyprinus carpio var. jian [J]. Journal of Shanghai Ocean University, 2012, 21(1): 173—179 [李紅霞, 劉楠楠, 浦天寧, 等. 建鯉IGF-Ia基因的SNPs位點篩選及其與增重的相關性分析. 上海海洋大學學報, 2012, 21(1): 173—179]
[24] Xia Z L, Yu J H, Li H X, et al. Sequences analysis of jlFABP2 and the correlation between polymorphisms and body weight gain in Cyprinus carpio var. jian [J]. Hereditas, 2013, 35(5): 628—636 [夏正龍, 俞菊華, 李紅霞, 等. 建鯉腸型脂肪酸結合蛋白基因的分離及其SNPs與增重的相關分析. 遺傳, 2013, 35(5): 628—636]
[25] Yu J H, Li H X, Li J L, et al. Sequences analysis of jlFABP3s and the correlation between polymorphisms and body weight gain in Cyprinus carpio var. jian [J]. Journal of Fisheries of China, 2012, 36(12): 1809—1818 [俞菊華, 李紅霞, 李建林, 等. 建鯉FABP3基因分離及其多態性與增重的相關分析. 水產學報, 2012, 36(12): 1809—1818]
CORRELATION ANALYSIS BETWEEN BODY WEIGHT GAIN AND ODC1 GENOTYPES IN CYPRINUS CARPIO var. JIAN
LI Hong-Xia, LI Jian-Lin, TANG Yong-Kai and YU Ju-Hua
(Key Laboratory of Freshwater Fisheries and Germplasm Resources Utilization, Ministry of Agriculture, Freshwater Fisheries Research Center, Chinese Academy of Fishery Sciences, Wuxi 214081, China)
Ornithine decarboxylase (ODC), arate-limiting enzyme in polyamine synthesis,is involved in several biological processes. PCR-RFLP was established to detect genotypes of ten SNPs (six for jlODC1a and four for jlODC1b) in about 900 individuals from 12 Cyprinus carpio var. jian families. The minimum allele frequency (MAF) was 0.14—0.48. The correlation between the genotypes of ten SNPs and body weight gain indicated that there are seven SNP loci in the female and four SNP loci in the male , and that the body weight gain is associated with the quantity of the SNPs. The individuals with four markers grew obviously faster than those with 0—3 markers, and grew 14% faster than those with 0 markers, which also reflected growth as a quantitative trait. The diplotype analysis of the screened SNPs demonstrated that individuals with four heterozygous advantage genotypes 4567 (XXXXXXACCTCTCT) were the fastest growth ones that were 26.6% faster than 0 advantage genotype individuals, which could be used in the fast-growth jian carp molecular breeding. Moreover, the diplotype analysis explored the exist of either antagonistic or synergistic interaction between different loci, suggesting that the choice of mutually synergistic advantages genotype and as much as possible SNP markers could benefit the future breeding programs.
Cyprinus carpio var. jian; Ornithine decarboxylase; Genotype; SNP-weight gain correlated analysis
Q344+.1
A
1000-3207(2014)03-0414-08
10.7541/2014.59
2013-04-16;
2014-01-27
國家科技部“863計劃”項目(2011AA100401); 公益性行業(農業)科研專項(200903045); 現代農業產業技術體系建設專項資金(CARS-46); 鯉肉質相關分子標記的挖掘(2013JBFM03)資助
李紅霞(1982—), 女, 山東聊城人; 碩士, 助理研究員; 主要從事水生生物技術。E-mail: lihx@ffrc.cn
俞菊華 (1966—), 女, 江蘇蘇州人; 博士, 研究員; 主要從事水生生物技術研究。E-mail: yujh@ffrc.cn

