促進劑對α—氰基丙烯酸酯膠固化反應動力學的影響
劉潔 聶聰 黃海江 師力
摘要:選用了3種α-氰基丙烯酸酯膠粘劑常用促進劑(18冠-6醚、PEG400DMA、杯4芳烴)分別加入到膠液中,采用非等溫DSC技術分析了不同升溫速率下3種促進劑對膠液固化反應動力學的影響。結果表明,和空白膠液相比,分別加入3種促進劑都能降低膠液固化的反應活化能,其中含有18冠-6醚的活化能最低,促進膠液固化的效果在3種促進劑中最好。
關鍵詞:α-氰基丙烯酸酯膠;固化促進劑;固化動力學
中圖分類號:TQ433.4+36 文獻標識碼:A 文章編號:1001-5922(2014)01-0050-04
1 前言
α-氰基丙烯酸酯膠粘劑由于具有單組分、固化快、強度高等特點而被廣泛應用,但在某些酸性材質上固化速度仍有待提高。據文獻報道,杯芳烴、氧雜杯芳烴、硅冠醚、環糊精、冠醚類、聚二(甲基)丙烯酸(乙二醇)酯、乙氧基化含氫化合物及其混合物等都可以用作氰基丙烯酸酯膠粘劑的促進劑,但這些促進劑對膠液固化反應動力學影響方面的報道,目前還較少。
本文選用了3類常用促進劑18冠-6醚、PEG400DMA、四丁基四[2-乙氧基-2-氧代乙氧基]杯4芳烴(杯4芳烴),采用非等溫DSC技術,研究不同促進劑對膠液固化反應動力學的影響。其中非等溫固化的方法包括單一加熱速率法和多個加熱速率法,且多個加熱速率法應用更為普遍。因此本文主要通過比較不同升溫速率(5 K/min、10 K/min、15 K/min、20 K/min)下3種促進劑對膠液固化反應動力學的影響,并通過計算固化反應的活化能,進一步驗證3種促進劑的促進效果。
2 實驗部分
2.1 試驗材料
自制α-氰基丙烯酸酯膠粘劑、促進劑18冠-6醚、促進劑PEG400DMA、杯4芳烴。
2.2 樣品制備
將不同促進劑以一定比例分別加入到氰基丙烯酸酯膠粘劑中,常溫攪拌至溶解即可。將配好的膠樣放置在陰涼干燥處待用。
2.3 非等溫DSC測試
采用美國TA公司的DSC Q2000 型差示掃描量熱儀,將樣品置于標準坩堝內,樣品質量約5~10 mg(精確到0.1 mg),氣氛為高純氮氣。分別選擇5 K/min、10 K/min、15 K/min、20 K/min 4種升溫速率,對樣品進行動態升溫掃描。
3 結果與討論
有關非等溫固化反應動力學的數據處理,有許多不同的方法,其中以Kissinger法[1,2]應用較多。主要是利用微分曲線的峰溫值與升溫速率的關系進行動力學計算,不涉及機理函數的選擇,從而避免了選擇反應機理可能帶來的誤差,被認為比較可靠。本文選用了Kissinger法對氰基丙烯酸酯膠的非等溫固化動力學進行研究。
Kissinger方程見式(1):
-ln(β/Tp2)=-ln(AR/Ea)+(1/Tp)(Ea/R) ( 1)
式中:Tp為各個升溫速率下的峰值溫度;β為升溫速率,K/min;A 為頻率因子;R 為理想氣體常數。根據Kissinger方程可知,以ln(β/Tp2)對1/Tp 作圖,線性回歸得到一條直線,由斜率和截距就能計算出Ea和A。
3.1 促進劑18冠-6醚對氰基丙烯酸酯膠固化反應動力學的影響
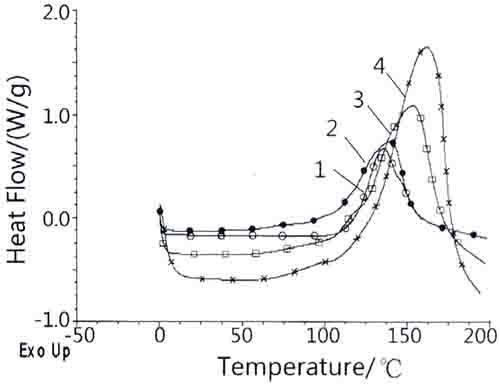
對添加有促進劑18冠-6醚的氰基丙烯酸酯膠液進行不同升溫速率(5 K/min、10 K/min、15 K/min、20 K/min)的DSC掃描,結果見圖1。對于同一樣品,升溫速率越快,整個峰形越高而窄。并按照Kissinger方程,對該DSC結果進行處理,結果如表1所示。
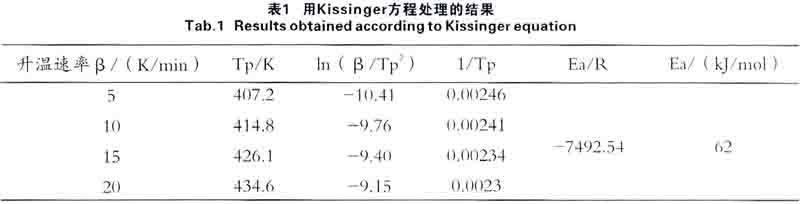
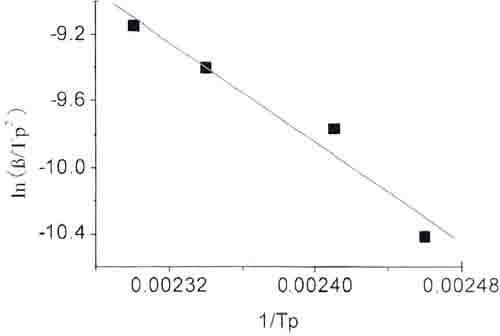
根據表1結果,以ln(β/Tp2)對1/Tp 作圖線性回歸得到圖2直線,由直線斜率計算得到體系的固化反應活化能為62 kJ/mol。
3.2 促進劑PEG400DMA對氰基丙烯酸酯膠固化反應動力學的影響
對添加有促進劑PEG400DMA的氰基丙烯酸酯膠液同樣進行不同升溫速率的DSC掃描。按照Kissinger方程,對該DSC結果進行處理,結果如表2所示。
根據表2結果,以ln(β/Tp2)對1/Tp 作圖線性回歸得到圖3直線,由直線斜率計算得到體系的固化反應活化能為65 kJ/mol。
3.4 未添加促進劑的氰基丙烯酸酯膠粘劑的固化反應
對未添加任何促進劑的氰基丙烯酸酯膠液進行同上的DSC掃描,并按照Kissinger方程,對該DSC結果進行處理,結果如表4所示。
根據表4結果,以ln(β/Tp2)對1/Tp 作圖線性回歸得到圖5直線,由直線斜率計算得到體系的固化反應活化能為75 kJ/mol。
由上述實驗結果可見,3種促進劑均能降低膠液的固化反應活化能,其中含促進劑18冠-6醚的膠液反應活化能最低,即促進膠液固化的效果最好。
4 結論
應用Kissinger方程計算活化能,表明3種促進劑的加入均能使膠液的固化反應活化能降低,即都能促進膠液的快速固化;其中加促進劑18冠-6醚的膠液反應活化能最低,促進膠液固化的效果最好。
參考文獻
[1]Lu Z R.Advan ces in th erm al analys is k inetics[J].Journal of Inorganic Chemistry,1998,14(2):119-126.
[2]胡榮祖,史啟禎,等.熱分析動力學[M].第2版.北京:科學出版社,2008.

